Académique Documents
Professionnel Documents
Culture Documents
4Dc213 PDF
Transféré par
amath ndiayeTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
4Dc213 PDF
Transféré par
amath ndiayeDroits d'auteur :
Formats disponibles
Année scolaire : 2012 /2013
Lycée secondaire Houmt-Souk 2
Lycée secondaire Sidi Zekri Devoir de contrôle n°2
Sections : 4ème Sc.Exp
Djerba Sciences physiques Durée : 2 heures
CHIMIE (9 points)
Exercice n°1 ( 5 points )
Dans une enceinte de volume V, on fait réagir 0,1 mol de méthane et 0,1 mol de vapeur d’eau, à la température
θ1 = 600°C.
Le système chimique aboutit à un état d’équilibre symbolisé par l’équation de la réaction suivante :
CH 4 g H 2 Og COg 3H 2 g
(1)
(2)
1°) A l’équilibre la quantité de matière de dihydrogène vaut n(H2)f = 0,24 mol.
a. Déterminer l’avancement final xf de cette réaction.
b. Déterminer la composition molaire du mélange à l’équilibre.
c. Déterminer le taux d’avancement final de cette réaction.
2°) On refait l’expérience précédante, à une température θ2 = 500°C, l’état d’équilibre est atteint lorsque 83%
de la quantité initiale de méthane a été consommée.
a. Montrer que la valeur de l’avancement final x’f = 0,083 mol.
b. Déduire le caractère énergitique de la réaction direct (sens (1)).
c. Préciser l’effet de cette diminution de la température sur la valeur de la constante d’équilibre K.
3°) La température est maintenue constante à la valeur θ2, le système est en équilibre, une variation de la
pression a déplacé l’équilibre dans le sens (2).
a. A-t-on augmenté ou diminué la pression ? Justifier.
b. Préciser l’effet de cette variation de pression sur la valeur de la constante d’équilibre K.
Exercice n°2 ( 4 points )
1°) On donne la classification des couples acide- base suivantes par ordre décroissant de base.
(1) (2) (3)
Force décroissante de la base
…… / NH - HClO / ClO HNO2 / NO 2
2
a. Donner l’acide conjugué de couple (1).
b. Attribuer à chaque couple acide-base le pKb correspondant. Justifier la réponse.
On donne : pKb 10,7 -9 6,5
c. Parmi les bases considérées ci-dessus, préciser la base forte.
d. Comparer en le justifiant, la force des acides des couples (2) et (3).
2°) On prépare deux solutions aqueuses (S1) et (S2), en dissolvant dans l’eau respectivement l’acide nitreux
HNO2 et l’acide hypochloreux HClO.
a. Ecrire l’équation de la dissociation de chaque acide dans l’eau.
b. Exprimer les constantes d’acidités Ka2 et Ka3, des couples (2) et (3), en fonction des concentrations des
espèces chimiques présentes dans chaque solution.
3°) On mélange les deux solutions (S2) et (S3), il s’établit un équilibre symbolisé par l’équation suivante :
HNO2 + ClO NO2 + HClO
a. Exprimer la constante K de cet équilibre en fonction de Ka2 et Ka3.
b. Calculer K. La valeur de K confirme-t-elle le résultat de la question 1°) d?
PHYSIQUE (11 points)
Exercice N° 1 ( 5 points )
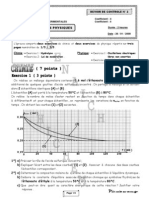
Figure 1
On réalise un circuit qui comporte :
Un condensateur initialement chargé de capacité C
Une bobine d’inductance L et de résistance négligeable.
Un interrupteur K .
A l’instant de date t0 = 0 s on ferme l’ interrupteur K.
Un oscilloscope convenablement branché permet de visualiser
la tension uC(t) aux bornes du condensateur de la figure 1.
1) a- Préciser la nature des oscillations. Justifier. Time/div : 0,2 ms/div
b- Déterminer à partir du graphe, la période propre T0
de l’oscillateur.
2) a- Exprimer l’énergie électromagnétique E de l’oscillateur en fonction de uC(t), C, L et de l’intensité du
courant i(t).
b- Déduire l’équation différentielle en uC(t).
3) a- Montrer que l’énergie magnétique emmagasinée dans la bobine est :
1
EL = C(U02 - uC (t) 2 ) ,avec U0 : la tension initiale aux
2 EL(µJ)
25
borne du condensateur.
b- Une étude expérimentale permet de tracer la courbe
EL = f(uC (t) 2) de la figure 2.
Justifier l’allure de la courbe.
Déterminer la valeur maximale de uC(t) .Déduire la
capacité C.
Déterminer l’inductance L. UC2 (V2)
b- Déterminer l’expression de la charge q(t). 0 25
Figure 2
Exercice n°2 ( 6 points )
Un oscillateur électrique est formé à partir d’un générateur GBF délivrant une tension sinusoïdal
u (t ) 1,3 sin (2 N e t ) de fréquence variable, et d’une portion de circuit électrique comportant les dipôles
suivants montés en série :
- un condensateur de capacité C = 0,47 μF.
- un résistor de résistance R ;
- une bobine d’inductance L et de résistance négligeable devant celle du résistor .
1°) Sur la figure 6, de l’annexe ci-joint, est schématisé un circuit électrique incomplet.
Placer convenablement la bobine, le condensateur, le résistor et effectuer les connexions convenables avec
l’oscilloscope afin de voir simultanément sur l‘écran de; l’oscilloscope :
- la tension u(t) à l’entrée Y1 ;
- la tension uc(t) aux bornes du condensateur à l’entrée Y2.
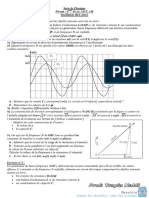
2°) Les oscillogrammes apparus sur l’écran de l’oscilloscope correspondants à u(t) et à uc(t), pour une valeur
N1 de la fréquence Ne sont donnés dans la figure 3.
uC(t)
u(t)
0V Y1Y2
Figure 3
Temps (s/Div) Y1 (V/Div) Y2 (V/Div)
a- En tenant compte du choix de la sensibilité horizontale et de la sensibilité verticale à l’entrée Y2 ,figure 6
500µs/Div 500mV/Div 1,0V/Div
de l’annexe, Montrer que la valeur de la fréquence de l’oscillateur N1 off
Couplage : DC Couplage : DC
232 Hz .
b- Déterminer la sensibilité verticale SV utilisée à l’entrée Y1. le choix adopté sera marqué par une flèche à
l’endroit qui convient sur l’annexe.
3°) a- Montrer que la tension u(t) est en quadrature avance de phase par rapport uC(t)..
b- Montrer que la valeur de déphasage = u - i = 0 rad.
c- En déduire que le circuit est le siège d’une résonance d’intensité.
d- Monter que l’amplitude de l’intensité de courant Imax = 2,46 mA.
e- Déduire la résistance R du résistor.
4°) On donne, à la résonance d’intensité sur la figure 5 de l’annexe et à l’échelle, le vecteur de Fresnel
relatif à la tension uC(t).
a- Compléter, dans l’ordre, la construction de Fresnel relative à l’équation différentielle suivante :
1 di
idt Ri L u (t )
C dt
b- Déduire la valeur de l’inductance L de la bobine.
5°) En gardant les mêmes sensibilités, et on faisant uC(t)
varier la fréquence du générateur ,On constate que pour
une fréquence N2 = 200 Hz, l’amplitude UCmax de u(t)
la tension uC prend une valeur maximale. (figure 4) 0V Y1Y2
a) Nommer le phénomène qui se produit dans le
circuit à cette fréquence.
b) Préciser si le circuit inductif, capacitif ou résistif. Figure 4
c) Donner l’expression de la fréquence N2.
Temps (s/Div) Y1 (V/Div) Y2 (V/Div)
d) Déterminer à cette fréquence l’expression de uC(t).
500µs/Div 500mV/Div 1,0V/Div
Bon courage
Couplage : DC
Couplage : DC off
Nom : ……………………. Prénom :……………………. Classe :……………...
Echelle : 1 cm 0,5 V
+
Figure 5
.5
G .5
.5
5 5
Y1 Y2
Figure 6
Vous aimerez peut-être aussi
- Exercices d'optique et d'électromagnétismeD'EverandExercices d'optique et d'électromagnétismeÉvaluation : 5 sur 5 étoiles5/5 (1)
- Travail Et PuissanceDocument7 pagesTravail Et Puissanceamath ndiayePas encore d'évaluation
- Série Physique LesOscillationsElectriquesLibres BacSci 1Document8 pagesSérie Physique LesOscillationsElectriquesLibres BacSci 1Belgasem Assel0% (1)
- DC2 (26 01 08)Document5 pagesDC2 (26 01 08)Seif Souid100% (4)
- 638db87da9cf6 - Enoncé-Devoir de Synthese N1Document10 pages638db87da9cf6 - Enoncé-Devoir de Synthese N1Imen Barhoumi0% (1)
- Série de Révision N°1Document5 pagesSérie de Révision N°1BaccariPas encore d'évaluation
- Bac Blanc 2021bisDocument7 pagesBac Blanc 2021bisSahbi Mabrouki YamenPas encore d'évaluation
- DC1 4SC 2022 2023 Boussada - AtefDocument4 pagesDC1 4SC 2022 2023 Boussada - Atefabderrazek0% (1)
- Akkari ds1Document5 pagesAkkari ds1Mhamed CherchariPas encore d'évaluation
- Devoir de Synthèse N°1 - Sciences Physiques - Bac Informatique (2013-2014) MR Rhida SlimiDocument4 pagesDevoir de Synthèse N°1 - Sciences Physiques - Bac Informatique (2013-2014) MR Rhida SlimiLifi SamPas encore d'évaluation
- Bac PCDocument56 pagesBac PCOumar Traoré100% (2)
- R, L, C Forcé - 1 - PDFDocument3 pagesR, L, C Forcé - 1 - PDFHouyem Latiri100% (6)
- Devoir de Synthèse N°1 2022 2023Document4 pagesDevoir de Synthèse N°1 2022 2023Mohamed Hamdene100% (2)
- Preparation Cours Du Soir 2bac PC Biof Exo RLC RL RC 25-06-2020Document5 pagesPreparation Cours Du Soir 2bac PC Biof Exo RLC RL RC 25-06-2020thailand.blanePas encore d'évaluation
- Devoir de Contrôle N°2 Avec Correction 2011 2012 (Sidi Zikri)Document8 pagesDevoir de Contrôle N°2 Avec Correction 2011 2012 (Sidi Zikri)fayePas encore d'évaluation
- Devoir de Cont N°1 4ème SC Expnovem2019-2020Document3 pagesDevoir de Cont N°1 4ème SC Expnovem2019-2020Mohamed HamdenePas encore d'évaluation
- 4DS1 2010Document5 pages4DS1 2010Riadh MarouaniPas encore d'évaluation
- MS18G2Document3 pagesMS18G2Rachid FardadiPas encore d'évaluation
- Devoir de Cont N°1 4ème Sci Novem2019Document3 pagesDevoir de Cont N°1 4ème Sci Novem2019Mohamed HamdenePas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences physiques - Bac Sciences exp (2011-2012) Mr ben salah lotfiDocument4 pagesDevoir de Contrôle N°2 - Sciences physiques - Bac Sciences exp (2011-2012) Mr ben salah lotfifelhimokhtar613Pas encore d'évaluation
- Devoir de Synthèse N°1 - Sciences Physiques - Bac Sciences Exp (2017-2018) MR Handoura Naceur PDFDocument4 pagesDevoir de Synthèse N°1 - Sciences Physiques - Bac Sciences Exp (2017-2018) MR Handoura Naceur PDFMohamed SaidiPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2013-2014) MR Alibi Anouar (1) - DecryptedDocument5 pagesDevoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2013-2014) MR Alibi Anouar (1) - DecryptedchihebPas encore d'évaluation
- Série Physique Dipole RLC Forcé 2011 2012 (Trayia Nabil)Document4 pagesSérie Physique Dipole RLC Forcé 2011 2012 (Trayia Nabil)Iyed SEPas encore d'évaluation
- MS15G2Document4 pagesMS15G2Anas FaidiPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2014-2015) MR Ramzi RebaiDocument4 pagesDevoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2014-2015) MR Ramzi RebaiImen AbbessiPas encore d'évaluation
- Devoir de Controle N 1 Physique Chimie 4an 2010 2011Document5 pagesDevoir de Controle N 1 Physique Chimie 4an 2010 2011chihebPas encore d'évaluation
- Control 2 Officiel 3Document5 pagesControl 2 Officiel 3salma benmiledPas encore d'évaluation
- Série N°1 Dipole RC 2011 2012 (Alibi Anouar)Document8 pagesSérie N°1 Dipole RC 2011 2012 (Alibi Anouar)rachi fadyaPas encore d'évaluation
- dc1 4eme Sadiki 10-11Document4 pagesdc1 4eme Sadiki 10-11ben zayed aliPas encore d'évaluation
- Dev Controle1 4scDocument4 pagesDev Controle1 4scSahbi Mabrouki YamenPas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences physiques - Bac Sciences exp (2011-2012) Mr ben salah lotfiDocument4 pagesDevoir de Contrôle N°2 - Sciences physiques - Bac Sciences exp (2011-2012) Mr ben salah lotfifelhimokhtar613Pas encore d'évaluation
- Série 1 - Dipole RLC - Soutien À Distance - Prof OTHMANEDocument20 pagesSérie 1 - Dipole RLC - Soutien À Distance - Prof OTHMANEmohamedelhafhouf2006Pas encore d'évaluation
- Devoir Bac MathDocument5 pagesDevoir Bac MathLotfi KhemiliPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2015-2016) MR ABDAOUI HAMMADI PDFDocument4 pagesDevoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2015-2016) MR ABDAOUI HAMMADI PDFMohamed SaidiPas encore d'évaluation
- Devoir Corrigé de Synthèse N°1 - Sciences Physiques - Bac Math (2016-2017) MR Moncef AmaraDocument13 pagesDevoir Corrigé de Synthèse N°1 - Sciences Physiques - Bac Math (2016-2017) MR Moncef AmaraHanine HmidaPas encore d'évaluation
- Po SP - Tle D..HervéDocument3 pagesPo SP - Tle D..HervémarioagbozoPas encore d'évaluation
- dc1 4eme Sadiki09-10-1Document3 pagesdc1 4eme Sadiki09-10-1ben zayed aliPas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences Physiques - Bac Mathématiques (2016-2017) MR Jalel CHAKROUNDocument5 pagesDevoir de Contrôle N°2 - Sciences Physiques - Bac Mathématiques (2016-2017) MR Jalel CHAKROUNwalidPas encore d'évaluation
- Serie RLC Force 2Document4 pagesSerie RLC Force 2dontknowwhatisthis123Pas encore d'évaluation
- CHIMIE: (7 Points)Document5 pagesCHIMIE: (7 Points)Mohamed SaidiPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - Bac Math (2010-2011) MR Attaoui HechmiDocument5 pagesDevoir de Contrôle N°1 - Physique - Bac Math (2010-2011) MR Attaoui HechmiHanine HmidaPas encore d'évaluation
- 4Dc107Document4 pages4Dc107kimou246Pas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - Bac Mathématiques (2011-2012) MR Ayadi FawziDocument2 pagesDevoir de Contrôle N°1 - Sciences Physiques - Bac Mathématiques (2011-2012) MR Ayadi FawziMajed GharibPas encore d'évaluation
- Série D'exercices #9 - Sciences Physiques Oscillations Électriques Forcées - Bac Sciences Exp (2014-2015) MR Adam BoualiDocument4 pagesSérie D'exercices #9 - Sciences Physiques Oscillations Électriques Forcées - Bac Sciences Exp (2014-2015) MR Adam BoualiAziz BenamorPas encore d'évaluation
- Devoir de Synthèse N° 1: Le Sujet Comporte Deux Exercices de Chimie Et Deux Exercices de Physique Répartie Sur 4 PagesDocument4 pagesDevoir de Synthèse N° 1: Le Sujet Comporte Deux Exercices de Chimie Et Deux Exercices de Physique Répartie Sur 4 PagesMohamed HamdenePas encore d'évaluation
- Série Oscillateur Amortie Et Non AmortieDocument5 pagesSérie Oscillateur Amortie Et Non Amortieala_1964Pas encore d'évaluation
- Devoir de Synthèse N°2 2013 2014 (Zgued Hichem)Document4 pagesDevoir de Synthèse N°2 2013 2014 (Zgued Hichem)Nourelhouda Bourguiba Ep BellyPas encore d'évaluation
- Serie Oscillations Électriques ForcéesDocument9 pagesSerie Oscillations Électriques ForcéesJannadi SabehPas encore d'évaluation
- Série N°13Document5 pagesSérie N°13Jihad ELPas encore d'évaluation
- Sujet 622 CHIMIEDocument7 pagesSujet 622 CHIMIEakramadd2006Pas encore d'évaluation
- DC2 Q M Copie FINALEDocument4 pagesDC2 Q M Copie FINALEomar sellemi0% (2)
- Exercice 1: Le Sujet Comporte Cinq Pages Numérotées 1/5 À 5/5Document5 pagesExercice 1: Le Sujet Comporte Cinq Pages Numérotées 1/5 À 5/5Mohamed SaidiPas encore d'évaluation
- Devoir de Contrôle N°1 Lycée Pilote - Sciences Physiques - Bac Math (2014-2015) MR MOHSEN BEN LAMINE PDFDocument4 pagesDevoir de Contrôle N°1 Lycée Pilote - Sciences Physiques - Bac Math (2014-2015) MR MOHSEN BEN LAMINE PDFyassine tanabene50% (4)
- Série D'exercices N°2 - Sciences Physiques Série de Revision 2eme Trimestre - Bac Toutes Sections (2012-2013) Mme Titouhi ImenDocument3 pagesSérie D'exercices N°2 - Sciences Physiques Série de Revision 2eme Trimestre - Bac Toutes Sections (2012-2013) Mme Titouhi ImenTawfiq Weld EL ArbiPas encore d'évaluation
- TD Oscillateurs Électriques 2016Document9 pagesTD Oscillateurs Électriques 2016Oumar TraoréPas encore d'évaluation
- Dev Synthese N°14scDocument6 pagesDev Synthese N°14scSahbi Mabrouki Yamen0% (1)
- Ex RLCDocument3 pagesEx RLCmohamed laghrib100% (1)
- 0708LC PDFDocument2 pages0708LC PDFMoufida ZouaghiPas encore d'évaluation
- AlcoolsDocument4 pagesAlcoolsamath ndiayePas encore d'évaluation
- Exos Energie MecaniqueDocument2 pagesExos Energie Mecaniqueamath ndiayePas encore d'évaluation
- Applications Des Bases de La DynamiqueDocument2 pagesApplications Des Bases de La Dynamiqueamath ndiayePas encore d'évaluation
- Serie C1 Las 2023Document1 pageSerie C1 Las 2023amath ndiayePas encore d'évaluation
- Dev 3 1S2B Sem2 2015-2016Document1 pageDev 3 1S2B Sem2 2015-2016amath ndiayePas encore d'évaluation
- Serie C1 Las 2023Document3 pagesSerie C1 Las 2023amath ndiayePas encore d'évaluation
- Serie p1 Las 2023Document4 pagesSerie p1 Las 2023amath ndiayePas encore d'évaluation
- Compo 1 20152016Document5 pagesCompo 1 20152016amath ndiayePas encore d'évaluation