Académique Documents
Professionnel Documents
Culture Documents
Thermo N
Transféré par
azaraadama7550 évaluation0% ont trouvé ce document utile (0 vote)
5 vues1 pageThermo
Copyright
© © All Rights Reserved
Formats disponibles
PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentThermo
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
5 vues1 pageThermo N
Transféré par
azaraadama755Thermo
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 1
TRAVAUX DIRIGES N°2 DE THERMODYNAMIQUE
Exercice 1 : Un gaz parfait à la température T0=0 °c. A quelle température faut-il
l'échauffer pour que sous la même pression son volume sera doublé ?
Exercice 2:
Quel volume occupe 1 kg d'air à 15 °c sous la pression de 100 bars absolus? A quelle
température faut-il porter cet air pour que sous la même pression, son volume sera
doublé? On donne : r air=287,1 J/kg.°C
Exercice 3:
La masse volumique d'un gaz de ville est 0.56 kg/m à 17 °c et sous une pression de
980 mbars.
1°/ Quelle est la valeur de sa constante r?
2°/ Quelle est sa densité par rapport à l'air?
Exercice 4:
A 50°C, un mélange de 2 moles d’oxygène et 5 moles d’azote est comprimé à 3 atm.
Calculer la fraction molaire de l’oxygène, sa pression partielle, le volume total du
mélange ainsi que le pourcentage en volume de l’oxygène (Calculer le volume qu’il
occuperait, s’il était exposé seul aux conditions indiquées de température et de pression
et donner le pourcentage de ce volume par rapport au volume entier du mélange).
Exercice 5
Un volume d’air (gaz parfait) occupe un volume de 20 litres à la pression p1
1,013.105 Pascal et sous une température T1 273 K subit deux transformations
définies comme suit :
1- Une compression isochore : l’air est chauffé jusqu’à ce que sa pression soit 3 fois sa
pression initiale.
2- 2- Dilatation isobare : l’air est chauffé jusqu’à ce que sa température soit égale à
876,1 K.
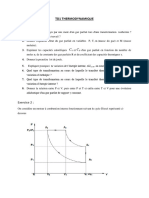
1°/ Représenter sur un diagramme de Clapeyron les deux transformations qu’à subi
l’air.
2°/ Quelle est la température atteinte par l’air à la fin de la première transformation ?
On donne : R=8,32 J/K.mol, =1,4, CV=708 J/K.mol, M=29 g/mole.
TD THERMO/BAC PRO/MVA/OUEDRAO.H Page 1 sur 1
Vous aimerez peut-être aussi
- TD 1 2 3 PDFDocument9 pagesTD 1 2 3 PDFBenouna Rajae AminaPas encore d'évaluation
- Série 1 TD Thermodynamique AP2 2020 - 2021Document2 pagesSérie 1 TD Thermodynamique AP2 2020 - 2021Hafsa ChadliPas encore d'évaluation
- Thermique 1Document39 pagesThermique 1Zakia ZikerPas encore d'évaluation
- Travaux Dirigés ThermodynamiqueDocument4 pagesTravaux Dirigés ThermodynamiqueRodolphe Sounou100% (2)
- Série de TD N1 2020Document2 pagesSérie de TD N1 2020Sara AkliPas encore d'évaluation
- TD N°4 Notions Générales Sur La Thermodynamique + SolutionDocument4 pagesTD N°4 Notions Générales Sur La Thermodynamique + SolutionAbd El Basset ünkutPas encore d'évaluation
- TD Thermo 21-22Document3 pagesTD Thermo 21-22Junior ALLODJIPas encore d'évaluation
- Thermodynamique TD, Tests, Exam CorrigeeDocument55 pagesThermodynamique TD, Tests, Exam CorrigeeAwatif BePas encore d'évaluation
- Exercice N1Document3 pagesExercice N1Harry Mongo100% (2)
- TD Serie 1 PDFDocument4 pagesTD Serie 1 PDFmohamed saadiPas encore d'évaluation
- TD Thermodynamique-2Document48 pagesTD Thermodynamique-2kawtar azzouziPas encore d'évaluation
- S Rie 2 ThermodynamiquenDocument3 pagesS Rie 2 Thermodynamiquenabdo issaouiPas encore d'évaluation
- Fiche de Travaux Diriges de ThermodynamiqueDocument3 pagesFiche de Travaux Diriges de ThermodynamiqueSerge KewouPas encore d'évaluation
- TD1-b PTD 012Document3 pagesTD1-b PTD 012Sif eddinePas encore d'évaluation
- S Rie 2 ThermodynamiqueDocument3 pagesS Rie 2 Thermodynamiquechakib abPas encore d'évaluation
- TD N°3 de PHYSIQUE IIIDocument3 pagesTD N°3 de PHYSIQUE IIIfjosephfabricePas encore d'évaluation
- Série N° 02. 2: (O (G) ) 29,26 J.K .MolDocument2 pagesSérie N° 02. 2: (O (G) ) 29,26 J.K .MolmimostarPas encore d'évaluation
- Exercices D'application - CopieDocument3 pagesExercices D'application - CopieAbbé Marc LESSAMBA100% (3)
- Exercices 2Document10 pagesExercices 2baklouty ferielPas encore d'évaluation
- TD Etudiant 2021Document2 pagesTD Etudiant 2021DIBIPas encore d'évaluation
- SÃrie 2 1Document6 pagesSÃrie 2 1bayou abderahimPas encore d'évaluation
- TD Drissa ThermoDocument11 pagesTD Drissa Thermoouedraogodri2016Pas encore d'évaluation
- TD Thermo en LigneDocument16 pagesTD Thermo en LigneDavi Nordel NgondzaPas encore d'évaluation
- Corrigés Chap1 Des ExoDocument3 pagesCorrigés Chap1 Des ExoChristophe AkitePas encore d'évaluation
- TD 4 Chimie 2-2021-2022Document3 pagesTD 4 Chimie 2-2021-2022Madrid Hz7Pas encore d'évaluation
- E 2ME PRINCIPE TD62emeprincipethermo PDFDocument6 pagesE 2ME PRINCIPE TD62emeprincipethermo PDFMosaab Echabane100% (1)
- Série N°01Document3 pagesSérie N°01mimostarPas encore d'évaluation
- Fiche TD 2Document2 pagesFiche TD 2Bouchiba leilaPas encore d'évaluation
- TD n1 ThermodynamiqueDocument1 pageTD n1 ThermodynamiqueKhalil LasferPas encore d'évaluation
- TD ThermodynamiqueDocument4 pagesTD ThermodynamiqueamenmhedhbiiPas encore d'évaluation
- Série de TD. Partie 2 Et 3. ActualiséeDocument2 pagesSérie de TD. Partie 2 Et 3. ActualiséeAddad FatimaPas encore d'évaluation
- TD 1 Thermochimie L2CDocument2 pagesTD 1 Thermochimie L2Cmeyemarion99Pas encore d'évaluation
- Ex Thermo 1Document10 pagesEx Thermo 1ArthurpetitPas encore d'évaluation
- Exercices de ThermodynamiqueDocument18 pagesExercices de ThermodynamiqueBadre-ezzamen KaddourPas encore d'évaluation
- TD Thermodynamique Serie2Document2 pagesTD Thermodynamique Serie2Kiliminii HanaPas encore d'évaluation
- Laboratorio de Mecánica de Fluidos 1 - FrancésDocument3 pagesLaboratorio de Mecánica de Fluidos 1 - FrancésDiego MezaPas encore d'évaluation
- TV Cte, T P Cte, PV Cte: Universite Mohammed V Svi-Stu Année 2005-2006 Faculte Des Sciences RabatDocument2 pagesTV Cte, T P Cte, PV Cte: Universite Mohammed V Svi-Stu Année 2005-2006 Faculte Des Sciences RabatkaderPas encore d'évaluation
- TD 1 Vca 1Document1 pageTD 1 Vca 1Adel AdilouPas encore d'évaluation
- TD4 ThermoDocument3 pagesTD4 ThermoYoussef BensaidPas encore d'évaluation
- TD DEC 21 #3 OkDocument2 pagesTD DEC 21 #3 OkLokossouPas encore d'évaluation
- TD 1 Rappels Sur Les Concepts de Base de La ThermodynamiqueDocument2 pagesTD 1 Rappels Sur Les Concepts de Base de La ThermodynamiqueAhmed Walid Arab100% (1)
- Série TD N°1. Chimie IIDocument2 pagesSérie TD N°1. Chimie IIchaima gasmi100% (1)
- TD 1thermoDocument2 pagesTD 1thermoGhassen BoussaaPas encore d'évaluation
- TD 1 ThermoDocument2 pagesTD 1 Thermomoney makerPas encore d'évaluation
- T5 TD PDFDocument2 pagesT5 TD PDFMario StiflerPas encore d'évaluation
- Fiche TD Machines Thermiques: Exercice 01Document3 pagesFiche TD Machines Thermiques: Exercice 01sino spagoPas encore d'évaluation
- TD1Document3 pagesTD1Randa BelaidiPas encore d'évaluation
- ZZZ Suppexos Th3 Th4 Premier Et Second PrincipesDocument12 pagesZZZ Suppexos Th3 Th4 Premier Et Second PrincipesOussama El BouadiPas encore d'évaluation
- Fiche de TD Valopro ThermoDocument5 pagesFiche de TD Valopro Thermomarcelina24Pas encore d'évaluation
- Examens Thermo 21 22Document2 pagesExamens Thermo 21 22Rawnek AkremiPas encore d'évaluation
- Cours Exercices Thermo4Document9 pagesCours Exercices Thermo4Fatou SECKPas encore d'évaluation
- TD de Thermodynamique CPGE1-2023Document5 pagesTD de Thermodynamique CPGE1-2023Ange Michel Romuald DjePas encore d'évaluation
- TD1 2022 2023Document2 pagesTD1 2022 2023blablaPas encore d'évaluation
- Serie01 23 Biophys-FinaleDocument2 pagesSerie01 23 Biophys-Finalezenasnidj160Pas encore d'évaluation
- Thermochimie TDDocument26 pagesThermochimie TDAmady DiengPas encore d'évaluation
- ThermoDocument13 pagesThermoYoussef Ben omarPas encore d'évaluation
- Exercices Corriges Thermo PDFDocument34 pagesExercices Corriges Thermo PDFLoubna MentarPas encore d'évaluation
- Mathématiques - BEPC - Blanc Du Balai Citoyen 2Document2 pagesMathématiques - BEPC - Blanc Du Balai Citoyen 2azaraadama755Pas encore d'évaluation
- Devoir de GEGAlprnbDocument2 pagesDevoir de GEGAlprnbazaraadama755Pas encore d'évaluation
- Exercice de GEGADocument2 pagesExercice de GEGAazaraadama755Pas encore d'évaluation
- Lycée Privé de Formation Technique THERMODocument2 pagesLycée Privé de Formation Technique THERMOazaraadama755Pas encore d'évaluation
- DEVGEGADocument4 pagesDEVGEGAazaraadama755Pas encore d'évaluation
- Cours SVT 3èmeDocument100 pagesCours SVT 3èmeazaraadama755Pas encore d'évaluation
- Tenue de Route Bep Ii MvaDocument13 pagesTenue de Route Bep Ii Mvaazaraadama755Pas encore d'évaluation