Académique Documents
Professionnel Documents
Culture Documents
cours2-TCH-analyse Par Méthodes Physiques
Transféré par
Christian BTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
cours2-TCH-analyse Par Méthodes Physiques
Transféré par
Christian BDroits d'auteur :
Formats disponibles
MÉTHODES PHYSIQUES D’ANALYSE
Quelles techniques expérimentales utiliser pour déterminer la composition d’un système chimique sans le faire
réagir ?
1°) Analyse spectroscopique
1.1) Principe
L’analyse spectroscopique est une technique basée sur l’absorbance de certains rayonnements par la substance à
analyser. Un rayonnement incident, de longueur d’onde λ connue, traverse la substance étudiée puis le
rayonnement transmis est analysé.
On distingue la spectroscopie UV-Visible de la spectroscopie IR car ces deux techniques utilisent des
rayonnements de longueurs d’onde différentes et fournissent des informations différentes.
1.2) Spectroscopie UV-Visible (voir cours de première)
Les solutions colorées absorbent dans le domaine visible (400 nm < λ < 800 nm).
Les solutions incolores peuvent absorber des radiations dans le domaine ultra-violet (100 nm < λ < 400 nm).
Le graphe qui représente l’absorbance A en fonction de la longueur d’onde λ est appelé spectre d’absorption
« UV-Visible ».
La valeur de la longueur d’onde correspondant à l’absorbance maximale du spectre d’absorption, de même que
l’allure du spectre, peuvent permettre l’identification d’une espèce chimique.
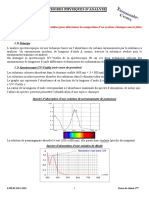
Spectre d’absorption d’une solution de permanganate de potassium
La solution de permanganate absorbe le vert (500 à 600 nm), elle paraît donc violette (proche du magenta).
Spectre d’absorption d’une solution de diiode
LFILM 2021-2022 1 Cours de chimie Tale
1.3) Spectroscopie infrarouge (voir cours de première)
La spectroscopie IR utilise des rayonnements de longueur d’onde comprise entre 2,5 µm et 25 µm (soit 4 000 à
400 cm−1). Quand une lumière IR traverse une molécule, chaque liaison covalente absorbe les longueurs d’ondes
particulières qui provoquent chez elle une vibration (élongation ou déformation) : on parle de bande d’absorption.
Sur le spectre IR, on analyse les bandes d’absorption pour identifier des liaisons et en déduire la présence de
groupes caractéristiques.
On mesure, pour chaque longueur d’onde, la transmittance T de l’entité étudiée.
On trace alors un graphique, avec :
1
En abscisse le nombre d’onde σ = avec λ en cm et σ en cm−1.
λ
En ordonnée la transmittance, T en %.
T en %
Empreinte
digitale
σ en cm-1
La largeur et la hauteur d’une bande d’absorption est caractéristique d’un type de liaison covalente.
Généralement, on ne considère que la partie gauche du spectre (1400 < σ < 4000 cm−1) car la partie de droite qui
constitue l’empreinte digitale est plus difficile à exploiter.
2°) Analyse par mesure d’absorbance (voir cours de première)
L’absorbance Aλ d’une solution dépend de la nature de la solution, de la longueur d’onde λ, de l’épaisseur de l
solution traversée par la lumière, de la température et de la concentration de la solution.
Pour une longueur d’onde λ fixée, si la solution est suffisamment diluée, l’absorbance A est proportionnelle à la
concentration C en espèce absorbante :
Loi de Beer-Lambert :
A : absorbance de la solution (sans unité)
ε : coefficient d’extinction molaire de l’espèce absorbante (L.mol−1.cm−1)
A = k×C avec k = ε×l
C : concentration en espèce absorbante (mol.L−1)
l : épaisseur de la cuve (cm)
Remarques : la proportionnalité entre l’absorbance d’une solution et sa concentration en soluté est valable :
• si l’absorbance reste inférieure à 2 ;
• si la solution est limpide ;
• si la solution est peu concentrée
LFILM 2021-2022 2 Cours de chimie Tale
3°) Analyse par mesure de conductance et de conductivité
3.1) Principe d’une cellule conductimétrique
Dans une solution électrolytique, la conductance du courant électrique est assurée par les ions. Les ions ne
contribuent pas tous de la même façon à la conductivité d’une solution.
La conductance G d'une portion de solution peut être mesurée grâce à une cellule de conductimétrie, constituée
de deux électrodes planes et parallèles, reliée à un système de mesure.
Le schéma de principe d’une cellule de conductimétrie est proposé ci-dessous.
La source de tension alternative de haute fréquence a pour rôle d'empêcher la polarisation des électrodes et les
phénomènes d'électrolyse.
3.2) Conductance d’une portion de solution
La conductance G de la portion de solution comprise entre les électrodes correspond au rapport du courant I sur
la tension U entre les électrodes.
U en volts (V)
1 I I en ampères (A)
G= =
R U R en ohms (Ω)
G en siemens (S)
3.3) Conductivité d’une solution
La conductance G de la solution dépend de la géométrie de la cellule (surface S et distance L) et de la nature de
la solution.
Pour une solution donnée, la conductance G d’une portion de solution est :
• proportionnelle à la surface S des plaques ;
• inversement proportionnelle à la distance L entre les plaques.
Pour une cellule de mesure donnée, la conductance G d’une portion de solution est :
•proportionnelle à la concentration C en soluté apporté de la solution ;
• dépend de la nature des ions en solution ;
• dépend de la température de la solution.
S surface des plaques (m2)
S L distance entre les plaques (m)
G =σ ×
L σ conductivité de la solution (S.m−1)
G conductance (S)
La conductivité σ de la solution dépend de sa composition, de sa concentration et de la température mais ne
dépend pas de la cellule de mesure.
S
On peut définir la constante de cellule de la façon suivante : kcellule = kcellule (m)
L
G
On peut alors exprimer la conductivité de la solution : σ = σ (S.m−1)
kcellule
LFILM 2021-2022 3 Cours de chimie Tale
Remarque : Les conductimètres du lycée ne mesurent pas la conductance G d’une portion de solution mais sa
conductivité σ puisque la constante de cellule est fixée par le constructeur.
3.4) Loi de Kohlrausch
Nous avons vu que la conductivité d’une solution dépend de la nature des ions en solution ainsi que de leur
concentration.
La capacité de chaque ion à conduire le courant est donnée par sa conductivité molaire ionique notée λ.
On donne, ci-dessous, quelques conductivités molaires ioniques théoriques à 25°C (C < 10−2 mol.L−1).
Cations Anions
Nom Symbole λ (S.m2.mol−1) Nom Symbole λ (S.m2.mol−1)
Oxonium H3O+ 349,8.10−4 Hydroxyde HO−aq 198,6.10−4
Potassium K+aq 73,5.10−4 Bromure Br−aq 78,1.10−4
Sodium Na+aq 50,1.10−4 Iodure I−aq 76,8.10−4
Ammonium NH4+aq 73,5.10−4 Chlorure Cl−aq 76,3.10−4
Lithium Li+aq 38,7.10−4 Fluorure F−aq 55,4.10−4
Argent Ag+aq 61,9.10−4 Éthanoate CH3COO−aq 40,9.10−4
La loi de Kohlrausch permet de calculer la conductivité d’une solution contenant les ions : X1(aq), X2(aq), …, Xn(aq).
σ =λ1 .[ X 1 ] + λ2 .[ X 2 ] + .... + λn .[ X n ]
n
σ =∑ λi .[ X i ] λi : conductivité molaire ionique de l’ion Xi (S.m2.mol−1)
i =1 [Xi] : concentration effective de l’ion Xi (mol.m−3)
Si la solution ionique est suffisamment diluée, (C < 10−2 mol.L−1) et ne contient qu’un seul soluté ionique, alors
la conductivité σ est proportionnelle à la concentration C en soluté apporté.
La loi de Kohlrausch correspond au domaine de linéarité de la courbe σ = f(C) :
σ =k.C avec k (S.L.m−1.mol−1)
4°) Analyse par mesure de pression
4.1) Modèle du gaz parfait
Le gaz parfait est un gaz idéal, un modèle, dans lequel les molécules sont supposées rigides et totalement
indépendantes des unes autres. Les seules interactions qu'elles peuvent subir lors de leur agitation sont les chocs
élastiques entre elles ou avec les parois du récipient contenant le gaz. Nous supposerons désormais dans le cours
de chimie que les gaz étudiés sont des gaz parfaits. Le gaz parfait est un modèle de gaz très simple. Il permet
comprendre les comportements des gaz réels.
4.2) Équation d’état du gaz parfait
Soit un échantillon de gaz parfait renfermant une quantité de matière n de gaz et occupant un volume V. En
notant P la pression dans ce gaz et T sa température absolue, l’équation d’état du gaz parfait s’écrit :
P×V = n×R×T
• P est la pression du gaz (Pa) Grandeur intensive (non additive)
• V est le volume de gaz (m3), Grandeur extensive (additive)
• n est la quantité de matière de gaz (mol) Grandeur extensive (additive)
• T est la température absolue du gaz (K) Grandeur intensive (non additive)
3 1 −1
• R est la constante des gaz parfaits : R = 8,32 Pa.m .mol .K
−
LFILM 2021-2022 4 Cours de chimie Tale
Conversions d’unités
• 1 bar = 105 Pa = 103 hPa
• T(K) = θ(°C) + 273,15
• 1 m3 = 1 000 L 1 dm3 = 1 L 1 cm3 = 1 mL
4.3) Volume molaire et quantité de matière
Dans les conditions normales de température et de pression, les C.N.T.P, (0°C, 1,013×105 Pa), le volume occupé
par une mole de gaz (volume molaire VM ) est 22,4 L : VM = 22,4 L.mol−1.
On peut ainsi calculer la quantité de matière ngaz renfermée dans un volume vgaz de gaz par la relation suivante :
vgaz
ngaz = vgaz (en L) VM (en L.mol−1)
VM
4.4) Complément historique: Comment a été établie cette équation d’état ?
a) Loi de Boyle-Mariotte (voir cours de première)
→ Lorsqu’un ballon sonde, rempli d'hélium, monte dans l'atmosphère, son volume augmente parce que la
pression extérieure diminue graduellement.
→ Inversement, quand on diminue le volume enfermé dans une pompe en enfonçant le piston, on augmente la
pression du gaz enfermé.
En 1662, le chimiste irlandais Robert Boyle a étudié le comportement des gaz.
En 1676, Edme Mariotte, un physicien français énonce la même loi que Boyle.
La loi de Boyle-Mariotte dit que le volume V d'une masse m donnée de gaz (ou une quantité de matière n
donnée) maintenu à température T constante est inversement proportionnel à sa pression :
1
V = k1× ⇔ P×V = k1 = cte avec m = cte (ou n = cte) et T = cte
P
Ainsi pour une masse de gaz donnée (pour une quantité de matière n donnée) dans des conditions de pressions
(P1 et P2) et de volumes (V1 et V2) différents, mais à température T = constante, on aura :
P1×V1 = P2×V2 avec m = cte (ou n = cte) et T = cte
b) Loi de Gay-Lussac-Charles
L'expérience montre que pour une masse m donnée de gaz (pour une quantité de matière n donnée) à pression P
constante, le volume augmente si la température augmente et le volume diminue si la température diminue.
Jacques Charles et Joseph Gay-Lussac, deux scientifiques français furent les premiers à étudier cette relation.
En 1787, Charles montre que pour une masse m donnée de gaz maintenu à pression P constante, le volume V du
gaz est directement proportionnel à sa température absolue T :
V
= k2 m = cte (ou n = cte) et P = cte
T
LFILM 2021-2022 5 Cours de chimie Tale
Pour une masse m de gaz donnée (pour une quantité de matière n donnée) dans des conditions de températures
(T1 et T2) et de volumes (V1 et V2) différents, mais à pression P constante, on aura :
V1 V
= 2 avec m = cte et P = cte
T1 T2
En 1807, Gay-Lussac indique que pour une masse m donnée de gaz maintenu à volume V constant, la pression
P du gaz est directement proportionnelle à sa température absolue T :
P
= k3 avec m = cte (ou n = cte) et V = cte
T
V P
Les deux expressions = k2 et = k3 correspondent à la même loi : la loi de Gay-Lussac-Charles.
T T
Remarque : Le rapport quantitatif entre les variations de volume et de température est remarquablement
constant : en extrapolant la droite obtenue pour une pression donnée jusqu'au volume zéro, celle-ci coupe l'axe
des températures à − 273,15 °C = 0 K.
En 1848, le physicien écossais, lord William Thomson Kelvin, comprit la signification de cette température
(le zéro absolu).
RELATION VOLUME-TEMPERATURE (ºC) D’UN GAZ
LFILM 2021-2022 6 Cours de chimie Tale
c) Loi d’Avogadro
Le travail du scientifique italien Amedeo Avogadro compléta les recherches de Boyle, de Charles et de Gay-
Lussac. En 1811, il propose l'hypothèse suivante :
« À la même température T et à la même pression P, des volumes égaux de gaz différents contiennent le même
nombre de molécules ».
Le volume V d'un gaz donné est donc proportionnel au nombre de molécules qu'il contient : V = k4×n
n = quantité de matière (nombre de moles) et k4 = constante de proportionnalité.
RELATION VOLUME-NOMBRE DE MOLES D’UN GAZ
d) L’équation d’état du gaz parfait
En combinant ces trois lois on obtient une seule équation générale : l’équation d’état du gaz parfait.
La loi de Boyle : P×V = k1 (T et n constants)
La loi de Gay-Lussac-Charles : V = k2×T (P et n constants)
ou P = k3×T (V et n constants)
La loi d'Avogadro : V = k4×n (P et T constants)
5°) Principe d’un dosage par étalonnage
Un dosage par étalonnage consiste à
déterminer la concentration d’une espèce en
solution par comparaison avec une gamme
de solutions de concentrations connues.
Pour réaliser la gamme de solutions étalons,
on procède généralement par dilution à
partir d’une solution mère, qui contient le
même soluté que la solution à analyser.
La concentration de l’espèce testée doit être
comprise dans l’intervalle des
concentrations utilisées pour l’étalonnage.
LFILM 2021-2022 7 Cours de chimie Tale
Vous aimerez peut-être aussi
- cours3-TPH-Déviation Dans EDocument33 pagescours3-TPH-Déviation Dans EChristian BPas encore d'évaluation
- cours2-TCH-analyse Par Méthodes PhysiquesDocument7 pagescours2-TCH-analyse Par Méthodes PhysiquesChristian BPas encore d'évaluation
- cours2-TPH-chute Libre ParaboliqueDocument14 pagescours2-TPH-chute Libre ParaboliqueChristian BPas encore d'évaluation
- Cours5 TCH Vitesse de Formation Et de DisparitionDocument6 pagesCours5 TCH Vitesse de Formation Et de DisparitionChristian BPas encore d'évaluation
- Cours1 TPH D Crire Un MouvementDocument8 pagesCours1 TPH D Crire Un MouvementChristian BPas encore d'évaluation
- Le TransformateurDocument7 pagesLe TransformateurTsade stevePas encore d'évaluation
- Exercice SDocument2 pagesExercice Sfeudjeularissa0% (1)
- Ex 14 STS1 MCCDocument82 pagesEx 14 STS1 MCCSi Mohamed Rahili78% (9)
- Chapitre 6 Flexion Simple - 2 PDFDocument7 pagesChapitre 6 Flexion Simple - 2 PDFRedouane AmigoPas encore d'évaluation
- Systèmes TriphasésDocument17 pagesSystèmes TriphasésAdil EL FARDAOUI100% (1)
- Klubprepa Extrait 4019Document0 pageKlubprepa Extrait 4019محمد الفاتحPas encore d'évaluation
- TD4 MQ1 2019-20Document25 pagesTD4 MQ1 2019-20Hasan Elmoumni100% (1)
- PumpflexDocument4 pagesPumpflexrpichoPas encore d'évaluation
- Introduction Générale Et Transfert Conductif: Table Des MatièresDocument8 pagesIntroduction Générale Et Transfert Conductif: Table Des MatièresjijiPas encore d'évaluation
- Oscillations Mécaniques ForcéesDocument4 pagesOscillations Mécaniques ForcéesBryce Ingram100% (1)
- DS1 - L1 Chimie S1 28 Octobre 2021 VFDocument1 pageDS1 - L1 Chimie S1 28 Octobre 2021 VFDang Hoang DungPas encore d'évaluation
- Série 2 (PR Mahdade Allal)Document6 pagesSérie 2 (PR Mahdade Allal)ayoubPas encore d'évaluation
- Examens Corrige Thermodynamique 2 Session Rattrapage SMP S3 2018 2019Document6 pagesExamens Corrige Thermodynamique 2 Session Rattrapage SMP S3 2018 2019bihi.102.haytamPas encore d'évaluation
- Garnier-Mallet Jean-Pierre - La Théorie Du DédoublementDocument34 pagesGarnier-Mallet Jean-Pierre - La Théorie Du Dédoublementeso06100% (1)
- Chapitre IIIDocument6 pagesChapitre IIISavana BellaPas encore d'évaluation
- Les Cellules Photovoltaiques PDFDocument5 pagesLes Cellules Photovoltaiques PDFkamel18100% (2)
- 20-21 TD3-Dynamique Des Fluides Parfaits PDFDocument4 pages20-21 TD3-Dynamique Des Fluides Parfaits PDFkhalil hari100% (1)
- TD 3-4 BiophDocument52 pagesTD 3-4 BiophAdonis Serghini100% (1)
- Cours Electricité Chap1 1BTS RIT+ELT 2021 22Document11 pagesCours Electricité Chap1 1BTS RIT+ELT 2021 22Moussa DossoPas encore d'évaluation
- ACFrOgBgargLnf0TSXIDTvB1o 9VBTXFnVNwZdgI4NCv2IfYlhOm967d2sSyWbje9E7lqwybmZxsE5s4 obWOwf11pRq4avUqFFYCKFWbn3gwOPHrAQyxT2-KR6PPvQHDM24Np8LYMM33lQHamQP PDFDocument1 pageACFrOgBgargLnf0TSXIDTvB1o 9VBTXFnVNwZdgI4NCv2IfYlhOm967d2sSyWbje9E7lqwybmZxsE5s4 obWOwf11pRq4avUqFFYCKFWbn3gwOPHrAQyxT2-KR6PPvQHDM24Np8LYMM33lQHamQP PDFkhalil stars1Pas encore d'évaluation
- Chapitre I - Mca - 2020 PDFDocument6 pagesChapitre I - Mca - 2020 PDFELMEHDI CHOUINEPas encore d'évaluation
- Chapitre DynamiqueDocument19 pagesChapitre Dynamiquecrbyounes123Pas encore d'évaluation
- 06 Resume Cours Statique GraphiqueDocument2 pages06 Resume Cours Statique GraphiqueYassine Lakhal100% (2)
- Pfe AmnDocument35 pagesPfe AmnImmamHadramy100% (2)
- TP 5 Essai de FlexionDocument6 pagesTP 5 Essai de FlexionJalel GhaliPas encore d'évaluation
- Contrôle 18 (PR Rachid Boumkehla)Document4 pagesContrôle 18 (PR Rachid Boumkehla)Mouhibi AbdellahPas encore d'évaluation
- Cours Eleves Chap5Document8 pagesCours Eleves Chap5Gohar ABRAHAMYANPas encore d'évaluation
- Projet RDM-Groupe 7Document12 pagesProjet RDM-Groupe 7COURS RDM 2017Pas encore d'évaluation
- Devoir Surveillé de Physique N°8: Les Calculatrices Sont InterditesDocument6 pagesDevoir Surveillé de Physique N°8: Les Calculatrices Sont InterditesSaliou SENEPas encore d'évaluation
- Comportementmécanique PDFDocument36 pagesComportementmécanique PDFabdallahPas encore d'évaluation
- Améliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesD'EverandAméliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesÉvaluation : 5 sur 5 étoiles5/5 (2)
- Harmonisation Energétique des Personnes: Manuel de Curothérapie 2020D'EverandHarmonisation Energétique des Personnes: Manuel de Curothérapie 2020Évaluation : 4 sur 5 étoiles4/5 (8)
- Manuel pour les débutants Fabriquez des savons naturelsD'EverandManuel pour les débutants Fabriquez des savons naturelsÉvaluation : 3 sur 5 étoiles3/5 (2)
- Secrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieD'EverandSecrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieÉvaluation : 5 sur 5 étoiles5/5 (2)
- Électrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsD'EverandÉlectrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Affirmations positives : Perte de poids pour les femmesD'EverandAffirmations positives : Perte de poids pour les femmesPas encore d'évaluation
- Géobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainD'EverandGéobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- L'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)D'EverandL'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)Évaluation : 4 sur 5 étoiles4/5 (3032)
- Le B.A.-Ba de la communication: Comment convaincre, informer, séduire ?D'EverandLe B.A.-Ba de la communication: Comment convaincre, informer, séduire ?Évaluation : 3 sur 5 étoiles3/5 (1)
- Technologie automobile: Les Grands Articles d'UniversalisD'EverandTechnologie automobile: Les Grands Articles d'UniversalisPas encore d'évaluation
- Anatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursD'EverandAnatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursPas encore d'évaluation
- Harmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020D'EverandHarmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020Évaluation : 2.5 sur 5 étoiles2.5/5 (3)
- Le profilage au service du football: Démarche scientifique pour un recrutement et entraînements optimisésD'EverandLe profilage au service du football: Démarche scientifique pour un recrutement et entraînements optimisésPas encore d'évaluation