Académique Documents
Professionnel Documents
Culture Documents
CP Mareme Baba: 1 L2 2023/2024 M Thiam Devoir de Sciences Physiques N°1: 1h 45' Exercice1
Transféré par
nabou190494Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
CP Mareme Baba: 1 L2 2023/2024 M Thiam Devoir de Sciences Physiques N°1: 1h 45' Exercice1
Transféré par
nabou190494Droits d'auteur :
Formats disponibles
CP MAREME BABA : 1ére L2 2023/2024
M THIAM
DEVOIR DE SCIENCES PHYSIQUES N°1 : 1h 45’
EXERCICE1
1) Définir la chimie organique
2) Définir un hydrocarbure et donner deux exemples.
3) Un hydrocarbure CxHy renferme en masse 82,76 % de carbone. Sa masse molaire
moléculaire est égale à 58 g/mol.
a) calculer sa formule brute
b) donner une formule développée possible
EXERCICE 2
Le paracétamol de formule brute C8H9O2N est un médicament de synthèse.
1. Déterminer la masse molaire moléculaire du paracétamol.
2. Déterminer la composition centésimale massique de chaque élément.
Données : masse molaire atomiques en g/mol : H=1; O=16 ; C=12 ; N=14 ; S=32 ;
Na=23 ; Mg=24.
Exercice4 :
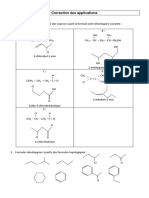
1) Nommer les composés ci-dessous : C2H5 CH3
a) CH3CHCHCH3
b) CH3CCH2CH2CHCH3 c) (CH3)3CCH2I
CH3 CH3
CH2CH2CH3
f) CH2CH CH2CH2CH3
d) CH2 CCl CH2CH2Br e) CH2CHCH2CH2CH3
C2H5 C2H5 CH3 CH3 CH2
2) Ecrire les formules semi-développées des alcanes dont les noms suivent :
a) 2-méthylbutane b) 2,3,6-triméthyloctane c) 2,4-diméthylpentane d) 3-éthyl-2,3-diméthyloctane
e) 3,4-diéthylhexane f) 2,3,4-triméthylhexane g) 1-éthyl-2-méthylcyclohexane
3) Ecrire les formules semi-développées des alcanes dont les noms suivent :
a) méthylpropane b) 3-éthyl-4-propyloctane c) 3,4,4-tripropylpentane d) 3-éthyl-2-isopropylbutane
Vous aimerez peut-être aussi
- AlcanesDocument2 pagesAlcanesmed-salem9Pas encore d'évaluation
- ANNALE PC EXO de 1SDocument55 pagesANNALE PC EXO de 1Skountiyou92% (13)
- Serie4 3 20Document1 pageSerie4 3 20Math PilotePas encore d'évaluation
- TD N°01 L01 - CHIMIE Tle GT, F3, F5, MVPL, MVTDocument2 pagesTD N°01 L01 - CHIMIE Tle GT, F3, F5, MVPL, MVTsouffotalonfookorogalvaniPas encore d'évaluation
- 1S ChimieDocument10 pages1S ChimiePFE100% (4)
- C2-1S AlcanesDocument2 pagesC2-1S AlcanesSerigne Abdou NiassePas encore d'évaluation
- Fascicule - Travaux Diriges de Chimie. Première C & D CamerounDocument10 pagesFascicule - Travaux Diriges de Chimie. Première C & D CamerounDavid Tagong100% (3)
- SEQ 2 CHIMIE THEORIQUE Tle CDDocument3 pagesSEQ 2 CHIMIE THEORIQUE Tle CDUlriche Enama EbandaPas encore d'évaluation
- TD AminesDocument1 pageTD AminesKenfack BryndaPas encore d'évaluation
- Exos Chimie Cours PRIAMSDocument60 pagesExos Chimie Cours PRIAMSLevier Poids86% (7)
- td1 corrDocument6 pagestd1 correlmaliky.ibtissamPas encore d'évaluation
- Chimie Organique Exercices Corr 01 - CompressedDocument11 pagesChimie Organique Exercices Corr 01 - CompressedAdilsonPas encore d'évaluation
- Exercices Organique Corrige Web PDFDocument11 pagesExercices Organique Corrige Web PDFYASSINPas encore d'évaluation
- Serie Sur Les SavonsDocument2 pagesSerie Sur Les Savonskhadidiatou baldePas encore d'évaluation
- Chapitre 01 - Chimie 1DDocument2 pagesChapitre 01 - Chimie 1DAmed SoumahoroPas encore d'évaluation
- Alcénes - Alcynes 1S1-1S2 AT 22 Renf FinDocument6 pagesAlcénes - Alcynes 1S1-1S2 AT 22 Renf Finpapaaliouba3Pas encore d'évaluation
- CHIMIE6CDocument5 pagesCHIMIE6CPc-med NouhPas encore d'évaluation
- Série N 1 Module de Chimie Organique SMP3Document2 pagesSérie N 1 Module de Chimie Organique SMP3chentouf fatima-zahraePas encore d'évaluation
- 1 Nomenclature Organique ExercicesDocument26 pages1 Nomenclature Organique ExercicesDjassouPas encore d'évaluation
- premiere-D-chimieDocument2 pagespremiere-D-chimieb60032595Pas encore d'évaluation
- M.ndoye Alcanes Renf 2023-2024Document2 pagesM.ndoye Alcanes Renf 2023-2024fatouthioune664Pas encore d'évaluation
- PC & D Fiche Du 23 Fevrier 2019Document2 pagesPC & D Fiche Du 23 Fevrier 2019LeNantais Sonderangebote100% (1)
- Chimie (SES)Document1 pageChimie (SES)Christopher SinvilPas encore d'évaluation
- Licence 2 (Parcours Physique-Chimie) Année 2016-2017 TD2: Alcanes, Alcènes Et Alcynes Exercice 1Document3 pagesLicence 2 (Parcours Physique-Chimie) Année 2016-2017 TD2: Alcanes, Alcènes Et Alcynes Exercice 1Najimou Alade TidjaniPas encore d'évaluation
- CAHIER D'Exercices ChimieDocument67 pagesCAHIER D'Exercices ChimieAdama MaigaPas encore d'évaluation
- Alcanes 2019Document2 pagesAlcanes 2019mouhamadousylla053Pas encore d'évaluation
- Corrige Serie 10 Examen s6 2012Document7 pagesCorrige Serie 10 Examen s6 2012Jamal LachgrePas encore d'évaluation
- TD-nomenclature CorrectionDocument2 pagesTD-nomenclature Correctionmm72c48gbgPas encore d'évaluation
- A E R M O S PharmacieDocument4 pagesA E R M O S PharmacieIssouf BerthePas encore d'évaluation
- Toute La Chimie en Tle S de c1 A c9 PDFDocument65 pagesToute La Chimie en Tle S de c1 A c9 PDFPatrice NyaPas encore d'évaluation
- Annale ChimieDocument53 pagesAnnale ChimiehamidouPas encore d'évaluation
- È Re Ere: Titiane A Placé Dans Un Eudiomètre 5cmDocument1 pageÈ Re Ere: Titiane A Placé Dans Un Eudiomètre 5cmAnita KounchouPas encore d'évaluation
- 1 Nomenclature Organique ExercicesDocument25 pages1 Nomenclature Organique Exerciceskabli ilyassPas encore d'évaluation
- Chimie Organique Exercices Corrigés 6Document25 pagesChimie Organique Exercices Corrigés 6Hossam Bendali100% (8)
- TD de Chimie Tle C&DDocument21 pagesTD de Chimie Tle C&DHaman Bello OumarouPas encore d'évaluation
- Ex OrganiqueDocument17 pagesEx OrganiqueYahya ElamraniPas encore d'évaluation
- Chimie Organique Série 01: Alcanes Et Cyclanes: Exercice 1Document36 pagesChimie Organique Série 01: Alcanes Et Cyclanes: Exercice 1brandonPas encore d'évaluation
- Examen Janvier 2018 Variante 2 PDFDocument10 pagesExamen Janvier 2018 Variante 2 PDFazzamPas encore d'évaluation
- Ero Ex c02Document3 pagesEro Ex c02maino100% (1)
- Exam Et Corrigé TP SMC3 17-18Document10 pagesExam Et Corrigé TP SMC3 17-18Hamza FaFouriPas encore d'évaluation
- 01 Chimie OrganiqueDocument9 pages01 Chimie OrganiqueHocine MichelPas encore d'évaluation
- Alcool Et Amine 2013 1Document8 pagesAlcool Et Amine 2013 1Armaalik PelitoPas encore d'évaluation
- TD CH 2 EspoirDocument6 pagesTD CH 2 EspoirRodrigue TchoffoPas encore d'évaluation
- PC 1ère CD-C3 Hydrocarbures InsaturésDocument12 pagesPC 1ère CD-C3 Hydrocarbures InsaturésJoconias Mongnonhoda100% (1)
- 1S - Wahab Diop-TD - Alcane - 2011lsll - NoRestriction PDFDocument2 pages1S - Wahab Diop-TD - Alcane - 2011lsll - NoRestriction PDFtarik100% (1)
- Les Hydrocarbures - ExercicesDocument3 pagesLes Hydrocarbures - ExercicesMohamed Ibn alfaridhPas encore d'évaluation
- T Science DevoirdDocument2 pagesT Science DevoirdOumar TraoréPas encore d'évaluation
- 1ered 2021Document2 pages1ered 2021Sadat Cisse100% (1)
- TSE ChimieDocument2 pagesTSE ChimieOumar TraoréPas encore d'évaluation
- Alcanes LMST 1ère S 2023-2024Document2 pagesAlcanes LMST 1ère S 2023-2024fatouthioune664Pas encore d'évaluation
- TD CH - Org.Serie N°1 - 2021 - 22Document2 pagesTD CH - Org.Serie N°1 - 2021 - 22mohamedaminedarrajPas encore d'évaluation
- Examen SV1s2 CO (21) Session1 2Document1 pageExamen SV1s2 CO (21) Session1 2Telia EbaderePas encore d'évaluation
- Chimie Organique TD1Document7 pagesChimie Organique TD1Mira MaroPas encore d'évaluation
- CHIMI DS 2Document3 pagesCHIMI DS 2williammerlindonfackPas encore d'évaluation
- 1 Terminale D ChimieDocument3 pages1 Terminale D ChimieJoel AsuraPas encore d'évaluation