Académique Documents
Professionnel Documents
Culture Documents
TD Amines
Transféré par
Kenfack Brynda0 évaluation0% ont trouvé ce document utile (0 vote)
216 vues1 pageTX classes de Terminal D
Titre original
TD AMINES
Copyright
© © All Rights Reserved
Formats disponibles
DOCX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentTX classes de Terminal D
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
216 vues1 pageTD Amines
Transféré par
Kenfack BryndaTX classes de Terminal D
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 1
COLLEGE DU LEVANT DE NGODI-BAKOKO
TRAVAUX DIRIGES Tle CD
CHIMIE THEORIQUE
THÈME : LES AMINES
-1 -1 -1
On donne : M (C) = 12 g.mol ; M(H) = 1 g.mol ; M (N) = 14 g.mol
Exercice 1
1- Nommer les composés suivants :
b) CH3 — CH-CH(CH3)NH2
a) CH3 — CH2 — CH(C2H5)— NH2 C2H5
c) C2H5 — CH2-NH — CH2 -CH2-C2H5 d) CH3 —N+(C2H5)2-CH3
f) CH3 —N-CH2 — CH2 — CH2 CH2 — CH3
C6H5
e) CH3— CH2 — NH —CH2 — CH3
g) CH(CH3)2 — CH2N(CH3)C2H5 h) CH3-(CH2)3-C(CH3)2- CH2N(C6H5)2
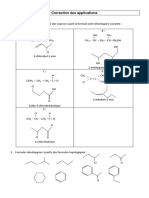
2- Écrire les formules semi-développées des composés suivants :
a) 3-méthyl pentan-2-amine f) N-éthyl-N-méthylpropan-2-amine
b) ion N-isopropyl 2-méthyl pentan-2-ammonium g) iodure de tétraméthylammonium c) N,N-
diméthylaniline
d) N-phénylaniline
e) N,N-diphényl 2-méthylhexan-2-amine
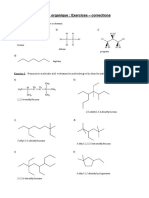
Exercice 2
1) En combien de classes les amines peuvent-elles être réparties ? Donner un exemple de chaque classe en précisant
le nom du corps.
Etablir la formule brute générale des amines, identique pour toutes les classes
2) Une solution aqueuse de l'amine A, de concentration molaire C = 0,2 mol.L -1, a été obtenue en dissolvant 20,4 g
d'amine pour 1 L de solution.
En déduire sa masse molaire, sa formule brute, et sa formule semi-développée sachant que A
renferme un noyau benzénique et sa classe est secondaire. Quel est son nom ? Exercice 3
On considère une amine primaire à chaîne carbonée saturée possédant n atomes de carbone.
1) Exprimer en fonction de n le pourcentage en masse d'azote qu'elle contient.
2) Une masse m = 15 g d'une telle amine contient 2,9 g d’azote.
2.a- Déterminer la formule brute de l’amine.
2.b- Ecrire les formules développées des isomères possibles des monoamines primaires compatibles avec
la formule brute trouvée.
3) On considère la monoamine à chaîne carbonée linéaire non ramifiée.
3.a- Ecrire l’équation de la réaction de cette monoamine primaire avec l’eau.
3.b- On verse quelques gouttes de phénolphtaléine dans un échantillon de la solution préparée.
Quelle est la coloration prise par la solution ?
(On rappelle que la phénolphtaléine est incolore en milieu acide et rose violacée en milieu basique)
Exercice 4
On considère une amine aromatique A de formule générale CxHyN ne comportant qu'un seul cycle.
1) Exprimer x et y en fonction du nombre n d'atomes de carbone qui ne font pas partie du cycle.
2) La microanalyse d'une telle amine fournit, pour l’azote, un pourcentage en masse de 13,08 %.
2.a- Déterminer n.
2.b- Ecrire les formules développées des différents isomères et donner leurs noms.
3) Identifier A sachant que l’amine A est de classe secondaire
4) Ecrire l’équation de la réaction de cette amine A avec l’eau
diagnensis@yahoo.f
r
Vous aimerez peut-être aussi
- ANNALE PC EXO de 1SDocument55 pagesANNALE PC EXO de 1Skountiyou92% (13)
- Nomenclature Des Carbocycles Et Des Hetero CyclesDocument5 pagesNomenclature Des Carbocycles Et Des Hetero CyclesJean-François Abena100% (3)
- Dosage Indirect Eau de JavelDocument6 pagesDosage Indirect Eau de JavelJean Leonardo100% (2)
- Exos Chimie Cours PRIAMSDocument60 pagesExos Chimie Cours PRIAMSLevier Poids86% (7)
- Annale ChimieDocument53 pagesAnnale ChimiehamidouPas encore d'évaluation
- Orga - 23 SN1 ET SN2Document7 pagesOrga - 23 SN1 ET SN2زيد بخليفةPas encore d'évaluation
- 11 Ester CorrectionDocument7 pages11 Ester CorrectionChartier Julien100% (2)
- Exam-Corrige Chimie PDFDocument4 pagesExam-Corrige Chimie PDFNassimaPas encore d'évaluation
- Alcool Et Amine 2013 1Document8 pagesAlcool Et Amine 2013 1Armaalik PelitoPas encore d'évaluation
- Amine Ter S SarayaDocument4 pagesAmine Ter S SarayaalphadzoPas encore d'évaluation
- TleD - CH - L3 - Les AminesDocument8 pagesTleD - CH - L3 - Les AminesBertrand FamaPas encore d'évaluation
- Alcool Amine Acide CarboxDocument5 pagesAlcool Amine Acide CarboxEssohanam AwatePas encore d'évaluation
- Toute La Chimie en Tle S de c1 A c9 PDFDocument65 pagesToute La Chimie en Tle S de c1 A c9 PDFPatrice NyaPas encore d'évaluation
- Serie4 3 20Document1 pageSerie4 3 20Math PilotePas encore d'évaluation
- Série D'exercices N°16 - Chimie Les Amides - Bac Sciences Exp (2013-2014) MR BARHOUMI EzedineDocument4 pagesSérie D'exercices N°16 - Chimie Les Amides - Bac Sciences Exp (2013-2014) MR BARHOUMI EzedineAfef Afef100% (4)
- Acide CarboxiliqueDocument3 pagesAcide CarboxiliquePFE100% (3)
- Serie c2 ts1 Ltye 2018 2019Document1 pageSerie c2 ts1 Ltye 2018 2019Joséphine NancassePas encore d'évaluation
- TD C5: Composes Organiques OxygenesDocument2 pagesTD C5: Composes Organiques Oxygenesbabacar mbayePas encore d'évaluation
- TD Amines Acides 2023 LSLL WahabdiopDocument4 pagesTD Amines Acides 2023 LSLL WahabdiopMouhamad Ibn Amine SegnanePas encore d'évaluation
- C3 Acides Carboxyliques Et DérivésDocument4 pagesC3 Acides Carboxyliques Et DérivésFerdinand MbayePas encore d'évaluation
- SEQ 2 CHIMIE THEORIQUE Tle CDDocument3 pagesSEQ 2 CHIMIE THEORIQUE Tle CDUlriche Enama EbandaPas encore d'évaluation
- TD AMINES 2024-Sabs - WahabdiopDocument3 pagesTD AMINES 2024-Sabs - Wahabdiopbibos8318Pas encore d'évaluation
- ExaaaaaaaaaDocument3 pagesExaaaaaaaaamyriam zemniPas encore d'évaluation
- Exam Et Corrigé TP SMC3 17-18Document10 pagesExam Et Corrigé TP SMC3 17-18Hamza FaFouriPas encore d'évaluation
- LES AMIDES MagazinesDocument3 pagesLES AMIDES Magazinesrania50% (2)
- Seriie #9 Les Amides Aliphatiques Derives D Acides CarboxyliquesDocument2 pagesSeriie #9 Les Amides Aliphatiques Derives D Acides CarboxyliquesMahmoud Essahbi Sahbi DaghsniPas encore d'évaluation
- 01 Chimie OrganiqueDocument9 pages01 Chimie OrganiqueHocine MichelPas encore d'évaluation
- CP Mareme Baba: 1 L2 2023/2024 M Thiam Devoir de Sciences Physiques N°1: 1h 45' Exercice1Document1 pageCP Mareme Baba: 1 L2 2023/2024 M Thiam Devoir de Sciences Physiques N°1: 1h 45' Exercice1nabou190494Pas encore d'évaluation
- Exercices AmidesDocument4 pagesExercices AmidesAmine NouarPas encore d'évaluation
- CHIMIE6CDocument5 pagesCHIMIE6CPc-med NouhPas encore d'évaluation
- Série Amine AT 23 TS2Document2 pagesSérie Amine AT 23 TS2y7mdwxk9x6Pas encore d'évaluation
- Fasicule Chimie TS1 - 220724 - 133207Document46 pagesFasicule Chimie TS1 - 220724 - 133207Paul andre FayePas encore d'évaluation
- TD ALCOOLSDocument3 pagesTD ALCOOLSnutsugadjifaPas encore d'évaluation
- Amines - Acides CarboxyliquesDocument2 pagesAmines - Acides Carboxyliquesdiengsalla diengPas encore d'évaluation
- 1S ChimieDocument10 pages1S ChimiePFE100% (4)
- AlcanesDocument2 pagesAlcanesmed-salem9Pas encore d'évaluation
- Serie Amide 19 20Document4 pagesSerie Amide 19 20hlimaPas encore d'évaluation
- Serie C4-benzene-WahabDiopDocument2 pagesSerie C4-benzene-WahabDiophamd kabore100% (2)
- TD N°01 L01 - CHIMIE Tle GT, F3, F5, MVPL, MVTDocument2 pagesTD N°01 L01 - CHIMIE Tle GT, F3, F5, MVPL, MVTsouffotalonfookorogalvaniPas encore d'évaluation
- TD CH 2 EspoirDocument6 pagesTD CH 2 EspoirRodrigue TchoffoPas encore d'évaluation
- Série D'exercices Sur Les Acides Carboxyliques Et Dérivés - Ts - SunudaaraDocument5 pagesSérie D'exercices Sur Les Acides Carboxyliques Et Dérivés - Ts - SunudaaraJule BaPas encore d'évaluation
- Chapitre C2 Amines_080203Document2 pagesChapitre C2 Amines_080203k77865467Pas encore d'évaluation
- 1cm432qpm 757086Document4 pages1cm432qpm 757086Nana DiakitéPas encore d'évaluation
- CHM317 - 202020 - Examen Final - SPCDocument7 pagesCHM317 - 202020 - Examen Final - SPCChris YPas encore d'évaluation
- TD CH - Org.Serie N°1 - 2021 - 22Document2 pagesTD CH - Org.Serie N°1 - 2021 - 22mohamedaminedarrajPas encore d'évaluation
- Série D'exercice 3S ALcools 2018Document3 pagesSérie D'exercice 3S ALcools 2018Ghada Daddou100% (4)
- 3 Séquence Lycée Bilingue de Mbalngong Tle C DR ANGODocument2 pages3 Séquence Lycée Bilingue de Mbalngong Tle C DR ANGOpublicité en flopOfficielPas encore d'évaluation
- Chimie TleC D TI Eval2Document11 pagesChimie TleC D TI Eval2bryanprince673Pas encore d'évaluation
- L1S1 Serie N°2Document3 pagesL1S1 Serie N°2emilie1946Pas encore d'évaluation
- ExtraitDocument8 pagesExtraitLewis HamiltonPas encore d'évaluation
- Chimie TCD N4Document2 pagesChimie TCD N4Häm's Ham'sPas encore d'évaluation
- Serie #7 Les Amides Aliphatiques Derives D Acides Carboxyliques Le Complet ResoluDocument3 pagesSerie #7 Les Amides Aliphatiques Derives D Acides Carboxyliques Le Complet ResoluMahmoud Essahbi Sahbi DaghsniPas encore d'évaluation
- CAHIER D'Exercices ChimieDocument67 pagesCAHIER D'Exercices ChimieAdama MaigaPas encore d'évaluation
- Epreuve de Chimie Tle C Lycee de MoukoDocument3 pagesEpreuve de Chimie Tle C Lycee de Moukocoulibaly emmanuelPas encore d'évaluation
- Bac CH 1999Document3 pagesBac CH 1999Haman Bello OumarouPas encore d'évaluation
- Série D'exercices - Chimie Les Amides Aliphatiques - Bac Sciences Exp (2012-2013) MR Trayia Nabil PDFDocument1 pageSérie D'exercices - Chimie Les Amides Aliphatiques - Bac Sciences Exp (2012-2013) MR Trayia Nabil PDFakrem300100% (1)
- M.ndoye Alcanes Renf 2023-2024Document2 pagesM.ndoye Alcanes Renf 2023-2024fatouthioune664Pas encore d'évaluation
- Exercices Organique Corrige Web PDFDocument11 pagesExercices Organique Corrige Web PDFYASSINPas encore d'évaluation
- Alc 2Document7 pagesAlc 2ymokdad773Pas encore d'évaluation
- Biochimie - PCEP1 (Lyon) - ED - Lipides Et Acides Aminés (Couleur) (2009)Document44 pagesBiochimie - PCEP1 (Lyon) - ED - Lipides Et Acides Aminés (Couleur) (2009)Hussein Termoss100% (1)
- AminesDocument2 pagesAminesHaykelGaouaPas encore d'évaluation
- Fer Et Acide Chlorhydrique Durandeau Correction309Document7 pagesFer Et Acide Chlorhydrique Durandeau Correction309anatolebakekolPas encore d'évaluation
- KHI741Document2 pagesKHI741Adel KridPas encore d'évaluation
- TP Cinétique Chimique reaction-1-ORDRE-1Document10 pagesTP Cinétique Chimique reaction-1-ORDRE-1kiritosunny30Pas encore d'évaluation
- Dosage Acide BaseDocument10 pagesDosage Acide BaseRajhiHoussemPas encore d'évaluation
- TP6 Analyses Des AnionsDocument11 pagesTP6 Analyses Des AnionsMimi Mimi100% (2)
- Villemin Gerard Free FRDocument4 pagesVillemin Gerard Free FRYoussef EttaajPas encore d'évaluation
- 2023 Reunion J1 Exo1 Sujet EauPoules 9ptsDocument3 pages2023 Reunion J1 Exo1 Sujet EauPoules 9ptsAsabothPas encore d'évaluation
- L2CI-02 Alcanes NomenclatureDocument32 pagesL2CI-02 Alcanes Nomenclatureamigos1989Pas encore d'évaluation
- La ManganimétrieDocument19 pagesLa ManganimétrieBsissaSoltaniPas encore d'évaluation
- MAX SAT: Test ConseilléDocument2 pagesMAX SAT: Test ConseilléMAPas encore d'évaluation
- Corre-Exo-Ch1 3Document28 pagesCorre-Exo-Ch1 3Jihen Ben SlimaPas encore d'évaluation
- Chapitre II Nomenclature Alcane Alcéne AlcyneDocument17 pagesChapitre II Nomenclature Alcane Alcéne AlcyneNawal ZakriPas encore d'évaluation
- Exercices P 128Document2 pagesExercices P 128Lauren StecyPas encore d'évaluation
- Corrigé 3Document5 pagesCorrigé 3Khalid ZegPas encore d'évaluation
- Chimie, Question D Cours 1Document5 pagesChimie, Question D Cours 1leyygee456Pas encore d'évaluation
- TD 1 CorrectionDocument13 pagesTD 1 CorrectionBernardine ViouPas encore d'évaluation
- Diaporama Biologie JBD 2020Document270 pagesDiaporama Biologie JBD 2020reemalfhad59Pas encore d'évaluation
- VSEPRDocument4 pagesVSEPRAmdjed Bahaa100% (1)
- TP Biochimie ExamDocument3 pagesTP Biochimie ExamLina BENMILOUDPas encore d'évaluation
- Controle 2 - 18 S1 3AC InterDocument2 pagesControle 2 - 18 S1 3AC InterAssia AchhabePas encore d'évaluation
- Chimie - UAA7 - Test Chapitre 3 v2-3Document3 pagesChimie - UAA7 - Test Chapitre 3 v2-3Véronique ThirotPas encore d'évaluation
- Chapitre 3 Solubilité CoursDocument6 pagesChapitre 3 Solubilité CoursAlex LakhPas encore d'évaluation
- Leçon 15Document15 pagesLeçon 15mpeveyalongoPas encore d'évaluation
- French ProcessDocument2 pagesFrench ProcessElmokded kacemPas encore d'évaluation
- Chapitre-5-Les Transformations Liées Par Des Réactions Acido-Basique - DosageDocument13 pagesChapitre-5-Les Transformations Liées Par Des Réactions Acido-Basique - Dosagea houssPas encore d'évaluation
- 4eme Séance Les Glucides Structre Et Propriétés 2020-2021 - Copie - CopieDocument14 pages4eme Séance Les Glucides Structre Et Propriétés 2020-2021 - Copie - Copiewassi laPas encore d'évaluation