Académique Documents
Professionnel Documents
Culture Documents
Devoir 4
Transféré par
Féz EyTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Devoir 4
Transféré par
Féz EyDroits d'auteur :
Formats disponibles
Niveau : 2BAC science Année scolaire …….
/……
Physique et chimie Durée :2 Heures
La présentation, le soin et la rédaction seront pris en compte pour un point dans la notation.
Justifier en expliquant votre démarche si cela est nécessaire.
Tout calcul doit être précédé de la formule utilisée.
La valeur numérique prise par une grandeur physique est toujours suivie d’une unité.
Respecter la notation des grandeurs utilisées dans l’énoncé.
EXERCICE 1 (7pts)
On étudie l’évolution au cours du temps de la
réaction d’oxydation des ions iodure I-(aq) par le
peroxyde d’hydrogène H2O2 (eau oxygénée) en
milieu acide. L’équation chimique qui symbolise
la réaction associée à la transformation chimique
étudiée est : H2O2 + 2I- + 2H+→ 2H2O + I2
À la date t=0, on mélange un volume V1=100mL
d’une solution (S1) d’eau oxygénée de
concentration molaire C1 avec un volume
V2=100mL d’une solution (S2) d’iodure de
potassium (KI) de concentration molaire C2 et
quelques gouttes d’acide sulfurique concentré.
Le suivi temporel de cette transformation
chimique a permis de tracer, sur le graphe ci-
dessous,
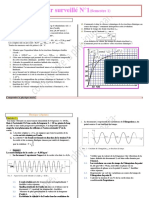
les courbes représentant les variations de la
molarité des ions iodure I- et celle des molécules
de diiode I2 en fonction du temps
1- Associer, en le justifiant, chacune des courbes (a) et (b) à la grandeur qu’elle représente.
2- L’ion iodure I-(aq) est-il le réactif limitant ? Justifier la réponse.
3- En exploitant le graphe, trouver la concentration initiale [I-(aq)]0 et finale [I-]f des ions iodures dans le
mélange.
4- Calculer la concentration initiale [H2O2 (aq)]0 de l’eau oxygénée dans le mélange.
5- Déterminer graphiquement la valeur de vitesse volumique à l’instant t =10 min.
6- Comment varie la vitesse de la réaction au cours du temps ? Interpréter cette variation.
7- Quelle est la valeur du temps de demi-réaction t1/2 ?
8- Dire, en le justifiant, comment varie t1/2 si :
8-1- On abaisse la température du milieu réactionnel ?
8-1- L’évolution s’effectuait dans un grand volume d’eau.
1-On réalise une expérience en utilisant un laser,
une fente de largeur réglable et un écran blanc. Le
dispositif est représenté ci-contre : Les mesures de
la largeur de la fente a, de la distance de la fente à
l'écran D et de la largeur de la zone lumineuse
centrale l conduisent aux résultats suivants :
a=0,200mm ; D=2,00m; L=12,6mm
1. Quel est le nom du phénomène observé?
2. L'angle étant petit et exprimé en radian, on
peut utiliser l'approximation tan =(rad). Calculer
l'angle en radian.
3. Quelle est la relation liant l'angle , la longueur d'onde de la lumière et la largeur a de la fente ?
4. Calculer la longueur d'onde .
5. Quelle est la relation entre , c (célérité de la lumière dans le vide) et (fréquence de la radiation
lumineuse)? Indiquer leurs unités dans le système international.
6. Exprimer la relation entre l et .
7. Quelles sont approximativement les longueurs d'onde dans le vide des radiations bleues et rouges?
8. Indiquer comment varie la largeur l lorsqu'on :
- remplace le laser émettant une lumière rouge par un laser émettant une
lumière bleue?
- diminue la largeur de la fente a?
9- On envoie sur un prisme de verre un rayon de lumière blanche, celui-ci
traverse le dioptre air-verre sans être réfracté mais il sera réfracté sur le
dioptre verre-air.
On considère la radiation rouge et la radiation bleue contenues dans ce
rayon de lumière blanche. On connaît les indices de réfraction du verre pour
ces deux radiations : n(Rouge) = 1,5 ; n(bleue) = 1,6.
9.1. Pourquoi le rayon ne se réfracte pas lors de son passage au niveau du
dioptre air-verre ?
9.2. Construisez, sur la figure jointe, les rayons rouge et bleu à la sortie du prisme. Vous justifierez vos
constructions par les calculs adéquats.
9.3. Calculer l’angle que fait le rayon bleu avec le rayon rouge à la sortie du prisme
EXERCICE 3 (6pts)
Au cours d'une séance de travaux pratiques, un élève réalise le montage de la figure 1. Il dispose du matériel
suivant:
- un émetteur d'ultrasons E et son alimentation électrique, sa plage d'émission est [20 kHz ; 60 kHz].
-deux récepteurs d'ultrasons R1 et R2;
- un système d'acquisition relie a un ordinateur muni d'un logiciel de traitement de données;
- une règle graduée.
L'émetteur E génère une onde ultrasonore progressive sinusoïdale qui se propage dans l'air jusqu'aux récepteurs
R1 et R2. L'émetteur et les deux récepteurs sont alignes. Le récepteur R1 est place au zéro de la règle graduée.
Les signaux captes par les récepteurs R1 et R2 sont visualises en même temps grâce a un logiciel de traitement de
données. Lorsque le récepteur R2 est situe a d=2,8cm du récepteur R1, les signaux reçus par les deux récepteurs
sont en phase (Fig. 2).
1- Indiquer quelle courbe représente le signal reçu par R2. (justifier)
2- Déterminer grâce a l'enregistrement la période T des ultrasons émis.
3- Exprimer la fréquence des ultrasons et la calculer. La valeur obtenue est-elle cohérente ?
4- On éloigne lentement R2 le long de la règle (Fig. 3) : on constate que le signal reçu par R2 se décalé vers la
droite. On continue à éloigner R2 jusqu'a ce que les signaux reçus par R1 et R2 soient a nouveau en phase. Soit R'2
la nouvelle position occupée par R2. La distance d' séparant désormais R1 de R'2 est d' = 4,2 cm.
4-1- Définir en une phrase la longueur d'onde λ.
4-2- Donner la valeur de la longueur d'onde de l'onde ultrasonore. (à justifier)
4-3- Exprimer le retard τ du signal reçu par R'2 par rapport a celui reçu par R2.
4-4- Exprimer puis calculer la célérité des ultrasons dans l'air.
4-5- Sans faire de calculs, indiquer quel est le retard de R'2 par rapport a R1. (justifier).
5- Cette expérience aurait-elle été facile a mettre en œuvre avec un haut parleur émettant un signal de 80 Hz et
deux micros ? (réponse à justifier par un calcul)
fin
Vous aimerez peut-être aussi
- Exercices d'optique et d'électromagnétismeD'EverandExercices d'optique et d'électromagnétismeÉvaluation : 5 sur 5 étoiles5/5 (1)
- Cours Fibre OptiqueDocument35 pagesCours Fibre Optiquezennouri96% (26)
- Optique GeoDocument58 pagesOptique GeoYassineZkl100% (1)
- QCM - Rayonnement IonisantsDocument14 pagesQCM - Rayonnement IonisantsFéz Ey100% (1)
- Livre Exo Bio v2020Document96 pagesLivre Exo Bio v2020MARRI Mustapha100% (6)
- Bac Blanc 2 SM (21-22)Document9 pagesBac Blanc 2 SM (21-22)Salma Bendaoud100% (1)
- Devoir 8Document6 pagesDevoir 8Féz Ey100% (1)
- Série Exercices ROTATION20323Document2 pagesSérie Exercices ROTATION20323Douae GhoulaichiPas encore d'évaluation
- 1à100 QCM FMA1 Bio Cell PR KHANFRI 2020Document12 pages1à100 QCM FMA1 Bio Cell PR KHANFRI 2020Féz Ey100% (1)
- La TrachéeDocument4 pagesLa TrachéeFéz EyPas encore d'évaluation
- Devoir 5Document1 pageDevoir 5Féz Ey100% (1)
- Contrôle 28 (PR Jenkal Rachid)Document4 pagesContrôle 28 (PR Jenkal Rachid)Mouhibi AbdellahPas encore d'évaluation
- Cont 1 s1 PC 2 Bac Prof - Filali (WWW - Pc1.ma)Document1 pageCont 1 s1 PC 2 Bac Prof - Filali (WWW - Pc1.ma)said youssfiPas encore d'évaluation
- 1 - Exercices de Fixation TC FRDocument2 pages1 - Exercices de Fixation TC FRait hssainPas encore d'évaluation
- Les Ondes Luminuse 1 2024Document4 pagesLes Ondes Luminuse 1 2024Saida AzzouziPas encore d'évaluation
- Exercices PC TC International 7 3Document3 pagesExercices PC TC International 7 3kamalPas encore d'évaluation
- RLClibre Exerc TS17 FRDocument6 pagesRLClibre Exerc TS17 FRMohamed El Ouahdani100% (1)
- Série N°1Document3 pagesSérie N°1Ahmad WhabiPas encore d'évaluation
- TD6 MP Mouvement À Forces Centrales 2020-2021 - 230511 - 012958Document4 pagesTD6 MP Mouvement À Forces Centrales 2020-2021 - 230511 - 012958RamboAkkkoPas encore d'évaluation
- Corrige ENI GEIPI Physique 2009Document8 pagesCorrige ENI GEIPI Physique 2009la physique selon le programme FrançaisPas encore d'évaluation
- 1519455359Document2 pages1519455359halim otmanePas encore d'évaluation
- Tle DDocument2 pagesTle Dbrice mouadjePas encore d'évaluation
- Séries D'exerices Électricité Examen National 2bacDocument9 pagesSéries D'exerices Électricité Examen National 2bacWalaa WalaaPas encore d'évaluation
- Controle 2 Bac Semestre 1Document3 pagesControle 2 Bac Semestre 1C'est Yana100% (1)
- L2S4 Electromag TD1Document2 pagesL2S4 Electromag TD1aladinPas encore d'évaluation
- TD Introduction ElectrotechniqueDocument9 pagesTD Introduction Electrotechniqueedem fiademPas encore d'évaluation
- Exercices 3 Mouvement de Rotation Autour D'un Axe FixeDocument1 pageExercices 3 Mouvement de Rotation Autour D'un Axe Fixemaryame jssPas encore d'évaluation
- Série+d'Exercices+ +Physique+Dipole+RC+ +Bac+Mathématiques+ (2012 2013) +Mr+AfdalDocument7 pagesSérie+d'Exercices+ +Physique+Dipole+RC+ +Bac+Mathématiques+ (2012 2013) +Mr+AfdalWiem BenchahbounPas encore d'évaluation
- Evaluation Diagnostique Tronc Commun InternationalDocument4 pagesEvaluation Diagnostique Tronc Commun InternationalMouad MoukhliPas encore d'évaluation
- Devoir 1Document1 pageDevoir 1Noureddine ElkouayPas encore d'évaluation
- Chute Verticale D Un SolideDocument2 pagesChute Verticale D Un Solidehakima032Pas encore d'évaluation
- Devoir 4Document2 pagesDevoir 4Ahmed Ahmed100% (1)
- Serie 1 Les Ondes Mecaniques BiofDocument3 pagesSerie 1 Les Ondes Mecaniques BiofAlae AnouarPas encore d'évaluation
- Devoir de Synthèse N°1 - Sciences Physiques - Bac Technique (2020-2021) MR Foued BahlousDocument4 pagesDevoir de Synthèse N°1 - Sciences Physiques - Bac Technique (2020-2021) MR Foued BahlousKhalil BkekriPas encore d'évaluation
- Controle 2 - 3 S2 PC 1bac FRDocument2 pagesControle 2 - 3 S2 PC 1bac FRAlae AnouarPas encore d'évaluation
- DM Vendredi 27 MarsDocument6 pagesDM Vendredi 27 MarsEroline GuelciPas encore d'évaluation
- Cours & Exercices Mesure de Quantités de Matière Par ConductimétrieDocument6 pagesCours & Exercices Mesure de Quantités de Matière Par ConductimétrieAmine AlaoUii AlaouiPas encore d'évaluation
- M12 Chute Libre FrottementsDocument11 pagesM12 Chute Libre FrottementsNeoXana01Pas encore d'évaluation
- Cahier: Mecanique Du Point MaterielDocument234 pagesCahier: Mecanique Du Point MaterielAhmed ikalPas encore d'évaluation
- Activité TP ReflexionDocument3 pagesActivité TP ReflexionkatPas encore d'évaluation
- Energie Interne Et Calorimètre Exercices FR 16Document2 pagesEnergie Interne Et Calorimètre Exercices FR 16Yassir Rochd100% (1)
- Serie Phy2 2021Document4 pagesSerie Phy2 2021Farid BelalPas encore d'évaluation
- TP14 Travail D'une Force EC2021Document4 pagesTP14 Travail D'une Force EC2021Maxime DecouvelaerePas encore d'évaluation
- Cours Transfert D'énergie Dans Un Circuit Électrique Puissance ÉlectriqueDocument2 pagesCours Transfert D'énergie Dans Un Circuit Électrique Puissance ÉlectriqueZoubi OmaimaPas encore d'évaluation
- 31-104 Optique Miroirs PDFDocument13 pages31-104 Optique Miroirs PDFKheria ZitouniPas encore d'évaluation
- 2 Bac Sobhi 03-Propagation-Dune-Onde-LumineuseDocument11 pages2 Bac Sobhi 03-Propagation-Dune-Onde-Lumineusekhalifa El harfiPas encore d'évaluation
- Cours 1 - 1bac Mouvement de Rotation D'un Corps Solide Autour D'un Axe FixeDocument5 pagesCours 1 - 1bac Mouvement de Rotation D'un Corps Solide Autour D'un Axe Fixefay mourPas encore d'évaluation
- TPno 4 MesuredescaracteristiquesdessignauxalternatifsDocument4 pagesTPno 4 MesuredescaracteristiquesdessignauxalternatifsTaki BenazzouzPas encore d'évaluation
- Examen National Physique Chimie Sciences Maths 2018 Normale Sujet PDFDocument8 pagesExamen National Physique Chimie Sciences Maths 2018 Normale Sujet PDFel ghazi benrrabhiPas encore d'évaluation
- Exercices Atome Et Mecanique de NewtonDocument4 pagesExercices Atome Et Mecanique de NewtonHAMADA1972Pas encore d'évaluation
- Soutien Scolaire TC PDFDocument4 pagesSoutien Scolaire TC PDFsine abdellah100% (1)
- Modification Du Squelette Carbone Cours 1Document4 pagesModification Du Squelette Carbone Cours 1Amoula Hayatie100% (1)
- Exercice 1: Lecture Oscilloscope (Difficulté ) : Voie1Document4 pagesExercice 1: Lecture Oscilloscope (Difficulté ) : Voie1Mohamed AliPas encore d'évaluation
- Cours: Interactions Onde-MatièreDocument12 pagesCours: Interactions Onde-Matièremaryem hamzaPas encore d'évaluation
- PrepaTS RadioactiviteDocument7 pagesPrepaTS RadioactivitepdfPas encore d'évaluation
- Exercices Vitesse Et Code de La Route CorrectionDocument6 pagesExercices Vitesse Et Code de La Route Correctionkilili benaliPas encore d'évaluation
- Mesure Et Essai 1ereDocument1 pageMesure Et Essai 1ereEssotina DADJA100% (1)
- Sans Nom 1Document1 pageSans Nom 1Med Amine HattakiPas encore d'évaluation
- Travail Et Énergie Interne - Resume de Cours - Dr. Karam OuharouDocument4 pagesTravail Et Énergie Interne - Resume de Cours - Dr. Karam OuharouKaram OUHAROUPas encore d'évaluation
- Chapitre 1 Généralités Sur La Compatibilité ÉlectromagnétiqueDocument31 pagesChapitre 1 Généralités Sur La Compatibilité ÉlectromagnétiqueVa LidPas encore d'évaluation
- TP Etk Ge 20 21Document17 pagesTP Etk Ge 20 21Ayman AssilaPas encore d'évaluation
- Examen National Physique Chimie SPC 2013 Rattrapage SujetDocument6 pagesExamen National Physique Chimie SPC 2013 Rattrapage Sujetothmane GbPas encore d'évaluation
- EXO 31-Son Et DispersifDocument1 pageEXO 31-Son Et DispersifSlimen Labiedh0% (1)
- Correction CPR 2013Document18 pagesCorrection CPR 2013Hamid El Bouabidi0% (2)
- C2Phy Ondes Mecaniques Progressives Periodiques PDFDocument2 pagesC2Phy Ondes Mecaniques Progressives Periodiques PDFAzizElheniPas encore d'évaluation
- Devoir 4Document3 pagesDevoir 4Mohamed El OuahdaniPas encore d'évaluation
- Devoir 1Document2 pagesDevoir 1Aicha Daou100% (3)
- Région Fessière & CuisseDocument6 pagesRégion Fessière & CuisseFéz EyPas encore d'évaluation
- Anatomie Du Membre Supérieur & Creux AxillaireDocument5 pagesAnatomie Du Membre Supérieur & Creux AxillaireFéz EyPas encore d'évaluation
- Avant-Bras & MainDocument3 pagesAvant-Bras & MainFéz EyPas encore d'évaluation
- Notes Harim MalakDocument5 pagesNotes Harim MalakFéz EyPas encore d'évaluation
- ExercicesDeRevision18 19Document2 pagesExercicesDeRevision18 19Féz EyPas encore d'évaluation
- Règlement Intérieur UIRDocument16 pagesRèglement Intérieur UIRFéz EyPas encore d'évaluation
- Les ProtéinesDocument11 pagesLes ProtéinesFéz EyPas encore d'évaluation
- Paroi ThoraciqueDocument6 pagesParoi ThoraciqueFéz EyPas encore d'évaluation
- Teste 1Document1 pageTeste 1Féz EyPas encore d'évaluation
- MathDocument5 pagesMathFéz EyPas encore d'évaluation
- 101à200 QCM FMA1 Bio CellDocument12 pages101à200 QCM FMA1 Bio CellFéz EyPas encore d'évaluation
- 1a Planning Semestre 1 - s12Document1 page1a Planning Semestre 1 - s12Féz EyPas encore d'évaluation
- EncéphaleDocument9 pagesEncéphaleFéz EyPas encore d'évaluation
- Myologie Salma THAKIDocument4 pagesMyologie Salma THAKIFéz EyPas encore d'évaluation
- Refdp - BSFP 155p11 14Document4 pagesRefdp - BSFP 155p11 14Féz EyPas encore d'évaluation
- Fma1s1-Biochimie Structurale PR Balouch V-08092018Document105 pagesFma1s1-Biochimie Structurale PR Balouch V-08092018Féz EyPas encore d'évaluation
- Devoir 10Document5 pagesDevoir 10Féz EyPas encore d'évaluation
- Devoir 6Document2 pagesDevoir 6Féz Ey100% (1)
- Devoir 7Document2 pagesDevoir 7Féz EyPas encore d'évaluation
- Lycée Abi Bakr Devoir Maison n1 s1Document4 pagesLycée Abi Bakr Devoir Maison n1 s1Chimie FinePas encore d'évaluation
- Correction TVNumerique 5ptsDocument2 pagesCorrection TVNumerique 5ptssa raPas encore d'évaluation
- Physiquechimie Cours1 PDFDocument4 pagesPhysiquechimie Cours1 PDFLéo LescourretPas encore d'évaluation
- Cours Complèt S1Document102 pagesCours Complèt S1Mohamed ElouakilPas encore d'évaluation
- Celerite Du SonDocument3 pagesCelerite Du SonriesmaelysPas encore d'évaluation
- Techniques Et Suports de Transmission-MCN-2021Document61 pagesTechniques Et Suports de Transmission-MCN-2021Jessi autisolPas encore d'évaluation
- Exo 2019Document44 pagesExo 2019mheba ddPas encore d'évaluation
- Correction Révision OndesDocument4 pagesCorrection Révision OndesI2NI 81Pas encore d'évaluation
- Chapitre Physique Les Sons UltrasonsDocument2 pagesChapitre Physique Les Sons UltrasonskouskousnaoualPas encore d'évaluation
- c1 s1 2BAC A Prof - Habib (WWW - Pc1.ma)Document4 pagesc1 s1 2BAC A Prof - Habib (WWW - Pc1.ma)elmrabatmohamed96100% (2)
- Effet de La Dispersion Modale D'une Fibre Optique Multimode DansDocument12 pagesEffet de La Dispersion Modale D'une Fibre Optique Multimode DansMohamed BenbarkPas encore d'évaluation
- TS Physique Chimie Cours PDFDocument12 pagesTS Physique Chimie Cours PDFDarrel Foweng TchoPas encore d'évaluation
- 3eme Eco Et Env 2019-2020 Cours Télédétection Et SIG. Beldjazia AminaDocument81 pages3eme Eco Et Env 2019-2020 Cours Télédétection Et SIG. Beldjazia AminaTJOMB THEODOREPas encore d'évaluation
- Bacc Blanc CDocument5 pagesBacc Blanc CFranck FouodjiPas encore d'évaluation
- 1 Cours PROF Chap15 Les Ondes MécaniquesDocument7 pages1 Cours PROF Chap15 Les Ondes Mécaniquessan gokuPas encore d'évaluation
- TD de Physique N 6: Électromagnétisme (Suite)Document13 pagesTD de Physique N 6: Électromagnétisme (Suite)bertrandossohou32Pas encore d'évaluation
- TPP 03Document3 pagesTPP 03De Carry AymardPas encore d'évaluation
- Exercice 1: PHYSIQUE / Unité:1 Propagation D'Une Onde-Ondes ProgressivesDocument1 pageExercice 1: PHYSIQUE / Unité:1 Propagation D'Une Onde-Ondes ProgressivesHamza AttabanePas encore d'évaluation
- Chapitre - 4 Optique Ondul PDFDocument6 pagesChapitre - 4 Optique Ondul PDFAnis DahnenPas encore d'évaluation
- cpp11 PDFDocument24 pagescpp11 PDFPatience ImanePas encore d'évaluation
- Thema InterferencesDocument12 pagesThema InterferencesRita A.J.Pas encore d'évaluation
- Les Ondes Lumineuse: National Polytechnic School of ConstantineDocument12 pagesLes Ondes Lumineuse: National Polytechnic School of ConstantineSamah BoughanemPas encore d'évaluation
- 02 Ondes SinusDocument2 pages02 Ondes SinusChartier JulienPas encore d'évaluation
- Theme Onde SM SujetDocument21 pagesTheme Onde SM SujetAlphaPas encore d'évaluation
- Bourkaibzahia ChertouhSoniaDocument121 pagesBourkaibzahia ChertouhSoniaguedri khensaPas encore d'évaluation
- 21.chapitre 1Document9 pages21.chapitre 1Ozias ZilhPas encore d'évaluation