Académique Documents
Professionnel Documents
Culture Documents
Sciences Et Technologies de L'Industrie Et Du Developpement Durable
Sciences Et Technologies de L'Industrie Et Du Developpement Durable
Transféré par
AaaaTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Sciences Et Technologies de L'Industrie Et Du Developpement Durable
Sciences Et Technologies de L'Industrie Et Du Developpement Durable
Transféré par
AaaaDroits d'auteur :
Formats disponibles
BACCALAURÉAT TECHNOLOGIQUE
ÉPREUVE D’ENSEIGNEMENT DE SPÉCIALITÉ
SESSION 2022
SCIENCES ET TECHNOLOGIES DE
L’INDUSTRIE ET DU
DEVELOPPEMENT DURABLE
Physique-Chimie et Mathématiques
ÉPREUVE DU MERCREDI 11 MAI 2022
Durée de l’épreuve : 3 heures
L’usage de la calculatrice avec mode examen actif est autorisé.
L’usage de la calculatrice sans mémoire, « type collège » est autorisé.
Dès que ce sujet vous est remis, assurez-vous qu’il est complet.
Ce sujet comporte 17 pages numérotées de 1/17 à 17/17.
PHYSIQUE-CHIMIE .................................................................................. 14/20 points
MATHÉMATIQUES ..................................................................................... 6/20 points
Le candidat sera attentif aux consignes contenues dans le sujet pour traiter les
4 exercices.
22-2DPCMAME1 Page: 1/17
EXERCICE 1 commun à tous les candidats (4 points)
(physique-chimie et mathématiques)
Modèle de la vitesse de refroidissement d’un lait écrémé
Dans le domaine de l’agroalimentaire, la question du refroidissement des produits
préparés peut être cruciale. On peut citer par exemple la problématique de la durée
de refroidissement du lait produit dans une ferme : afin d’éviter la prolifération
microbienne, il convient de minimiser cette durée de refroidissement.
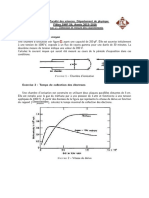
Afin d’étudier l’évolution de la température d’une masse de liquide en contact avec
l’atmosphère d’une pièce en fonction du temps, l’expérience suivante est réalisée.
Une masse de lait écrémé 𝑚 = 150 g est chauffée à une température de 63,4 °C. On
laisse ensuite le lait se refroidir à l’air libre en relevant sa température toutes les
minutes.
Pendant toute la durée de l’expérience, la température de l’air de la pièce reste
constante et inférieure à celle du lait.
Résultats de l’expérience : température de la masse de lait en fonction du temps 𝑡.
𝑡(en min) 0 1 2 3 4 5 6 7
température
63,4 61,7 60,2 58,6 57,4 56,2 54,7 53,6
(en °C)
𝑡 (en min) 8 9 10 11 12 13 14 15
température
52,4 51,2 50,4 49,4 48,5 47,4 46,6 45,9
(en °C)
Donnée :
- Pour la capacité thermique massique du lait, on prendra :
𝑐lait = 4,0 kJ. kg −1 . K −1.
1. Citer les trois modes de transferts thermiques.
2. Préciser, en le justifiant, le sens du transfert thermique entre la masse de lait et
l’air de la pièce.
3. Calculer, d’après les résultats expérimentaux, la valeur du transfert thermique 𝑄
entre la masse de lait et l’air de la pièce entre les dates 𝑡 = 1 min et 𝑡 = 2 min.
Sans calcul, préciser si la valeur du transfert thermique est plus petite ou plus
grande que 𝑄 entre les dates 𝑡 = 6 min et 𝑡 = 7 min.
22-2DPCMAME1 Page: 2/17
La température du lait, exprimée en degré Celsius, en fonction du temps 𝑡, exprimé
en minute, est modélisée par la fonction 𝑇 définie sur [0; +∞[ par :
20𝑡
𝑇(𝑡) = 37×e− 459 + 26,4.
4. Calculer 𝑇(0) et interpréter ce résultat dans le contexte de l’exercice.
5. Déterminer lim 𝑇(𝑡).
𝑡→+∞
Selon ce modèle, quelle est la température de l’air de la pièce ? Justifier.
6. Selon ce modèle, au bout de combien de temps la température du lait vaut-elle
40°C ? Donner le résultat en minute et seconde.
22-2DPCMAME1 Page: 3/17
EXERCICE 2 commun à tous les candidats (6 points)
(physique-chimie)
Le son de la guitare électrique
Cet exercice a pour but d'étudier deux paramètres connus pour modifier le son
produit par une guitare électrique : l'oxydation des cordes et l'influence du câble
reliant la guitare à l'amplificateur.
1. Les cordes de guitare
Les cordes de guitare sont un élément essentiel pour la production du son. C'est la
vibration de celles-ci qui est transformée en signal électrique par les micros de la
guitare. Ainsi les cordes sont le plus souvent en alliage de fer pour pouvoir interagir
avec les aimants présents dans les micros.
A l'air libre les cordes s'oxydent progressivement car elles sont le siège de réactions
d'oxydoréduction.
Dans l’air humide, du fait de la condensation, la transformation chimique peut être
modélisée à l’aide des deux demi-équations électroniques suivantes :
Fe(s) +2HO-(aq) = Fe(OH)2(s) + 2 e-
O2(g) + 2 H2O(l) + 4 e- = 4 HO-(aq)
1.1. À partir des deux demi-équations proposées, écrire l'équation de la réaction
d'oxydoréduction qui modélise la transformation chimique subie par le fer
contenu dans les cordes.
1.2. Montrer qu’il est justifié de considérer que le fer subit une oxydation dans cette
transformation chimique.
Afin de limiter cette oxydation, une des méthodes actuelles consiste à recouvrir la
corde avec un enduit transparent très fin qui sert de revêtement à la corde.
1.3. Indiquer la propriété que doit posséder l’enduit pour éviter efficacement le
phénomène d'oxydation.
22-2DPCMAME1 Page: 4/17
Conséquences de l'oxydation des cordes sur le son d'une guitare.
En utilisant la même échelle verticale, on réalise le spectre d'amplitude d'une note
jouée par une guitare électrique équipée de cordes neuves puis de cordes oxydées.
fréquence (en Hz) fréquence (en Hz)
Corde neuve Corde oxydée
Note La1 Do2 Sol2 La2 Ré3 Fa3 Sol3 Ré4
Fréquence
110 130 196 220 294 349 392 587
(Hz)
1.4. À partir du spectre obtenu pour la corde neuve, déterminer, en justifiant la
fréquence fondamentale de la note jouée.
1.5. Indiquer la note jouée par la guitare.
1.6. Indiquer, en justifiant, si le son produit par la corde neuve a la même hauteur
que celui produit par la corde oxydée.
1.7. Préciser, en justifiant, quelle caractéristique du son produit par la guitare est
modifiée selon que l’on utilise des cordes neuves ou oxydées.
22-2DPCMAME1 Page: 5/17
2. Le câble reliant la guitare à l'amplificateur
Les musiciens évoquent souvent l’influence du câble reliant la guitare à
l’amplificateur sur le son obtenu. Selon eux, le câble provoquerait une diminution
d’amplitude des harmoniques de hautes fréquences, produisant un son plus terne,
moins riche en composantes aigues.
Nous réalisons deux études afin de vérifier la pertinence de cette observation.
Une première étude est réalisée sur un câble de guitare d'une longueur de 10 m, non
relié à la guitare. Il s’agit de déterminer une éventuelle atténuation du signal
électrique transporté par le câble.
Une tension sinusoïdale de fréquence connue est délivrée par un générateur basses
fréquences. À l'aide d'un oscilloscope, l'amplitude Ue de la tension en entrée du câble
est comparée à l'amplitude US de la tension en sortie du câble.
On peut calculer alors l’affaiblissement R (en dB) subi par le signal lors de de son
transport par le câble grâce à la relation suivante :
Ue R
=10 20
US
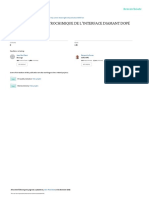
Les mesures de l’affaiblissement généré par le câble pour des signaux sinusoïdaux
de fréquence comprise entre 500 Hz et 10 kHz permettent d’établir le graphe suivant.
Affaiblissement R en fonction de la fréquence
0,1
0,09
Affaiblissement R (dB)
0,08
0,07
0,06
0,05
0,04
0,03
0,02
0,01
0
500 1500 2500 3500 4500 5500 6500 7500 8500 9500 10500
Fréquence (en Hz)
2.1. Montrer qu'une valeur d’affaiblissement positif correspond à une atténuation
du signal lors du passage dans le câble.
2.2. En considérant une tension d'entrée d’amplitude Ue = 20,0 mV, déterminer la
tension de sortie dans les conditions de l'expérience, pour une valeur de
l’affaiblissement R = 0,09. Commenter le résultat.
22-2DPCMAME1 Page: 6/17
2.3. Exploiter la courbe ci-dessus pour déterminer si les propriétés électriques du
câble seul peuvent expliquer une modification du timbre du son obtenu.
Justifier la réponse.
Cette première expérience ne prenant pas en compte le branchement de la guitare
sur le câble et sur l’amplificateur, on réalise une seconde étude en connectant le
câble, en entrée et en sortie, à des dipôles ayant respectivement des propriétés
électriques semblables à celles de la guitare et de l’entrée de l’amplificateur.
Pour isoler l’influence du câble, on réalise des mesures d’affaiblissement avec un
câble très court puis avec le câble de 10 m. On obtient les graphiques ci-dessous.
50
Courbe 2
Courbe 1 : Affaiblissement avec câble très court
40 Courbe 2 : Affaiblissement avec câble de 10 m
Courbe 1
30
Affaiblissement (dB)
20
10
0
100 1000 10000 100000
-10
Etude réalisée à partir des caractéristiques
Fréquence (Hz) du micro utilisé https://www.seymourduncan.com/
2.4. En ne considérant que les fréquences pour lesquelles l’affaiblissement R a
une valeur positive, indiquer si l’allure de ces graphiques est compatible avec
les problèmes évoqués par les musiciens lors de l’utilisation d'un long câble.
22-2DPCMAME1 Page: 7/17
EXERCICE 3 commun à tous les candidats (4 points)
(mathématiques)
Le candidat doit traiter quatre questions parmi les six numérotées de 1 à 6 que
comporte l’exercice. Les questions sont indépendantes les unes des autres.
Le candidat choisit les quatre questions auxquelles il répond et indique
clairement leur numéro sur sa copie en début d’exercice. Seules ces questions
sont évaluées. Chacune d’elles est notée sur un point. Traiter une question
supplémentaire ne rapporte aucun point.
Question 1
1. Montrer, en détaillant vos calculs, que :
ln(2025) = 4 ln(3) + 2 ln(5).
2. Simplifier le nombre 𝐴 ci-dessous en détaillant les calculs :
1
𝐴 = 2 ln(e4 ) − 3 ln ( ).
e
Question 2
π
On désigne par i le nombre complexe de module 1 et d’argument .
2
On considère le nombre complexe suivant :
−1 + i
𝑧= .
3i
1. Mettre 𝑧 sous forme algébrique. Détailler les calculs.
2. Mettre 𝑧 sous forme exponentielle. Détailler les calculs.
Question 3
On considère l’équation différentielle (𝐸) ∶ 2 𝑦 ′ + 𝑦 = 0, où 𝑦 est une fonction de la
variable 𝑥, définie et dérivable sur 𝐑 et 𝑦′ la fonction dérivée de 𝑦.
1. Déterminer les solutions sur 𝐑 de l'équation différentielle (𝐸).
2. Le plan est muni d'un repère.
Déterminer la solution 𝑓 de (𝐸), dont la courbe représentative 𝐶𝑓 dans ce repère
passe par le point 𝐴(ln(9) ; 1).
22-2DPCMAME1 Page: 8/17
Question 4
On considère la fonction 𝑓 définie sur R par 𝑓(𝑥) = 𝑎 + 𝑏e𝑥 , où 𝑎 et 𝑏 sont deux
nombres réels.
On considère la fonction 𝑔 définie sur R par 𝑔(𝑥) = 𝑥 2 − 4𝑥 − 1.
On note 𝐶𝑓 et 𝐶𝑔 les courbes représentatives des fonctions 𝑓 et 𝑔, tracées dans le
repère orthogonal ci-dessous.
1. On admet que les deux courbes 𝐶𝑓 et 𝐶𝑔 ont un unique point en commun, noté A
d’abscisse 0.
Calculer 𝑔(0), puis en déduire que 𝑎 + 𝑏 = −1.
2. On admet que les deux courbes 𝐶𝑓 et 𝐶𝑔 ont la même tangente 𝑇 au point A.
a. Donner, pour tout réel 𝑥, une expression de 𝑔′(𝑥) puis calculer 𝑔′(0).
b. En déduire la valeur de 𝑏, puis celle de 𝑎.
22-2DPCMAME1 Page: 9/17
Question 5
Soit 𝑔 la fonction définie sur l’intervalle ]0 ; +∞[ par :
1
𝑔(𝑥) = 𝑥 2 – ln(𝑥).
2
1. On admet que 𝑔 est dérivable sur l’intervalle ]0 ; +∞[ et on note 𝑔′ sa fonction
dérivée. Montrer que pour tout réel 𝑥 de l’intervalle ]0 ; +∞[,
(𝑥−1)(𝑥+1)
𝑔′ (𝑥) = .
𝑥
2. Montrer que la fonction 𝑔 admet un minimum, dont on précisera la valeur exacte,
sur l’intervalle ]0 ; +∞[.
Question 6
Rappel : pour 𝑎 et 𝑏 deux réels, on a les formules suivantes :
cos(𝑎 + 𝑏) = cos(𝑎) cos(𝑏) − sin(𝑎) sin(𝑏)
cos(𝑎 − 𝑏) = cos(𝑎) cos(𝑏) + sin(𝑎) sin(𝑏)
sin(𝑎 + 𝑏) = sin(𝑎) cos(𝑏) + cos(𝑎) sin(𝑏)
sin(𝑎 − 𝑏) = sin(𝑎) cos(𝑏) − cos(𝑎) sin(𝑏)
La tension 𝑢, exprimée en volt, aux bornes d’un dipôle en fonction du temps 𝑡,
exprimé en seconde, est donnée par : 𝑢(𝑡) = cos(50𝑡) + √3sin(50𝑡).
1. Pour tout nombre réel 𝑡, écrire 𝑢(𝑡) sous la forme 𝑢(𝑡) = 𝑈max cos(𝜔𝑡 + 𝜑) où :
• 𝑈max représente la tension maximale (exprimée en volt) ;
• 𝜔 représente la pulsation (exprimée en rad.s-1) ;
• 𝜑 représente le déphasage (exprimé en rad).
𝜔
2. En déduire la fréquence correspondante 𝑓 = , exprimée en Hz. Arrondir le
2𝜋
résultat à l’unité.
22-2DPCMAME1 Page: 10/17
EXERCICE 4 au choix du candidat (6 points)
(physique-chimie)
Le candidat choisit de traiter l’exercice 4 – A ou l’exercice 4 – B.
Vous indiquerez sur votre copie l’exercice 4 choisi : exercice 4 – A ou exercice 4 – B
EXERCICE 4 – A : Produit détachant et lessive
Mots clés : réaction acido-basique, réactions d’oxydo-réduction, ondes
électromagnétiques.
1. Composition de la lessive
Les lessives liquides sont composées de fortes quantités de carbonates ; en
moyenne 30 % de la masse d’une lessive est constituée de carbonate de calcium
CaCO3(s).
La dissolution du CaCO3(s) libère des ions calcium Ca2+(aq) et des ions carbonate
CO32- (aq) selon l’équation-bilan :
CaCO3(s) = Ca2+(aq)+ CO32-(aq)
L’ion carbonate CO32-(aq), appartient au couple acido-basique HCO3-(aq)/CO32-(aq).
L’eau intervient alors dans le couple acido-basique H2O(l)/HO-(aq).
1.1. Lors d’un cycle de lavage, une masse de 50 g de lessive est introduite dans le
tambour où se trouve un volume d’eau égal à 20 L.
Calculer la concentration molaire en ions carbonate résultant de la dissolution
totale de la lessive dans l’eau contenue dans le tambour de la machine à
laver.
Données :
Masses molaires : M(Ca) = 40 gmol-1 ; M(O) = 16 gmol-1 ; M(C) = 12,0 gmol-1
1.2. Écrire l’équation-bilan de la réaction de l’ion carbonate CO32-(aq) sur l’eau H2O(l)
En déduire l’influence de la présence d’ions carbonate sur le pH de l’eau de
lavage.
2. Agents de blanchiment
Dans les lessives dites à « l’oxygène actif » le peroxyde d’hydrogène H2O2 (ou eau
oxygénée) est l’agent de blanchiment. Comme le peroxyde d'hydrogène H2O2 est
difficile à conserver longtemps en solution aqueuse, les lessives contiennent des
produits capables de libérer de l’eau oxygénée au contact de l’eau. C’est le cas du
perborate de sodium tétrahydraté NaBO3,4H2O. Ce composé est stable à
température ambiante mais réagit avec l’eau à 60°C, la réaction libérant du peroxyde
d'hydrogène.
Données :
Couples d’oxydoréduction mis en jeu : NaBO3(aq) / NaBO2(aq) et H2O2(aq) / H2O(l)
2.1. Écrire l’équation de la réaction qui modélise l’action du perborate de sodium
sur l’eau, conduisant à la formation du peroxyde d’hydrogène.
22-2DPCMAME1 Page: 11/17
En solution aqueuse, le peroxyde d’hydrogène peut réagir avec lui-même (on parle
de réaction de dismutation), ce qui explique que l’on ne peut le conserver longtemps
sous cette forme. Cette réaction met en évidence les propriétés oxydantes et
réductrices du peroxyde d’hydrogène.
Les deux demi-équations électroniques correspondantes sont :
H2O2(aq) + 2H+(aq) + 2e– = 2H2O(l) (1)
H2O2(aq) = O2(g) + 2H+(aq) + 2e– (2)
2.2. Préciser si, dans la demi-équation (1), le peroxyde d'hydrogène H2O2(aq) est
l’oxydant ou le réducteur. Justifier.
2.3. Préciser le couple oxydant/réducteur mis en jeu dans la demi-équation (2).
2.4. Écrire l’équation de la réaction qui modélise l’action du peroxyde d’hydrogène
sur lui-même à partir des demi-équations (1) et (2). Identifier les produits de la
réaction.
3. Azurants optiques
Certaines fibres naturelles absorbent la lumière bleue, ce qui donne un aspect
jaunâtre au linge. Pour éviter cet effet, les lessives contiennent des azurants
optiques. Ces molécules absorbent les rayonnements électromagnétiques
ultraviolets et réémettent ensuite cette énergie sous forme de rayonnement visible
(c’est le phénomène de fluorescence). Un azurant optique émet des ondes
électromagnétiques avec un maximum dans les longueurs d’onde correspondant à la
couleur bleue.
L’azurant optique donne ainsi un « éclat de blancheur » au tissu lavé.
3.1. Préciser les longueurs d’ondes qui délimitent le domaine électromagnétique
visible. Indiquer où se situe le domaine des longueurs d’ondes des
rayonnements ultraviolets par rapport à celui du domaine visible.
3.2. Déterminer, à l’aide des spectres suivants, la valeur de la longueur d’onde
correspondant au maximum d’émission de l’azurant optique.
22-2DPCMAME1 Page: 12/17
Les agents azurants sont peu ou pas toxiques. Ils sont difficilement biodégradables
et leur potentiel de bioaccumulation est considéré comme étant négligeable. En
raison de leur utilisation majeure dans les détergents, leur principal impact
écotoxicologique devrait se situer au niveau des espèces aquatiques.
D’après l’article https://fr.wikipedia.org/wiki/Agent_azurant
3.3. Identifier le pictogramme de danger des azurants optiques en indiquant son
code.
Pictogrammes de la réglementation européenne.
Chacun des 9 pictogrammes de la règlementation européenne possède un code
composé de la façon suivante : « GHS* » + « 0 » + 1 chiffre.
*GHS : Globally Harmonized System
GHS01 GHS02 GHS03
GHS04 GHS05 GHS06
GHS07 GHS08 GHS09
22-2DPCMAME1 Page: 13/17
EXERCICE 4 – B : Dormir en refuge, un mode d’hébergement écologique ?
Mots clés : énergie électrique, combustion, groupes caractéristiques.
Dans le cadre d’une démarche de développement durable, la rénovation énergétique
du refuge de Bostan (Samoëns, Haute-Savoie) en 2016 s'est concrétisée par
l'installation de panneaux solaires hybrides photovoltaïque/thermique. Un poêle à
bois assure toujours le chauffage tandis que les 12 panneaux solaires hybrides
photovoltaïque/thermique (8 panneaux au sud-est et 4 panneaux à l’ouest)
produisent de l’électricité et de l’eau chaude pour le refuge. L’installation sud-est est
active de 8 h du matin jusqu’à midi. De midi jusqu’à 15h les deux installations sont
actives. Enfin, après 15h c’est l’installation orientée ouest qui prend le relais jusqu'à
18 h.
Informations techniques de l’installation :
Caractéristiques de Refuge de montagne (capacité 70 personnes)
l’installation
Nombre de panneaux 12 panneaux hybrides
Puissance électrique 3,00 kW
Puissance thermique 4,49 kW
https://dualsun.com/fr/realisations/samoens-fr-2016-12pvt/
Caractéristiques physiques des panneaux pour un ensoleillement de 1000 W.m- 2 :
Longueurs 1677 mm
Largeur 990 mm
Tension à puissance maximale 30,7 V
Intensité à puissance maximale 8,15 A
https://www.alaska-energies.com/wp-content/uploads/2016/08/Dualsun_FR_FT_Wave_0816.pdf
1. Étude des panneaux photovoltaïques
Informations sur les panneaux photovoltaïques
Pour convertir l’énergie des photons en énergie électrique, on utilise des cellules
solaires constituées de semi-conducteurs. Ces matériaux sont caractérisés par une
bande d’énergie interdite nommée « gap ». La valeur de ce gap dépend de la nature
chimique et de la structure du matériau ; sa valeur est de 1,1 eV pour le silicium
monocristallin.
Un photon est absorbé par un semi-conducteur quand son énergie est supérieure au
gap, sinon il le traverse. Ainsi, tous les photons d’énergie supérieure au gap peuvent
être absorbés. Cependant, l’énergie en excès est vite perdue sous forme de chaleur
et l’énergie électrique maximale que l’on peut récupérer est égale à celle du gap.
D’après Pour La Science, juillet/octobre 2010
Données :
- 1 eV = 1,60 × 10-19 J
- Constante de Planck h = 6,63 × 10-34 J.s
- Célérité de la lumière dans le vide c = 3,0 × 108 m.s-1
- 1 Wh : énergie associée à une puissance d’un watt pendant une heure
- 1 Wh = 3600 J ; 1 kWh = 1000 Wh ; 1 MWh = 1000 kWh
22-2DPCMAME1 Page: 14/17
1.1. Donner l’expression de la fréquence f d’un photon susceptible de provoquer
une variation d’énergie ΔE.
Calculer alors la longueur d’onde d’un photon qui fournit, par absorption,
une énergie ΔE égale à la valeur du gap de silicium (1,1 eV) et préciser si
cette radiation se situe dans le domaine visible.
1.2. L’installation du refuge de Bostan
1.2.1. À l’aide des caractéristiques physiques des panneaux, données
en début d’exercice, montrer que la valeur de la puissance
électrique maximale d’un panneau solaire est de 250 W pour un
ensoleillement de 1000 W.m-2.
1.2.2. Calculer la valeur du rendement énergétique d’un tel panneau
solaire.
1.2.3. Évaluer l’énergie électrique en kWh que l’on peut récupérer par
une belle journée d’été (pour un ensoleillement de 1000 W.m-2)
en prenant en compte les durées de fonctionnement respectives
de chacune des deux installations Sud-Est et Ouest.
1.2.4. À partir des informations suivantes, discuter de la nécessité de la
présence d’un poêle à bois pour le chauffage.
Consommation
Type de Nombre Usage type
moyenne
refuge de lits
journalière
Éclairage, réfrigérateur, petit
Refuge électroménager, traitement
<30 2000 à 5000 Wh/j
moyen UV de l’eau potable.
Éclairage, réfrigérateur,
Refuge 5000 à 15000 congélateur, traitement UV
>30
important Wh/j au minimum de l’eau potable, cuisine,
petit et gros électroménager.
https://www.researchgate.net/publication/269915723_Energie_en_site_isole_d'altitude
22-2DPCMAME1 Page: 15/17
2. Étude du poêle à bois
Informations sur la combustion du bois
Lors de sa combustion, le bois ne fait que libérer le dioxyde de carbone utilisé pour la
croissance de l’arbre dont il est tiré. Selon les règles de l’ADEME, les chauffages au
gaz, au fioul et à l’électricité émettent respectivement 222 kg, 480 kg et environ
180 kg de CO2 par MWh. Le bilan net pour le chauffage au bois est de 40 kg de CO2
émis par MWh.
Ainsi l’utilisation du bois permet de diviser les émissions de CO 2 par 12 par rapport
au fioul et par 6 par rapport au gaz.
https://presse.ademe.fr/wp-content/uploads/2014/11/guide-pratique-se-chauffer-au-bois.pdf
Données :
- Bois : assimilé ici à de la cellulose de formule brute C6H10O5 ;
- Énergie libérée par la combustion, par kilogramme de bois (pouvoir
calorifique) : PC = 4,0 kWh.kg-1 ;
- Masses molaires : M(C) = 12,0 gmol-1 ; M(H) = 1,0 gmol-1 ; M(O) = 16,0 gmol-1 .
2.1. Montrer que la quantité de matière de bois nécessaire à l'obtention d'une
d’énergie de valeur 1 MWh est proche de 1,5 103 mol.
2.2. Calculer alors la masse de dioxyde de carbone libérée lors de la
combustion du bois afin d’obtenir 1MWh d’énergie.
2.3. Expliquer pourquoi la valeur trouvée est très supérieure à celle donnée par
l'ADEME.
Expliquer l’intérêt écologique d’avoir installé un poêle à bois au refuge
plutôt qu’un autre système de chauffage (fioul ou gaz).
3. Aspect « thermique » des panneaux
Les panneaux solaires thermiques fonctionnent grâce à un fluide caloporteur
(mélange eau-propylène glycol) qui y circule et est chauffé par le rayonnement
solaire. Cette énergie thermique est ensuite fournie au ballon d’eau chaude.
Données :
- Formule semi-développée de la molécule de propylène glycol :
Propriétés du propylène glycol
Température de fusion -59 °C
Température d’ébullition 188,2 °C
Miscibilité Miscible à l’eau, l’acétone et l’éthanol
Masse volumique 1036 kgm-3
22-2DPCMAME1 Page: 16/17
3.1. Recopier la formule semi-développée de la molécule de propylène
glycol et entourer les groupes caractéristiques. Nommer ce(s)
groupe(s).
3.2. Expliquer pourquoi on ne peut pas utiliser l’eau pure comme fluide
caloporteur, notamment dans le cas d’un refuge de montagne et
préciser l’intérêt d’employer le propylène glycol.
22-2DPCMAME1 Page: 17/17
Vous aimerez peut-être aussi
- Sti2d Spe Physique Chimie Mathematiques 2022 Metropole Remplacement Sujet OfficielDocument14 pagesSti2d Spe Physique Chimie Mathematiques 2022 Metropole Remplacement Sujet OfficielOlivier PolidoroPas encore d'évaluation
- Modéle 18Document4 pagesModéle 18BOUDALI ZEGMOUTPas encore d'évaluation
- Capture D'écran . 2023-10-24 À 21.39.43Document7 pagesCapture D'écran . 2023-10-24 À 21.39.43ALIENN 51Pas encore d'évaluation
- 2 PT E1 EO 2 EO PT 4. 2 2 PT 5. PT 2: Chimie 16Document2 pages2 PT E1 EO 2 EO PT 4. 2 2 PT 5. PT 2: Chimie 16Emma Nti100% (1)
- Exercices Rli 2 Couche PhysiqueDocument5 pagesExercices Rli 2 Couche PhysiquesevemassePas encore d'évaluation
- Compte Rendu TP Filtrage Et BruitDocument15 pagesCompte Rendu TP Filtrage Et BruitAchraf BemmouinaPas encore d'évaluation
- (WWW - Al7ibre - Com) Contrôle 1 Semestre 1 PC 2bac Sciences Exp Exemple 1Document5 pages(WWW - Al7ibre - Com) Contrôle 1 Semestre 1 PC 2bac Sciences Exp Exemple 1Oussama OussamaPas encore d'évaluation
- DS 7 991 2020-2021 31Document4 pagesDS 7 991 2020-2021 31marcellinvignonPas encore d'évaluation
- TD Général Métrologie Acquisition Master RechercheDocument5 pagesTD Général Métrologie Acquisition Master RechercheAssane SenghorPas encore d'évaluation
- BAC STI2D 2022 - Physique-Chimie Et Maths PolynésieDocument14 pagesBAC STI2D 2022 - Physique-Chimie Et Maths PolynésieLETUDIANT0% (1)
- 1-1-Devoir 1 S 1 PC 2BAC PDFDocument5 pages1-1-Devoir 1 S 1 PC 2BAC PDFmoon100% (3)
- TD Telnum PersoDocument4 pagesTD Telnum PersoMedChoukairiPas encore d'évaluation
- DST 04 Ts 03-04Document3 pagesDST 04 Ts 03-04Enidroun OutPas encore d'évaluation
- TP Crab PDFDocument7 pagesTP Crab PDFthierryPas encore d'évaluation
- TD Supports Trans 2artfi Isge 23 24Document4 pagesTD Supports Trans 2artfi Isge 23 24sawadogofaojiya61Pas encore d'évaluation
- Bac Blanc N4 BiofDocument9 pagesBac Blanc N4 BiofAnas TalhiPas encore d'évaluation
- 8199 E4 U41 Ab Bts TM 2013 Partie 1 SujetDocument6 pages8199 E4 U41 Ab Bts TM 2013 Partie 1 SujetChokri AtefPas encore d'évaluation
- Bac Blanc 1 2013 PDFDocument16 pagesBac Blanc 1 2013 PDFHafidi AhmedPas encore d'évaluation
- 1035a02efs PDFDocument16 pages1035a02efs PDFMohamed0% (1)
- Devoir de Contrôle N°1 2012 2013 (Imed Radhouani)Document5 pagesDevoir de Contrôle N°1 2012 2013 (Imed Radhouani)Sai DaPas encore d'évaluation
- Epreuve Zero de Physiquechimie - Bac Industriel - Session 2023 CamerounDocument4 pagesEpreuve Zero de Physiquechimie - Bac Industriel - Session 2023 Camerounyvankriss3Pas encore d'évaluation
- Exo AcoustiqueDocument7 pagesExo AcoustiqueMohamed DallagiPas encore d'évaluation
- Exercices Corriges 4Document9 pagesExercices Corriges 4Adam El'merzoukiPas encore d'évaluation
- Sujet Aero Septembre Francais 2019Document8 pagesSujet Aero Septembre Francais 2019Nouhad OhPas encore d'évaluation
- SERIE2 CorrigeeDocument7 pagesSERIE2 CorrigeeAhmed Jebbouri100% (1)
- Nu Examen Esa Passage TH - p2 CorrigéDocument10 pagesNu Examen Esa Passage TH - p2 CorrigéTaoufik RouidniPas encore d'évaluation
- Ateliers Et Examens Pratiques de TransmiDocument17 pagesAteliers Et Examens Pratiques de TransmizidPas encore d'évaluation
- PhysiqueDocument3 pagesPhysiqueAurelien jahlibere KinkoengPas encore d'évaluation
- Bruit Thermique Departement de Physique - CompressDocument7 pagesBruit Thermique Departement de Physique - CompressdrapPas encore d'évaluation
- 238-Lab 3-Dephasage RC Serie-H24 2Document9 pages238-Lab 3-Dephasage RC Serie-H24 2aganzecredoPas encore d'évaluation
- Serie N1Document2 pagesSerie N1Hassan DriouachPas encore d'évaluation
- Filtre Passe BasDocument6 pagesFiltre Passe BasYoan NyockPas encore d'évaluation
- Physique Chimie Tsi Exemple 2017Document9 pagesPhysique Chimie Tsi Exemple 2017ZH hasnaePas encore d'évaluation
- Etude D'Un Signal Retrodiffuse: TS2 Photonique Exercices FibresDocument3 pagesEtude D'Un Signal Retrodiffuse: TS2 Photonique Exercices Fibresato ndongo fabricePas encore d'évaluation
- Epreuve U32 Sujet Bts Fed 2023Document8 pagesEpreuve U32 Sujet Bts Fed 2023Je suis Je suisPas encore d'évaluation
- Cadre AirDocument3 pagesCadre AirelkhadimiPas encore d'évaluation
- 2000 13ForumDBO PDFDocument11 pages2000 13ForumDBO PDFMý ÇhãäìÿPas encore d'évaluation
- 2017 Metro STI2D Correction UdPPCDocument7 pages2017 Metro STI2D Correction UdPPCtagueulePas encore d'évaluation
- DEVOIR 2nde D 23-24 DU DEUXIEME TRIMESTREDocument3 pagesDEVOIR 2nde D 23-24 DU DEUXIEME TRIMESTREjustsdedePas encore d'évaluation
- Ateliers Et Examens Pratiques de TransmiDocument17 pagesAteliers Et Examens Pratiques de TransmiMohamed BenrahalPas encore d'évaluation
- Ateliers Et Examens Pratiques de Transmi PDFDocument17 pagesAteliers Et Examens Pratiques de Transmi PDFMohamed BenrahalPas encore d'évaluation
- TP HYDROELECTRICITE Corrigé KAZIDocument8 pagesTP HYDROELECTRICITE Corrigé KAZIÉnoch Kazimoto JuniorPas encore d'évaluation
- 31RS11 PDFDocument8 pages31RS11 PDFMoufida ZouaghiPas encore d'évaluation
- Recette D'une Installation Les 3 Méthodes de TestDocument9 pagesRecette D'une Installation Les 3 Méthodes de TestAbdelhamid SammoudiPas encore d'évaluation
- Fiche TD Serie 3 CHM355Document3 pagesFiche TD Serie 3 CHM355Raphaël DjakbaPas encore d'évaluation
- Modulation de FrequenceDocument19 pagesModulation de Frequenceensetasse100% (1)
- Bepc Jec BepcDocument3 pagesBepc Jec BepcAntoine SawadogoPas encore d'évaluation
- Chap - 10 Exos Proprietes Electriques Des Materiaux CorrigeDocument7 pagesChap - 10 Exos Proprietes Electriques Des Materiaux CorrigeCharles KouaméPas encore d'évaluation
- Epreuve U32 Sujet Bts Fed 2018 GCFDocument9 pagesEpreuve U32 Sujet Bts Fed 2018 GCFJe suis Je suisPas encore d'évaluation
- Sti2d Spe Physique Chimie Mathematiques 2023 Nouvelle Caledonie Sujet OfficielDocument10 pagesSti2d Spe Physique Chimie Mathematiques 2023 Nouvelle Caledonie Sujet Officielyakitori.yaya2006Pas encore d'évaluation
- Controle 2017Document4 pagesControle 2017Khaled LechhebPas encore d'évaluation
- Solution TD1Document4 pagesSolution TD1faycalboughedda234Pas encore d'évaluation
- SP 2004Document34 pagesSP 2004BarackPas encore d'évaluation
- Devoir 3è PCDocument2 pagesDevoir 3è PCAdams KOURAOGO100% (1)
- 2023 SujetDocument14 pages2023 SujetBen RachidPas encore d'évaluation
- Examen 04 02 2005Document7 pagesExamen 04 02 2005Mohamed DallagiPas encore d'évaluation
- TP 1Document6 pagesTP 1mouna zouaouiPas encore d'évaluation
- Livret Lansad University of Clermont Ferrand FranceDocument30 pagesLivret Lansad University of Clermont Ferrand FranceAlessandro PasseraPas encore d'évaluation
- Dossier PCRSDocument2 pagesDossier PCRSBachir FethizaPas encore d'évaluation
- Introduction À L - Épistémologie - A. Virieux-ReymondDocument12 pagesIntroduction À L - Épistémologie - A. Virieux-ReymondErwan MorelPas encore d'évaluation
- Devis EstimatifDocument4 pagesDevis EstimatifAnonymous FIZzeYDCgpPas encore d'évaluation
- Cours AJEL Université de Bordj Bou Arreridj PDFDocument24 pagesCours AJEL Université de Bordj Bou Arreridj PDFRe Sab RinaPas encore d'évaluation
- Optique Géométrique SMPDocument36 pagesOptique Géométrique SMPMOHAMMED ZAKARIA BAALIPas encore d'évaluation
- M Arnaud LerayDocument298 pagesM Arnaud LerayphysiotobiePas encore d'évaluation
- Lean ManagementDocument21 pagesLean ManagementNadhir NadPas encore d'évaluation
- RECAP - DPS - Atteintes À La Nation, À L'état Et À La Paix PubliqueDocument1 pageRECAP - DPS - Atteintes À La Nation, À L'état Et À La Paix PubliquedelphouPas encore d'évaluation
- Fascicule IcDocument21 pagesFascicule IcWagane FAYEPas encore d'évaluation
- La Cité de La Peur - ScriptDocument26 pagesLa Cité de La Peur - Scriptjbkern1431Pas encore d'évaluation
- Crédit ScoringDocument11 pagesCrédit ScoringAshraf Borzym100% (1)
- TDR - Perso 2 PCI AFRISTATDocument3 pagesTDR - Perso 2 PCI AFRISTATVanawaPas encore d'évaluation
- La Petite Danseuse de Quatorze Ans by Laurens CamilleDocument104 pagesLa Petite Danseuse de Quatorze Ans by Laurens CamilleClarisse Meunier100% (1)
- Avantis 70 HV - Fenêtres en Aluminium Avec Ouvrant Caché - Sapa Building SystemDocument12 pagesAvantis 70 HV - Fenêtres en Aluminium Avec Ouvrant Caché - Sapa Building SystemSapa Building SystemPas encore d'évaluation
- Processus de RecrutementDocument8 pagesProcessus de Recrutementnassy13100% (1)
- Hippolyte - Commentaire Sur DanielDocument200 pagesHippolyte - Commentaire Sur DanielAnatolie26100% (1)
- dpt06 Service - Tourisme Clef VerteDocument1 pagedpt06 Service - Tourisme Clef Verteoumayma oufirPas encore d'évaluation
- LIVRESCOLAIRE 2nde - Livre Du Professeur - Chapitre 10 - Statistiques DescriptivesDocument28 pagesLIVRESCOLAIRE 2nde - Livre Du Professeur - Chapitre 10 - Statistiques DescriptivesplumagathaPas encore d'évaluation
- Formation SpssDocument33 pagesFormation Spsslfg fsegn100% (1)
- Glucides (NXPowerLite)Document131 pagesGlucides (NXPowerLite)Mohamed Habib BrinsiPas encore d'évaluation
- Catalogo 2021 FraDocument17 pagesCatalogo 2021 FraMarvin PathPas encore d'évaluation
- AtheismeDocument27 pagesAtheismeElena ErmolieffPas encore d'évaluation
- IMSLP569176 PMLP917211 Me Thode - Pour - La - Trompette - Pre Ce de e - ... Methode - 1Document83 pagesIMSLP569176 PMLP917211 Me Thode - Pour - La - Trompette - Pre Ce de e - ... Methode - 1wwdlvjhumgr100% (1)
- Fiche Analyse Du Cycle de VieDocument2 pagesFiche Analyse Du Cycle de VieAndré TuoPas encore d'évaluation
- B-P-U Tout Laes PartiesDocument18 pagesB-P-U Tout Laes PartiesSabri RemremPas encore d'évaluation
- Troubles NVDocument26 pagesTroubles NVEccoPas encore d'évaluation
- Plano - Topografico - de - La - Ciudad - de Caracas - Siglo XIXDocument3 pagesPlano - Topografico - de - La - Ciudad - de Caracas - Siglo XIXEloisaOTPas encore d'évaluation
- ESE Solar - Schéma de Principe SSC Avec Module Production ECS Instantanée - V2Document1 pageESE Solar - Schéma de Principe SSC Avec Module Production ECS Instantanée - V2monnomPas encore d'évaluation
- Les Cahiers de Droit: François OstDocument28 pagesLes Cahiers de Droit: François OstPaul BununuPas encore d'évaluation