Académique Documents
Professionnel Documents
Culture Documents
B5.2 Sujet TP1 - Dosage Par Étalonnage Et Incertitudes
Transféré par
penelopeouali2006Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
B5.2 Sujet TP1 - Dosage Par Étalonnage Et Incertitudes
Transféré par
penelopeouali2006Droits d'auteur :
Formats disponibles
Thème : matière TP1 dosage par étalonnage du sérum physiologique
TP1 DOSAGE PAR ETALONNAGE DU SERUM PHYSIOLOGIQUE
NOM :
Compétence APP REA CON ANA VAL COM NOTE
points
Sur
Objectif : Mesurer une conductance.
Tracer une courbe d’étalonnage pour déterminer une concentration.
Estimer et calculer des incertitudes-type de type A et B.
L’étiquette d’une unidose de sérum physiologique précise : "Chlorure de sodium 0,9 %" soit une
concentration en chlorure de sodium NaCl de 9,0 g/L. Votre travail est de vérifier cette indication à l’aide
d’un dosage par étalonnage conductimétrique.
Document 1 : Sérum physiologique
Le sérum physiologique est composé de chlorure de sodium et d'eau purifiée, de même composition
moléculaire que le plasma sanguin. Il est conseillé chez le nourrisson, l'enfant et l'adulte pour l'hygiène
nasale, le rinçage oculaire, le lavage des plaies. Il peut être injecté par voie veineuse pour réhydrater un
patient. Par mesure d’hygiène, une unidose entamée ne doit pas être conservée plus de 24h.
http://www.plurielles.fr/sante-forme/le-serum-physiologique-definition-et-utilisations-wcod157837.html
S’APPROPRIER
Document 2 : Conductance et conductivité d’une solution
La conductance G caractérise la capacité d’une portion de solution ionique à conduire le courant, elle
s’exprime en Siemens (S) et varie comme l’inverse de la résistance R de cette portion de solution. La
conductance dépend de la concentration et la nature des ions en solution, de la température, du solvant,
et de la forme de la cellule de mesure.
I
G =
U
i : intensité (en A) ; u : tension (en V) ; G : conductance (en S ou Ω-1)
La conductivité σ d’une solution ionique caractérise son aptitude à conduire le courant électrique
indépendamment des caractéristiques de la cellule de mesure (surface immergée des électrodes S et
distance L les séparant). Elle est proportionnelle à la conductance selon la relation :
L
σ = kcell .G avec kcell =
S
S surface (en m²) ; L distance (en m) ; σ conductivité (en S.m-1)
On souhaite, dans un premier temps, vérifier la relation entre la conductance et la
conductivité évoquée dans le document 2.
➢ Réaliser le montage ci – contre. Le bécher contiendra 100 mL d’une solution
de chlorure de sodium (Na+(aq), Cl-(aq)) à 1,0 x 10-2 mol.L-1.
➢ Allumer le GBF et lire les valeurs de U et I sur les multimètres.
Spécialité physique – chimie terminale
Thème : matière TP1 dosage par étalonnage du sérum physiologique
➢ Enlever les électrodes du bécher et y plonger la sonde conductimétrique reliée au conductimètre
étalonné. Relever la valeur de la conductivité.
1) Donner le schéma électrique en justifiant les positions de l’ampèremètre et du voltmètre.
2) Calculer la conductance de la solution et la constante de cellule.
3) Exprimer la conductivité de la solution en fonction de I, U, L et S puis la calculer.
4) À l’aide de de la fiche méthode, déterminer l’incertitude-type pour la conductivité u(σ).
5) Comparer la valeur mesurée de la conductivité à la valeur de référence obtenue à l’aide du conductimètre
et conclure (voir fiche méthode).
En pratique, un conductimètre mesure la conductance de la portion de solution entre les deux plaques de
l’électrode et transforme en conductivité grâce à la connaissance de la constante de cellule déterminée
automatiquement au cours de l’étalonnage.
REALISER
Document 3 : la loi de Kohlraush
σ = Σi.λi.[Xi]
λi la conductivité molaire ionique de l’ion i de concentration [Xi] dans la solution.
Dans le cas d’une solution obtenue par dissolution d’un solide ionique de concentration C, la conductivité
de la solution est proportionnelle à la concentration des espèces ioniques en solutions.
On procède au dosage par étalonnage conductimétrique du chlorure de sodium dans la solution.
➢ À l’aide du matériel disponible, compléter le tableau en indiquant le volume de solution mère à
prélever pour réaliser 100 mL de chaque solution fille. Détailler les calculs pour réaliser S3.
Solution fille S1 S2 S3 S4
Concentration Ci en mol.L-1 2,5 x 10-3 2 x 10-3 1 x 10-3 5 x 10-4
Volume Vi de solution mère à prélever en mL
σ en μS/cm
➢ Réaliser la solution S1 et la transvaser dans un bécher de 100 mL.
➢ Mesurer la conductivité de la solution et noter la valeur dans le tableau.
➢ Recommencer les 2 étapes précédentes pour les solutions S2, S3, S4.
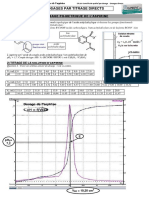
➢ Tracer sur un tableur le graphique σ = f(C) pour ces solutions étalons ainsi que la droite d’étalonnage.
Imprimer le graphique obtenu avec l’équation de la droite d’étalonnage.
➢ Mesurer la conductivité de la solution de sérum physiologique dilué 80 fois puis déterminer sa
concentration à l’aide de l’équation de la droite d’étalonnage.
ANALYSER
6) Déterminer la concentration molaire puis massique du sérum physiologique non dilué en chlorure de
sodium.
7) À l’aide de la fiche méthode à compléter déterminer l’incertitude-type de type A sur la concentration et
la comparer à la valeur de référence (voir Fiche méthode).
VALIDER
8) En utilisant la loi de Kohlraush, montrer que la conductivité d’une solution d’une solution de chlorure de
sodium de concentration C s’écrit : σ = (λNa+ + λCl-).C.
9) En déduire la valeur théorique du coefficient directeur de la droite et le comparer à la valeur obtenue
expérimentalement. (λNa+ = 5,0 x 10-3 S.m².mol-1 ; λCl- = 7,6 x 10-3 S.m².mol-)1.
Spécialité physique – chimie terminale
Vous aimerez peut-être aussi
- Chapitre C3 ConductimetrieDocument5 pagesChapitre C3 ConductimetrieLahcen Ben SalmPas encore d'évaluation
- 9-tp Dosage Srum PDFDocument3 pages9-tp Dosage Srum PDFWassim Hamdan0% (1)
- TPchim3 Cinetique SaponificationDocument3 pagesTPchim3 Cinetique SaponificationKESSAB MOHAMEDPas encore d'évaluation
- Chapitre C3 Conductimetrie PDFDocument5 pagesChapitre C3 Conductimetrie PDFMANSOURIPas encore d'évaluation
- 1059 TP Doser Par ConductimetrieDocument3 pages1059 TP Doser Par ConductimetrieAli TrikiPas encore d'évaluation
- Conductim PDFDocument4 pagesConductim PDFMokhtarBensaidPas encore d'évaluation
- Conductivite Des SolutionsDocument4 pagesConductivite Des Solutionsmohamed laghribPas encore d'évaluation
- CHAPITRE III La SolubilitéDocument9 pagesCHAPITRE III La Solubilitéfullhd qatkaPas encore d'évaluation
- Preparation Des SolutionsDocument4 pagesPreparation Des Solutionsmad469469Pas encore d'évaluation
- Travaux Pratique 4 de ChimieDocument5 pagesTravaux Pratique 4 de ChimiekaderPas encore d'évaluation
- Chapitre IDocument12 pagesChapitre INak awadPas encore d'évaluation
- TP D'éléctrochimieDocument7 pagesTP D'éléctrochimieHanou BouPas encore d'évaluation
- Chap.6 TP12 Titrage PH Metrique D Un Vinaigre Correction PDFDocument2 pagesChap.6 TP12 Titrage PH Metrique D Un Vinaigre Correction PDFYouSsef EchafaiPas encore d'évaluation
- dc3 4eme Sadiki 12 MathsDocument5 pagesdc3 4eme Sadiki 12 MathsLotfi BoucharebPas encore d'évaluation
- Newcours Seance1 Vitesse Réaction Chap1.Ppt 0Document35 pagesNewcours Seance1 Vitesse Réaction Chap1.Ppt 0mohammed laadiliPas encore d'évaluation
- DM PhysiqueDocument5 pagesDM Physiqueالقي السمع وٱفتح قلبكPas encore d'évaluation
- TP N 3 Chimie Sem1 2022 Sujet IodometrieDocument4 pagesTP N 3 Chimie Sem1 2022 Sujet IodometrieRaouf RamoulPas encore d'évaluation
- BAC Physique-Chimie-Specialite 2009 SDocument11 pagesBAC Physique-Chimie-Specialite 2009 SLetudiant.fr100% (7)
- TP DissolutionDocument8 pagesTP DissolutionNadia amelPas encore d'évaluation
- Série 1 2022-2023Document2 pagesSérie 1 2022-2023Zineb Sassi100% (1)
- Partie1 CorriDocument31 pagesPartie1 CorriMeryam MessaoudiPas encore d'évaluation
- 2005 Reunion Sujet Exo2 Ammoniac 6 5ptsDocument3 pages2005 Reunion Sujet Exo2 Ammoniac 6 5ptsla physique selon le programme Français100% (1)
- FICHE Dosage WebDocument4 pagesFICHE Dosage Webفيديو بالعربيPas encore d'évaluation
- TP1 Transformations Lentes Ou Rapides 2-Correction PDFDocument5 pagesTP1 Transformations Lentes Ou Rapides 2-Correction PDFIkram ChamixoPas encore d'évaluation
- TP2 Chimie MineralDocument7 pagesTP2 Chimie MineralNà ZimPas encore d'évaluation
- Cours Dynamique Des StructuresDocument2 pagesCours Dynamique Des StructuresAbderrahim Boulanouar100% (1)
- Python Exemple 3Document2 pagesPython Exemple 3Lazhar BOUCHAOURPas encore d'évaluation
- Tp11 Deshydratation Methylbutan 2 OlDocument3 pagesTp11 Deshydratation Methylbutan 2 Olالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- tp13 Cinetique Catalyse CorrigeDocument2 pagestp13 Cinetique Catalyse CorrigePR〇FESS〇R・MPas encore d'évaluation
- Exercices Corriges Equilibrer Des Reactions Nucleaires Reaction de Fusion Dans Le SoleilDocument3 pagesExercices Corriges Equilibrer Des Reactions Nucleaires Reaction de Fusion Dans Le Soleilroudy100% (1)
- Activité Chapitre 4 Chimie Facteurs Cinétiques Et de LDocument3 pagesActivité Chapitre 4 Chimie Facteurs Cinétiques Et de LMalia TATEPas encore d'évaluation
- TPCorrCeFe 4Document2 pagesTPCorrCeFe 4Amelie Pinchon100% (1)
- Titrages Acido-Basiques PDFDocument4 pagesTitrages Acido-Basiques PDFtarikPas encore d'évaluation
- TP Chimie n1Document2 pagesTP Chimie n1Oussoufi Mze Kaanbi100% (2)
- TSP2SP1Ch18T11-TP10 Corrige Destop AspirineDocument5 pagesTSP2SP1Ch18T11-TP10 Corrige Destop AspirineAyoub AinanePas encore d'évaluation
- Chapitre 2, Suivi Temporel D'une Transformation Chimique, Cours, Activités, Exercices D'application, 2BAC BIOF PR JENKAL RACHIDDocument11 pagesChapitre 2, Suivi Temporel D'une Transformation Chimique, Cours, Activités, Exercices D'application, 2BAC BIOF PR JENKAL RACHIDKarim EL HAJJIPas encore d'évaluation
- Exercices ConductivitéDocument4 pagesExercices ConductivitéAya AyaaaPas encore d'évaluation
- 11.les Dosages Redox 1Document6 pages11.les Dosages Redox 1Souad MahiPas encore d'évaluation
- TP ThermoDocument7 pagesTP Thermosofia safaaPas encore d'évaluation
- Cinetique ChimiqueDocument4 pagesCinetique ChimiqueHoussam MazouzPas encore d'évaluation
- TS-TP No4 - cinetique-H2O2 I2 Thios-EvalueDocument4 pagesTS-TP No4 - cinetique-H2O2 I2 Thios-EvalueMLAN Hesna100% (2)
- Compte Rendu TP 2 ÉlectrochimieDocument8 pagesCompte Rendu TP 2 ÉlectrochimieAbdessemed Shiraz NadaPas encore d'évaluation
- ch13 Separation Extraction BenzocaineDocument3 pagesch13 Separation Extraction Benzocaineالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Cours - Chimie - Solubilité Et Précipitation Des Électrolytes - 3ème Informatique (2017-2018) MR Hedfi KhemaisDocument3 pagesCours - Chimie - Solubilité Et Précipitation Des Électrolytes - 3ème Informatique (2017-2018) MR Hedfi KhemaisBAATOUT OUMAIMAPas encore d'évaluation
- Controle Dosage1sDocument2 pagesControle Dosage1sKhalid khalid100% (1)
- Acides Et Bases Selon BrönstedDocument3 pagesAcides Et Bases Selon BrönstedLotfi Chimie100% (1)
- 2010 AmNord Exo1 Sujet Eau 6 5ptsDocument3 pages2010 AmNord Exo1 Sujet Eau 6 5ptsHarakat ElhoucinePas encore d'évaluation
- Cin Exo PDFDocument10 pagesCin Exo PDFImed SeghierPas encore d'évaluation
- Chapitre 5 La Cinetique ChimiqueDocument11 pagesChapitre 5 La Cinetique Chimiquemarwan2nouichiPas encore d'évaluation
- Corrosion Et ProtectionDocument3 pagesCorrosion Et ProtectionMariam ZouhairPas encore d'évaluation
- Serie de RevisionDocument3 pagesSerie de Revisionacademie archimedePas encore d'évaluation
- TP Cinetique ChimiqueDocument1 pageTP Cinetique ChimiqueAyoub GuerriPas encore d'évaluation
- Electrolytes CoursDocument4 pagesElectrolytes CoursOussama El Bouadi100% (2)
- Exercice 1 (7 Points) Cinétique de La Décomposition de L'eau OxygénéeDocument8 pagesExercice 1 (7 Points) Cinétique de La Décomposition de L'eau Oxygénéeأمال بلقاسم100% (1)
- Devoir de Synthèse N°2 2011 2012 (Mtarrab Badr) (Elahd Eljadid Douz)Document3 pagesDevoir de Synthèse N°2 2011 2012 (Mtarrab Badr) (Elahd Eljadid Douz)Moufida ZouaghiPas encore d'évaluation
- Activite1 Dosage Conductimetrique Par ComparaisonDocument4 pagesActivite1 Dosage Conductimetrique Par ComparaisonCharbonPas encore d'évaluation
- Conductance Et Conductivité 1BAC Int EL AAMRANIDocument5 pagesConductance Et Conductivité 1BAC Int EL AAMRANIfatima marradoPas encore d'évaluation
- S4 - Conductance Et Conductivité - 1BAC - IntDocument5 pagesS4 - Conductance Et Conductivité - 1BAC - Intchakourali67Pas encore d'évaluation
- T.D. N°2 - Les AmortissementsDocument3 pagesT.D. N°2 - Les Amortissementsangelinaa.bento05Pas encore d'évaluation
- Fin OofDocument24 pagesFin OofAhmed Ouss0% (1)
- Guide de Logiciel Sap20000 CopierDocument54 pagesGuide de Logiciel Sap20000 CopierAbdou HababaPas encore d'évaluation
- RégimeDocument12 pagesRégimeernestito2010Pas encore d'évaluation
- Cour 1 - VirtualisationDocument24 pagesCour 1 - Virtualisationjeremie zehouPas encore d'évaluation
- Boc 20221230Document23 pagesBoc 20221230electronicsobed the son of GODPas encore d'évaluation
- UltrafiltrationDocument10 pagesUltrafiltrationsoufyanePas encore d'évaluation
- Gagner de L'argent Avec YoutubeDocument7 pagesGagner de L'argent Avec Youtubeanon_811149744Pas encore d'évaluation
- Guide Investir Dans Les PME en AfriqueDocument74 pagesGuide Investir Dans Les PME en AfriquePDG EYAFPas encore d'évaluation
- InstallationDocument9 pagesInstallationfatihaPas encore d'évaluation
- Premier Exercice: (7 Points) Chauffe-Eau Solaire: Lire Attentivement L'extrait Suivant Puis Répondre Aux QuestionsDocument4 pagesPremier Exercice: (7 Points) Chauffe-Eau Solaire: Lire Attentivement L'extrait Suivant Puis Répondre Aux QuestionsHouda ChanPas encore d'évaluation
- 3eme Biochimie 2019-2020 Bouzidi A L3 Bioch Cours ToxicologieDocument14 pages3eme Biochimie 2019-2020 Bouzidi A L3 Bioch Cours ToxicologieM.B. IsmailPas encore d'évaluation
- Audit Cycle VenteDocument38 pagesAudit Cycle VenteaminePas encore d'évaluation
- Document 1249Document11 pagesDocument 1249MrYodaaPas encore d'évaluation
- Question Et Réponse 4Document15 pagesQuestion Et Réponse 4saraPas encore d'évaluation
- Mouteur DCDocument7 pagesMouteur DCElmokh LassaadPas encore d'évaluation
- UM Operation Manual FRFR 27021611646554123Document299 pagesUM Operation Manual FRFR 27021611646554123Georges TaradauxPas encore d'évaluation
- Entretien Du Reseau D'Eclairage Public Au Sein de La CommuneDocument24 pagesEntretien Du Reseau D'Eclairage Public Au Sein de La CommuneMProd AmmoPas encore d'évaluation
- Katalogs-19-Fusibles A Couteaux NHDocument8 pagesKatalogs-19-Fusibles A Couteaux NHhakimPas encore d'évaluation
- Practice+exam+chap+3 - 1 - 1Document7 pagesPractice+exam+chap+3 - 1 - 1Box OfficePas encore d'évaluation
- L1 - GPL - Cours Numéro 01 La QualitéDocument13 pagesL1 - GPL - Cours Numéro 01 La Qualitéformation distancePas encore d'évaluation
- TP 02 La Masse VolumiqueDocument5 pagesTP 02 La Masse VolumiqueDai MentPas encore d'évaluation
- These ND PAreconf VF PDFDocument174 pagesThese ND PAreconf VF PDFRachid HamianiPas encore d'évaluation
- Tome 2 Impacts EnvironnementauxDocument49 pagesTome 2 Impacts EnvironnementauxUlrich Ralph NjoyaPas encore d'évaluation
- T 200 IDocument36 pagesT 200 Iref100% (1)
- Réussir Aux Différentes Évaluations D'un Entretien Part 1Document30 pagesRéussir Aux Différentes Évaluations D'un Entretien Part 1Daniel Constant AttaPas encore d'évaluation
- François Brune - La Vierge Du MexiqueDocument681 pagesFrançois Brune - La Vierge Du MexiquethanosPas encore d'évaluation
- D61PXi MoniteurDocument38 pagesD61PXi MoniteurXavier FontainePas encore d'évaluation
- UN ASPECT MÉCONNU D'AVALOKITEŚVARA - de MallmannDocument9 pagesUN ASPECT MÉCONNU D'AVALOKITEŚVARA - de MallmannClaudia RamassoPas encore d'évaluation
- Aid Memoire XP 18-545Document2 pagesAid Memoire XP 18-545Lotfi Merabet75% (4)