Académique Documents
Professionnel Documents
Culture Documents
DS1 TS2 Ecole Excellence
Transféré par
Naouma ChahdCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
DS1 TS2 Ecole Excellence
Transféré par
Naouma ChahdDroits d'auteur :
Formats disponibles
20 Septembre 2023
- DEVOIR SURVEILLE N°1 - Durée : 60 min
CONSIGNES DE RÉDACTION :
Tout calcul et toute réponse devront être justifiés si vous voulez qu’il ou elle soit pris(e) en compte. Il est demandé de faire attention
au soin et à la présentation. Par souci de clarté, vous encadrerez en rouge l’expression littérale de la grandeur recherchée, et vous
soulignerez son application numérique.
EXERCICE 1 : COURS DE CHIMIE (~ 5 MIN) A FAIRE SUR L’ANNEXE
EXERCICE 2 : (~ 20 MIN)
1) Donner les demi-équations d’oxydo-réduction des couples oxydant/réducteur suivants :
NO3- (aq) / NO(g) ; Cu2+(aq)/Cu(s) ; MnO4-(aq)/Mn2+(aq) ; Fe3+(aq)/Fe2+(aq) ; IO3-(aq)/I2(aq) ; I2(aq)/I-(aq).
2) Écrire les équations des réactions :
a. de l’ion nitrate et du métal cuivre (en milieu acide) ;
b. de l’ion fer(II) et permanganate (en milieu acide) ;
c. de la dismutation du diiode (en milieu basique).
EXERCICE 3 : ÉTUDE D’UNE RÉACTION D’OXYDOREDUCTION (~ 30 MIN)
On s’intéresse aux couples oxydant / réducteur suivants : H2O2 (aq) / H2O (l) et I2 (aq) / I- (aq).
Les expériences qui suivent sont réalisées en milieu acide, la température des solutions est de 20°C.
Première expérience :
Dans un erlenmeyer, on mélange 10 mL d’une solution aqueuse de diiode I 2 (aq) à une
concentration égale à 1,0×10-3 mol.L-1 avec 40 mL d’eau acidifiée. La solution a une coloration
brune, et aucun changement d’aspect n’est observé au bout de 10 minutes.
Deuxième expérience :
Dans un erlenmeyer, on mélange 20 mL d’une solution aqueuse d’eau oxygénée, H 2O2 (aq) à
1,0×10-1 mol.L-1 avec 20 mL d’une solution aqueuse acidifiée d’iodure de potassium , (K +(aq)+ I-(aq))
à 5,0×10-1 mol.L-1. Au bout de 10 minutes, la solution initialement incolore s’est colorée en brun.
1) a. Quelle est l’espèce chimique en solution responsable de la coloration brune ?
b. À partir des observations précédentes (expérience 2), indiqué quels sont l’oxydant et le réducteur qui
réagissent ensemble.
c. En déduire l’équation de la réaction d’oxydoréduction considérée.
d. Pourquoi est-il nécessaire de travailler en milieu acide ?
e. Compléter littéralement le tableau d’avancement donné en annexe.
f. En déduire xmax et le réactif qui limite la transformation étudiée.
2) On dispose d’un bain-marie à 0°C et d’un autre à 60°C. Quel bain-marie faut-il utiliser pour diminuer la
durée de la transformation ? Justifier.
Troisième expérience :
À 20°C et en milieu acide, on mélange 20 mL d’une solution aqueuse d’eau oxygénée H 2O2 (aq) à 1,0×10-1
mol.L-1, avec 20 mL d’une solution aqueuse acidifiée d’iodure de potassium à 8,0×10-1 mol.L-1.
3) Compléter numériquement le tableau d’avancement donné en annexe pour la troisième expérience.
4) La coloration brune de la solution à l’état final est-elle la même que lors de la deuxième expérience ?
5) Lors de quelle expérience l’état final du système sera-t-il atteint le plus vite ? Justifier.
1
École d’Excellence - Mr. Saleban - Année 2023 / 2024
Nom : ……………………………………………………………………………………………………… TS2
- FEUILLE ANNEXE -
EXERCICE 1 : COURS DE CHIMIE
1) Un oxydant est une espèce chimique capable de .................................. un ..................................
Il subit alors une ................................................
2) On considère l’équation de la réaction de titrage suivante : aA + bB cC + dD
a) Donner la définition du titrage d’une espèce chimique.
…………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………
b) La réaction de titrage est-elle une transformation lente ? Si non, définir une transformation lente.
…………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………
3) Le couple H+(aq) / H2 (g) est-il un couple acido-basique ou d’oxydoréduction ?
Écrire la demi-équation correspondante.
…………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………
…………………………………………………………………………………………………………………………………………………………
EXERCICE 3 : ÉTUDE D’UNE RÉACTION D’OXYDOREDUCTION
Deuxième expérience : Tableau d’avancement à compléter littéralement
Réaction
t=0 x=0
t x
t xmax
Troisième expérience : Tableau d’avancement à compléter numériquement
Réaction
t=0 x=0
t X
xmax =
t …………………
École d’Excellence - Mr. Saleban - Année 2023 / 2024
Vous aimerez peut-être aussi
- Devoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2021-2022) MR ZAOUAM ABDELHAMID-1Document3 pagesDevoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2021-2022) MR ZAOUAM ABDELHAMID-1firas marsawiPas encore d'évaluation
- Seq1 4èDocument3 pagesSeq1 4èMineur NdieulaPas encore d'évaluation
- Devoir 5 - 2019Document2 pagesDevoir 5 - 2019boumalik mohamedPas encore d'évaluation
- TP N 3 Chimie Sem1 2022 Compte RenduDocument2 pagesTP N 3 Chimie Sem1 2022 Compte RenduHîş TörîăPas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2020-2021) MR KHCHINI KAMELDocument4 pagesDevoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2020-2021) MR KHCHINI KAMELwalidPas encore d'évaluation
- Cinetique ChimiqueDocument4 pagesCinetique ChimiqueHoussam MazouzPas encore d'évaluation
- SMPC S2 Exam 2016Document4 pagesSMPC S2 Exam 2016Abdelhakim BailalPas encore d'évaluation
- 22 23 Devoir de Controle N2.1annee DYDocument4 pages22 23 Devoir de Controle N2.1annee DYslouati470Pas encore d'évaluation
- SMC S3 Ratt 2021Document7 pagesSMC S3 Ratt 2021Abdelhakim BailalPas encore d'évaluation
- Devoir de Synthèse N°3 - Sciences Physiques - 2ème Sciences (2010-2011) MR Adam Bouali 2Document4 pagesDevoir de Synthèse N°3 - Sciences Physiques - 2ème Sciences (2010-2011) MR Adam Bouali 2walidPas encore d'évaluation
- Devoir de Controle N°2: A - CHIMIE:8 PointsDocument3 pagesDevoir de Controle N°2: A - CHIMIE:8 PointsHanine HmidaPas encore d'évaluation
- A.E C6 Decomposition Thermique de NaHCO3 2020-2021 MBADocument4 pagesA.E C6 Decomposition Thermique de NaHCO3 2020-2021 MBAtania biardPas encore d'évaluation
- Devoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2013-2014) MR Mesrati AliDocument2 pagesDevoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2013-2014) MR Mesrati AliimedPas encore d'évaluation
- DC2 1ERE FEV 2024 MR Malki ADocument3 pagesDC2 1ERE FEV 2024 MR Malki AmanelbelhajlakdarPas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2021-2022) MR Fethi JellitiDocument2 pagesDevoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2021-2022) MR Fethi JellitichihebPas encore d'évaluation
- Controle 1 - 11 S1 1AC InterDocument4 pagesControle 1 - 11 S1 1AC InterAMIN100% (1)
- Devoir de Contrôle N°3: Chimie (6 Points) : Exercice N° 1 (3 PTS)Document2 pagesDevoir de Contrôle N°3: Chimie (6 Points) : Exercice N° 1 (3 PTS)Hammadi RekikPas encore d'évaluation
- Devoir de Contrôle N°2 - Physique - 2ème Sciences Exp (2006-2007)Document8 pagesDevoir de Contrôle N°2 - Physique - 2ème Sciences Exp (2006-2007)Boubaker ChaabaniPas encore d'évaluation
- Devoir Physique 1 Éme AnnéeDocument5 pagesDevoir Physique 1 Éme Annéedali.info.servicePas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2016-2017) MR ARYANI AhmedDocument2 pagesDevoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2016-2017) MR ARYANI AhmedMohamed HamdenePas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2010-2011) Mme Liala 2Document4 pagesDevoir de Contrôle N°2 - Sciences Physiques - 1ère AS (2010-2011) Mme Liala 2AliMchirguiPas encore d'évaluation
- Transformation Lente Et Rapide: ActivitésDocument6 pagesTransformation Lente Et Rapide: ActivitésAbd Elmooti HijaziPas encore d'évaluation
- Dev Synt2 1ereDocument3 pagesDev Synt2 1ereSahbi Mabrouki YamenPas encore d'évaluation
- Simili 2 À Distance SMDocument7 pagesSimili 2 À Distance SMSAIDPas encore d'évaluation
- 01 Controle #3 Semestre 2Document6 pages01 Controle #3 Semestre 2JOKER YTPas encore d'évaluation
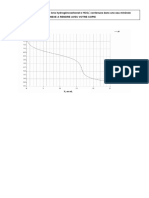
- Titration Curves & Buffers 9701Document46 pagesTitration Curves & Buffers 9701Mansimar KaurPas encore d'évaluation
- Examen Local PC - Janvier 2020 - Collège Ibn Hamdoune Kertili - Meknes FR (WWW - Pc1.ma) - 2Document2 pagesExamen Local PC - Janvier 2020 - Collège Ibn Hamdoune Kertili - Meknes FR (WWW - Pc1.ma) - 2hakilsd9Pas encore d'évaluation
- Devoir de Controle N 3 Physique 1ere As 2009 2010 MR Khemili Lotfi 3Document3 pagesDevoir de Controle N 3 Physique 1ere As 2009 2010 MR Khemili Lotfi 3HanajPas encore d'évaluation
- Sujet CAP B Juin2018Document10 pagesSujet CAP B Juin2018franckPas encore d'évaluation
- Examen Normalisé 2023 - V.ADocument3 pagesExamen Normalisé 2023 - V.Anetflix2p099Pas encore d'évaluation
- Devoir de Contrôle N°1 2009 2010 (Abdelhakim) (Menzel Temime Nabeul)Document5 pagesDevoir de Contrôle N°1 2009 2010 (Abdelhakim) (Menzel Temime Nabeul)wajdidirom123Pas encore d'évaluation
- Devoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2013-2014) MR Omri RafikDocument2 pagesDevoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2013-2014) MR Omri RafikMohamed HamdenePas encore d'évaluation
- Devoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2019-2020) MR Sdiri AnisDocument3 pagesDevoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2019-2020) MR Sdiri AnisKarem SaadPas encore d'évaluation
- DSN2-1ere 2021.Document3 pagesDSN2-1ere 2021.Boussetta ZouhaierPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - 1ère AS (2012-2013) MR JLIDI NABILDocument0 pageDevoir de Contrôle N°1 - Sciences Physiques - 1ère AS (2012-2013) MR JLIDI NABILMouf55Pas encore d'évaluation
- 05 Controle #3 Semestre 1Document2 pages05 Controle #3 Semestre 1hoissinekhadija59Pas encore d'évaluation
- Devoir de Contrôle N°3 - Sciences Physiques - 1ère AS (2010-2011) MR Adam Bouali 2Document3 pagesDevoir de Contrôle N°3 - Sciences Physiques - 1ère AS (2010-2011) MR Adam Bouali 2Mariem MouPas encore d'évaluation
- Edp Hilbert1718Document50 pagesEdp Hilbert1718Rachid KridiPas encore d'évaluation
- Devoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2013-2014) MR Alibi AnouarDocument3 pagesDevoir de Synthèse N°2 - Sciences Physiques - 1ère AS (2013-2014) MR Alibi AnouarimedPas encore d'évaluation
- SMPC s2 Exam 2016Document5 pagesSMPC s2 Exam 2016Abdelhakim BailalPas encore d'évaluation
- Ds PhysiqueDocument4 pagesDs PhysiqueLamya LoukiliPas encore d'évaluation
- Évaluation À Domicile N°2 3AC 2023 2024Document2 pagesÉvaluation À Domicile N°2 3AC 2023 2024mohamedlehardouz157Pas encore d'évaluation
- TP 15 1s9 Notion de Reaction ChimiqueDocument2 pagesTP 15 1s9 Notion de Reaction ChimiquesaanounPas encore d'évaluation
- EVAL 1 PCT 4e RRDocument2 pagesEVAL 1 PCT 4e RRTAKOUO LEDOUXPas encore d'évaluation
- Devoir de Contrôle N°3 - Physique - 1ère AS (2015-2016) MR Bayrem GhidaouiDocument3 pagesDevoir de Contrôle N°3 - Physique - 1ère AS (2015-2016) MR Bayrem GhidaouiwalidPas encore d'évaluation
- Examne Locale 1 - Janvier 2023Document2 pagesExamne Locale 1 - Janvier 2023Home erriahiPas encore d'évaluation
- Ais 2122 2apic S1 C3 PCDocument2 pagesAis 2122 2apic S1 C3 PCRayan BouhouchyPas encore d'évaluation
- dc2... 1ere ..... 2016Document3 pagesdc2... 1ere ..... 2016Hanine HmidaPas encore d'évaluation
- Devoir 2 Modele 2 Physique Chimie 3ac Semestre 1Document2 pagesDevoir 2 Modele 2 Physique Chimie 3ac Semestre 1larbi bassou100% (1)
- Devoir de Contrôle 1AS Lycée Pilote by Galaï Abdelhamid Avec Correction PDFDocument5 pagesDevoir de Contrôle 1AS Lycée Pilote by Galaï Abdelhamid Avec Correction PDFTarek BouallegPas encore d'évaluation
- Devoir PC 3college International FR s1 25Document2 pagesDevoir PC 3college International FR s1 25Toni KrossPas encore d'évaluation
- Controle GDocument2 pagesControle GAbdelmajid RAMIPas encore d'évaluation
- Controle 1 S 1Document3 pagesControle 1 S 1Khalid OualiPas encore d'évaluation
- Sujet 1: Restitution Des Connaissances (7 Points)Document2 pagesSujet 1: Restitution Des Connaissances (7 Points)marlenevendaniPas encore d'évaluation
- Lecon Chim 2Document10 pagesLecon Chim 2Mohamed ElouakilPas encore d'évaluation
- TP GRDocument6 pagesTP GRMalouda Merzkani100% (3)
- Controle 3 - 1 S2 TC 19 - 20Document4 pagesControle 3 - 1 S2 TC 19 - 20Chaoui YoussefPas encore d'évaluation
- Ds 2010Document3 pagesDs 2010ESSOME ESSOME OLIVIER STEPHANEPas encore d'évaluation
- C3 S1 PC 1AC FR EX 9 WWW - DIMASCHOOL.COM - 2Document1 pageC3 S1 PC 1AC FR EX 9 WWW - DIMASCHOOL.COM - 2mariam chokairiPas encore d'évaluation
- TP 2 CONDUCTANCE PythonpdfDocument4 pagesTP 2 CONDUCTANCE PythonpdfNaouma ChahdPas encore d'évaluation
- 1-1 AtomeDocument4 pages1-1 AtomeHanine HmidaPas encore d'évaluation
- 0.CH04 Suivi Transformation ChimiqueDocument6 pages0.CH04 Suivi Transformation ChimiqueNaouma ChahdPas encore d'évaluation
- AP04 Outils Mathématiques - Des Dérivées Aux Primitives (Cours Au 19 Octobre 2023)Document6 pagesAP04 Outils Mathématiques - Des Dérivées Aux Primitives (Cours Au 19 Octobre 2023)Naouma ChahdPas encore d'évaluation
- 0.TP CH03Document11 pages0.TP CH03Naouma ChahdPas encore d'évaluation
- Chemie 1Document1 pageChemie 1Jose YoussefPas encore d'évaluation
- Exercices Transformations Acide BaseDocument4 pagesExercices Transformations Acide BaseNaouma ChahdPas encore d'évaluation
- Bac Blanc 2023Document14 pagesBac Blanc 2023Naouma ChahdPas encore d'évaluation
- Corrige DS2 - EVALUDocument5 pagesCorrige DS2 - EVALUNaouma ChahdPas encore d'évaluation
- Corebl1 1s 09-10Document3 pagesCorebl1 1s 09-10Naouma ChahdPas encore d'évaluation
- TP 2 CONDUCTANCE PythonpdfDocument4 pagesTP 2 CONDUCTANCE PythonpdfNaouma ChahdPas encore d'évaluation
- DevoirmaisonDocument4 pagesDevoirmaisonNaouma ChahdPas encore d'évaluation
- Ex2 DC LPGBDocument5 pagesEx2 DC LPGBNaouma ChahdPas encore d'évaluation
- Ex1 DC LPGBDocument7 pagesEx1 DC LPGBNaouma ChahdPas encore d'évaluation
- Devoir Surveillé N 3 KesselDocument4 pagesDevoir Surveillé N 3 KesselNaouma ChahdPas encore d'évaluation
- Annexes DScommunDocument2 pagesAnnexes DScommunNaouma ChahdPas encore d'évaluation
- DST 4-2Document16 pagesDST 4-2Naouma ChahdPas encore d'évaluation
- 8PYOSME3Document11 pages8PYOSME3Naouma ChahdPas encore d'évaluation
- 2nde DS2 LumiereDocument5 pages2nde DS2 LumiereNaouma ChahdPas encore d'évaluation
- bb06 - Obligatoire 10Document1 pagebb06 - Obligatoire 10Naouma ChahdPas encore d'évaluation
- Bac S Sept09 OBLIDocument12 pagesBac S Sept09 OBLINaouma ChahdPas encore d'évaluation
- Bac Blanc 2016Document12 pagesBac Blanc 2016Naouma ChahdPas encore d'évaluation
- Devoir Commun Frévier 2022 TERMINAL KesselDocument11 pagesDevoir Commun Frévier 2022 TERMINAL KesselNaouma ChahdPas encore d'évaluation
- Sujets Expression ÉcriteDocument8 pagesSujets Expression ÉcriteNaouma ChahdPas encore d'évaluation
- Exercices Sur Le DosageDocument13 pagesExercices Sur Le DosageNaouma ChahdPas encore d'évaluation
- Exercices Sur Le DosageDocument13 pagesExercices Sur Le DosageNaouma ChahdPas encore d'évaluation
- 2ND9 Devoir Echelle de Long Et GravitationDocument3 pages2ND9 Devoir Echelle de Long Et GravitationNaouma ChahdPas encore d'évaluation
- Recyclage Et Valorisation de Sédiments Fins de Dragage À Usage de Matériaux RoutiersDocument11 pagesRecyclage Et Valorisation de Sédiments Fins de Dragage À Usage de Matériaux RoutiersSaid MOHAFIDPas encore d'évaluation
- Presse Cours 1Document2 pagesPresse Cours 1Hélène HofbauerPas encore d'évaluation
- These Garcia ArandaDocument188 pagesThese Garcia ArandadarkeyesesPas encore d'évaluation
- FST Equipes Oct 2018Document4 pagesFST Equipes Oct 2018Mohamed HnaPas encore d'évaluation
- Cours de Formulation Master INGMATDocument154 pagesCours de Formulation Master INGMATNohad AriouaPas encore d'évaluation
- Transformations Acide - Base Eleve NDocument2 pagesTransformations Acide - Base Eleve Nblack HPas encore d'évaluation
- PDF Le Grafcet Cours Exercices Corriges - TextmarkDocument186 pagesPDF Le Grafcet Cours Exercices Corriges - Textmarkousmane kanePas encore d'évaluation
- 04-La Malveillance PDFDocument41 pages04-La Malveillance PDFRachid Richard100% (2)
- Memoire & Resume GODRIX BastienDocument116 pagesMemoire & Resume GODRIX BastienRiadh A.HPas encore d'évaluation
- Caifanes - Afuera (G2)Document4 pagesCaifanes - Afuera (G2)Víctor IbarraPas encore d'évaluation
- Combiner PDF Apercu MacDocument2 pagesCombiner PDF Apercu MacJonPas encore d'évaluation
- Tabeau de FluxDocument7 pagesTabeau de FluxZakaria AchirPas encore d'évaluation
- Formation Continue Vieillissement Et Stabilisation Des Polymeres Et ElastomeresDocument1 pageFormation Continue Vieillissement Et Stabilisation Des Polymeres Et ElastomeresAtomer FormationPas encore d'évaluation
- La Nouvelle Norme 5 Les Nouveautés Et Les EnjeuxDocument47 pagesLa Nouvelle Norme 5 Les Nouveautés Et Les EnjeuxSami JaballahPas encore d'évaluation
- Imparfait de LDocument2 pagesImparfait de LNastja VogrincPas encore d'évaluation
- Analyse Urbaine MiramarDocument13 pagesAnalyse Urbaine MiramarSkruuu LyPas encore d'évaluation
- Catalogue Techni-Contact - Broyeur de PlastiqueDocument13 pagesCatalogue Techni-Contact - Broyeur de PlastiquewidadPas encore d'évaluation
- A-TESE 1976 - PesquisaDocument400 pagesA-TESE 1976 - PesquisaBelchiorCosta0% (1)
- Portail SNCF ManagerisDocument5 pagesPortail SNCF ManagerislamiamaziliPas encore d'évaluation
- TP UltrasonDocument8 pagesTP UltrasonZaki ZaidiPas encore d'évaluation
- 16chapitre Hydrochimie1Document20 pages16chapitre Hydrochimie1Hayat MegdoudPas encore d'évaluation
- Activité N°3 A3 Vitesse Et DéplacementDocument2 pagesActivité N°3 A3 Vitesse Et DéplacementEmmanuel VionPas encore d'évaluation
- Plomb SanitDocument31 pagesPlomb Sanitfado fifita0% (1)
- Memoire DagnicourtDocument134 pagesMemoire DagnicourtRoc Elyion ThomasPas encore d'évaluation
- La Scence Et La CriseDocument8 pagesLa Scence Et La CriseNicolas VantisPas encore d'évaluation
- ApacheDocument31 pagesApacheAbdelmoumene BoulghalghPas encore d'évaluation
- Instructions de CréationDocument4 pagesInstructions de CréationMimi DzPas encore d'évaluation
- Service de Démarrage de Baie de Stockage HPE Niveau 1-A00023078freDocument4 pagesService de Démarrage de Baie de Stockage HPE Niveau 1-A00023078freOlivier DuhamelPas encore d'évaluation
- Mode Operatoire Access 2016 Page 1Document5 pagesMode Operatoire Access 2016 Page 1amoucha sarfdaPas encore d'évaluation
- 165 12092010Document18 pages165 12092010elmoudjahid_dzPas encore d'évaluation