Académique Documents
Professionnel Documents
Culture Documents
La Cellule Cancéreuse
Transféré par
hizballah27Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
La Cellule Cancéreuse
Transféré par
hizballah27Droits d'auteur :
Formats disponibles
Oncologie
B 325
La cellule cancéreuse
Anomalies génétiques (oncogènes et anti-oncogènes), facteurs de croissance,
d’apoptose et de dissémination, incidence pronostique
PR Jean-Yves BLAY1-2, PR Alain PUISIEUX 2
1. Hôpital Édouard-Herriot, 69437 Lyon Cedex 03.
2. INSERM U453, centre Léon-Bérard, 69008 Lyon.
Points Forts à comprendre Phénotype et clonalité des cellules
cancéreuses
• Les cellules cancéreuses ont 2 caractéristiques :
elles se divisent sans être soumises aux contrôles Quel que soit leur tissu d’origine, les cellules cancé-
normaux de la croissance cellulaire reuses présentent des anomalies phénotypiques et fonc-
et sont capables d’envahir des tissus tionnelles communes. La taille de la cellule cancéreuse
normalement réservés à d’autres cellules. et de son noyau est fréquemment augmentée par rapport
à la cellule normale et varie au sein de la population
• La transformation cancéreuse résulte
cellulaire tumorale (anisocytose, anisocaryose). Elle
de lésions génétiques multiples sur des gènes conserve souvent une morphologie arrondie comme les
régulant la croissance et la différenciation cellules en mitose. Son noyau présente une chromatine
cellulaire : les proto-oncogènes normaux irrégulière et la proportion des cellules en mitose (index
qui vont subir des mutations activatrices mitotique) est augmentée. Sur le plan fonctionnel, les
dans les cellules cancéreuses, les transformant cellules cancéreuses présentent des altérations de
ainsi en oncogènes (capables notamment l’expression ou de la fonction de molécules d’adhésion
d’entraîner une division cellulaire à la matrice extracellulaire, une réorganisation du cyto-
inappropriée) et les anti-oncogènes, ou plutôt squelette d’actine du cortex cellulaire, une motilité
gènes suppresseurs de tumeurs, détruits accrue, une augmentation de la production de facteurs
ou non fonctionnels dans les cellules de croissance, d’activateurs du plasminogène et d’en-
zymes capables de dégrader les composants de la matrice.
cancéreuses. Le cancer est essentiellement
Les principales anomalies fonctionnelles des cellules
une maladie des gènes. cancéreuses portent cependant sur leurs capacités de
• La plupart des oncogènes codent pour croissance et de division : elles peuvent se diviser en
des protéines impliquées dans la transmission présence de très faibles concentrations de facteurs de
du signal mitotique induit par les facteurs croissance et ont perdu la capacité d’arrêter de se diviser
de croissance de la membrane jusqu’au noyau. lorsque la densité cellulaire est élevée et que les cellules
Ces facteurs fréquemment produits en excès sont en contact les unes avec les autres (perte de l’inhi-
par les cellules cancéreuses vont parfois jouer bition de contact). Elles sont capables de se diviser sans
des rôles multiples : facteur de survie (anti- attache avec une surface solide (perte de la dépendance
apoptotique), facteur mitogénique, de motilité d’ancrage) et peuvent pousser dans des milieux semi-
ou angiogénique. Les lésions des oncogènes solides tels que l’agar mou. Enfin, elles sont capables
d’un nombre illimité de divisions cellulaires sans
et des gènes suppresseurs de tumeur affectent
subir le phénomène de sénescence (immortalisation) et
l’interaction des cellules tumorales avec leur d’induire des tumeurs après injection chez des animaux
environnement normal et permettent leur susceptibles (souris athymiques). Bien que le terme
dissémination dans l’organisme, en altérant « transformation » ne désigne stricto sensu que la
la structure ou la fonction des molécules modification transmissible à la descendance des
d’adhésion cellulaire, en induisant la production propriétés d’une cellule eucaryote, dans le cas des
de facteurs de motilité et d’enzymes capables cellules animales en culture, le terme « transformation »
de détruire la matrice extracellulaire. est fréquemment utilisé pour désigner l’acquisition de
Ces altérations permettent aux cellules propriétés analogues à celles des cellules cancéreuses.
tumorales de coloniser et de se diviser dans On classe les cancers selon le tissu et le type cellulaire
les tissus où elles ne résident pas normalement. dont ils proviennent. On distingue ainsi les carcinomes
(tumeurs malignes issues de cellules épithéliales) qui
sont les cancers les plus fréquents de l’adulte ; les
LA REVUE DU PRATICIEN 2000, 50 1135
LA CELLULE CANCÉREUSE
sarcomes (cancers provenant des cellules du tissu ce fait, l’incidence de la plupart des cancers augmente
conjonctif, spécialisé ou non) ; les tumeurs du système de manière exponentielle avec l’âge. Chez les individus
hématopoïétique (leucémies ou lymphomes) ; les porteurs d’une mutation constitutionnelle de certains
tumeurs du système nerveux central ; les tumeurs gènes, notamment de gènes suppresseurs de tumeurs
embryonnaires… Dans ces différents types cellulaires, tels que p53, APC ou BRCA-1 (v. infra), les cancers
les voies de contrôle de la différenciation et de la surviennent plus précocement, une première « étape »
croissance cellulaire utilisent souvent des mécanismes dans le processus de transformation cancéreuse ayant
moléculaires communs. La cancérisation de la cellule été franchie dans toutes les cellules somatiques de
est la conséquence de mutations de gènes codant pour l’individu.
des protéines impliquées dans ces différentes voies de Le développement d’un cancer peut également être
régulation. favorisé par des facteurs qui n’induisent pas de mutation
Les cancers correspondent le plus souvent à la proliféra- de l’ADN mais stimulent la prolifération cellulaire ou
tion d’un clone cellulaire dérivant d’une seule cellule bloquent la différenciation. Ces produits non mutagènes
anormale. Cela a pu être démontré chez les femmes par sont appelés promoteurs tumoraux. Dans un premier
l’analyse de l’origine paternelle ou maternelle du chro- temps, l’exposition a un carcinogène induit une première
mosome X inactivé dans les cellules tumorales qui lésion génétique latente. Cette étape est parfois appelée
montre que toutes les cellules tumorales ont le même initiation tumorale. La lésion génétique ainsi induite
chromosome X inactivé. Cela a pu être confirmé plus permet la transformation cancéreuse à la faveur soit de
finement par l’analyse de la séquence nucléotidique des l’acquisition d’anomalies génétiques supplémentaires
sites de translocations chromosomiques spécifiques, telles que celles décrites ci-dessus, soit après exposition
telles que la t(9,22) dans la leucémie myéloïde chro- répétée à ces promoteurs tumoraux qui vont stimuler la
nique (LMC), qui sont toujours identiques dans une division cellulaire ou bloquer le processus normal de
même tumeur chez un individu, mais le plus souvent différenciation. Comme exemple de promoteurs tumo-
différentes dans deux tumeurs de même histologie chez raux, on peut citer les esters de phorbol qui agissent en
deux individus différents. Ces observations démontrent activant la protéine kinase C. Les corrélations épidémio-
l’origine clonale de la plupart des cancers. Il existe logiques entre les antécédents gynéco-obstétricaux
cependant quelques exceptions et certaines proliféra- d’une patiente (âge des premières règles, de la première
tions cellulaires tumorales, notamment des lymphomes grossesse, de la ménopause) et le risque relatif de cancer
de sujets immunodéprimés, peuvent comporter une du sein suggèrent que les hormones sexuelles, notamment
population cellulaire polyclonale ou oligoclonale. les œstrogènes, jouent un rôle de promoteur tumoral
pour certains cancers du sein.
Anomalies génétiques des cellules Au total, le processus de transformation cancéreuse est
la conséquence de l’accumulation de mutations de l’ADN
cancéreuses pour la plupart des tumeurs humaines et animales.
Mutations de l’ADN nécessaires Gènes impliqués dans la transformation
pour la transformation cancéreuse maligne
Des mutations de l’ADN de la cellule sont à l’origine de La progression tumorale correspond à un phénomène
la majorité des cancers. Il existe une corrélation entre le dynamique qui, à chaque étape, sélectionne une cellule
potentiel mutagène pour l’ADN de produits chimiques ayant acquis un avantage de croissance (soit une activa-
(méthylcholanthrène, 2-naphtylamine) et leur potentiel tion de la multiplication cellulaire, soit une inhibition de
carcinogène. Il est cependant rare qu’une seule mutation la mort cellulaire). Notre organisme est composé d’envi-
soit suffisante pour entraîner la transformation maligne. ron 5 x 1012 cellules réparties dans plus de 200 types
En général, plusieurs mutations dans des gènes différents cellulaires différents. Leur multiplication et leur durée
sont requises pour l’acquisition d’un phénotype cancé- de vie sont rigoureusement contrôlées : certaines
reux. On estime ainsi qu’il faut entre 3 et 7 mutations cellules, telles les cellules nerveuses, ne nécessitent pas
indépendantes pour transformer une cellule normale en un renouvellement constant, d’autres, telles les cellules
cellule cancéreuse. La nécessité de plusieurs mutations sanguines, sont perpétuellement en cours de division. Le
indépendantes pour la transformation d’une cellule contrôle de la croissance cellulaire résulte d’un équilibre
explique le délai souvent long (plusieurs années) entre permanent entre facteurs stimulateurs et facteurs
l’exposition à un carcinogène et l’apparition d’un cancer. inhibiteurs de la croissance cellulaire.
Au cours de cet intervalle, les cellules initialement Au cours de la vie cellulaire, l’ADN est soumis à des
mutées acquièrent des mutations supplémentaires dans agressions qui peuvent résulter d’erreurs de la machinerie
d’autres gènes qui contribuent à la transformation can- cellulaire de réplication ou d’agents extérieurs comme
céreuse. Chez les individus non exposés à des carcino- les agents génotoxiques carcinogènes mentionnés
gènes, la transformation maligne survient au hasard et ci-dessus. De façon générale, ces altérations de l’ADN
provient de plusieurs mutations aléatoires dans une sont immédiatement réparées par des mécanismes
même cellule, qui mettent des années à se constituer. De spécialisés. Cependant, dans de rares cas, la réparation
1136 LA REVUE DU PRATICIEN 2000, 50
Oncologie
ne se fait pas ou mal, et une mutation génique apparaît. désigné c-src et qui est présent dans le génome de la plu-
Si cette mutation atteint et modifie la structure d’un part des vertébrés. Le gène cellulaire c-src code pour
gène codant pour un facteur qui contrôle la prolifération une protéine membranaire qui intervient dans la trans-
cellulaire ou le phénomène de mort cellulaire (apoptose), duction du signal mitotique. Les modifications qualita-
la cellule peut acquérir un avantage de croissance à tives du gène src chez le virus provoquent une activation
l’origine d’une expansion clonale. anormale de la protéine, expliquant ses capacités trans-
La description de gènes impliqués dans la transformation formantes. On s’est secondairement rendu compte que
maligne a permis d’élaborer une théorie unifiée concer- beaucoup de tumeurs humaines, non induites par un
nant les mécanismes moléculaires mis en jeu dans la virus, présentaient des mutations activatrices du proto-
genèse d’une tumeur. Deux grandes catégories de gènes oncogène c-src qui le transforment en un oncogène.
peuvent ainsi être distinguées : les gènes dont les pro- D’autres oncogènes contenus dans des rétrovirus res-
duits contribuent à stimuler la prolifération cellulaire et ponsables de sarcomes ou de leucémies chez les oiseaux
ceux dont le produit réprime la prolifération cellulaire. ou les mammifères ont été individualisés (tableau I).
Les premiers gènes sont appelés en général oncogènes Ces oncogènes viraux (v-onc) possèdent un homologue
et les seconds anti-oncogènes ou plutôt gènes suppres- cellulaire (c-onc), qui est muté dans certaines tumeurs
seurs de tumeur. humaines non liées à des rétrovirus. Ces oncogènes sont
très souvent impliqués dans la transmission d’un signal
1. Oncogènes de prolifération cellulaire du milieu extracellulaire jus-
Si l’on exclut certains oncogènes viraux (notamment de qu’au noyau (fig. 1) : ce sont des gènes codant pour des
virus à ADN), les oncogènes sont le plus souvent des facteurs de croissance ou cytokines (v-sis, homologue
gènes cellulaires mutés. Le terme proto-oncogène de la chaîne B du platelet derived growth factor, PDGF),
désigne le gène cellulaire normal, qui est muté en onco- des récepteurs de cytokines (v-erb-B1, v-kit, v-fms), des
gène dans une cellule tumorale, favorisant ainsi la trans- tyrosine kinases du feuillet interne de la membrane plas-
formation cancéreuse de la cellule. La mutation d’un mique (v-src), intracytosoliques (v-fes), des sérine thréonine
oncogène rend en général le gène « hyperactif » et ces kinases (v-raf), des protéines fixant le guanosine triphos-
mutations sont généralement dominantes. phate (GTP) (H-ras), des facteurs régulateurs de la trans-
Les oncogènes ont été découverts initialement dans cription (v-fos, v-jun, v-rel), des récepteurs d’hormone
des rétrovirus responsables de tumeurs animales. Le liposoluble (v-erbA). Tous les oncogènes n’ont cepen-
premier rétrovirus ainsi individualisé est un virus du dant pas été identifiés dans des rétrovirus. D’autres
poulet, le virus de sarcome de Rous. Il contient un gène oncogènes, et donc d’autres proto-oncogènes, ont été
appelé v-src, qui n’est pas indispensable à la réplication identifiés dans les tumeurs humaines par transfection de
virale mais qui a été prélevé accidentellement par le lignées de fibroblastes immortalisées NIH 3T3 par de
virus dans une cellule hôte antérieure. Le gène viral l’ADN provenant de lignées tumorales. Au total, près
v-src possède ainsi un homologue cellulaire normal, d’une centaine d’oncogènes ont désormais été identifiés.
TABLEAU I
Oncogènes de rétrovirus transformants
Oncogènes Fonction du proton-oncogène Hôte Tumeur induite
par le virus
v-sis PDGF B Singe Sarcome
v-erb-B1 Tyrosine kinase : récepteur de l’EGF Poulet Leucémie, sarcome
v-fms Tyrosine kinase : récepteur du M-CSF Chat Sarcome
v-kit Récepteur tyrosine kinase du stem cell factor (SCF) Chat Sarcome
H-ras Protéine liant le GTP Rat Sarcome, leucémie
v-src Protéine kinase (tyrosine) Poulet Sarcome
v-fes Tyrosine kinase Chat/poulet Sarcome
K-ras Protéine liant le GTP Rat Sarcome, leucémie
v-abl Tyrosine kinase Souris, chat Leucémie, sarcome
v-raf Sérine/thréonine kinase Poulet/souris Sarcome
v-erb-A Récepteur de l’hormone T3 Poulet Leucémie
v-myc Protéine régulatrice de la famille HLH Poulet Sarcome, leucémie
carcinome
v-rel Facteur de transcription NFkB Réticulo-endothéliose
v-fos Association pour former le facteur de transcription AP1 Souris Sarcome
v-jun Poulet
LA REVUE DU PRATICIEN 2000, 50 1137
LA CELLULE CANCÉREUSE
Les mutations observées dans les proto-oncogènes héréditaire de cette maladie, les individus atteints pré-
modifient la séquence des acides aminés de la protéine sentent souvent plusieurs tumeurs tandis que les formes
en modifiant ses propriétés fonctionnelles, lui conférant sporadiques de rétinoblastome sont en général des
une activité permanente et non régulable par les processus tumeurs uniques. Le gène Rb a pu être identifié dans une
normaux de contrôle. Les rétrovirus peuvent également région du chromosome 13 touchée par une délétion chez
activer un proto-oncogène en s’insérant à proximité de les individus atteints dans certaines de ces familles.On a
ses séquences régulatrices, conduisant ainsi à sa surex- pu montrer que dans les cellules de rétinoblastome, les
pression : on parle alors de mutagenèse insertionnelle. 2 copies du gène sont inactivées, une 2e mutation ayant
En fait, différents mécanismes d’activation d’un onco- inactivé le gène Rb sur l’autre chromosome dans la
gène cellulaire peuvent être observés. cellule tumorale. La probabilité de survenue de cette
• La mutation ponctuelle a pour exemple classique la 2e mutation est donc élevée dans ces cellules présentant
mutation des codons 12, 13 ou 61 du gène H-ras, qui toutes une mutation du 1er gène Rb, et plusieurs tumeurs
empêche son produit protéique d’hydrolyser le GTP, lui peuvent ainsi survenir dans les cellules rétiniennes des
conférant ainsi une activité biologique permanente. 2 yeux ; en revanche chez les individus dépourvus de
• Lors de la délétion d’une partie de la séquence codante, mutation de Rb constitutionnelle, le risque de survenue
le gène c-erbB1 code pour le récepteur de l’epidermal d’une mutation sur chacun des 2 gènes Rb dans la même
growth factor (EGF) ; dans certaines tumeurs, on observe cellule est très faible, expliquant ainsi la rareté de cette
une délétion de la partie extracellulaire capable de fixer affection en dehors des formes familiales.
EGF et des mutations dans sa portion intracyto- La perte du gène Rb joue un rôle important dans des
plasmique conférant à la protéine une activité tyrosine tumeurs plus fréquentes que le rétinoblastome. Les
kinase permanente. 2 copies du gène sont fréquemment altérées dans les
• La translocation chromosomique va réunir dans une cancers du poumon, du sein, de la vessie, les sarcomes.
protéine de fusion le produit d’un gène activement trans- La protéine Rb, lorsqu’elle est déphosphorylée, inhibe la
crit et une partie des séquences codantes de l’oncogène, transcription de certains gènes, permettant l’entrée dans
conduisant à la synthèse d’une protéine hyperactive ; un le cycle cellulaire. Lorsque les 2 copies du gène sont
exemple de ce type de fusion est la protéine bcr-abl, perdues ou lorsque la protéine Rb est phosphorylée
produit de la translocation t(9,22) de la leucémie myé- (v. infra), il n’empêche plus la transcription et permet
loïde chronique. ainsi à la cellule d’accomplir une nouvelle division.
• Parfois, la translocation va simplement mettre l’oncogène Depuis la description initiale du gène Rb comme modèle
sous la dépendance du promoteur d’un gène activement de gène suppresseur de tumeur, de nombreux autres
transcrit, comme le gène des chaînes lourdes des immuno- gènes suppresseurs de tumeurs ont été identifiés dans les
globulines pour la t(8,14) des lymphomes de Burkitt. tumeurs humaines : APC et DCC dans les tumeurs
• L’amplification génique est décrite pour les gènes coliques, WT1 dans les tumeurs de Wilms, BRCA-1 et 2
N-myc dans le neuroblastome. dans les adénocarcinomes du sein, p53 dans une large
• L’insertion d’un élément génétique mobile (tel qu’un variété de cancers.
rétrovirus) à proximité du proto-oncogène entraîne La protéine p53 est mutée dans une large variété de
l’activation de la transcription du gène. Le gène codant cancers humains. Une des fonctions de p53 est d’induire
pour le fibroblast growth factor 3 (FGF-3) est ainsi la production d’une protéine p21/WAF1 inhibitrice des
activé par le mouse mammary tumour virus chez la kinases dépendantes des cyclines qui permettent à la
souris conduisant à l’apparition de tumeurs mammaires. cellule de passer le point de contrôle G1 du cycle cellu-
Les mutations des oncogènes ne surviennent pas isolé- laire ; p53 est induite en réponse à des altérations de
ment dans les tumeurs et très souvent, la mutation de l’ADN et permet à la cellule d’arrêter sa progression
plusieurs oncogènes est synergique pour l’acquisition dans le cycle, de réparer les lésions de l’ADN ou, si
d’un phénotype cancéreux. Ce phénomène est connu celles-ci sont irréparables, d’entraîner l’apoptose de la
sous le nom de coopération des oncogènes. cellule altérée. Les mutations de p53 permettent à la
cellule à la fois de se diviser et d’acquérir des mutations
2. Anti-oncogènes ou gènes suppresseurs supplémentaires sur d’autres gènes. Les mutations
de tumeurs (voir : Pour approfondir 1) constitutionnelles de p53 sont responsables d’un syn-
Certaines mutations vont inactiver des gènes dont le drome de prédisposition génétique aux cancers appelé
produit est impliqué dans le blocage de l’entrée dans le syndrome de Li-Fraumeni.
cycle cellulaire : on parle parfois à leur propos d’anti- D’autres gènes suppresseurs de tumeurs sont mutés chez
oncogènes, mais le terme gène suppresseur de tumeur des sujets porteurs de prédispositions héréditaires au
est généralement préféré. cancer. La polypose colique adénomateuse familiale
Beaucoup de gènes suppresseurs de tumeurs ont été résulte d’une mutation somatique d’un gène appelé
identifiés grâce à l’étude des syndromes de prédisposition APC ; les gènes de réparation msh-2 et mlh-1 sont altérés
héréditaire aux cancers. C’est le cas du gène du rétino- dans les cancers coliques familiaux non polyposiques, le
blastome (Rb), premier gène suppresseur de tumeur gène WT1 dans les tumeurs de Wilms familiales (tableau II).
identifié (1984) grâce à l’étude des familles atteintes de Certains gènes suppresseurs de tumeurs, comme p53 ou
formes héréditaires de rétinoblastome. Dans la forme Rb, sont inactivés par d’autres mécanismes que des
1138 LA REVUE DU PRATICIEN 2000, 50
Oncologie
TABLEAU II
Syndromes de prédisposition au cancer et gènes suppresseurs de tumeurs
Syndromes Gènes Types
de prédisposition au cancer suppresseurs de cancers
Rétinoblastome familial Rb Rétinoblastome, ostéosarcome
Syndrome de Li-Fraumeni p53 Carcinomes, sarcomes, leucémies
Polypose adénomateuse familiale APC Adénocarcinomes du côlon et du rectum
Cancer colique familial non polyposique msh-2, mlh-1 Adénocarcinomes : côlon, estomac, voie biliaire,
endomètre
Ataxie télangiectasie ATM Lymphomes, tumeurs cérébrales
Tumeur de Wilms familiale WT1 Tumeur de Wilms
Neurofibromatose type 1 NF1 Sarcome, gliomes
Neurofibromatose type 2 NF2 Méningiomes, neurinomes du VIII
Cancer du sein familial BRCA-1, BRCA-2 Adénocarcinome du sein, de l’ovaire
mutations inactivatrices. Les virus oncogènes à ADN, taires variables d’une tumeur à l’autre, à la faveur de
tels que les papillomavirus (impliqués dans les cancers l’instabilité génétique provoquée par la perte de p53.
du col de l’utérus) ou le virus polyome contiennent des Chez les individus porteurs de mutations somatiques du
protéines virales (protéines E6 et E7 de papillomavirus, gène APC et présentant une polypose adénomateuse
antigène T et t de polyome) qui se fixent aux protéines familiale, toutes les cellules somatiques de l’individu et
p53 et à Rb bloquant ainsi leur fonction. Le virus peut notamment les cellules épithéliales du colon ont franchi
ainsi utiliser à son profit les protéines cellulaires de une 1re étape dans le processus de carcinogenèse, qui se
réplication de l’ADN de l’hôte pour se répliquer. Dans produit donc avec une fréquence beaucoup plus élevée
certaines cellules, ces virus oncogènes à ADN vont s’in- que dans la population générale et à un âge plus précoce.
tégrer à l’ADN cellulaire et les protéines virales sont
produites en permanence, bloquant ainsi en permanence 4. Défaut de réparation de l’ADN
la fonction des protéines Rb et p53 et favorisant la D’une manière générale, tout phénomène biologique qui
division cellulaire. À la différence des rétrovirus, augmente le taux de mutation de l’ADN augmente le
ces protéines oncogènes des virus à ADN n’ont pas risque de développer un cancer. On a identifié ainsi
d’équivalent cellulaire et sont indispensables à la plusieurs syndromes de prédisposition au cancer qui
réplication virale. résultent d’altération des systèmes de réparation de
l’ADN. Le xeroderma pigmentosum est un syndrome
3. Modèle du carcinome colique dans lequel les individus, le plus souvent des enfants,
Plusieurs mutations de proto-oncogènes ou de gènes présentent une anomalie d’un gène codant pour une des
suppresseurs de tumeurs sont donc requises pour la protéines impliquées dans la réparation des lésions de
transformation d’une cellule normale en cellule cancé- l’ADN dues aux ultraviolets et vont présenter des
reuse. La genèse des anomalies moléculaires, de l’épi- cancers cutanés multiples dans les 2 premières décennies
thélium normal, à l’adénome puis à l’adénocarcinome a de la vie. Les cancers héréditaires du côlon non polypo-
été particulièrement bien étudiée dans les cancers recto- siques sont également liés à des altérations des gènes
coliques. La plupart des cellules d’adénocarcinome (msh-2, mlh-1) d’un système de réparation de l’ADN
colique acquièrent au cours de leur transformation can- (réparation des mésappariements de l’ADN). L’inactivation
céreuse des mutations sur des gènes précis : le gène sup- de ce système entraîne l’apparition d’une instabilité
presseur de tumeur APC est perdu souvent avant l’appa- génétique qui favorise l’accumulation progressive de
rition de l’adénome, l’oncogène K-ras est muté et le mutations. L’instabilité génétique observée dans ce syn-
gène suppresseur de tumeur DCC est perdu au cours de drome prédispose aux cancers du côlon et à d’autres
la dédifférenciation de l’adénome ; puis une perte du cancers (endomètre, voies biliaires, estomac) à un âge
gène p53 est observée lorsque le carcinome devient précoce. D’autres mutations de gènes impliqués dans la
invasif. L’ordre de survenue de ces mutations peut pro- réparation et la réplication de l’ADN sont responsables
bablement varier selon les tumeurs. Au-delà, la cellule de maladies génétiques augmentant le risque de cancers
tumorale acquiert des anomalies génétiques supplémen- comme le gène ATM dans l’ataxie télangiectasie.
LA REVUE DU PRATICIEN 2000, 50 1139
LA CELLULE CANCÉREUSE
Facteurs de croissance croissance est transmis jusqu’au noyau induisant ainsi la
transcription de certains gènes et permettant l’entrée
Chez les eucaryotes supérieurs, dont l’homme, la dans le cycle cellulaire (fig. 1).
majorité des cellules sont en G0 où elles exercent leurs Les facteurs de croissance induisent l’expression de
fonctions spécialisées. L’entrée d’une cellule dans le 2 grandes classes de gènes, des gènes à réponse précoce
cycle cellulaire requiert la présence de facteurs de crois- (dont les proto-oncogènes c-fos et c-jun) et des gènes à
sance dans le milieu extracellulaire et de l’ancrage de réponse retardée, qui sont activement transcrits au-delà
la cellule à la matrice extracellulaire par l’intermédiaire d’une heure après l’exposition de la cellule au facteur de
de molécules d’adhésion. Les cellules cancéreuses pro- croissance. Parmi ces derniers figurent les protéines de
duisent fréquemment ces facteurs de croissance en la machinerie de contrôle du cycle cellulaire, c’est-à-
excès, ou présentent une activation permanente de leurs dire les cyclines, et les protéines kinases dépendant des
récepteurs et des voies de transduction du signal en aval. cyclines qui permettent aux cellules de passer le point de
Les facteurs de croissance sont des petites protéines de restriction de fin de G1 et d’entrer en phase S. La protéi-
signalisation extracellulaire (cytokines) actives à très ne Rb joue un rôle important dans ce phénomène : dans
faibles concentrations (10-9 à 10-10 mmol) qui vont induire la cellule en G0, Rb se lie sous sa forme déphosphorylée
l’entrée de la cellule en phase S et parfois moduler la à des protéines régulatrices de la transcription qu’elle
différenciation, la fonction et (ou) la migration des inactive. Après exposition à un facteur de croissance, Rb
cellules cibles exprimant leurs récepteurs spécifiques. va être phosphorylée, libérant ainsi ces facteurs régula-
Ils agissent selon un mécanisme paracrine, parfois auto- teurs de la transcription, permettant ainsi l’induction de
crine et, plus rarement, endocrine. Plus d’une centaine la transcription de gènes tardifs. Ainsi, 2 phénomènes
de facteurs de croissance ont désormais été identifiés. biologiques aussi différents que l’inactivation fonction-
Leur nom provient des circonstances de leur découverte nelle de Rb par mutation des 2 copies du gène et l’acti-
ou de leur fonction EGF et PDGF. Certains agissent sur vation permanente d’une voie de signalisation d’un fac-
une très grande variété de cellules (EGF, PDGF), teur de croissance ont des conséquences assez similaires
d’autres sur une population cellulaire très limitée (inter- sur l’entrée d’une cellule dans le cycle cellulaire.
leukine 2, érythropoïétine). Certains facteurs de crois- Les facteurs de croissance, les récepteurs de facteurs de
sance, comme le TGFβ (transforming growth factor β) croissance ou les protéines cellulaires qu’ils activent en
exercent des effets biologiques opposés (effet prolifératif cascade sont des proto-oncogènes fréquemment mutés
ou antiprolifératif) dans des types cellulaires différents. (c-erbB-1, c-ras, c-raf), surexprimés (c-erbB-2), ampli-
Plusieurs de ces facteurs de croissance sont des proto- fiés (c-erbB-2) dans les cellules cancéreuses induisant
oncogènes qui vont contribuer à l’acquisition d’un phéno- ainsi une activation permanente des voies de transduc-
type cancéreux lorsqu’ils sont produits en excès (PDGF, tion du signal indépendamment de la présence du ligand
EGF, macrophage colony stimulating factor ou M-CSF) (fig. 1). De ce fait, les cellules cancéreuses ont une
en agissant souvent selon un mécanisme autocrine (fig. 1). moindre dépendance aux facteurs de croissance que les
Ces facteurs de croissance interagissent avec la portion cellules normales. La perte de l’inhibition de contact
extracellulaire des récepteurs transmembranaires spéci- résulte en fait d’une compétition entre les cellules
fiques présents à la surface de la cellule, parfois consti- poussant à haute densité pour l’utilisation des facteurs
tués d’une ou plusieurs chaînes différentes. Dans leur de croissance présents en faible quantité en culture. Les
portion intracellulaire, ces récepteurs, après interaction cellules cancéreuses affranchies de cette dépendance
avec leur ligand, exercent une activité enzymatique peuvent continuer à se diviser même en présence de très
variable, tyrosine kinase (récepteur de l’EGF ou du faibles concentrations de ces facteurs de croissance dans
PDGF), sérine thréonine kinase (récepteur du TGFβ), le milieu de culture.
ou interagissent avec des protéines G ancrées dans le
feuillet interne de la membrane plasmique. D’autres Apoptose
récepteurs sont dépourvus d’activité enzymatique intrin-
sèque, mais s’associent à des protéines cytosoliques qui Le terme d’apoptose désigne un processus actif de mort
vont transmettre directement le signal ; c’est le cas de cellulaire programmée, au cours duquel la cellule procède,
récepteurs d’interleukines (IL2, IL4, IL6), qui inter- par l’activation d’enzymes intracellulaires notamment, à
agissent avec des kinases (janus kinases ou Jak) qui vont une destruction de son ADN et de certaines protéines
phosphoryler et activer directement des facteurs de conduisant à sa propre mort. L’apoptose est un processus
transcription. essentiel pour l’homéostasie de l’individu, intervenant
Les récepteurs tyrosine kinases se « dimérisent » après dans des processus aussi divers que l’embryogenèse, la
interaction avec leur ligand, permettant ainsi une auto- destruction des lymphocytes T autoréactifs, la destruc-
phosphorylation de tyrosine dans leur portion intracyto- tion des cellules en sénescence, des cellules infectées
plasmique ; les récepteurs ainsi phosphorylés interagis- par des virus, des cellules porteuses de mutations de
sent alors avec d’autres protéines cytosoliques, qui l’ADN. Sur le plan morphologique, l’apoptose se traduit
activent la protéine ras, qui active elle-même d’autres par une diminution de la taille de la cellule et de son
kinases intracytoplasmiques (c-raf). Par une cascade de noyau, qui se fragmente. L’ADN cellulaire est clivé en
phosphorylations, le signal induit par le facteur de fragments multiples de 200 paires de bases correspondant
1140 LA REVUE DU PRATICIEN 2000, 50
Oncologie
de mort ») qui activent la
PDGF (sis)
cascade des caspases dans
EGF la cellule. Leur mode
M-CSF d’action est ainsi très
voisin de celui des facteurs
Récepteur PDGF de croissance et ils
Récepteur de l'EGF (c-er peuvent d’ailleurs parfois
Récepteur du M-CSF (c-fm (TNFα) agir comme des
c-Erb-B2
facteurs de croissance et
Shc non pas d’apoptose pour
certains types cellulaires.
GRB2 La privation de facteurs
de croissance entraîne
c-src :
tyrosines kinases associées
l’apoptose de certains
à la membrane ou au types cellulaires notam-
cytosquelette Protéines liant le GTP : ment de cellules du sys-
H-ras tème hématopoïétique.
N-ras Les lésions irréparables
K-ras de l’ADN, causées par
des agents mutagènes
comme les radiations
ionisantes ou les agents
c-raf
sérine-thréonine kinase
cytotoxiques utilisés en
chimiothérapie antican-
céreuse entraînent l’apop-
MAPK tose. La protéine p53
(mitogen activated protein kinase) normale intervient dans
ce phénomène.
Les cellules cancéreuses
présentent fréquemment
une altération des voies
d’induction ou d’inhibi-
erb-A : Protéines
tion de l’apoptose. La
récepteur denucléaires
l’hormone myc
tumeur pour laquelle une
thyroïde fos altération des voies de
jun l’apoptose a été la mieux
documentée est le lym-
phome folliculaire, une
tumeur maligne du lym-
phocyte B, caractérisé
par la translocation chro-
1 Les proto-oncogènes dans la transduction du signal mitotique. mosomique spécifique
t(14,18) : cette transloca-
tion juxtapose le gène
à la longueur du brin d’ADN nucléosomique. Ce proces- antiapoptotique bcl-2 avec les séquences régulatrices d’un
sus de dégradation des composants intracellulaires est gène des immunoglobulines, entraînant ainsi une surex-
exécuté en partie par une catégorie d’enzymes particu- pression de bcl-2 dans le clone cellulaire tumoral. Cette
lières appelées caspases dont on connaît désormais plus translocation confère au clone tumoral une survie pro-
d’une dizaine de membres. L’entrée en apoptose et l’ac- longée. Cela a pu être démontré dans des lignées
tivation de ces caspases est également sous le contrôle cellulaires où la surexpression de l’oncogène c-myc
d’une famille de protéines intracellulaires situées dans permet à la cellule d’entrer en cycle mais la conduit en
les membranes d’organites intracellulaires dont les mito- apoptose. La surexpression de bcl-2 avec c-myc dans la
chondries, les protéines de la famille bcl-2 ; certaines de même lignée permet à la cellule d’échapper à l’apoptose
ces protéines induisent l’apoptose, d’autres l’inhibent. et lui confère un phénotype cancéreux. Une surexpres-
Plusieurs types de signaux entraînent la cellule à s’engager sion de bcl-2 ou d’autres protéines antiapoptotiques de
dans un processus d’apoptose. Des protéines solubles ou la même famille a désormais été observée dans d’autres
transmembranaires (tumour necrosis factor alpha, TNF; types de cancers notamment des carcinomes. Cette
ligand de Fas, TRAIL) interagissent avec des récepteurs surexpression est parfois associée à une agressivité
spécifiques à la surface de la cellule cible (« récepteurs clinique particulière de la tumeur.
LA REVUE DU PRATICIEN 2000, 50 1141
LA CELLULE CANCÉREUSE
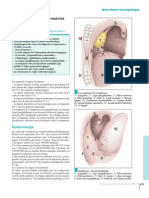
Dissémination tumorale
Molécules exprimées
É TA P E S par les cellules tumorales
L’une des caractéristiques de la cellule impliquées
tumorale est sa capacité à envahir des dans la dissémination
régions de l’organisme où elle ne
devrait pas se retrouver. La capacité à Altération de la cohésion Perte de la cadhérine E
intercellulaire dans l’épithélium Facteurs de motilité
disséminer dans des tissus adjacents est
la première étape conduisant à l’appari-
tion de métastases (fig. 2). La cellule can- Upa/PAI
Franchissement collagénase IV, protéases
céreuse, par exemple d’origine épithé- de la membrane basale TIMP
liale, a ainsi la capacité de s’affranchir Facteurs de motilité
de ses interactions avec les cellules
normales environnantes, détruire la Facteurs angiogéniques
membrane basale sous-jacente, progres- Croissance locale Facteurs de croissance
ser à travers le tissu conjonctif, franchir
la paroi du vaisseau lymphatique ou Upa/PAI
Protéases, métalloprotéases
sanguin, migrer dans la circulation lym- Progression dans le tissu Héparanase
phatique ou sanguine, franchir la paroi conjonctif / franchissement TIMP(inhibiteur tissulaire
du capillaire dans une autre région de de la paroi vasculaire des métalloprotéases)
Facteurs de motilité
l’organisme, pour s’établir, survivre et Intégrines
croître dans ce nouvel environnement.
Cette succession d’étapes limitantes Fixation sur l’endothélium Plaquettes sélectines
nécessite l’acquisition par la cellule vasculaire de l’organe cible CD44 intégrines
cancéreuse de nouvelles propriétés.
La perte de l’adhésion des cellules
tumorales aux cellules normales adja- Upa/PAI
Protéases, métalloprotéases
centes peut résulter de plusieurs méca- Pénétration à travers la paroi Héparanase
nismes par exemple la perte de l’expres- du vaisseau et dans le chorion TIMP
sion de molécules d’adhésion Facteurs de motilité
Intégrines
intercellulaire, comme la cadhérine E,
ou l’inactivation fonctionnelle de ces
molécules d’adhésion après exposition Facteurs angiogéniques
Croissance au site métastasique Facteurs de croissance
à des cytokines telles que certains
membres de la famille des FGF. Dans
Upa : urokinase like plasminogen activator ; PAI : plasminogen activator inhibitor
les lignées cellulaires dans lesquelles
l’expression de la cadhérine E est per- 2 Étapes de dissémination pour une cellule tumorale épithéliale.
due, la transfection par la cadhérine E
permet de renverser le phénotype méta-
statique, cette molécule d’adhésion se
comportant donc comme un gène suppresseur de produisent divers facteurs de motilité, des cytokines
tumeur. L’étape suivante dans la dissémination métasta- (FGF1 et FGF2, IL6, TGFβ…), des composants
tique est la dégradation des composants de la matrice solubles de la matrice extracellulaire (fibronectine,
extracellulaire pour permettre la progression de la cellu- laminine, thrombospondine…) qui vont jouer un rôle
le tumorale dans le tissu conjonctif environnant, c’est-à- parfois opposé selon qu’ils sont sous forme soluble
dire la membrane basale, le chorion sous-jacent et la circulante ou insérés dans la matrice conjonctive.
paroi des vaisseaux sanguins ou lymphatiques. Plusieurs Seule la minorité des cellules tumorales qui franchit la
familles d’enzymes impliquées physiologiquement dans paroi vasculaire et qui migre par la circulation sanguine
le remodelage du tissu conjonctif jouent un rôle essen- se fixe dans un tissu à distance et forme une métastase.
tiel dans la dégradation des protéines fibreuses, des pro- Dans la circulation, les cellules tumorales interagissent
téoglycanes et des glycoprotéines de la matrice extracel- avec des plaquettes par l’intermédiaire de molécules
lulaire : les héparanes, les sérine-, asparatyl- et d’adhésion (de la famille des intégrines notamment).
cystéine-protéases, et les métalloprotéases (matrix Pour sortir du flux sanguin, les amas de cellules tumo-
metalloproteinase, MMP). La cellule tumorale utilise les rales et de plaquettes interagissent avec des molécules
MMP pour remodeler le tissu extracellulaire environ- d’adhésion situées au niveau des capillaires de l’organe
nant, mais à la différence des cellules normales, ce pro- cible selon des mécanismes probablement voisins de
cessus s’associe à une motilité accrue de la cellule ceux mis en jeu pour l’extravasation des leucocytes.
tumorale, lui permettant de progresser dans les tissus et L’amas de cellules tumorales et de plaquettes induit la
de les coloniser (voir : pour approfondir 2). Pour pro- production de médiateurs locaux permettant une rétrac-
gresser dans le tissu conjonctif, les cellules tumorales tion des cellules endothéliales et l’exposition de la
1142 LA REVUE DU PRATICIEN 2000, 50
Oncologie
membrane basale. La cellule tumorale pénètre la matrice ments cytotoxiques pour le traitement des tumeurs
conjonctive de l’organe cible en utilisant les facteurs de disséminées. Actuellement, des facteurs inhibiteurs des
motilité et les MMP, induit une néovascularisation avant métalloprotéase, et de l’angiogenèse sont en expérimen-
de proliférer pour donner une métastase. tation clinique.
La relative spécificité des organes sièges de métastases
pour un type de cancer donné est encore mal comprise. Il Incidence pronostique
est certain que cette spécificité résulte en partie de phéno-
mènes mécaniques : les organes qui sont des points de pas- La meilleure compréhension des mécanismes biolo-
sage obligés du flux sanguin pour certains organes (pou- giques de la cancérogenèse et notamment des altérations
mon, foie) sont plus fréquemment le siège de métastase. génétiques des cellules tumorales a conduit à de nou-
Cependant, d’autres paramètres interviennent probable- velles classifications des tumeurs humaines. Certaines
ment : des molécules d’adhésion avec des cellules tumo- maladies néoplasiques sont désormais identifiées sur la
rales spécifiques des cellules endothéliales d’un organe base d’une altération génétique spécifique (translocation)
donné ont été décrites dans certains modèles. En outre, il autant que sur l’analyse cytologique ou histologique
est probable que l’environnement tissulaire normal de classique : c’est le cas de la leucémie myéloïde chro-
l’organe touché (composants de la matrice, facteurs de nique et de la t(9,22), des sarcomes d’Ewing et de la
croissance produits in situ) favorise le développement de t(11, 22) et ses variantes, des lymphomes du manteau et
tel ou tel type cellulaire dans un site métastatique donné. de la t(11,14). Cette nosologie moléculaire des maladies
Enfin, l’un des paramètres essentiels influençant la a parfois permis d’individualiser des groupes de patients
croissance tumorale est la capacité d’une cellule tumorale avec un pronostic complètement différent d’autres
à susciter le développement d’une néovascularisation patients porteurs de maladies voisines ou similaires sur
tumorale et, en particulier, la différenciation et la crois- des bases cytologiques histologiques ou phénotypiques :
sance de cellules endothéliales. Ce processus, dénommé les lymphomes du manteau caractérisés par leur t(11,14)
angiogenèse, est indispensable à la croissance tumorale ont un pronostic moins bon que les patients porteurs
au-delà d’un volume de quelques millimètres cubes de d’autres lymphomes diffus B à petites cellules, les leu-
tumeur dans de nombreux modèles expérimentaux. La cémies aiguës non lymphoblastiques de l’enfant avec
croissance tumorale est en effet limitée au-delà de ce t(9,22) ou une translocation en 11q23 sont associées à
volume par la disponibilité en nutriments et en oxygène un pronostic défavorable.
des cellules tumorales. La capacité d’une tumeur à susci- En outre au sein d’un même groupe de maladies néo-
ter une néovascularisation semble indispensable au déve- plasiques, par exemple les adénocarcinomes du sein,
loppement de la tumeur, à la fois localement et au site des l’altération de l’expression d’un gène spécifique est
métastases. On a ainsi pu décrire dans certaines tumeurs corrélée à un pronostic particulier, souvent moins bon.
(carcinomes in situ du col de l’utérus) in vivo, un état C’est le cas pour les mutations inactivatrices de gènes
« prévasculaire », au cours duquel un petit amas de cel- suppresseurs de tumeur (p53 ou Rb pour des cancers du
lules tumorales est présent mais ne peut se développer au- sein, lymphomes, leucémies) pour la surexpression de
delà d’un certain volume, et une phase « vasculaire » où la proto-oncogènes codant pour des tyrosine kinases
tumeur développe une néovascularisation et peut croître récepteurs de facteurs de croissance (c-erbB2, dans les
et éventuellement disséminer. Des mécanismes similaires cancers du sein dans certains sarcomes), pour l’amplifi-
sont mis en jeu pour le démarrage de la croissance de cation de proto-oncogènes codant pour des facteurs de
métastases « dormantes » dans des modèles animaux et transcription (N-myc dans le neuroblastome), pour la
peut être chez l’homme. production in vivo de facteurs de croissance (VEGF,
Le passage d’une phase prévasculaire à une phase vas- IL6). Ces paramètres biologiques ne sont pas pour la
culaire est lié à la production, le plus souvent par les plupart étudiés en routine à l’heure actuelle. La présence
cellules tumorales elles-mêmes, de facteurs de croissance de ces anomalies moléculaires semble cependant
des cellules endothéliales, appelés facteurs angiogé- influencer la réponse à certains traitement antinéo-
niques. Ces facteurs de croissance sont des cytokines plasiques (efficacité des cytotoxiques) et il est donc
qui sont parfois également des facteurs de croissance possible qu’ils soient plus largement utilisés dans les
autocrines pour les cellules tumorales elles-mêmes. années à venir. En outre, le développement de traite-
Parmi ces facteurs on peut citer, le vascular endothelial ments spécifiques dirigés contre ces oncogènes (par
growth factor ou VEGF, l’angiogénine, les FGF1, 2 et 4, exemple, un anticorps monoclonal anti-erb-B2) nécessi-
le TGFα, l’hepatocyte growth factor ou HGF. tera probablement une analyse systématique de sa sur-
Ces cytokines produites par les cellules tumorales exer- expression. Enfin, la mise à disposition d’outils tels que
cent ainsi fréquemment des propriétés biologiques les puces à ADN, permettant l’analyse de milliers de
multiples et interviennent à des étapes différentes de la gènes dans une tumeur donnée et ainsi une analyse éten-
progression tumorale, modulant aussi bien la croissance due des anomalies génétiques de milliers de tumeurs, va
de la cellule, que sa motilité et sa capacité à induire une probablement bouleverser dans les années à venir à la
néovascularisation. La compréhension des mécanismes fois la classification nosologique de ces maladies et
biologiques de la dissémination tumorale permet désor- conduire à identifier des sous-groupes pronostiques et
mais d’envisager des stratégies autres que les traite- thérapeutiques encore insoupçonnés actuellement. ■
LA REVUE DU PRATICIEN 2000, 50 1143
LA CELLULE CANCÉREUSE
POUR EN SAVOIR PLUS Points Forts à retenir
Alberts B, Bray D, Lewis J, Raff M, Roberts K, Watson JD. Biologie • Les proto-oncogènes sont des gènes normaux
moléculaire de la cellule. 3e édition. Paris : Flammarion Médecine qui vont subir des mutations activatrices dans
Science, 1995. les cellules cancéreuses, les transformant ainsi
Les fiches résumés des oncogènes. Bull Cancer 1998 et 1999,
en oncogènes capables d’induire une division
volumes 85 et 86.
cellulaire incontrôlée.
• Ils codent souvent pour des protéines
impliquées dans la transmission du signal
mitogénique de la membrane plasmique
au noyau. Leur mutation induit généralement
leur activation permanente, rendant les cellules
POUR APPROFONDIR moins dépendantes aux facteurs de croissance
exogènes pour l’entrée en mitose.
• Les gènes suppresseurs de tumeurs ont
1 / Anti-oncogènes ou gènes suppresseurs pour rôle physiologique de freiner la division
de tumeurs cellulaire, lorsque la cellule n’est pas dans
une situation adéquate (manque de facteur
Ce sont les expériences de fusions cellulaires qui ont permis de montrer
de croissance, mutations de l’ADN). Leur
que le processus de transformation cellulaire pouvait provenir de la
destruction permet à la cellule cancéreuse
d’entrer en division, d’accumuler des anomalies
perte de fonction d’allèles normaux. En effet, la fusion d’une cellule
génétiques supplémentaires ou d’échapper
normale et d’une cellule maligne donne généralement naissance à une
aux signaux entraînant l’apoptose.
cellule ayant perdu le phénotype malin. Cela est dû à l’apport, par la • La surexpression de protéines anti-apoptotiques
cellule normale, de gènes qui sont altérés dans la cellule cancéreuse. est l’un des mécanismes moléculaires conduisant
Ces altérations sont de type récessif, puisque le phénotype tumoral à la cancérogenèse dans certains modèles.
ne peut pas s’exprimer dans la cellule hybride. Dans certains cas, la • La transformation d’une cellule normale
fusion de 2 cellules cancéreuses donne naissance à une cellule ayant en cellule cancéreuse fait intervenir plusieurs
perdu les caractères de malignité. Cette observation conforte l’hypo- des mutations consécutives de gènes suppresseurs
thèse selon laquelle un certain nombre de changements génétiques de tumeurs et d’oncogènes. Chez la plupart
différents interviennent au cours de la cancérogenèse. Enfin, par des individus, ces altérations génétiques de la
microtransfert, il est possible de supprimer le phénotype tumoral de cellule tumorale sont acquises. Cependant,
certaines cellules cancéreuses par transfert d’un seul chromosome. dans certains syndromes de cancers familiaux,
Les gènes perdus ou inactivés au cours de transformation maligne les individus atteints présentent une mutation
sont appelés gènes suppresseurs de tumeur car, à l’état physiolo- somatique qui inactive un gène, généralement
gique, ils codent pour des protéines impliquées dans le contrôle néga- un gène suppresseur de tumeur. Les individus
tif de la croissance cellulaire. affectés présentent ainsi une incidence accrue
de certaines tumeurs qui surviennent en outre
à un âge précoce.
• Les facteurs de croissance sont fréquemment
2 / Dissémination produits en excès par les cellules cancéreuses.
Ils interviennent à plusieurs étapes dans
la progression du cancer, agissant comme
Les métalloprotéases (matrix metalloproteinases, MMP) sont classées facteur anti-apoptotique, facteur de croissance,
en différentes familles : les collagénases interstitielles, les collagénases facteur de motilité cellulaire ou comme facteurs
de type IV, les stromélysines. L’expression de ces enzymes est phy- angiogéniques.
siologiquement très finement régulée dans le temps et dans l’espace. • La dissémination des cellules tumorales,
Dans les cellules cancéreuses, l’expression de ces enzymes est très à travers la membrane basale, dans le tissu
fortement corrélée à leur potentiel métastatique. Les collagénases de conjonctif, à travers la paroi des vaisseaux
type IV sont ainsi exprimées dans les cellules tumorales de cancers et dans les sites métastatiques fait intervenir
cutanés invasifs, mais pas dans les cellules épidermiques normales. l’altération de la structure ou de la fonction
Ces enzymes peuvent cependant être produites également par les des molécules d’adhésion à leur surface,
cellules non tumorales du stroma et, dans ce cas, les cellules tumo- la production d’enzymes capables de détruire
rales produisent des facteurs capables de convertir les pro-enzymes les fibres et les glycoprotéines de la matrice,
inactives en enzymes actives capables de dégrader le stroma. la production en excès de cytokines agissant
L’activation de ces enzymes s’effectue ainsi en cascade et la plasmine comme des facteurs de motilité, la production
paraît essentielle à l’activation de cette cascade. De fait, la production de néovaisseaux capables de vasculariser la
d’activateurs du plasminogène proche de l’urokinase (Upa) est très tumeur primaire ou la métastase en croissance.
fréquemment observée par les cellules tumorales in vitro et in vivo. • La caractérisation des anomalies moléculaires
Physiologiquement, l’activité enzymatique de ces métalloprotéases des cellules cancéreuses permet la mise en place
est contrôlée par des molécules appelées, inhibiteurs tissulaires des d’une nouvelle classification de ces maladies
métalloprotéases (TIMP-1 et 2). La capacité métastatique des lignées reposant sur des critères moléculaires.
tumorales résulte ainsi probablement d’une balance entre l’expres- Certaines anomalies génétiques constituent en
sion des MMP ou d’activateurs de ces enzymes (Upa) et la présence outre un facteur pronostique pour certaines
d’inhibiteurs de ces enzymes (TIMP) ou de leurs activateurs (plasmi- affections néoplasiques.
nogen activator inhibitors ou PAI).
1144 LA REVUE DU PRATICIEN 2000, 50
Vous aimerez peut-être aussi
- 98 1011Document7 pages98 1011hizballah27100% (1)
- 98 905Document4 pages98 905hizballah27Pas encore d'évaluation
- 98 913Document6 pages98 913hizballah27Pas encore d'évaluation
- 98 875Document5 pages98 875hizballah27Pas encore d'évaluation
- 98 787Document10 pages98 787hizballah27Pas encore d'évaluation
- 98 771Document6 pages98 771hizballah27100% (1)
- 98 765Document5 pages98 765hizballah27Pas encore d'évaluation
- 98 667Document4 pages98 667hizballah27Pas encore d'évaluation
- 98 661Document6 pages98 661hizballah27Pas encore d'évaluation
- 98 671Document4 pages98 671hizballah27Pas encore d'évaluation
- 98 545Document4 pages98 545hizballah27100% (1)
- Nouveaux Sujets MédecineDocument44 pagesNouveaux Sujets MédecineMoustapha SarrPas encore d'évaluation
- 173 12Document150 pages173 12Pride Algerian ツPas encore d'évaluation
- CoursDocument16 pagesCoursKoki kokiPas encore d'évaluation
- 6-Cytotoxicité Nécrose ApoptoseDr - Boudemagh KDocument11 pages6-Cytotoxicité Nécrose ApoptoseDr - Boudemagh KAnouar BezzichePas encore d'évaluation
- Huile de Nigelle Le Guide Complet Pour Toutes Les Maladies3Document32 pagesHuile de Nigelle Le Guide Complet Pour Toutes Les Maladies3Ziyad Akchouch100% (2)
- Fiche 10. ApoptoseDocument12 pagesFiche 10. ApoptoseMey ZPas encore d'évaluation
- Le Cycle CellulaireDocument30 pagesLe Cycle CellulaireMohamadou Lamine KanePas encore d'évaluation
- 1-S2.0-S2405844022037951-Main FRDocument18 pages1-S2.0-S2405844022037951-Main FRmalak boudjemaPas encore d'évaluation
- ApoptoseDocument34 pagesApoptoseYouness Khalfaoui100% (1)
- Cytotoxicité, Nécrose, ApoptoseDocument10 pagesCytotoxicité, Nécrose, ApoptoseAyoub BENSAKHRIAPas encore d'évaluation
- Échappement Et Tolérance Des Tumeurs À L'apoptose: Pierre-Yves Dietrich Paul R. WalkerDocument8 pagesÉchappement Et Tolérance Des Tumeurs À L'apoptose: Pierre-Yves Dietrich Paul R. WalkerNsangwaPas encore d'évaluation
- Mort CellulaireDocument43 pagesMort CellulaireRahil KamasPas encore d'évaluation
- Guide Complet de La Nigelle V2.2Document35 pagesGuide Complet de La Nigelle V2.2Jee ProdPas encore d'évaluation
- Les Voies Métaboliques RevuDocument305 pagesLes Voies Métaboliques Revulord47Pas encore d'évaluation
- Apoptose PDFDocument38 pagesApoptose PDFbruno100% (1)
- CB Sujet Biocell/Embryo/HistoDocument21 pagesCB Sujet Biocell/Embryo/Histosun-nee-chan9Pas encore d'évaluation