Académique Documents
Professionnel Documents
Culture Documents
98 787
Transféré par
hizballah27Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
98 787
Transféré par
hizballah27Droits d'auteur :
Formats disponibles
Gynécologie - Obstétrique
B 153
Cancers du sein
Epidémiologie, anatomie pathologique, dépistage, diagnostic,
évolution, principes du traitement
Pr Serge UZAN, Dr Rodolphe GAUDET
Service de gynécologie-obstétrique et médecine de la reproduction, département des tumeurs du sein (Pr S. Uzan),
hôpital Tenon, 75020 Paris
Points Forts à comprendre Facteur de risque (voir : pour approfondir / 1)
1. Risque familial
• Cancer fréquent, avec une incidence annuelle Il est un des plus importants. Une histoire familiale de can-
de 25 à 30 000 nouveaux cas, le cancer du sein est cer du sein est un facteur de risque dont l’importance est
la première cause de décès féminin par cancer variable :
(23 %). – risque relatif (RR) > 4 en cas d’existence chez une femme
• L’âge moyen du diagnostic est de 55 ans et, quel de la famille d’un cancer du sein bilatéral ;
que soit le mode de découverte, seule l’histologie – risque relatif de 2 à 3 en cas d’existence d’un cancer chez
apporte la certitude diagnostique. une parente au premier degré (mère, sœur, fille) ;
• La prise en charge thérapeutique doit être – risque relatif de 1,5 en cas de lien de parenté au second
multidisciplinaire, et l’amélioration du pronostic degré (cousine, grand-mère, tante).
passe par un dépistage le plus précoce possible, Le risque familial est d’autant plus élevé que la maladie
avant la dissémination métastatique. s’est déclarée de façon plus précoce chez la parente. Si la
femme est porteuse d’un ou plusieurs gènes de prédispo-
sition familiale au cancer du sein (type BRCA 1 ; Breast
Cancer gene 1), le risque relatif est de 10.
2. Risque histologique
Épidémiologie Il concerne :
– antécédents personnels de cancer du sein (risque relatif
Fréquence
> 4) ;
Le cancer du sein est le plus fréquent des cancers féminins – hyperplasie atypique, canalaire ou lobulaire (risque rela-
avec de 25 à 30 000 nouveaux cas par an en France, 23 % tif de 4 à 5, en l’absence d’antécédent familial).
des cancers de la femme sont des cancers du sein. Statis- – hyperplasie sans atypie, adénoses (risque relatif < 2) ;
tiquement, on estime qu’une femme sur 11 développera un – pas de risque pour la mastose sclérokystique et les adé-
cancer du sein au cours de sa vie. L’incidence annuelle, nofibromes.
régulièrement croissante (1,5 % par an), est estimée à envi-
ron 80 pour 100 000 femmes. 3. Risque hormonal
L’âge moyen du diagnostic est de 55 ans, et 60 % des • Facteurs endogènes (risque relatif de 2).
patientes ont entre 45 et 75 ans. Il est rare avant 40 ans Ce sont : puberté précoce ; cycles anovulatoires ; nulli-
(10 %). gestité ; première grossesse tardive ; absence d’allaite-
ment ; ménopause tardive.
C’est une maladie grave, responsable d’environ 10 000 • Facteurs exogènes
décès par an. Le cancer du sein représente la première cause L’absence d’impact des traitements hormonaux substitu-
de mortalité chez les femmes de 35 à 55 ans. Il occupe le tifs ou de la contraception orale est remise en cause actuel-
premier rang de mortalité par cancer chez la femme. L’in- lement, en particulier en fonction de la durée d’exposition.
cidence annuelle de décès par cancer du sein est de 20 à 25
pour 100 000 femmes. 4. Risque environnementaux
La survie globale, tous stades confondus (avec des écarts Ils sont représentés par des conditions socio-économiques
importants selon les stades) est d’environ 65 % à 5 ans. élevées, et des facteurs alimentaires (obésité, régime riche
Ainsi le cancer du sein constitue un problème majeur de en graisses animales, alcool).
santé publique, justifiant la mise en place et la poursuite 5. Risque radique
des actions de prévention, de dépistage et de recherche thé- Il est classique, et constitue une situation à risque relatif
rapeutique. de 3.
LA REVUE DU PRATICIEN (Paris) 1998, 48 787
CANCERS DU SEIN
Anatomie pathologique Dépistage
Carcinomes primitifs du sein But
Ce sont des adénocarcinomes (tumeurs épithéliales D’intérêt majeur, son objectif est de dépister le cancer à un
malignes à différenciation glandulaire). stade précoce, au mieux infra-clinique et surtout avant l’at-
teinte ganglionnaire afin d’améliorer le taux de survie et
1. Carcinomes in situ de permettre une chirurgie conservatrice (voir : pour appro-
Il sont soit canalaires (galactophore) soit lobulaires (unité fondir / 2).
terminale ducto-lobulaire) et présentent tous les critères Deux types de dépistage peuvent être envisagés : le dépis-
cytologiques de la malignité, sans dépasser la membrane tage de masse, visant 65 à 70 % d’une tranche d’âge de la
basale ni infiltrer le tissu conjonctif sous-jacent. Ils n’ont population totale ; et le dépistage individuel orienté par
pas de risque métastatique. l’âge et les facteurs de risque.
Technique
2. Carcinomes infiltrants
L’autopalpation et l’examen clinique sont certes utiles, mais
On distingue : ne sont plus recommandés comme des techniques de dépis-
– carcinome canalaire infiltrant de forme commune (forme tage, même si l’examen clinique des seins reste un élément
la plus fréquente (81 %)) ; essentiel de l’examen systématique.
– carcinome canalaire infiltrant avec composante intraca- Le dépistage de masse comporte un à deux clichés par sein
nalaire prédominante (4 %) ; avec double ou triple lecture. Les campagnes les plus effi-
– carcinome lobulaire infiltrant (10 %), volontiers bilaté- caces concernent la tranche d’âge 50-65 ans avec une mam-
ral ; mographie tous les 2 ans.
– formes particulières : carcinome mucineux ou colloïde Le dépistage individuel commence plus tôt (5 ans avec le
(1 %), de la femme âgée, de bon pronostic ; carcinome premier cas de cancer familial) et sa fréquence dépend de
médullaire, de bon pronostic ; carcinome tubuleux, de bon l’« intensité » du risque.
pronostic ; carcinome adénoïde hystique ou cylindrome,
de bon pronostic ; carcinome papillaire (très rare). Diagnostic
3. Cancers inflammatoires Circonstances de découverte
Ils sont liés à des emboles lymphatiques disséminés avec Elles sont variées :
invasions multiples atteignant le derme profond. Ils pré- – tuméfaction découverte par la patiente ou lors d’un exa-
sentent un haut risque métastatique. men systématique ;
– mammographie systématique ou de dépistage ;
4. Maladie de Paget du mamelon (2 %) – écoulement mamelonnaire séreux ou sanglant ;
Cette lésion correspond à une extériorisation au niveau du – anomalie du mamelon : maladie de Paget (ulcération, pru-
mamelon d’un carcinome mammaire sous-jacent, de nature rit, lésion eczématiforme) ; rétraction du mamelon ;
canalaire, in situ et parfois infiltrant. – déformation du sein par une masse tumorale ou par le
Elle se manifeste par une érosion ou une lésion eczémati- « capiton » d’une attraction cutanée ; voire une tumeur
forme du mamelon et correspond à une infiltration des infiltrant ou ulcérant la peau ;
couches épidermiques par les cellules carcinomateuses. – sein inflammatoire ;
– rarement une adénopathie ou une métastase, et beaucoup
Autres tumeurs malignes du sein plus rarement une gêne fonctionnelle (mastodynie).
1. Sarcomes primitifs du sein Examen clinique
Ils se subdivisent en 2 catégories : Il comporte trois étapes.
– sarcomes phyllodes et sarcomes stromaux : rares (< 1 %),
ils peuvent survenir à tout âge et il n’existe pas de terrain 1. Interrogatoire
prédisposant tant sur le plan des lésions mammaires pré- Il précise : l’âge, la profession, le statut familial ; les anté-
existantes que des facteurs hormonaux ; l’évolution est don- cédents médico-chirurgicaux et gynéco-obstétricaux (fac-
née par l’extension locale ; l’extension ganglionnaire est teurs de risque, ménopause, traitement hormonal, antécé-
exceptionnelle ; dent d’irradiation…) ; les antécédents familiaux du cancer
– angiosarcomes : de pronostic défavorable. du sein (intérêt de réaliser un arbre généalogique s’il existe
plus d’un cas) ; le délai passé depuis le premier symptôme ;
2. Lymphomes malins non hodgkiniens du sein le mode évolutif ; le caractère douloureux ou non ; s’il existe
d’anciens clichés de mammographie ou des échographies.
3. Métastases mammaires 2. Examens cliniques (voir : pour approfondir / 3)
Elles sont rares et peuvent témoigner d’un cancer primitif • À l’inspection, il recherche : une asymétrie, une défor-
de nature variable : mélanome, ou cancers pulmonaire, mation du contour mammaire, une modification du galbe
digestif, uro-génital. (fossette, tuméfaction) ; une anomalie de surface : ride cuta-
788 LA REVUE DU PRATICIEN (Paris) 1998, 48
Gynécologie - Obstétrique
née, peau d’orange, signes inflammatoires ; un nodule face, de profil et des prolongements axillaires. Son inter-
cutané ou une ulcération dans les cas avancés ; une ano- prétation est parfois difficile chez les femmes jeunes (seins
malie du mamelon : rétraction, déviation de son axe, sur- denses) et pour les tumeurs très postérieures ou du pro-
élévation, érosion. longement axillaire.
• À la palpation, on retrouve le plus souvent une tumeur Elle est très évocatrice de la malignité si elle retrouve les
unique, unilatérale et indolore. anomalies suivantes.
Les arguments en faveur de la malignité sont : le caractère • Opacité stellaire : c’est la traduction mammographique la
mal limité ; la dureté ; l’adhérence à la peau soit sponta- plus classique du cancer du sein. Elle est constituée d’un
née réalisant une fossette, soit lors du pincement avec signe centre dense associé à une collerette de spicules plus ou
du capiton ; une peau d’orange ; l’adhérence au plan pro- moins longues. Il peut s’y associer des microcalcifications,
fond (muscle grand pectoral) qui se recherche par la un halo clair périlésionnel, un épaississement et (ou) une
manœuvre d’adduction contrariée de Tillaux : la mobilité rétraction cutanée en regard de la lésion, une désorganisa-
du nodule en l’absence de contraction musculaire et sa tion architecturale, des adénopathies axillaires à centre dense.
fixité lors de la contraction signent l’adhérence au grand • Opacité nodulaire arrondie ou ovalaire, à contours régu-
pectoral ; l’existence d’adénopathies dures voire fixées. liers ou non. Elle peut parfois simuler une lésion bénigne
L’examen de l’autre sein doit être systématique car 10 % (carcinome médullaire). Elle peut aussi présenter un bord
des cancers sont bilatéraux d’emblée. en queue de comète, correspondant à des spicules locali-
sés. Une opacité à limites apparemment nettes doit faire
3. Examen gynécologique (frottis cervico- rechercher des signes évocateurs de malignité : densité éle-
vaginaux) et général complet vée, perte partielle du contour, microcalcifications dans ou
au voisinage de l’opacité.
Examens complémentaires • Une désorganisation architecturale : aspects de désaxa-
tion et de convergences des travées fibreuses.
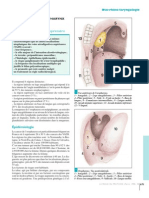
1. Mammographie (fig. 1 à 4) • Microcalcifications : elles peuvent être associées à une
(voir : pour approfondir / 4) opacité tumorale ou, à l’inverse, être isolées. Elles sont
Examen essentiel, réalisé dans les 10 premiers jours du alors le seul marqueur radiologique d’un cancer infracli-
cycle, elle est bilatérale et comparative avec des clichés de nique. Les aspects possibles des microcalcifications sont
1 3
Opacité stellaire typique en mammo- Microcalcification type V, suspecte de
graphie avec très fines microcalcifications malignité (comédocarcinome) : cliché
(et une calcification vasculaire). 2 agrandi.
Opacité nodulaire maligne en mam-
mographie.
4 5
Microcalcification type V avec guide en place Échographie mammaire avec image typique-
pour microbiopsie sous stéréotaxie. ment suspecte : grand axe vertical, image irrégu-
lière, atténuation postérieure avec cône d’ombre.
LA REVUE DU PRATICIEN (Paris) 1998, 48 789
CANCERS DU SEIN
très polymorphes. Il faut rechercher des critères de mali- particulier des seins porteurs de prothèses (aide au dia-
gnité parmi les suivants : forme vermiculaire, irrégulière, gnostic de rupture prothétique et aide à la détection de petits
polymorphisme, taille et densité différentes, nombre impor- cancers juxtaprothétiques).
tant, regroupement en foyer, foyer de forme triangulaire à
sommet mamelonnaire. 6. Galactographie
Elle peut parfois retrouver : une image d’aspect bénin, Elle est systématiquement pratiquée devant un écoulement
homogène et bien limitée ; un kyste à paroi épaisse ; une mamelonnaire à la recherche d’un refoulement, d’une
lésion multifocale ; une lésion controlatérale ; l’absence lacune irrégulière ou d’une amputation d’un galactophore.
d’anomalie radiologique, dans 3 % des cas.
7. Écho-doppler couleur
2. Échographie L’étude par écho-doppler couleur de la vascularisation ne
Examen de complément indispensable de la mammogra- permet pas de prédire de façon fiable la malignité d’un
phie dès lors qu’il existe une anomalie clinique, radiolo- nodule.
gique ou une suspicion de cancer, elle permet une meilleure
définition chez la femme jeune aux seins denses. 8. Imagerie par résonance magnétique
L’image échographique maligne typique est celle d’une Encore réservée à certains centres, elle semble prometteuse,
masse hypoéchogène, hétérogène, solide, à cône d’ombre en particulier dans les cas de diagnostic difficile, notam-
postérieur, non compressible, à contours irréguliers et pré- ment lorsque le couple mammographie-échographie est le
sentant des dimensions antéro-postérieures supérieures à moins performant : récidive après traitement conservateur,
ses dimensions transversales (à grand axe vertical) (fig. 5). récidive sur reconstruction, apparition de zones carcino-
Il existe parfois des végétations à l’intérieur d’une tumeur mateuses au sein d’une mastopathie à risque.
nécrosée d’aspect kystique. L’imagerie par résonance magnétique (IRM) présente aussi
un intérêt diagnostique dans la recherche de la multifoca-
3. Cytologie
lité d’une lésion maligne déjà décelée.
Intéressante en cas de tumeur palpable, de nodule mam- Enfin, certains l’utilisent pour étudier la réponse à la chi-
mographique et surtout échographique, elle est réalisée par miothérapie.
ponction à l’aiguille fine de la masse. Sa fiabilité repré- Sa valeur prédictive négative est excellente : l’absence de
sente une spécificité supérieure à 95 % et une valeur pré- rehaussement du signal une minute après injection de gado-
dictive positive de cancer de 99 %. Néanmoins sa négati- linium élimine quasi totalement le diagnostic de malignité
vité n’élimine pas le diagnostic (5 à 10 % de faux négatif). (moins de 3 % de faux négatifs).
Sa performance est améliorée lorsqu’elle est pratiquée sous
contrôle échographique. Elle est toutefois non significative 9. Triplet diagnostique
dans 5 à 10 % des cas. En cas de triplet concordant (tumeur cliniquement maligne
4. Anatomopathologie + mammographie typique + cytologie positive), le dia-
Seule l’étude anatomopathologique affirme avec certitude gnostic de cancer est fiable dans 99 % des cas. Si le triplet
le caractère néoplasique de la lésion. Elle est le préalable est discordant, la vérification histologique s’impose.
indispensable à toute attitude thérapeutique, ainsi qu’au
bilan d’extension. elle permet, en outre, de préciser les
Formes cliniques
caractéristiques histologiques de la tumeur, de réaliser la 1. Cancers infracliniques
gradation histopronostique de Scarff, Bloom et Richard- Leur nombre augmente du fait du dépistage. Il peut s’agir :
son (SBR) (voir : pour approfondir / 5) et, enfin, d’effec- soit de cancers in situ, découverts à l’occasion de micro-
tuer une évaluation des récepteurs hormonaux aux œstro- calcification, qui peuvent être multifocaux et/ou bilatéraux
gènes et à la progestérone par dosage biochimique et (ou) (en particulier pour les lobulaires in situ) ; soit de petits
par immunohistochimie. cancers invasifs ou micro-invasifs.
Plusieurs méthodes peuvent être employées :
– le forage biopsique (tru-cut, forage biopsique), sur une 2. Cancers avec écoulement mamelonnaire
tumeur palpable ; L’écoulement suspect est typiquement uni-orificiel, san-
– la microbiopsie sous repérage en cas de lésion infracli- glant et unilatéral. Mais il peut être pluriorificiel ou sim-
nique (on utilise la stéréotaxie en cas de lésion radiolo- plement sale. L’examen cytologique avec frottis de l’écou-
gique, et le repérage échographique en cas de lésion visible lement peut orienter le diagnostic en montrant des cellules
en échographie) ; néoplasiques. La mammographie, l’échographie et la galac-
– la biopsie/exérèse chirurgicale avec examen histologique tograophie doivent être systématiques, permettant de visua-
extemporané. liser une petite lésion. Mais seule l’exérèse chirurgicale du
galactophore pathologique avec examen histologique
5. Radiographie numérisée
affirme le diagnostic de cancer.
Sa résolution spatiale est très inférieure à celle obtenue en
mammographie traditionnelle. Elle peut cependant se révé- 3. Formes topographiques
ler utile dans la recherche de microcalcifications ou d’al- On distingue les formes suivantes :
térations structurales dans les seins très denses. Elle per- – cancer des glandes mammaires accessoires (du prolon-
met d’améliorer la surveillance des seins opérés et en gement axillaire au sillon sous-mammaire) ;
790 LA REVUE DU PRATICIEN (Paris) 1998, 48
Gynécologie - Obstétrique
– cancer du prolongement axillaire : caractérisé par sa loca- – cancers en poussée évolutive : ils correspondent à une
lisation le long du bord inférieur du grand pectoral et par entité clinique regroupant les carcinomes présentant des
leur adhérence précoce à la peau, il faut le différencier signes cliniques d’inflammation au niveau de la peau sus-
d’une adénopathie axillaire ; le pronostic et le traitement jacente (rougeur, chaleur, douleur, œdème) (voir : pour
sont identiques à ceux d’une tumeur des quadrants externes approfondir / 6). Ils représentent 5 à 10 % des cancers quel
du sein ; que soit l’âge et contre-indiquent une prise en charge chi-
– cancer du sillon sous-mammaire : de diagnostic parfois rurgicale première.
difficile chez la femme obèse aux seins lourds, il répond
souvent à une tumeur de petite taille adhérent à la peau et Diagnostic différentiel
(ou) au plan profond ;
– cancer des quadrants externes : diffusant vers les gan- 1. Devant un nodule du sein
glions axillaires ; • L’adénofibrome, tumeur bénigne de la femme jeune,
– cancer des quadrants internes ou central : diffusant vers ferme, mobile et indolore, répond à la mammographie à
les chaînes axillaires et mammaires internes ; une image régulière avec parfois des macrocalcifications,
– cancers bilatéraux ; et dont la taille clinique est identique à la taille radiolo-
– cancers multifocaux. gique.
4. Formes selon le terrain • Le kyste, tumeur rénitente, douloureuse, est variable sui-
• Chez l’homme : il est 100 fois plus rare que chez la vant le cycle, anéchogène à l’échographie ; la ponction
femme, mais grave avec extension lymphatique précoce. ramène un liquide citrin de cytologie négative, et affaisse
• Chez la femme enceinte : sa fréquence est de l’ordre de le kyste.
1 à 3 cancers pour 10 000 grossesses (2 % de l’ensemble • L’hématome et la cytostéatonécrose post-traumatique
des cancers du sein). sont envisagés selon le contexte ; la mammographie peut
révéler des calcifications, mais celles-ci sont souvent arci-
La grossesse ne semble pas en soi aggraver le pronostic de
formes et situées en périphérie de la lésion traumatique.
ces cancers, mais il faut préciser que les cancers survenant
en cours de grossesse sont déjà diagnostiqués à un stade • L’abcès du sein peut poser des problèmes diagnostiques
avancé, que l’âge médian de survenue est de 35 ans, que avec les formes inflammatoires de cancer.
l’atteinte ganglionnaire est plus fréquente et qu’il s’agit Néanmoins, le cancer du sein peut simuler toutes ces
souvent de formes peu différenciées (SBR 3, récepteurs formes ou y être associé. Ainsi, tout nodule du sein doit
hormonaux négatifs). Ces éléments sont des facteurs pro- faire l’objet d’une exploration minutieuse et complète pour
nostiques péjoratifs indipendants de la grossesse. écarter une suspicion de malignité.
Étant donné qu’il existe souvent un important retard au dia- 2. Devant un écoulement mamelonnaire
gnostic du fait d’une grossesse et des difficultés cliniques
d’examen liées aux modifications gravidiques mammaires, L’ectasie galactophorique et le papillome sont de diagnos-
il importe de ne pas différer les explorations, et ce quel que tic histologique sur pièce d’exérèse chirurgicale.
soit le stade de la grossesse. Rappelons que la palpation
des seins doit systématiquement être effectuée dès le pre- 3. Devant des microcalcifications
mier examen de grossesse. Il importe de définir le type, le nombre, l’aspect et la dis-
Sur le plan thérapeutique, la chirurgie est toujours possible. position des microcalcifications : la classification de Legal
La radiothérapie est déconseillée et sera effectuée en post- est la plus couramment employée. Néanmoins seule l’ana-
partum. La chimiothérapie, sauf nécessité vitale (cancer lyse histologique permet d’affirmer un diagnostic de béni-
inflammatoire en poussée évolutive, forme métastatique), gnité ou de malignité.
ne sera administrée qu’à partir du 2e trimestre (risque téra-
togène au 1er trimestre).
L’interruption thérapeutique de grossesse est à réserver aux Évolution
formes graves nécessitant une prise en charge thérapeu-
tique urgente. Si le cancer survient dans la seconde moitié Bilan d’extension
du 2e trimestre, ou au 3e trimestre de la grossesse et que la
femme souhaite mener celle-ci à terme, il importe de trai-
1. Extension locorégionale
ter la patiente sans retard et d’effectuer l’accouchement une Elle est jugée sur l’examen clinique et les explorations
fois la viabilité fœtale établie. radiologiques, permettant de classer la tumeur selon sa
taille et l’existence ou non d’adénopathies satellites. Elle
5. Formes anatomiques est complétée par l’exploration chirurgicale. L’apprécia-
On distingue : tion clinique de l’évolutivité locale permet la codification
– maladie de Paget du mamelon ; PeV (poussée évolutive) de valeur pronostique.
– squirrhe atrophique de la femme âgée : d’évolution lente,
avec adénopathies tardives, cette forme est caractérisée par 2. Extension générale
l’importance de la réaction fibreuse entraînant une rétrac- La réalisation d’un examen clinique complet et de divers
tion progressive avec disparition de la glande mammaire, examens paracliniques permet d’orienter la recherche de
puis une ulcération plaquée sur le gril costal ; métastases :
LA REVUE DU PRATICIEN (Paris) 1998, 48 791
CANCERS DU SEIN
– hépatiques (bilan biologique avec dosage de la gamma – un groupe de très mauvais pronostic dont la survie sans
GT et des phosphatases alcalines, transaminases, bilirubine récidive à 5 ans est inférieure à 30 % (cancers inflamma-
et échographie hépatique) ; toires et cancers à forte invasion axillaire avec plus de
– osseuses (scintigraphie osseuse corps entier, radiogra- 8 ganglions histologiquement envahis) ;
phies osseuses orientées par des signes fonctionnels) ; – un groupe de très bon pronostic dont la survie sans réci-
– pulmonaires et pleurales (radiographie pulmonaire de dive à 5 ans est proche de 95 % (cancers de moins de 1 cm,
face et de profil, scanner thoracique si anomalies) ; de grade SBR I, sans invasion axillaire, et a fortiori can-
– cutanées (examen clinique) ; cers in situ) ;
– cérébrales (examen neurologique complet et scanner sur – un groupe de pronostic intermédiaire, représentant la
signe d’appel) ; majorité des cancers du sein, et dans lequel la survie est
– ovaires (échographie pelvienne pour le cancer lobulaire). corrélée au T, au N, au SBR et aux paramètres biopatho-
Le dosage initial des marqueurs tumoraux (CA 15-3) a sur- logiques (récepteurs hormonaux, ploïdie, phase S…).
tout un intérêt lors de la surveillance ultérieure.
3. Évolution du terrain Principes du traitement
Elle permet de préciser l’état général de la patiente, et
recherche une éventuelle contre-indication à un traitement. Méthodes
Pronostic Le cancer du sein est à considérer comme une maladie hété-
rogène à la fois locale et générale. Schématiquement, le
1. Facteurs pronostiques traitement devra avoir pour but le contrôle locorégional
L’analyse des facteurs pronostiques permet d’identifier les (rôle de la chirurgie et de la radiothérapie) et la prévention
patientes à haut risque métastatique et (ou) de récidive ou le traitement des métastases (rôle de la chimiothérapie
locale. Ils sont subdivisés en trois classes. et de l’hormonothérapie).
• Éléments cliniques et morphologiques de mauvais pro- La prise en charge thérapeutique ne se conçoit qu’en équipe
nostic : pluridisciplinaire.
– taille anatomique de la tumeur (> 3 cm) ;
– caractère multifocal ou bilatéral ; 1. Traitement locorégional
– envahissement histologique des ganglions axillaires (sur- • Chirurgie : le traitement chirurgical aura trois objectifs :
tout si leur nombre est supérieur à trois et s’il existe une – la confirmation du diagnostic : examen histologique
rupture capsulaire) ; extemporané de la pièce de tumorectomie ;
– âge (< 40 ans) ; – le recueil des principaux éléments du pronostic ;
– grade histopronostique (SBR) coté à III ; – le traitement locorégional proprement dit : la mammec-
– type histologique de la tumeur ; tomie radicale modifiée selon Patey, retire la totalité de la
– présence d’emboles lymphatiques ou vasculaires ; glande mammaire, la plaque aréolo-mamelonnaire et
– envahissement cutané ou pariétal profond ; conservant les muscles pectoraux ; on y associe un curage
– dissémination au mamelon si mastectomie. axillaire homolatéral. Dans certains cas, la mammectomie
• Éléments évaluant l’activité proliférative tumorale : le est complétée par une radiothérapie ; la chirurgie limitée
taux des récepteurs hormonaux systématiquement utilisés, (tumorectomie, quadrantectomie) associée à un curage axil-
est corrélé au degré de différenciation de la tumeur ; ils laire homolatéral (étages inférieur et moyen du creux axil-
définissent des indices de bon pronostic et une hormono- laire) est de plus en plus fréquente. Elle est toujours suivie
sensibilité de la tumeur. d’une irradiation complémentaire. Elle est pratiquée chez
L’étude du cycle cellulaire par cytométrie de flux permet une femme prévenue du risque de mammectomie.
de déterminer deux critères : l’index d’ADN et le pour- • Radiothérapie : l’irridiation externe utilise des photons
centage de cellules en phase S de synthèse d’ADN sont de de haute énergie : Cobalt 60 (puissance énergétique de
plus en plus utilisés. 1,25 MeV) ou accélérateurs de particules (6 MeV). Cette
Les oncogènes et anti-oncogènes : C-erb b2, c-myc. irradiation doit inclure la totalité de la glande mammaire
• Éléments évaluant le potentiel invasif tumoral (traitement conservateur) et (ou) de paroi thoracique (mam-
On peut évaluer : mectomie), ainsi que les aires ganglionnaires (axillaires,
– protéases : cathepsine D (sélectionne en cas de taux élevé sus- et sous-claviculaires et la chaîne mammaire interne).
les patientes à haut risque métastatique, notamment chez L’irridiation de base délivre de 45 à 50 Gray en 5 à
les N-) ; inhibiteurs et activateurs du plasminogène ; 6 semaines. En cas de traitement conservateur, le lit tumo-
– collagénases. ral est susceptible de recevoir un complément soit par une
radiothérapie externe localisée, soit par une irradiation
2. Survie interstitielle (curiethérapie par des fils d’iridium 192
La survie globale est de 65 % à 5 ans, et de 50 % à 10 ans implantés localement).
(tous stades confondus).
Elle dépend de nombreux facteurs pronostiques et théra- 2. Traitement général
peutiques et l’on peut schématiquement individualiser trois Il comporte deux volets volontiers associés : la chimiothé-
grands groupes : rapie et l’hormonothérapie. Le rôle du traitement général
792 LA REVUE DU PRATICIEN (Paris) 1998, 48
Gynécologie - Obstétrique
est d’éradiquer la maladie micro-métastatique infraclinique
potentiellement présente au moment du diagnostic. Sché- Stratégie thérapeutique :
matiquement, 40 % des cancers du sein sont virtuellement forme typique - tumeur < 3 cm
guéris après un traitement locorégional exclusif. Les trai-
tements systémiques sont donc administrés à des patientes
sélectionnées comme étant à haut risque métastatique (fac- Tumorectomie
+ examen histologique extemporané
teurs pronostiques).
• Chimiothérapie : les protocoles, à type de polychimio-
Négatif :
thérapie, varient selon les équipes mais les agents les STOP Positif
plus utilisés sont : le 5FU, le cyclophosphamide, le
méthotrexate, les anthracyclines et les taxoïdes. Curage axillaire
Les indications sont les suivantes :
– formes métastatiques, permettant d’améliorer la survie
Histologie complète
(médiane légèrement inférieure à 2 ans) ;
– chimiothérapie néoadjuvante : avant tout traitement loco-
régional dans les formes évoluées (en particulier si un trai- N+ N– Mastectomie
ou facteurs bon pronostic
tement conservateur est recherché), ou en poussée inflam- de mauvais Si taille > ou si composante
matoire ; pronostic intracanalaire étendue (> 2,5 cm)
– chimiothérapie adjuvante afin de diminuer la fréquence
des métastases, son efficacité n’a été démontrée que chez Chimiothérapie
les femmes ayant des facteurs de pronostic défavorable.
Auparavant réservée aux patientes préménopausées, elle
Radiothérapie
est aujourd’hui également utilisée en postménopause.
• Hormonothérapie : elle est employée pour les tumeurs
présentant des récepteurs aux œstrogènes. On utilise des Ménopausée Non ménopausée
anti-œstrogènes (tamoxifène) de façon isolée chez les
Si facteurs pronostiques Rien
patientes ménopausées ou associés chez les femmes non Hormonothérapie très défavorables
ménopausées à une castration chimique (analogues de la
LH-RH luteiniging hormone - releasing hormone), chirur- d'autant que récepteurs +
/ tamoxifène / 5 ans Castration
gicale (ovariectomie bilatérale) ou radiothérapique (irri-
diation ovarienne bilatérale). Ces molécules en se fixant
sur le récepteur des œstrogènes (avec une grande affinité) Hormonothérapie
provoquent une inhibition compétitive, bloquant l’action
des œstrogènes sur le sein et l’os, d’où la nécessité d’une
castration (spontanée ou provoquée). Il faut noter l’action
agoniste de ce traitement sur la muqueuse endométriale. irradiation), puis chimiothérapie adjuvante (+ ou - hormo-
L’hormonothérapie est aussi utile en cas d’échappement nothérapie).
thérapeutique.
3. En cas de métastases
Indications thérapeutiques On associe au traitement locorégional, une chimiothérapie
(voir : pour approfondir / 7, 8) néoadjuvante puis adjuvante et une hormonothérapie. Le
1. Tumeurs limitées traitement local des métastases sera fonction de leur siège
(radiothérapie, chirurgie de stabilisation d’une fracture…).
• Les tumeurs de petit volume : T1, T2 < 3 cm, N0, N1,
M0, peuvent bénéficier d’un traitement conservateur asso- 4. Formes particulières
ciant tumorectomie, curage axillaire et irradiation post-
• Carcinome canalaire in situ : le traitement se limite en
opératoire.
principe au traitement locorégional. La fréquente multifo-
• Les tumeurs T2 > 3 cm sont traitées par mammectomie,
calité des lésions invite à un geste chirurgical très large
curage axillaire et irradiation postopératoire. Cette attitude
(mammectomie), d’autant préférable qu’il s’agit d’une
est discutée, certaines équipes proposant une chimiothéra-
lésion de haut grade et de taille supérieure à 2 cm. En cas
pie néoadjuvante pour réduire le volume tumoral afin de
de cancer in situ très localisé et peu agressif, on peut pro-
réaliser un traitement conservateur.
poser un traitement conservateur radiochirurgical.
• S’il existe un envahissement axillaire histologique ou
des facteurs de mauvais pronostic, on associe une chi- • Carcinome lobulaire in situ : l’absence de transforma-
miothérapie adjuvante et (ou) une hormonothérapie (avec tion infiltrante de cette forme histologique conduit à une
castration en préménopause). attitude thérapeutique très peu agressive. L’exérèse de la
lésion suivie d’une surveillance attentive est désormais
2. Tumeurs évoluées : T3, T4, N2, N3, PeV2, PeV3, M0 reconnue par la plupart des auteurs. Cependant, certains
Elles bénéficient d’une chimiothérapie néoadjuvante, sui- complètent par une radiothérapie.
vie du traitement locorégional (mammectomie + curage + • Tumeur phyllode : l’évolution des tumeurs phyllodes est
LA REVUE DU PRATICIEN (Paris) 1998, 48 793
CANCERS DU SEIN
pronostic et le délai écoulé depuis le traitement) 1.
Stratégie thérapeutique : Par ailleurs, la prescription de tamoxifène doit faire prati-
forme avec lésion > 3 cm quer une surveillance spécifique, en particulier gynécolo-
gique annuelle avec échographie pelvienne endovaginale
(vérification de l’endomètre) et hystéroscopie en cas d’ano-
Pev –
malie, notamment des métrorragies 2.
Pev + Au point de vue thérapeutique, les traitements hormonaux
Histologie / TC* œstroprogestatifs restent classiquement contre-indiqués.
Traitement conservateur
privilégié dans la stratégie Il n’existe pas d’attitude consensuelle sur le délai entre trai-
Chimiothérapie
histologie / TC* tement d’un cancer du sein et survenue d’une grossesse,
on admet que la grossesse n’aggrave pas le risque de
Chimiothérapie rechute locale ou métastatique. Il paraît raisonnable d’at-
tendre que la probabilité de ce risque devienne plus faible,
Régression taille Taille reste > 3 cm c’est-à-dire en moyenne 3 à 5 ans (et ce pour des formes
II I
de bon pronostic).
Quadrantectomie Le dépistage chez les descendantes et les collatérales est
+ curage utile avec conseil génétique, en cas de suspicion de forme
Mastectomie
+ curage familiale. ■
± Complément
chimiothérapie
Chimiothérapie 1. Pour de nombreux auteurs ce bilan est également biologique : NFS,
VS, transaminases, phosphatases.
Radiothérapie soit adjuvante (I) 2. Surveillance également des traitements utilisés en particulier chi-
soit 2e ligne si échec miothérapie
néoadjuvante (II)
Hormonothérapie
(castration si non ménopausée) Points Forts à retenir
tamoxifène
* Histologie / TC : histolgoie par tru cut
• Malgré l’amélioration de la prise en charge
diagnostique et thérapeutique, le cancer du sein
ambigüe, parfois toujours bénigne, parfois récidivante sur reste une maladie grave dont le pronostic a peu
le plan local, exceptionnellement métastatique. La récidive évolué en 30 ans : 65 % de survie à 5 ans et 50 % à
locale est le plus souvent la règle, essentiellement fonction 10 ans.
de l’étendue de l’exérèse chirurgicale initiale, mais aussi • Un dépistage systématique des lésions au stade
du grade histologique de la tumeur. Le traitement est chi- infraclinique est souhaitable afin de traiter les
rurgical, soit tumorectomie large, soit mammectomie dans patientes avant la dissémination métastatique.
les tumeurs de très grande taille. • Une vérification histologique de tout nodule
clinique et (ou) d’anomalie radiologique est
Surveillance indispensable.
L’examen clinique rigoureux, la mammographie et le • La forme histologique la plus fréquente est
dosage du CA 15-3 constituent les trois éléments de base l’adénocarcinome canalaire infiltrant.
de la surveillance du cancer du sein traité. Pour de nom- • Le cancer du sein est hormonodépendant (intérêt
breuses équipes les autres examens ne sont prescrits qu’en dans la recherche des facteurs de risque et du
présence de signes d’appels cliniques ou biologiques. Il traitement).
faut aussi nuancer cette surveillance en fonction de la sévé- • Le traitement en équipe pluridisciplinaire associe
rité du pronostic. Enfin, pour certains, radiographie pul- un traitement locorégional (chirurgie et
monaire, échographie abdominale et scintigraphie osseuse radiothérapie) et un traitement général
sont pratiquées systématiquement. [chimiothérapie et (ou) hormonothérapie] visant à
Quelle que soit la prise en charge thérapeutique, la sur- éviter ou à retarder l’apparition des métastases.
veillance doit être poursuivie à vie.
Le rythme de la surveillance est adapté en fonction des élé-
ments pronostiques initiaux :
– en cas de pronostic péjoratif, on pratique un examen cli- POUR APPROFONDIR
nique tous les 4 mois pendant 2 ans, tous les 6 mois pen-
dant 3 ans, puis 1 fois par an ; 1 / Cancer du sein et groupes à risque
– dans les autres cas, la surveillance clinique a lieu tous les Groupe à haut risque (RR > 4)
6 mois pendant 2 ans, puis 1 fois par an ; • Antécédent personnel de cancer du sein
– dans tous les cas, une mammographie est pratiquée tous • Antécédent personnel d’hyperplasie atypique
les ans ; quant au CA 15-3, il n’existe pas de consensus sur • Syndrome de prédisposition familiale au cancer du sein
la périodicité de sa surveillance (1 à 3 fois par an selon le • Antécédent familial de cancer du sein bilatéral et (ou) préménopausique
794 LA REVUE DU PRATICIEN (Paris) 1998, 48
Gynécologie - Obstétrique
Groupe à risque modéré (RR 2 à 4) bénigne du sein connue et suivie, en l’absence d’orientation fournie par
• Antécédent familial de cancer du sein unilatéral postménopausique la mammographie, d’associer à celle-ci une échographie systématique.
• Première grossesse tardive ou nulliparité 2. Il n’y a pas lieu, chez une patiente asymptomatique, même si elle pré-
• Obésité postménopausique sente des facteurs de risque de cancer de sein, de répéter une mammo-
• Antécédent personnel de cancer de l’ovaire ou de l’endomètre graphie qui s’est révélée normale, plus d’une fois l’an.
• Mastopathie proliférative bénigne Il faut signaler à l’aide de la lettre R les actes et prescriptions pour toute
• Antécédent d’irradition situation où un médecin demande ou pratique une mammographie et (ou)
Groupe à risque faible (RR 1 à 2) une échographie mammaire. Le médecin prescripteur et le radiologue
• Consommation d’alcool sont tous deux responsable de la RMO et doivent tous deux la signaler.
• Premières règles avant 12 ans Si le contexte clinique le justifie, on peut toutefois pratiquer une mam-
• Traitement hormonal substitutif après un certain délai d’utilisation ? mographie, même en présence d’un bilan d’imagerie considéré comme
• Contraceptifs oraux ? normal et datant de moins d’un an.
• Niveau socio-économique élevé La réalisation d’un bilan radiologique de contrôle 4 à 6 mois après la
• Facteurs alimentaires découverte d’une image douteuse, afin de vérifier sa stabilité n’entre pas
dans le cadre de la RMO. De même si le radiologue; au vu de la mam-
mographie, juge qu’une échographie est nécessaire à l’établissement d’un
2 / Histoire naturelle du cancer diagnostic, il ne doit pas hésiter à la réaliser.
• Maladie locale
Il y a passage du stade d’hyperplasie simple à celui d’hyperplasie aty- 5 / Classification histopronostique
pique, puis carcinome in situ et enfin carcinome invasif par rupture de la de Scarff Bloom et Richardson (SBR)
membrane basale et invasion du tissu conjonctif sous-jacent. Cette
« séquence » n’est pas toujours retrouvée et ne semple pas obligatoire. Elle est fondée sur le degré de différenciation de la tumeur, l’anisonu-
Le temps de doublement de la tumeur est d’environ 3 mois, et il faut entre cléose et l’activité mitotique, chacun coté de 1 à 3 ; l’addition de ces cotes
6 et 12 ans pour qu’une tumeur atteigne un volume décelable. aboutit à un total de 3 à 9 permettant de classer la tumeur dans trois grades,
La bilatéralisation (10 %) est soit présente d’emblée (délai d’apparition I (total de 3, 4, 5), II (total de 6 ou 7), et III (total de 8 ou 9) de pronos-
entre les deux tumeurs inférieur à 24 mois), soit successivement. tic de plus en plus défavorable.
• Maladie régionale
L’envahissement ganglionnaire est un reflet du potentiel métastatique de 6 / Classification clinique des signes
la tumeur, ce qui lui confère un important caractère pronostique. Il est évolutifs locaux
fonction du siège de la tumeur : axillaire pour les tumeurs externes, de
PeV0 : absence de signe inflammatoire
bas en haut avec atteinte successive des trois étages puis vers le creux sus-
PeV1 : doublement du volume tumoral en moins de 6 mois
claviculaire ; mammaire interne et axillaire pour les tumeurs centrales ou
PeV2 : signes inflammatoires en regard de la tumeur et affectant moins
internes .
du tiers de la peau du sein
• Maladie générale PeV3 : signes inflammatoires étendus à tout le sein (mastite carcinoma-
La précocité des métastases, souvent à un stade infraclinique, témoigne teuse).
du caractère généralisé du cancer du sein (emboles lymphatiques et vas-
culaires), et du peu d’influence du traitement locorégional sur le taux de
survie de certaines formes. Ces éléments rendent compte de l’intérêt de 7 / Classification TNM-UICC
la chimiothérapie associée au traitement locorégional en cas de facteurs (Union Internationale Contre le Cancer)
de mauvais pronostic.
Elle recueille cliniquement les informations concernant la taille de la
Les sites métastatiques les plus fréquents et par ordre décroissant sont :
tumeur, les adénopathies satellites, l’existence de métastases.
le foie, l’os, les poumons et la plèvre, les glandes surrénales, la peau et
• Tumeur : T
le cerveau.
Tx : détermination de la tumeur primitive impossible
T0 : tumeur cliniquement imperceptible
Tis : présence de carcinome in situ ou de maladie de Paget sans tumeur
3 / Examen clinique décelable
T1 : tumeur inférieure à 20 mm
Il doit être minutieux, bilatéral et comparatif, femme nue jusqu’à la cein-
T1a : moins de 5 mm
ture, les bras levés puis le long du corps, patiente assise puis couchée, à
jour frisant. Il est ensuite consigné sur un schéma daté précisant le siège T1b : de 5 à 10 mm
et les mensurations de la tumeur (avec éventuellement des photographies). T1c : de 11 à 20 mm
• L’inspection est réalisée avec un bon éclairage, en modifiant les angles T2 : tumeur de 20 à 50 mm
de vue. T3 : tumeur supérieure à 50 mm
• La palpation est effectuée main à plat, plaquant le sein contre le gril T4 : tumeur mammaire quelle qu’en soit la taille avec :
costal et à bout de doigts à deux mains. L’exploration se fait quadrant par T4a : extension à la paroi thoracique
quadrant, sans oublier le prolongement axillaire. La recherche d’un écou- T4b : extension à la peau
lement mamelonnaire est systématique. Enfin, la palpation des aires gan- T4c : extension à la paroi et à la peau
glionnaires de façon bilatérale doit être un reflexe lors de tout examen T4d : tumeur inflammatoire
des seins : chaîne axillaire (doigts en crochet dans le creux axillaire et le • Atteinte ganglionnaire : N
long de la paroi thoracique) et chaîne sus-claviculaire. Nx : appréciation ganglionnaire impossible
La négativité de la recherche clinique d’envahissement ganglionnaire N0 : pas d’adénopathie perceptible cliniquement
n’élimine pas le diagnostic de cancer ou d’envahissement histologique. N1 : présence d’une ou plusieurs adénopathies axillaires homolatérales
mobiles
N1a : présumées non atteintes
4 / Références médicales opposables N1b : présumées atteintes
N2 : adénopathies axillaires homolatérales fixées entre elles ou à d’autres
(RMO) en imagerie mammaire structures
La RMO : thème n° XXII concerne l’imagerie mammaire. N3 : atteinte mammaire interne homolatérale
L’intitulé de ce thème est le suivant : • Atteinte métastatique : M
Mammographies dans le dépistage individuel du cancer du sein Mx : détermination impossible de l’extension métastatique
1. Il n’y a pas lieu, lors du dépistage individuel concernant les femmes M0 : absence de métastase
asymptomatiques dont l’examen clinique est normal, sans pathologie M1 : présence d’une métastase ou d’une adénopathie sus-claviculaire
LA REVUE DU PRATICIEN (Paris) 1998, 48 795
CANCERS DU SEIN
8 / Classification en stades POUR EN SAVOIR PLUS
Elle regroupe les patientes en fonction du TNM. Contesso G, Bertin F, Mathieu MC, Terrier P. Anatomie patho-
logique des cancers mammaires - Éditions techniques - Encycl
Stade 0 Tis N0 M0 Med Chir (Paris-France), Gynécologie, 865 B10, 1991, 17 p.
Stade 1 T1 N0 M0 Espie M, Gorins A. Le sein. Paris : Eska, 1995.
Stade IIA T0 N1 M0
Merviel P, Antoine M, Seror JY, Richaud S, Uzan S. Stratégie dia-
T1 N1 M0 gnostique et thérapeutique à l’égard des microcalcifications mam-
T2 N0 M0 maires - Encycl Med Chir (Paris-France), Gynécologie, 810 G35,
1995, 4 p.
Stade IIB T2 N1 M0
Rouesse J, Martin PM, Contesso G. Le praticien face au cancer
T3 N0 M0 du sein. Paris : Arnette, 1997.
Stade IIIA T0 N2 M0 Saglier J, Antoine EC. Cancer du sein : questions et réponses au
T1 N2 M0 quotidien. Paris : Abrégés Masson, 1996.
T2 N2 M0 Uzan S, Merviel P, Seror JY et al. Place des microbiopsies dans la
stratégie diagnostique et thérapeutique à l’égard des microcalci-
T3 N1, N2 M0 fications mammaires - In XI° JTA, Fort-de-France, 11-18 janvier
Stade IIIB T4 tous N M0 1996. Paris : AGPA, 1996 : 283-90.
tous T N3 M0 Cancer du sein (Monographie) Rev Prat (Paris) 1998 ; 48 : 19-78.
Stade IV tous T tous N
796 LA REVUE DU PRATICIEN (Paris) 1998, 48
Vous aimerez peut-être aussi
- Comment Traiter Les Kystes Ovariens ? Savoir Vivre Spiritualité PDFDocument4 pagesComment Traiter Les Kystes Ovariens ? Savoir Vivre Spiritualité PDFHadji BienfaiteurPas encore d'évaluation
- Gastro4an-Appendicite Aigue2021remacheDocument55 pagesGastro4an-Appendicite Aigue2021remacheZayneb ZeroualPas encore d'évaluation
- ParfumDocument46 pagesParfumtabella25Pas encore d'évaluation
- 34-Pseudokyste Du PancrèasDocument17 pages34-Pseudokyste Du PancrèasChemsou MedPas encore d'évaluation
- UnknownDocument194 pagesUnknownSam Ath SanPas encore d'évaluation
- 039 Algies Pelviennes Chez La FemmeDocument2 pages039 Algies Pelviennes Chez La FemmeAboubacar SomparePas encore d'évaluation
- Gyneco5an-Avortements Spontanes2019loucifDocument21 pagesGyneco5an-Avortements Spontanes2019loucifZaki ZikouPas encore d'évaluation
- Cours Voies Biliaires Extra 2020-ConvertiDocument4 pagesCours Voies Biliaires Extra 2020-ConvertiAghasy LittlePas encore d'évaluation
- Brûlures Caustiques de L' Sophage: XIII Séminaire Atelier National de Formation en HGE Alger Le 19-20 Mai 2010Document39 pagesBrûlures Caustiques de L' Sophage: XIII Séminaire Atelier National de Formation en HGE Alger Le 19-20 Mai 2010HindāPas encore d'évaluation
- Les AvortementsDocument32 pagesLes AvortementsSara SouPas encore d'évaluation
- Ad en Op A TiesDocument14 pagesAd en Op A TiesZaabothPas encore d'évaluation
- Pr. EttayebiDocument32 pagesPr. EttayebiAsma LOTFI100% (1)
- ECBUDocument61 pagesECBUadamo2Pas encore d'évaluation
- CAT Devant Une Adénopathie Isolée PDFDocument28 pagesCAT Devant Une Adénopathie Isolée PDFSofiene KeffiPas encore d'évaluation
- Profil Epidemiologique Et Evolutif Des Insuffisances Renales Aigues GravidiquesDocument208 pagesProfil Epidemiologique Et Evolutif Des Insuffisances Renales Aigues GravidiquesSana GuedaouraPas encore d'évaluation
- La Culture Hydroponique de TomatesDocument4 pagesLa Culture Hydroponique de TomatesMohammedPas encore d'évaluation
- Je Vis Avec Du DiabèteDocument152 pagesJe Vis Avec Du Diabètefrancisomgba317Pas encore d'évaluation
- Endometriose Cours PR KemfangDocument40 pagesEndometriose Cours PR KemfangSteve Epoune100% (3)
- Brochure Herbes ThaiesDocument48 pagesBrochure Herbes Thaiesapi-230132006Pas encore d'évaluation
- Polypes Et PolyposesDocument30 pagesPolypes Et PolyposesBMA-medecinePas encore d'évaluation
- KC Du SeinDocument7 pagesKC Du SeinHana Ne DjrPas encore d'évaluation
- La chimiothérapie: Une brochure de la Fondation contre le CancerD'EverandLa chimiothérapie: Une brochure de la Fondation contre le CancerPas encore d'évaluation
- Les cancers du sein: Une brochure de la Fondation contre le CancerD'EverandLes cancers du sein: Une brochure de la Fondation contre le CancerPas encore d'évaluation
- Maladies Du Péricarde Chez L'enfantDocument7 pagesMaladies Du Péricarde Chez L'enfantBarinaPas encore d'évaluation
- 3) DiuDocument24 pages3) DiuIsmail MoumenPas encore d'évaluation
- Dyspnée Laryngée - Complement A L - ED - A Lire Car CA Resume La Reference Et Couvre Les ObjectifsDocument22 pagesDyspnée Laryngée - Complement A L - ED - A Lire Car CA Resume La Reference Et Couvre Les ObjectifsGeorges BakhosPas encore d'évaluation
- 6 Cancer Du SeinDocument93 pages6 Cancer Du Seinchristian omgbaPas encore d'évaluation
- Appendicite AigueDocument12 pagesAppendicite AigueSandra LouPas encore d'évaluation
- Motifs de Consultation en Gynécologie Au CHU Gabriel Touré: TheseDocument126 pagesMotifs de Consultation en Gynécologie Au CHU Gabriel Touré: Thesefefago7978100% (1)
- Chirurgie de La Grossesse Extra-UtérineDocument12 pagesChirurgie de La Grossesse Extra-UtérineCristinaCaprosPas encore d'évaluation
- Cours GEU PDFDocument22 pagesCours GEU PDFjheff limsonPas encore d'évaluation
- Delivrance ArtificielleDocument10 pagesDelivrance ArtificielleMACON824Pas encore d'évaluation
- CAT Devant L'hypertension IntracrânienneDocument27 pagesCAT Devant L'hypertension IntracrânienneMostafa El Attaoui100% (1)
- Chirurgie Digestive PDFDocument218 pagesChirurgie Digestive PDFAro MandaPas encore d'évaluation
- Orchi-Épididymite AigueDocument15 pagesOrchi-Épididymite AigueDdsn Diba100% (1)
- Néphropathies Glomérulaires: DR Jebali Hela Service de Néphrologie-La RabtaDocument33 pagesNéphropathies Glomérulaires: DR Jebali Hela Service de Néphrologie-La Rabtahela bergaouiPas encore d'évaluation
- Fièvres Prolongées InexpliquéesDocument38 pagesFièvres Prolongées InexpliquéesMrTriumphantPas encore d'évaluation
- Sein Benin 2Document109 pagesSein Benin 2Abir KAROUI BEN CHAABANEPas encore d'évaluation
- 8 - KC Anus - SS - VDDocument7 pages8 - KC Anus - SS - VDHouda El Moufid100% (1)
- Gyneco5an Allo Immunisation-DiaposDocument42 pagesGyneco5an Allo Immunisation-Diaposben salem salahPas encore d'évaluation
- Gyneco5an-Tumeurs Ovaire2019bichaDocument13 pagesGyneco5an-Tumeurs Ovaire2019bichaHindPas encore d'évaluation
- RX de La TBC Abdominale 2Document56 pagesRX de La TBC Abdominale 2ElbordjiPas encore d'évaluation
- Pathologies Bénignes Des SeinsDocument54 pagesPathologies Bénignes Des SeinsYi Fong100% (1)
- Eventration OdpDocument28 pagesEventration OdpRania RitaPas encore d'évaluation
- Derma To LogieDocument84 pagesDerma To Logiem.aPas encore d'évaluation
- Généralité en CancerologieDocument37 pagesGénéralité en CancerologiechinarPas encore d'évaluation
- Chirurgie Digestive 2019Document4 pagesChirurgie Digestive 2019husseinmariam2022Pas encore d'évaluation
- Cancer Du CavumDocument5 pagesCancer Du CavumSaada AminaPas encore d'évaluation
- Anatomo Physio FoieDocument7 pagesAnatomo Physio FoieDjallal HassaniPas encore d'évaluation
- 2016 EvcpDocument144 pages2016 EvcpnessyPas encore d'évaluation
- Cancer de L'oesophageDocument34 pagesCancer de L'oesophageDean WinchesterPas encore d'évaluation
- Trauma-Thoracique 0000Document35 pagesTrauma-Thoracique 0000ElbordjiPas encore d'évaluation
- PROTOCOLE SULFATE-DE-MAGNESIUM 10062021 CompressedDocument5 pagesPROTOCOLE SULFATE-DE-MAGNESIUM 10062021 CompressedKader ToéPas encore d'évaluation
- Atrésie Des Voies Biliaires. Traitement Chirurgical PDFDocument11 pagesAtrésie Des Voies Biliaires. Traitement Chirurgical PDFroata cristianPas encore d'évaluation
- Oeil Et GrossesseDocument21 pagesOeil Et GrossesseAssia CardioPas encore d'évaluation
- Item 25 - Douleur Abdo Femme Enceinte PDFDocument1 pageItem 25 - Douleur Abdo Femme Enceinte PDFMohamed IkbalPas encore d'évaluation
- 15M252 PDFDocument82 pages15M252 PDFSebzi TraorePas encore d'évaluation
- ANAPATHDocument15 pagesANAPATHMisaki DocPas encore d'évaluation
- Hemorragie Genitale de La FemmeDocument5 pagesHemorragie Genitale de La FemmeABDOUL MOUMOUNI HarissouPas encore d'évaluation
- Conduite A Tenir Devant Une Occlusion Intestinale Aigue (OiaDocument41 pagesConduite A Tenir Devant Une Occlusion Intestinale Aigue (OiaCharbelle HessaPas encore d'évaluation
- N°352 - Peritonite Aiguë Chez L'enfant - 06-03-2015Document8 pagesN°352 - Peritonite Aiguë Chez L'enfant - 06-03-2015Floroiu AncaPas encore d'évaluation
- Syllabus Urologie d2 UniluDocument67 pagesSyllabus Urologie d2 UniluEmmanuel mbbfPas encore d'évaluation
- Prise en Charge de La Grossesse Extra-Utérine À L'hôpital UniversitaireDocument4 pagesPrise en Charge de La Grossesse Extra-Utérine À L'hôpital UniversitaireMahefa Serge RakotozafyPas encore d'évaluation
- TheseDocument105 pagesTheseKABORE FelixPas encore d'évaluation
- 98 1011Document7 pages98 1011hizballah27100% (1)
- 98 875Document5 pages98 875hizballah27Pas encore d'évaluation
- 98 913Document6 pages98 913hizballah27Pas encore d'évaluation
- 98 905Document4 pages98 905hizballah27Pas encore d'évaluation
- 98 771Document6 pages98 771hizballah27100% (1)
- 98 671Document4 pages98 671hizballah27Pas encore d'évaluation
- 98 765Document5 pages98 765hizballah27Pas encore d'évaluation
- 98 667Document4 pages98 667hizballah27Pas encore d'évaluation
- 98 661Document6 pages98 661hizballah27Pas encore d'évaluation
- 98 545Document4 pages98 545hizballah27100% (1)
- Melanome Cutane Version 40 Publiee Du 11 04 2019Document10 pagesMelanome Cutane Version 40 Publiee Du 11 04 2019Moatez HlmPas encore d'évaluation
- Malpositions Et Malformations Congénitales Du Pied de L'enfantDocument23 pagesMalpositions Et Malformations Congénitales Du Pied de L'enfantespritdeboisPas encore d'évaluation
- BELOT, Jean (1913) Dictionnaire Francaise Arabe Vol 02Document898 pagesBELOT, Jean (1913) Dictionnaire Francaise Arabe Vol 02juan_de_heratPas encore d'évaluation
- Item 153 - Infection Osteoarticulaire - 0Document7 pagesItem 153 - Infection Osteoarticulaire - 0prince yac100% (1)
- GUIDE PEDIATRIQUE MSF Premiere Edition Version Finale June 2016Document384 pagesGUIDE PEDIATRIQUE MSF Premiere Edition Version Finale June 2016didierkakitsaPas encore d'évaluation
- Abc-321328-51168-Marqueurs Biologiques Du Diabete Apports Et Discordances Des Nouvelles Technologies. A Propos Dun Cas Clinique-94836-UDocument7 pagesAbc-321328-51168-Marqueurs Biologiques Du Diabete Apports Et Discordances Des Nouvelles Technologies. A Propos Dun Cas Clinique-94836-UYasmine BendarkawiPas encore d'évaluation
- Pommade L-M PDFDocument1 pagePommade L-M PDFBioafrica BioafricaPas encore d'évaluation
- FR HSG Microbiology - V3 2022 MR 046Document1 pageFR HSG Microbiology - V3 2022 MR 046Sigma QualPas encore d'évaluation
- SaplDocument6 pagesSaplkameliPas encore d'évaluation
- Cours Produits Parapharmaceutiques Et Dispositifs MédicauxDocument77 pagesCours Produits Parapharmaceutiques Et Dispositifs MédicauxWalid MasmoudiPas encore d'évaluation
- Parodontites ApicalesDocument10 pagesParodontites Apicalesrima dentairePas encore d'évaluation
- BLOC Tableau Des AgesDocument2 pagesBLOC Tableau Des AgesZn TkPas encore d'évaluation
- Guide Du Professeur 1 AmDocument181 pagesGuide Du Professeur 1 AmNourredine SabriPas encore d'évaluation
- Diagnostic Et Prise en Charge de La Keratite MicrobienneDocument4 pagesDiagnostic Et Prise en Charge de La Keratite MicrobienneZaki RakiaPas encore d'évaluation
- Cat A Tenir Devant Une Dyspnee Chronique - Google DocsDocument5 pagesCat A Tenir Devant Une Dyspnee Chronique - Google DocsHajar El hayaniPas encore d'évaluation
- 065 072DreDrouin1112Document8 pages065 072DreDrouin1112Gabrielle RizziPas encore d'évaluation
- Q 077 AsciteDocument8 pagesQ 077 AsciteMed AllouchePas encore d'évaluation
- Bats de Medecine LegaleDocument7 pagesBats de Medecine LegaleKakwataPas encore d'évaluation
- Pourquoi Vous Faites La Gueule On Ne Se Connaît Même Pas From PsionDocument62 pagesPourquoi Vous Faites La Gueule On Ne Se Connaît Même Pas From Psiondavid_herz_1Pas encore d'évaluation
- ANESTHESIEDocument163 pagesANESTHESIErayene mznPas encore d'évaluation
- Evaluation de L'activité Anti-Inflammatoire Des Extraits Aqueux de Deux Plantes Médicinales Punica Granatum Et Cistus SP, Chez Les Rats DiabétiquesDocument135 pagesEvaluation de L'activité Anti-Inflammatoire Des Extraits Aqueux de Deux Plantes Médicinales Punica Granatum Et Cistus SP, Chez Les Rats DiabétiquesArmel Géraldo HOUNDETONPas encore d'évaluation
- PsoriasisDocument34 pagesPsoriasisavounviPas encore d'évaluation
- Microbio s3 Cours 10Document10 pagesMicrobio s3 Cours 10Jamila ridaPas encore d'évaluation
- Memoire Anne VraieDocument33 pagesMemoire Anne VraieJob Ezechiel Nunda JenPas encore d'évaluation