Académique Documents
Professionnel Documents
Culture Documents
TP 1 - Dilution D'un Acide Et PH Texte À Trou-Correction Élève
Transféré par
thierryleprofesseurdephysique bristolTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
TP 1 - Dilution D'un Acide Et PH Texte À Trou-Correction Élève
Transféré par
thierryleprofesseurdephysique bristolDroits d'auteur :
Formats disponibles
Partie 1 - Constitution et
transformation de la
matière
TP 1 – Dilution d’un acide et pH
Chapitre 1 - Correction
Transformation acide-
base et pH
1° Représentation de Lewis du chlorure d'hydrogène :
Δχ (HCl) = 3,16 – 2,20 = 0, 96 > 0,4 ………………………………………………………….
Ainsi la liaison entre H et Cl peut se ……………………………………., cela confère au chlorure d’hydrogène un
caractère acide car il y a …………………………………………………………………………………………… .
2°
Couples HCl / Cl- HCl = H+ + Cl-
H3O+ / H2O H2O + H+ = H3O+
Réaction chimique
3° Si la réaction est ……………………. , alors d’après la stœchiométrie de la …………… on a :
n(HCl) = n(H3O+)
Ainsi C(HCl) = [ H3O+]
Cmère V fille
4° Relation sur la dilution : F = = .
C fille V mère
On dispose d’une fiole jaugée de 50 mL ainsi
V fille
Vmère = = ………………. = 5 mL et on utilisera une pipette jaugée de 5mL.
F
Protocole :
- On prélève avec une pipette jaugée de 5 mL une solution d’acide chlorhydrique de C 0 = 0,10 mol.L-1.
- On introduit cette solution dans une fiole jaugée de 50 mL en complétant jusqu’au trait de jauge avec de l’eau distillée.
- On bouche et on agite pour homogénéiser.
5°
La relation sur le pH est :
Avec c° = 0,1 mol.L-1 et C(HCl) = [ H3O+] (d’après la question 3)
Donc on doit pouvoir vérifier expérimentalement que …………………………………………………..
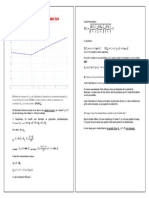
En plaçant le pH sur l'axe des ………………………………. Et - log(c) sur l'axe des …………………………….., on a
bien après modélisation sur Régressi une droite de type ……………………………….. de coefficient directeur ………… et
passant par l'origine des axes (modèle ………………….. ).
Vous aimerez peut-être aussi
- SP20-TE-01-19 S01 Sentrainer CorrectionDocument4 pagesSP20-TE-01-19 S01 Sentrainer CorrectionBatungwanayo EnzoPas encore d'évaluation
- TP 4 - Dosage Du Vinaigre-CorrectionDocument1 pageTP 4 - Dosage Du Vinaigre-Correctionthierryleprofesseurdephysique bristolPas encore d'évaluation
- Killian - 2022 - Tp1Document9 pagesKillian - 2022 - Tp1amandine gaianiPas encore d'évaluation
- Exos AvancementDocument2 pagesExos AvancementPhysique MehdaouiPas encore d'évaluation
- 12-13 ChimieDocument4 pages12-13 ChimieSouhail Mouradi (“ninocity3”)Pas encore d'évaluation
- Traveaux Dirigés 2Document6 pagesTraveaux Dirigés 2Aymen BaccouchePas encore d'évaluation
- 201703080733551Document8 pages201703080733551سمير دبيليPas encore d'évaluation
- Lec 15 Les PHDocument12 pagesLec 15 Les PHPierreEustachePas encore d'évaluation
- Chimie: - Chimie en Solution AqueuseDocument35 pagesChimie: - Chimie en Solution AqueuseAyoub Maverick100% (1)
- TD3 Chimie Des SolutionDocument12 pagesTD3 Chimie Des SolutionsoumiagpoPas encore d'évaluation
- PHDocument5 pagesPHalex soumbitaPas encore d'évaluation
- Correction de La Série 1Document3 pagesCorrection de La Série 1zohirPas encore d'évaluation
- DecapageConducti 5pts CorrectionDocument2 pagesDecapageConducti 5pts CorrectionRATIARIVELO Mamy FrédéricPas encore d'évaluation
- Deca Page Conduct IDocument2 pagesDeca Page Conduct IRATIARIVELO Mamy FrédéricPas encore d'évaluation
- M.douezy Enonce Et Corrige Interrogation 2 2-5-12 Solutions Aqueuses Interrogation 2 2 5 12 Solutions Aqueuses 1428560285Document2 pagesM.douezy Enonce Et Corrige Interrogation 2 2-5-12 Solutions Aqueuses Interrogation 2 2 5 12 Solutions Aqueuses 1428560285Amdjed BahaaPas encore d'évaluation
- 2023 Liban J1 Exo2 Correction Assouplissant 5ptsDocument3 pages2023 Liban J1 Exo2 Correction Assouplissant 5ptsfatimazahramadanialaoui983Pas encore d'évaluation
- TPChi10 Corrige 1S1Document3 pagesTPChi10 Corrige 1S1henryPas encore d'évaluation
- Chimie-B-chap5-transfo Totales Ou LimiteesDocument4 pagesChimie-B-chap5-transfo Totales Ou LimiteesMed yahyaPas encore d'évaluation
- Chapitre 4Document11 pagesChapitre 4srhconnor_31Pas encore d'évaluation
- Cin ExoDocument10 pagesCin ExoHarakat ElhoucinePas encore d'évaluation
- SEQUENCE06 Acidefortbaseforte 1 STLDocument6 pagesSEQUENCE06 Acidefortbaseforte 1 STLMed BriniPas encore d'évaluation
- 2019 AmNord Exo3 Correction LaitChevre 5ptsDocument3 pages2019 AmNord Exo3 Correction LaitChevre 5ptssaladeaucacaPas encore d'évaluation
- Ch13 Reaction Chimique Echange ProtonDocument5 pagesCh13 Reaction Chimique Echange Protonالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Brochure de Chimie PDFDocument12 pagesBrochure de Chimie PDFAbdoul karim DansokoPas encore d'évaluation
- AcidimétrieDocument15 pagesAcidimétriezineb elmaslouhyPas encore d'évaluation
- Ae Concentration en Solute Apporte Et Concentration Des IonsDocument3 pagesAe Concentration en Solute Apporte Et Concentration Des IonshugostranzPas encore d'évaluation
- Rapport de La Chimie en SolutionDocument13 pagesRapport de La Chimie en SolutionHAMZA AZZAARIPas encore d'évaluation
- 12-TP Destop PH MetrieDocument4 pages12-TP Destop PH MetriesoufianePas encore d'évaluation
- Nouveau Document Microsoft Office WordDocument18 pagesNouveau Document Microsoft Office WordAnonymous b9f4AjwPPas encore d'évaluation
- C6Chim - Titrages - Exos - Ph&conduct&color PDFDocument9 pagesC6Chim - Titrages - Exos - Ph&conduct&color PDFAzizElheniPas encore d'évaluation
- FSR TDs CHIMIE DES SOLUTIONS 2020Document34 pagesFSR TDs CHIMIE DES SOLUTIONS 2020Mohamd BobsPas encore d'évaluation
- TD Eq - CHMQ L1-S2 (CPGE)Document5 pagesTD Eq - CHMQ L1-S2 (CPGE)Btn Princii IsraëlPas encore d'évaluation
- Transformations Chimiques S Effectuant Dans Les 2 Sens Exercices Non Corriges 1 1Document4 pagesTransformations Chimiques S Effectuant Dans Les 2 Sens Exercices Non Corriges 1 1boufdili0% (2)
- DS 7 735 2019-2020 25Document2 pagesDS 7 735 2019-2020 25Joliette KplokaPas encore d'évaluation
- Les Reactions Chimiques-Uua8Document113 pagesLes Reactions Chimiques-Uua8bafoa.ifmPas encore d'évaluation
- TD C567Document7 pagesTD C567Mouhamed SarryPas encore d'évaluation
- Analyse Et Methodes de Separation 2Document5 pagesAnalyse Et Methodes de Separation 24rghr8spkvPas encore d'évaluation
- EquilibreQoutionReactionExercices 16-17 PDFDocument4 pagesEquilibreQoutionReactionExercices 16-17 PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- TP Esterification Web PDFDocument2 pagesTP Esterification Web PDFDadati Sou67% (3)
- Corrigé Série 2Document7 pagesCorrigé Série 2Doudou SamiPas encore d'évaluation
- Correction AlcanesDocument2 pagesCorrection AlcanesMichael VoulnangPas encore d'évaluation
- Exercice de Chimie GénéralDocument3 pagesExercice de Chimie GénéralBOUKSSESSA YOUSRA100% (1)
- TSpe-TPC1-MesurespH-Fiche TPP Synthèse Du HCL GazeuxDocument6 pagesTSpe-TPC1-MesurespH-Fiche TPP Synthèse Du HCL GazeuxLou BalonPas encore d'évaluation
- Chim205a TD PDFDocument32 pagesChim205a TD PDFmerz RimPas encore d'évaluation
- Série 2 PH (1) - 2021-07-20T143107.674Document30 pagesSérie 2 PH (1) - 2021-07-20T143107.674Abdel OihabPas encore d'évaluation
- Exercices Transformations Acide BaseDocument4 pagesExercices Transformations Acide BaseNaouma ChahdPas encore d'évaluation
- La Reaction Chimique Exercices 1Document2 pagesLa Reaction Chimique Exercices 1Chesnel Chasles La Logique0% (1)
- Chap 02 Re - Action Chimique Par e - Change de Proton2019Document8 pagesChap 02 Re - Action Chimique Par e - Change de Proton2019Younes HoumadiPas encore d'évaluation
- Etat D - Equilibre D'un SystemeDocument8 pagesEtat D - Equilibre D'un SystemeOskar GottliebPas encore d'évaluation
- Cours Chim 02 La Transformation Toujours TotaleDocument11 pagesCours Chim 02 La Transformation Toujours Totalebeebac2009Pas encore d'évaluation
- 201702210942075Document9 pages201702210942075HAMADA1972Pas encore d'évaluation
- Exercices Supplementaires en Chimie Analytique PDFDocument18 pagesExercices Supplementaires en Chimie Analytique PDFyacine100% (1)
- C3Chim - Transformations - Limitees - Exercices - Sabatier PDFDocument5 pagesC3Chim - Transformations - Limitees - Exercices - Sabatier PDFAzizElheni0% (1)
- Présentation Cours N°6Document13 pagesPrésentation Cours N°6inessPas encore d'évaluation
- 2006 Pondichery Exo1 Sujet Acide Base 7ptsDocument4 pages2006 Pondichery Exo1 Sujet Acide Base 7ptsasakuma2006Pas encore d'évaluation
- Transformations Acide - Base Eleve NDocument2 pagesTransformations Acide - Base Eleve Nblack HPas encore d'évaluation
- Correction DS Titrage LaitDocument2 pagesCorrection DS Titrage Laitcqfd242Pas encore d'évaluation
- Fichier Produit 2232Document48 pagesFichier Produit 2232FlorinaPas encore d'évaluation
- Activité N°3-Comprendre Internet-CorrectionDocument3 pagesActivité N°3-Comprendre Internet-Correctionthierryleprofesseurdephysique bristolPas encore d'évaluation
- Activité N°1-Internet (Introduction) - SujetDocument2 pagesActivité N°1-Internet (Introduction) - Sujetthierryleprofesseurdephysique bristolPas encore d'évaluation
- TP 5 - Dosage Conductimétrique - CorrectionDocument1 pageTP 5 - Dosage Conductimétrique - Correctionthierryleprofesseurdephysique bristolPas encore d'évaluation