Académique Documents
Professionnel Documents
Culture Documents
Fiche Methode Modele Lewis
Transféré par
El Mehdi Akhatar0 évaluation0% ont trouvé ce document utile (0 vote)
160 vues23 pagesExercice : modele de Lewis
Copyright
© © All Rights Reserved
Formats disponibles
PPTX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentExercice : modele de Lewis
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
160 vues23 pagesFiche Methode Modele Lewis
Transféré par
El Mehdi AkhatarExercice : modele de Lewis
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 23
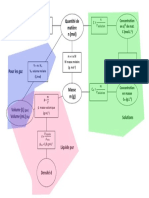
Mthode suivre
pour construire le
modle de Lewis
dune molcule
Pour construire ce modle, nous allons
apprendre remplir un tableau, voici sa
forme :
Procdons par tapes :
1. Dans la premire ligne, on crira la formule
brute de la molcule et ventuellement son
nom.
HCl: chlorure d'hydrogne
Procdons par tapes :
1. Dans la premire ligne, on crira la formule
brute de la molcule et ventuellement son
nom.
2.On crit le nom et le symbole de chaque atome
prsent dans la molcule puis leur
configuration lectronique.
HCl: chlorure d'hydrogne
H: hydrogne (Z = 1)
Cl: chlore (Z = 17)
(K)1
(K)2(L)8(M)7
Procdons par tapes :
1. Dans la premire ligne, on crira la formule
brute de la molcule et ventuellement son
nom.
2.On crit le nom et le symbole de chaque atome
prsent dans la molcule puis leur
configuration lectronique.
3.On donne le nombre dlectrons sur la couche
externe de chaque atome.
HCl: chlorure d'hydrogne
H: hydrogne (Z = 1)
Cl: chlore (Z = 17)
(K)1
(K)2(L)8(M)7
Procdons par tapes :
1. Dans la premire ligne, on crira la formule
brute de la molcule et ventuellement son
nom.
2.On crit le nom et le symbole de chaque atome
prsent dans la molcule puis leur
configuration lectronique.
3.On donne le nombre dlectrons sur la couche
externe de chaque atome.
4.On crit le nom du gaz rare le plus proche de
latome considr et la configuration
lectronique de ce gaz rare.
On rappelle que pour se stabiliser, les atomes
respecte la rgle du duet ou de loctet : ils
cherchent se rapprocher de la configuration
lectronique du gaz rare qui leur est proche
dans la classification priodique.
HCl: chlorure d'hydrogne
H: hydrogne (Z = 1)
Cl: chlore (Z = 17)
(K)1
(K)2(L)8(M)7
He : (K)2
Ar : (K)2(L)8(M)8
5.On cherche le nombre de liaison covalente
que doit former chaque atome pour
respecter les rgles du duet ou de loctet :
Latome dhydrogne en (K)1 (1 lectron sur
sa couche externe) veut se rapprocher de
lhlium (K)2 pour respecter la rgle du duet
et ainsi avoir 2 lectrons sur sa couche
externe :
2 1
Pour cela, il forme 1 liaison covalente avec un
autre atome.
HCl: chlorure d'hydrogne
H: hydrogne (Z = 1)
Cl: chlore (Z = 17)
(K)1
(K)2(L)8(M)7
He : (K)2
1
Ar : (K)2(L)8(M)8
Latome de chlore en (K)2(L)8(M)7
(7 lectrons sur sa couche externe) veut se
rapprocher de largon (K)2(L)8(M)8 pour
respecter la rgle de loctet et ainsi avoir
8 lectrons sur sa couche externe :
8 7 1
Pour cela, il forme 1 liaison covalente avec
un autre atome.
HCl: chlorure d'hydrogne
H: hydrogne (Z = 1)
Cl: chlore (Z = 17)
(K)1
(K)2(L)8(M)7
He : (K)2
Ar : (K)2(L)8(M)8
6.On calcule le nombre de doublet non liant
quil y aura autour de chaque atome :
Latome dhydrogne en (K)1, 1 lectron sur sa
couche externe, met cet lectron en commun
pour former une liaison covalente.
Il ne reste pas dlectrons sur la couche
externe de latome :
pas de doublet non liant
HCl: chlorure d'hydrogne
H: hydrogne (Z = 1)
Cl: chlore (Z = 17)
(K)1
(K)2(L)8(M)7
He : (K)2
Ar : (K)2(L)8(M)8
Latome de chlore en (K)2(L)8(M)7,
7 lectrons sur sa couche externe, met en
commun 1 de ces 7 lectrons pour former une
liaison covalente.
Il reste donc 7
1 6 lectrons sur
la couche externe de latome qui se regroupe
en :
3 doublets non liants
HCl: chlorure d'hydrogne
H: hydrogne (Z = 1)
Cl: chlore (Z = 17)
(K)1
(K)2(L)8(M)7
He : (K)2
Ar : (K)2(L)8(M)8
7.Il ne reste plus qu rpartir les liaisons
covalentes entre les atomes et placer les
doublets non liants autour de chaque atome :
Chaque atome doit partager une liaison
covalente : latome dhydrogne et latome
de chlore sont lis par une liaison
covalente.
HCl: chlorure d'hydrogne
H: hydrogne (Z = 1)
Cl: chlore (Z = 17)
(K)1
(K)2(L)8(M)7
He : (K)2
Ar : (K)2(L)8(M)8
Cl
7.Il ne reste plus qu rpartir les liaisons
covalentes entre les atomes et placer les
doublets non liants autour de chaque atome :
Chaque atome doit partager une liaison
covalente : latome dhydrogne et latome
de chlore sont lis par une liaison
covalente.
Latome dhydrogne na pas de doublet non
liant alors que latome de chlore est entour
par trois doublets non liants.
HCl: chlorure d'hydrogne
H: hydrogne (Z = 1)
Cl: chlore (Z = 17)
(K)1
(K)2(L)8(M)7
He : (K)2
Ar : (K)2(L)8(M)8
Cl
Modle de Lewis de la
molcule HCl
Vous aimerez peut-être aussi
- Aplus1 Eva U5-6Document16 pagesAplus1 Eva U5-6Edzer Jean Louis100% (1)
- Mon Mini Fichier de Fluence: Entraînement À La LectureDocument8 pagesMon Mini Fichier de Fluence: Entraînement À La LectureElodie HoareauPas encore d'évaluation
- Jeu de Carte Je Mime Je Décris Je DessineDocument6 pagesJeu de Carte Je Mime Je Décris Je DessineDanoush &Liloush100% (1)
- Séquence 3 Le VerbeDocument12 pagesSéquence 3 Le VerbelotusetjasminPas encore d'évaluation
- Exercice 4-Apprentissage Clavier L'accent CirconflexeDocument1 pageExercice 4-Apprentissage Clavier L'accent CirconflexeSAIDA HAMMADOUPas encore d'évaluation
- Corrige Exercices Conductimetrie Feuille Travaux DirigesDocument3 pagesCorrige Exercices Conductimetrie Feuille Travaux Dirigesla physique selon le programme Français89% (9)
- Chimie de 2nd Recent-1Document23 pagesChimie de 2nd Recent-1Ouedraogo HarounaPas encore d'évaluation
- Jeu de Cartes NomenclatureDocument58 pagesJeu de Cartes NomenclatureMaria Pilar Carilla50% (2)
- Methode de Lecture 2022 SCT Avec Cahier Des Sons Avec Compression - 1 Compresse Mars 2022Document189 pagesMethode de Lecture 2022 SCT Avec Cahier Des Sons Avec Compression - 1 Compresse Mars 2022fatimatou2607100% (1)
- Evaluation Stabilité Des Entités Chimiques 23Document4 pagesEvaluation Stabilité Des Entités Chimiques 23Omar Rahat100% (1)
- Jouer Avec Les Verbes Activites Ludiques Dictionnaire Visuel Exercice GR - 42988Document3 pagesJouer Avec Les Verbes Activites Ludiques Dictionnaire Visuel Exercice GR - 42988Ane Oliveira100% (1)
- Expressions ImagéesDocument3 pagesExpressions ImagéesGabriela MirandaPas encore d'évaluation
- Module 1 NostalgieDocument3 pagesModule 1 NostalgieWiem HabbassiPas encore d'évaluation
- Cartes ActionsDocument12 pagesCartes ActionsBaby Blue100% (1)
- Nouveau Syllabe Francais 2023Document4 pagesNouveau Syllabe Francais 2023Sanveer Keshav Jugtah100% (1)
- Fluence Gammes 2 MotsDocument8 pagesFluence Gammes 2 MotsLeandro MartinsPas encore d'évaluation
- 6 Cours1Document2 pages6 Cours1Nahil100% (1)
- 4 6037156664350606938Document80 pages4 6037156664350606938MR. PROPas encore d'évaluation
- Tous Semblables Et Tous Differents CoursDocument6 pagesTous Semblables Et Tous Differents CoursdrissPas encore d'évaluation
- Livret Lecture1 PDFDocument32 pagesLivret Lecture1 PDFsherrie_gimenez100% (1)
- مقترح امتحان الموحد الإقليمياللغة الفرنسية للمستوى السادس إبتدائي دورة 2022Document3 pagesمقترح امتحان الموحد الإقليمياللغة الفرنسية للمستوى السادس إبتدائي دورة 2022mohammed belaouchiPas encore d'évaluation
- Imagier Materiel Ms 2 ÉcrituresDocument28 pagesImagier Materiel Ms 2 ÉcrituresEspoire Amel100% (1)
- Classification Périodique (STSM Usthb - Blogspot.com)Document29 pagesClassification Périodique (STSM Usthb - Blogspot.com)younesPas encore d'évaluation
- Livret Mémo Français CE1 - 2Document13 pagesLivret Mémo Français CE1 - 2Mélane Mo100% (1)
- MCEM Imagier FermeDocument22 pagesMCEM Imagier FermeADRIANA SEQUEDA CUBIDES100% (1)
- 3 Racines OperationsDocument1 page3 Racines OperationsJefred WilbarPas encore d'évaluation
- Ce1 Trace Ecrite Lettre CDocument1 pageCe1 Trace Ecrite Lettre CChehira Doghmen100% (1)
- Comptines Vers Laphono AcessDocument13 pagesComptines Vers Laphono AcessDinaPas encore d'évaluation
- Leçon 4 Droites-Paralleles-Et-Perpendiculaires-Cours-De-Maths-En-6eme - CopieDocument7 pagesLeçon 4 Droites-Paralleles-Et-Perpendiculaires-Cours-De-Maths-En-6eme - CopieChristian NoelPas encore d'évaluation
- Cours TS 5 Procreation SuiteDocument5 pagesCours TS 5 Procreation Suitebeebac2009Pas encore d'évaluation
- Fiches Exercices CP PDFDocument28 pagesFiches Exercices CP PDFbassem zouariPas encore d'évaluation
- Leçon CM Sur Le Verbe D'action Et Verbe D'étatDocument1 pageLeçon CM Sur Le Verbe D'action Et Verbe D'étatIolanda PălimaruPas encore d'évaluation
- CHAPITRE 5 L'alimentation VégétauxDocument12 pagesCHAPITRE 5 L'alimentation VégétauxGıptatullahPas encore d'évaluation
- C2A10 - Les Chaines Alimentaires.Document2 pagesC2A10 - Les Chaines Alimentaires.jad mamouPas encore d'évaluation
- Carte Mentale Mole Complétée - Physique-ChimieDocument1 pageCarte Mentale Mole Complétée - Physique-ChimieDodiePas encore d'évaluation
- Cm2 Evaluation Ecrire NombresDocument2 pagesCm2 Evaluation Ecrire NombresJelly fruit 307Pas encore d'évaluation
- Les Aliments: Du Beurre Une Bière Un Biscuit Un BonbonDocument26 pagesLes Aliments: Du Beurre Une Bière Un Biscuit Un BonbonMélanie GexPas encore d'évaluation
- SVT - Hormones Et ProcréationDocument10 pagesSVT - Hormones Et ProcréationfontainePas encore d'évaluation
- PPS - Fiches Dexercices CE2 LBDocument2 pagesPPS - Fiches Dexercices CE2 LBNoun Nona100% (2)
- Barbarismes Lexicaux Et ImpropriétésDocument14 pagesBarbarismes Lexicaux Et ImpropriétésHarouna Liman Salifou RoufaiPas encore d'évaluation
- Mon Lexique MathematiquesDocument16 pagesMon Lexique Mathematiquesapi-335239597100% (2)
- 2nde Travail Sur La Competence Realiser Effectuer Des Calculs Cedric MARANGONIDocument30 pages2nde Travail Sur La Competence Realiser Effectuer Des Calculs Cedric MARANGONIIbrahima DiopPas encore d'évaluation
- Devoir de Synthèse N°3 - Français - 1ère AS (2008-2009) MR CherifDocument2 pagesDevoir de Synthèse N°3 - Français - 1ère AS (2008-2009) MR CherifSassi LassaadPas encore d'évaluation
- Soustraction PoséeDocument2 pagesSoustraction PoséeFlorian BulotPas encore d'évaluation
- Référentiel Animaux de La FermeDocument12 pagesRéférentiel Animaux de La FermeSERBIA CERTIND100% (1)
- Fluence 3 ÉtoilesDocument6 pagesFluence 3 ÉtoilesadioufPas encore d'évaluation
- Cours - Français Module 3 L'Accord Du Participe Passée - 9ème (2011-2012) Mlle Sarra 1Document5 pagesCours - Français Module 3 L'Accord Du Participe Passée - 9ème (2011-2012) Mlle Sarra 1Karem SaadPas encore d'évaluation
- Lecture-Atelier Renforcement de La Combinatoire (Liste de Mots Avec Graphie Au Debut, Au Milieu Et A La Fin)Document226 pagesLecture-Atelier Renforcement de La Combinatoire (Liste de Mots Avec Graphie Au Debut, Au Milieu Et A La Fin)manuwubiPas encore d'évaluation
- Atomix - Physique Chimie - 4eme Année Secondaire - Section Sciences de L'informatiqueDocument354 pagesAtomix - Physique Chimie - 4eme Année Secondaire - Section Sciences de L'informatiqueMarcq Valérie100% (2)
- Nombres Decimaux Cours de Maths en 6emeDocument6 pagesNombres Decimaux Cours de Maths en 6emeMissy & FeushyPas encore d'évaluation
- Examen Normalisé Provincial de La Langue Française 6ème AEPDocument4 pagesExamen Normalisé Provincial de La Langue Française 6ème AEPjaouds100% (2)
- Cours MatricesDocument23 pagesCours MatriceskouamePas encore d'évaluation
- Droites Perpendiculaires Et Droites ParallèlesDocument5 pagesDroites Perpendiculaires Et Droites Parallèleskahina kahinaPas encore d'évaluation
- Essebil Au Bac Maths TleDocument132 pagesEssebil Au Bac Maths Tlemagnanga111Pas encore d'évaluation
- Programmation Gs Prog 2015 PicassoDocument9 pagesProgrammation Gs Prog 2015 Picassojazze77Pas encore d'évaluation
- Cours Decimaux 2Document4 pagesCours Decimaux 2RHC BITPas encore d'évaluation
- Socio Affectif PDFDocument19 pagesSocio Affectif PDFhouda BELGHITIPas encore d'évaluation
- Aie FauneDocument8 pagesAie Faunesportsaid688Pas encore d'évaluation
- FrancaisDocument50 pagesFrancaisMohamed Helmi ChebbiPas encore d'évaluation
- La Geometrie de Quelques Molecules Resume de Cours 1 1Document2 pagesLa Geometrie de Quelques Molecules Resume de Cours 1 1maryam.zagririPas encore d'évaluation
- COURS-Géométrie de Quelques MoléculesDocument5 pagesCOURS-Géométrie de Quelques MoléculesHamza AskharPas encore d'évaluation
- Le CND Par GC Et CGDocument2 pagesLe CND Par GC Et CGEl Mehdi AkhatarPas encore d'évaluation
- Resolution Par Methode Norton Millman Kennely 14Document7 pagesResolution Par Methode Norton Millman Kennely 14chabane_148549100% (1)
- Serie CondensateurDocument4 pagesSerie CondensateurEl Mehdi Akhatar100% (1)
- Ex Blanc07-08Document2 pagesEx Blanc07-08El Mehdi AkhatarPas encore d'évaluation
- Notion de Base Electricite 11Document8 pagesNotion de Base Electricite 11zemabder100% (1)
- Presentation Des OndesDocument26 pagesPresentation Des OndesEl Mehdi AkhatarPas encore d'évaluation
- 1S - DS4 PDFDocument2 pages1S - DS4 PDFEl Mehdi AkhatarPas encore d'évaluation
- Chapitre 1 Controle Non Destructif GeneralitesDocument7 pagesChapitre 1 Controle Non Destructif GeneralitesmarzooPas encore d'évaluation
- Dispositif de Controle de L'état de L'huile MoteurDocument16 pagesDispositif de Controle de L'état de L'huile MoteurEl Mehdi AkhatarPas encore d'évaluation
- Automates Programmables IndustrielsDocument16 pagesAutomates Programmables IndustrielsEl Mehdi AkhatarPas encore d'évaluation
- Tableau de Caractérisation Des Ions en Solutions.Document3 pagesTableau de Caractérisation Des Ions en Solutions.mohamed laghrib75% (4)
- Correction Physique Chimie S 2013Document8 pagesCorrection Physique Chimie S 2013El Mehdi AkhatarPas encore d'évaluation
- Bac S 2013 Physique Chimie ObligDocument9 pagesBac S 2013 Physique Chimie ObligLETUDIANT100% (1)
- Bac S 2013 Physique Chimie ObligDocument9 pagesBac S 2013 Physique Chimie ObligLETUDIANT100% (1)
- Bac S 2013 Physique Chimie ObligDocument9 pagesBac S 2013 Physique Chimie ObligLETUDIANT100% (1)
- Piles Et AccusDocument14 pagesPiles Et AccusEl Mehdi AkhatarPas encore d'évaluation
- Bac S 2013 Physique Chimie ObligDocument9 pagesBac S 2013 Physique Chimie ObligLETUDIANT100% (1)
- Exercices de Physique TSDocument116 pagesExercices de Physique TSerrairachid100% (4)
- Exercices de Physique TSDocument116 pagesExercices de Physique TSerrairachid100% (4)
- Comment Rediger Un Rapport Un Memoire Une TheseDocument100 pagesComment Rediger Un Rapport Un Memoire Une TheseAzzedine BakaPas encore d'évaluation
- Physique Et PhilosophieDocument11 pagesPhysique Et PhilosophieeuaggPas encore d'évaluation
- TraductionDocument57 pagesTraductionEl Mehdi AkhatarPas encore d'évaluation
- Quantique CognitionDocument24 pagesQuantique CognitionEl Mehdi AkhatarPas encore d'évaluation
- HeisenbergDocument28 pagesHeisenbergEl Mehdi Akhatar100% (1)
- Structures de LewisDocument4 pagesStructures de LewisEl Mehdi AkhatarPas encore d'évaluation
- Articolo Bitbol 1Document15 pagesArticolo Bitbol 1El Mehdi AkhatarPas encore d'évaluation
- TraductionDocument57 pagesTraductionEl Mehdi AkhatarPas encore d'évaluation
- TraductionDocument57 pagesTraductionEl Mehdi AkhatarPas encore d'évaluation
- 10 6 TP Dosage de La BétadineDocument3 pages10 6 TP Dosage de La BétadinemranonimosPas encore d'évaluation
- Communication MoléculaireDocument10 pagesCommunication MoléculairemnoubirPas encore d'évaluation
- Transfo HTDocument60 pagesTransfo HTAbderrahmane BinPas encore d'évaluation
- Vérifications ELU Et ELS (Poteau)Document13 pagesVérifications ELU Et ELS (Poteau)Guillaume HounakePas encore d'évaluation
- A02 Actions Mecaniques Et Forces PDFDocument3 pagesA02 Actions Mecaniques Et Forces PDFKarimm Karim100% (1)
- SN016 ADocument8 pagesSN016 Asaidgénie01Pas encore d'évaluation
- Theorie de BetzDocument2 pagesTheorie de Betzmohammed jadiriPas encore d'évaluation
- Verification PannesDocument5 pagesVerification PannesAsting elboujidi abdessamadPas encore d'évaluation
- Mov RectilineoDocument11 pagesMov RectilineoALEXANDERPas encore d'évaluation
- BAEP 1 - Flexion ComposeeDocument11 pagesBAEP 1 - Flexion ComposeebensofienPas encore d'évaluation
- Cours Murs EcransDocument50 pagesCours Murs EcransmohamedouffaPas encore d'évaluation
- MaintenanceDocument11 pagesMaintenanceEL MONADY Mohammed100% (1)
- Corrige L 2016Document2 pagesCorrige L 2016Khady DionguePas encore d'évaluation
- 2 Caractéristiques Mécaniques Du Bois EC5Document7 pages2 Caractéristiques Mécaniques Du Bois EC5Tellache MohamedPas encore d'évaluation
- Ressource VerinsDocument2 pagesRessource Verinsdxsszsz50% (2)
- 1994TH Youssef e NS18471Document272 pages1994TH Youssef e NS18471Youness CharihPas encore d'évaluation
- Assemblages Par Boulons NormauxDocument19 pagesAssemblages Par Boulons NormauxmohamedagendaPas encore d'évaluation
- DS Grafcet Logique Combinatoire CORRECTIONDocument7 pagesDS Grafcet Logique Combinatoire CORRECTIONchaouch.najeh100% (2)
- Programme de Formation RSA - BADocument3 pagesProgramme de Formation RSA - BAAbdel Monaim MaghraouiPas encore d'évaluation
- Cours de Chimie OrganiqueDocument114 pagesCours de Chimie Organiqueosefresistance100% (1)
- M24 Analyse circuit pneum أ©lectropneumatiq-GE-EMIDocument169 pagesM24 Analyse circuit pneum أ©lectropneumatiq-GE-EMIhavoc2012Pas encore d'évaluation
- Apprendre L' Electronique en Partant de Zéro - Niveau 1 - Leçons 01 À 28Document297 pagesApprendre L' Electronique en Partant de Zéro - Niveau 1 - Leçons 01 À 28fantikomed100% (2)
- EndommagementDocument8 pagesEndommagementBaghli houdaPas encore d'évaluation
- 68593342ge Chap 1 Complexes Exercices Corriges PDFDocument6 pages68593342ge Chap 1 Complexes Exercices Corriges PDFYousséf Mors LeePas encore d'évaluation
- Durcissement Par Précipitation Des Alliages D'alluminium PDFDocument37 pagesDurcissement Par Précipitation Des Alliages D'alluminium PDFAkram Ben Khemis100% (2)
- OptiqueCoursn°3 Partie1 15 1 6 ENTDocument3 pagesOptiqueCoursn°3 Partie1 15 1 6 ENTJeffPas encore d'évaluation
- Catalogue Wiha PDFDocument381 pagesCatalogue Wiha PDFredaPas encore d'évaluation
- Signaux Physiques - Chapitre 3-Circuits Lineaires Du Premier Ordre PDFDocument46 pagesSignaux Physiques - Chapitre 3-Circuits Lineaires Du Premier Ordre PDFDavid KonanPas encore d'évaluation
- RGC17 Section 04Document23 pagesRGC17 Section 04Serge RinaudoPas encore d'évaluation
- Hydraulique Janvier2018Document131 pagesHydraulique Janvier2018Lengani Kader EvaricePas encore d'évaluation