Académique Documents
Professionnel Documents
Culture Documents
2010 PC Bfem
Transféré par
FALLOUCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
2010 PC Bfem
Transféré par
FALLOUDroits d'auteur :
Formats disponibles
2010 Brevet de fin d’études moyennes (BFEM)
Epreuve DE SCIENCES PHYSIQUES
Exercice 1 (4 points)
Un briquet neuf rempli de gaz butane (C4 H10 ) a une masse de 14,8 g. Utilisé pendant quelques
jours, le briquet est vidé de son contenu ; sa masse est alors 9 g. Tout le butane a réagi avec le
dioxygène de l’air et la combustion est supposée complète.
2.1 : Ecrire l’équation-bilan de la combustion complète du butane. (01 pt)
2.2 : Calculer la quantité de matière (nombre de mol) de butane brûlée. (01 pt)
2.3 : En déduire le volume de dioxygène nécessaire à cette combustion. (01 pt)
2.4 : Calculer la quantité de chaleur libérée sachant que la combustion d’une mole de gaz butane
libère une quantité de chaleur de 2800 kJ. (01 pt)
On donne : Volume molaire Vm = 24L.mol−1 ; M (C) = 12g.mol−1 ; M (H) = 1g.mol−1
Exercice 2 (4 points)
On dispose d’une solution d’acide chlorhydrique (H + + Cl− ) de concentration molaire Ca in-
connue.
1.1 : On prélève quelques millilitres de la solution que l’on introduit dans un tube à essais
contenant de la grenaille de zinc. Il se produit une réaction chimique et on observe un dégagement
gazeux. En approchant une flamme au dessus de l’ouverture du tube, on entend une petite
explosion.
1.1.1 : Quel est le nom du gaz qui se dégage ? Quelle est sa formule chimique ? (01 pt)
1.1.2 : Sachant qu’il se forme aussi des ions Zn2+ , écrire l’équation-bilan de la réaction entre
les ions H + et les atomes de zinc. (01 pt)
1.2 : On prélève à nouveau 10 mL de la solution d’acide que l’on met dans un bêcher, on y
ajoute quelques gouttes de bleu de bromothymol (BBT). On dose alors l’acide par une solu-
tion d’hydroxyde de sodium (N a+ + HO− ) de concentration molaire Cb = 5.10−2 mol.L−1 . Le
volume de base versé à l’équivalence est Vb = 20 mL.
1.2.1 : Quelle observation expérimentale permet d’affirmer que l’équivalence est atteinte ? (01
pt)
1.2.2 : Déterminer la concentration Ca de la solution d’acide.(01 pt)
Exercice 3 (6 points)
On a mesuré la résistance de deux fils cylindriques, de même section S, mais de métaux différents.
Les résultats obtenus sont regroupés dans le tableau ci-après.
Métal Longueur du fil (m) Résistance du fil (O)
Aluminium 10 7,8
Cuivre 50 25
3.1 : Calculer pour chaque fil la résistance pour une longueur de 100 m. (02 pts)
3.2 : Lequel des métaux est meilleur conducteur électrique ? Justifier la réponse. (02 pts)
3.3 : La résistivité du cuivre vaut ρ = 1, 8.10−8 Ω.m. En déduire la valeur de la section S des
fils. (02 pts)
www.troisieme.examen.sn RESAFAD - Sénégal avec le soutien de l’OIF
Exercice 4 (6 points)
4.1 : L’objectif de l’appareil sera assimilé à une lentille convergente de distance focale 50 mm.
Calculer la vergence de cette lentille. (01 pt)
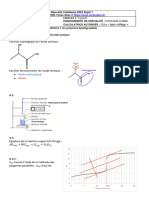
4.2 L’arbre AB étant situé à une distance D de l’objectif de l’appareil, l’image A’B’, de hauteur
h, se forme à la distance d du centre optique de la lentille comme indiqué sur le schéma ci-contre.
4.2.1 : Donner les caractéristiques de l’image (02 pts)
4.2.2 Le groupe d’élèves calcule la hauteur de l’arbre à partir de la relation : H = Dh
d
.
a) Retrouver cette relation à partir du schéma. (01,5 pt)
b) Calculer la hauteur de l’arbre avec les données suivantes : D = 10 m ; d = 50,2 mm et h =
1,5 cm. (01,5pt)
NB : les distances ne sont pas respectées sur le schéma.
www.troisieme.examen.sn RESAFAD - Sénégal avec le soutien de l’OIF
Vous aimerez peut-être aussi
- Quantité de MatièreDocument17 pagesQuantité de MatièreOumar TraoréPas encore d'évaluation
- Mathématiques: (3 Points) Exercice 1Document2 pagesMathématiques: (3 Points) Exercice 1SergePas encore d'évaluation
- 3194 v2 RG Ossature Mtallique Isol Therm Des Bardages Rapports PDFDocument68 pages3194 v2 RG Ossature Mtallique Isol Therm Des Bardages Rapports PDFEtude La FacadePas encore d'évaluation
- Kervran Transmutation BiologiqueDocument193 pagesKervran Transmutation Biologiquegabkoz100% (5)
- La ThermistanceDocument2 pagesLa ThermistanceSaidi Abdelillah100% (1)
- Devoir Commun de Mathematiques 4eme - 2011 Version 1Document3 pagesDevoir Commun de Mathematiques 4eme - 2011 Version 1Didactic math ديداكتيك الرياضيات0% (1)
- Chimie:: O Et N C HDocument3 pagesChimie:: O Et N C Hsaid khachouPas encore d'évaluation
- Bfem 2021 PCDocument2 pagesBfem 2021 PCSerigne Abdou DiopPas encore d'évaluation
- Droites Remarquables D Un Triangle Cours Et Exercices MaDocument4 pagesDroites Remarquables D Un Triangle Cours Et Exercices Mailyas merroun ouahabiPas encore d'évaluation
- Mathématiques - Examen 2004/2005Document2 pagesMathématiques - Examen 2004/2005OverDoc100% (2)
- Devoir de Contrôle N°3 Avec Correction - Sciences Physiques - 1ère AS (2015-2016) MR BARHOUMI Ezedine PDFDocument3 pagesDevoir de Contrôle N°3 Avec Correction - Sciences Physiques - 1ère AS (2015-2016) MR BARHOUMI Ezedine PDFNadhir SakouhiPas encore d'évaluation
- Examen National SVT Sciences Physiques 2016 Rattrapage SujetDocument6 pagesExamen National SVT Sciences Physiques 2016 Rattrapage SujetAlae AnouarPas encore d'évaluation
- Serie 1Document2 pagesSerie 1Ranim Jouini100% (1)
- Examen National Physique Chimie Sciences Maths 2018 Normale CorrigeDocument12 pagesExamen National Physique Chimie Sciences Maths 2018 Normale CorrigeWahbi AbdollahPas encore d'évaluation
- Serie 1 E Et 2 E (Cinétique Chimique) PDFDocument9 pagesSerie 1 E Et 2 E (Cinétique Chimique) PDFbouaounPas encore d'évaluation
- 1er Devoir Du 2ème Semestre PCT 5ème 2021-2022 Ceg Le NokoueDocument2 pages1er Devoir Du 2ème Semestre PCT 5ème 2021-2022 Ceg Le NokoueHaroldPas encore d'évaluation
- Le Parallelogramme Exercices Maths 1AC 4Document1 pageLe Parallelogramme Exercices Maths 1AC 4Home erriahi100% (1)
- TD N°1 Classe de 4èDocument3 pagesTD N°1 Classe de 4èJoël DabiréPas encore d'évaluation
- Serie D'exo ReparageDocument2 pagesSerie D'exo ReparageMoussa dialloPas encore d'évaluation
- DS Energie Changement Etat1Document5 pagesDS Energie Changement Etat1stéphan KrysPas encore d'évaluation
- Devoir de Contrôle N°2 - Math - 8ème (2016-2017) MR RIADH ZAIRI PDFDocument2 pagesDevoir de Contrôle N°2 - Math - 8ème (2016-2017) MR RIADH ZAIRI PDFRafik RafikPas encore d'évaluation
- (5 Points) (3 Points)Document2 pages(5 Points) (3 Points)Dispo OptimoPas encore d'évaluation
- Serie 2 Rotation 2024 Avec CorrectionDocument3 pagesSerie 2 Rotation 2024 Avec Correctionasmamajoul8Pas encore d'évaluation
- 8 EmeDocument2 pages8 EmeWougens VincentPas encore d'évaluation
- CalapproDocument3 pagesCalapprosanders traorePas encore d'évaluation
- Série D'exercices - Math - Equations Inequations (2) - 2ème InfoDocument3 pagesSérie D'exercices - Math - Equations Inequations (2) - 2ème InfoPaul Mbede SedenaPas encore d'évaluation
- 1ère S Cours Équations Et Inéquations TrigonométriquesDocument11 pages1ère S Cours Équations Et Inéquations TrigonométriquesmohamedPas encore d'évaluation
- 3emeevaluation2019 2020 PDFDocument1 page3emeevaluation2019 2020 PDFSantos AlexPas encore d'évaluation
- Devoir N°1 Maths Semestre 1 3eme 2020 2021 PDFDocument1 pageDevoir N°1 Maths Semestre 1 3eme 2020 2021 PDFTourech FrizeurPas encore d'évaluation
- Controle Maths 3ème (14.04.20) - 1Document2 pagesControle Maths 3ème (14.04.20) - 1Serge NoumbaPas encore d'évaluation
- Activite Numeriques 1 2016 2017 (Activite Numeriques 1) (Lycée Pilote Ariana)Document5 pagesActivite Numeriques 1 2016 2017 (Activite Numeriques 1) (Lycée Pilote Ariana)saidi sawssenPas encore d'évaluation
- Conducteur Ohmique 3èmeDocument3 pagesConducteur Ohmique 3èmeNemir Mimir100% (1)
- CCP 2012 MP m2 CorrigeDocument7 pagesCCP 2012 MP m2 CorrigeAmira ZarglayounPas encore d'évaluation
- TD 2Document21 pagesTD 2youssef sadkiPas encore d'évaluation
- CI02 TD03 Sujet - Interpréter Un Schéma CinématiqueDocument3 pagesCI02 TD03 Sujet - Interpréter Un Schéma CinématiqueKhaled JberiPas encore d'évaluation
- Devoir 3 Modele 2 Mathematiques 2ac Semestre 1 PDFDocument2 pagesDevoir 3 Modele 2 Mathematiques 2ac Semestre 1 PDFzahid zahid100% (3)
- Avancement de Grade ReclassementDocument19 pagesAvancement de Grade ReclassementGuedjeo Suh100% (1)
- Matrices Et Déterminants - TraceDocument5 pagesMatrices Et Déterminants - TraceHamza PrintoOsPas encore d'évaluation
- Exercice TC Prof-Boussakine-AbdelilahDocument36 pagesExercice TC Prof-Boussakine-Abdelilahmagadioo44Pas encore d'évaluation
- Cours - Math - Trigonométrie Et Mesure de Grandeurs - 2ème Sciences (2020-2021) MR Ayadi Mondher PDFDocument4 pagesCours - Math - Trigonométrie Et Mesure de Grandeurs - 2ème Sciences (2020-2021) MR Ayadi Mondher PDFjomma selmiPas encore d'évaluation
- 19 BEPCblanc PHYSCHIMIE 3 LHBKDocument2 pages19 BEPCblanc PHYSCHIMIE 3 LHBKUSiaka DaoPas encore d'évaluation
- La Rotation Dans Le Plan Cours Et Exercices Corriges 1Document4 pagesLa Rotation Dans Le Plan Cours Et Exercices Corriges 1Safaa El achhabPas encore d'évaluation
- Exercice Atome de Bohr1Document8 pagesExercice Atome de Bohr1islam rifiPas encore d'évaluation
- Série 1 Equations Inéquations 3APICDocument1 pageSérie 1 Equations Inéquations 3APICTech ChannelPas encore d'évaluation
- (5e) 0 Corrigé ExercicesDocument6 pages(5e) 0 Corrigé ExercicesAbđė Ěł ŁğđPas encore d'évaluation
- Physique EAC 2023Document2 pagesPhysique EAC 2023oblight39Pas encore d'évaluation
- Upload - Série D'exercices N°1-3Tech - Systèmes de Numération Et Codes-2013-2014 PDFDocument1 pageUpload - Série D'exercices N°1-3Tech - Systèmes de Numération Et Codes-2013-2014 PDFayman turkiPas encore d'évaluation
- TD CG CorrectionDocument34 pagesTD CG Correctionaminesassi20102002100% (1)
- DS - 7 - 1472 - 2021 2022 - 86 17 24 28 26 27 25Document13 pagesDS - 7 - 1472 - 2021 2022 - 86 17 24 28 26 27 25Armel Marc KouchoewanouPas encore d'évaluation
- Devoir 2 Modele 3 Mathematiques 3ac Semestre 1Document1 pageDevoir 2 Modele 3 Mathematiques 3ac Semestre 1Mohamed houl100% (1)
- Nouha Ramadan Hamou Mouna Exercices 1 Decroissance RadioactiveDocument1 pageNouha Ramadan Hamou Mouna Exercices 1 Decroissance Radioactiverihab0% (1)
- Exercice 1 Exercice 5: +ze - Nulle - Numéro Atomique - Gagné - PerduDocument2 pagesExercice 1 Exercice 5: +ze - Nulle - Numéro Atomique - Gagné - PerduHicham Eddaoudi100% (1)
- Programme - Mathématiques - Physique - EAC INGDocument6 pagesProgramme - Mathématiques - Physique - EAC INGsagesse MoukakouPas encore d'évaluation
- Bfem 1998 1Document1 pageBfem 1998 1Diabel DiopPas encore d'évaluation
- Cours Covid19Document15 pagesCours Covid19Japhet BAOUNDOULAPas encore d'évaluation
- Examen National Physique Chimie 2 Bac SVT 2020 Rattrapage CorrigeDocument9 pagesExamen National Physique Chimie 2 Bac SVT 2020 Rattrapage CorrigeMohamed SaidiPas encore d'évaluation
- DEVOIR 2nde D DU 3ème TRIMESTRE 22-23.bakhitadocx PDFDocument2 pagesDEVOIR 2nde D DU 3ème TRIMESTRE 22-23.bakhitadocx PDFHonorat Wekpon100% (1)
- Agir CompétentDocument2 pagesAgir CompétentANDRE ELOCKPas encore d'évaluation
- M. Sow MPC Année Scolaire: 2020-2021 Durée: 2h00min ClasseDocument1 pageM. Sow MPC Année Scolaire: 2020-2021 Durée: 2h00min ClasseNdeye diama Diop100% (1)
- Devoir de Contrôle 1AS Lycée Pilote by Galaï Abdelhamid Avec Correction PDFDocument5 pagesDevoir de Contrôle 1AS Lycée Pilote by Galaï Abdelhamid Avec Correction PDFTarek BouallegPas encore d'évaluation
- 2019 PCDocument2 pages2019 PCReal Capital INVESTMENTPas encore d'évaluation
- Compil Bfem PCDocument38 pagesCompil Bfem PCfalilou lo100% (1)
- 1cm5qeoaq 26957Document5 pages1cm5qeoaq 26957ndiayePas encore d'évaluation
- MR O DouinatDocument4 pagesMR O DouinatChoubane LaminePas encore d'évaluation
- Https0330088s.index Education - netpronoteFichiersExternes8aDocument7 pagesHttps0330088s.index Education - netpronoteFichiersExternes8athomasPas encore d'évaluation
- VCF Acetone (Dimethyl Ketone)Document2 pagesVCF Acetone (Dimethyl Ketone)Edgar GuardiaPas encore d'évaluation
- Les Facteurs Edaphiques Et Leurs Relations Avec Les Etres Vivants Documents 1Document10 pagesLes Facteurs Edaphiques Et Leurs Relations Avec Les Etres Vivants Documents 1Ndoumbé Sarr100% (1)
- 4 - Norme CM66 - Dimens°. LissesDocument4 pages4 - Norme CM66 - Dimens°. LisseslhabsPas encore d'évaluation
- Recueil de Petrographie LMDDocument42 pagesRecueil de Petrographie LMDkellynkiki2Pas encore d'évaluation
- Fer Forge de Protection ConsultationDocument2 pagesFer Forge de Protection ConsultationAyed YazidiPas encore d'évaluation
- Géotechnique - Théorie - TOME 1 - Mécanique Des Sols - 2016Document183 pagesGéotechnique - Théorie - TOME 1 - Mécanique Des Sols - 2016Har mc2Pas encore d'évaluation
- Chapitre - 1 Composites MateriauxDocument14 pagesChapitre - 1 Composites Materiauxulys1922Pas encore d'évaluation
- Pétrographie Exogene IllustrationsDocument23 pagesPétrographie Exogene IllustrationsBass NgomPas encore d'évaluation
- Note de Calcul Charpente MetalliqueDocument42 pagesNote de Calcul Charpente Metalliquetaibi100% (1)
- Cours Traitement Sol Ens-CachanDocument41 pagesCours Traitement Sol Ens-Cachanmichalakis483100% (4)
- BLPC 280-281 51-62Document13 pagesBLPC 280-281 51-62Ahmad ZreikPas encore d'évaluation
- Chapitre IV - Les Armatures en Aciers TG 3e AnneeDocument5 pagesChapitre IV - Les Armatures en Aciers TG 3e AnneebahPas encore d'évaluation
- Récupération Des Matières Non Métalliques RecyclablesDocument1 pageRécupération Des Matières Non Métalliques RecyclablesTouha FedinePas encore d'évaluation
- Ponts Cadres - Manuel de L'utilisateurDocument22 pagesPonts Cadres - Manuel de L'utilisateurific69100% (6)
- Propriétés Mécaniques Des BimatériauxDocument4 pagesPropriétés Mécaniques Des BimatériauxRahma EL MAAROUFIPas encore d'évaluation
- Tube Fluoropolymère PFADocument1 pageTube Fluoropolymère PFAKhalid PagesPas encore d'évaluation
- DechetDocument7 pagesDechetsalsabilePas encore d'évaluation
- Calcul Du PH Des Solutions AqueusesDocument5 pagesCalcul Du PH Des Solutions AqueusesHassen JinyorPas encore d'évaluation
- Correction Un Polymere BiodegradableDocument5 pagesCorrection Un Polymere BiodegradablegrajzgrPas encore d'évaluation
- Etude de La Qualite Des Huiles - Mohammed FEDOUL - 4025Document43 pagesEtude de La Qualite Des Huiles - Mohammed FEDOUL - 4025TAMKOUKT MohamedPas encore d'évaluation
- Tresses de Masse Tresses de Masse Avec CosseDocument2 pagesTresses de Masse Tresses de Masse Avec CossetestPas encore d'évaluation
- Chap. 2 Les AlcanesDocument12 pagesChap. 2 Les AlcanesNguettia Yao jean Daniel Adou100% (2)
- 4-Tous Les TD CorrigésDocument103 pages4-Tous Les TD CorrigéssaifounkhPas encore d'évaluation
- Barrage CH 03 PDFDocument21 pagesBarrage CH 03 PDFfaouziPas encore d'évaluation