Académique Documents
Professionnel Documents
Culture Documents
Plan de Travail - Module 2.5
Transféré par
edikola1Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Plan de Travail - Module 2.5
Transféré par
edikola1Droits d'auteur :
Formats disponibles
CHE0501P – Chimie générale
Automne 2019
PLAN DE TRAVAIL
MODULE 2.5 – PHASES, ÉQUILIBRE ET INGÉNIERIE
Objectifs du module :
Équilibres de phases
• Expliquer les propriétés d’exceptions de l’eau.
• Décrire un diagramme de phases.
Équilibre liquide-vapeur
• Expliquer le concept d’équilibre liquide-vapeur.
• Calculer la tension de vapeur d’un liquide.
Loi de Raoult et applications
• Appliquer la loi de Raoult.
Chaleur spécifique et applications
• Calculer l’énergie requise pour chauffer ou refroidir une substance.
1. Vidéos à écouter
Pour les capsules théoriques, remplissez la fiche d’aide à la prise de notes.
Vidéo à écouter Durée Fait
Entrevue – Le système de distillation 8 :52 ☐
Capsules théoriques – Équilibres de
phases
C1 8 :41 et C2 6 :30 ☐
Capsules théoriques – Équilibre
liquide-vapeur
C1 8 :59 et C2 12 :31 ☐
Capsule théorique – Loi de Raoult et
applications
C1 12 :13 et C2 11 :21 ☐
Capsules théoriques – Chaleur
spécifique et applications
C1 11 :42 et C2 6 :46 ☐
2. Questions de compréhension et exercices
Capsules Nombre de questions Fait
Capsules théoriques – Équilibres de phases 10 questions ☐
Capsules théoriques – Équilibre liquide-
vapeur
10 questions ☐
Capsule théorique – Loi de Raoult et
applications
10 questions ☐
Capsules théoriques – Chaleur spécifique et
applications
10 questions ☐
Retour sur l’entrevue 10 questions ☐
Test – Phases, équilibre et ingénierie
(à faire avant le 2 décembre à 12h)
10 questions ☐
3. Laboratoire
• Réaliser le laboratoire Distillation et loi de Raoult et répondre aux 10 questions.
4. Travail à remettre avant le lundi 2 décembre à 12h au bureau A578.
• Devoir no. 2.5
5. Encadrement
• N’hésitez pas à passer à mon bureau (A578.2) pour me poser vos questions. Il est toujours
préférable de prendre un rendez-vous au préalable.
Bravo ! Vous avez terminé votre cours de chimie générale.
Vous pouvez être fier de vous !
CHE0501P – Chimie générale
Automne 2019
Devoir no. 2.5 (exercices adaptés de M. Jean Paiement et du livre Chimie
générale de Chang, R. et Goldsby, K.)
MODULE 2.5 – PHASES, ÉQUILIBRE ET INGÉNIERIE
Ce travail est à remettre individuellement avant le lundi 2 décembre à 12h au bureau A578. Portez une
attention particulière à la clarté de vos démarches et à la propreté de votre travail. Un travail manquant
de rigueur ne sera pas accepté et la note de 0 lui sera attribuée.
1. Calculez l’énergie nécessaire pour chauffer 1,00 X 102g d’eau de -30,0oC à 120,0oC ?
ΔHf = 6,01 kJ/mol Cp(s) = 37,2 J/mol • oC
ΔHv = 40,8 kJ/mol Cp(l) = 75,2 J/mol • oC
Cp(g) = 33,1 J/mol • oC
2. Le Fréon-11 (CCl3F) a une température d’ébullition normale de 23,8oC. La chaleur spécifique du
liquide est de 0,87 J/g*K et elle est de 0,59 J/g*K pour le gaz. L’enthalpie de vaporisation est de
24,75 kJ/mol. Calculez l’énergie pour convertir 10,0 g de Fréon-11 liquide à -50,0oC en gaz à 50,0oC.
3. La pression de vapeur du benzène (C6H6) est de 40,1 mmHg à 7,6oC. Quelle est la pression de vapeur
du benzène à 60,6 oC ? La chaleur molaire de vaporisation du benzène est de 31,0 kJ/mol.
4. Une masse d’eau pesant 1,20 g est injectée dans une fiole de 5,00 L dans laquelle nous avons
préalablement fait le vide. La température est de 65oC. Quel pourcentage de l’eau sera en phase
vapeur lorsque le système aura atteint l’équilibre ? La pression de vapeur de l’eau à 65oC est de
187,5 mm Hg.
5. On introduit une mole de benzène dans un cylindre à piston dont la section est de 0,074 m2 et dont
le volume initial est de 10,0 L. Après que l’équilibre liquide-vapeur soit atteint pour une
température constante de 50,0oC, le manomètre affiche une pression de 272 mm Hg.
A) On soulève le piston jusqu’à une hauteur correspondant à un volume de 20,0 L, toujours à
50,0oC. Un nouvel équilibre s’établit, où on observe une diminution de volume du liquide. Pour
quelle raison le liquide a-t-il diminué de volume et quelle pression le manomètre affiche-t-il ?
B) À quelle hauteur faut-il soulever le piston pour que la dernière goutte de liquide disparaisse ?
C) Sachant que la tension de vapeur du benzène à 60,0oC est de 383 mm Hg, calculez l’enthalpie de
vaporisation (ΔHv) du benzène.
6. Au terme de votre cours en ligne, veuillez rédiger 3 conseils que vous donneriez à un étudiant qui
désire suivre ce cours dans le futur. Basez-vous sur de bonnes et de moins bonnes stratégies que
vous avez utilisées.
7. Au terme de votre cours en ligne, veuillez donner 3 conseils à vos collègues (et à vous-même…) pour
bien vous préparer à votre examen final.
Vous aimerez peut-être aussi
- Gros Labo 1 en 4Document14 pagesGros Labo 1 en 4Afaf AchkanouPas encore d'évaluation
- Uaa4 ProfDocument11 pagesUaa4 ProfMannsPas encore d'évaluation
- Plan de Travail - Module 1.4Document4 pagesPlan de Travail - Module 1.4edikola1Pas encore d'évaluation
- Plan de Travail - Module 1.3Document3 pagesPlan de Travail - Module 1.3edikola1Pas encore d'évaluation
- Plan de Travail - Module 1.1Document5 pagesPlan de Travail - Module 1.1edikola1Pas encore d'évaluation
- Bonjour, Ceci Est Un DM À Rendre Pour Demain Mais Je N Arrive Pas À La Faire. Pouvez-Vous M'aiderDocument1 pageBonjour, Ceci Est Un DM À Rendre Pour Demain Mais Je N Arrive Pas À La Faire. Pouvez-Vous M'aiderky9qxbk42hPas encore d'évaluation
- Exp. 1 - Pesee Et Chiffres Significatifs - Prelab A22Document2 pagesExp. 1 - Pesee Et Chiffres Significatifs - Prelab A22Arthur ZhangPas encore d'évaluation
- Plan de Travail - Module 1.5Document3 pagesPlan de Travail - Module 1.5edikola1Pas encore d'évaluation
- Livre Chimie 1ere AnnéeDocument173 pagesLivre Chimie 1ere AnnéeToons Land100% (1)
- Livre de Chimie 1èreDocument160 pagesLivre de Chimie 1èreAbdelhak Sadik100% (6)
- TP Lampe A LaveDocument2 pagesTP Lampe A LaveRAZA LUCPas encore d'évaluation
- Vapeur Saturée-EnthalpieDocument7 pagesVapeur Saturée-EnthalpieYacine Er-rbahPas encore d'évaluation
- TP Transfert Thermique 2deDocument4 pagesTP Transfert Thermique 2desumaleePas encore d'évaluation
- DOC312.77.94029 1ed LCK914Document2 pagesDOC312.77.94029 1ed LCK914Ornevalde JulphinPas encore d'évaluation
- TD1-Complèmentaire-Corps PurDocument5 pagesTD1-Complèmentaire-Corps PurmennanesalaheddinePas encore d'évaluation
- DOC312.77.94026 1ed LCK514Document2 pagesDOC312.77.94026 1ed LCK514Ornevalde JulphinPas encore d'évaluation
- Fiche de TD BisDocument6 pagesFiche de TD BisBenito BenitoPas encore d'évaluation
- Séquence Exercice - Les Réactions de Combustions - Niveau 4°Document16 pagesSéquence Exercice - Les Réactions de Combustions - Niveau 4°douzi nourPas encore d'évaluation
- Travaux Pratiques de Thermodynamique Et de Cinétique ChimiquesDocument18 pagesTravaux Pratiques de Thermodynamique Et de Cinétique Chimiquesami rPas encore d'évaluation
- Physique Indus Et ThermodynamiqueDocument26 pagesPhysique Indus Et ThermodynamiqueollhPas encore d'évaluation
- ECE 22 PC 07 Bdf5be8228Document6 pagesECE 22 PC 07 Bdf5be8228ArthurpetitPas encore d'évaluation
- Enonce TD29Document3 pagesEnonce TD29anas achmitPas encore d'évaluation
- Effets Thermiques D'une Transformation Chimique: Document 1: Un Réchauffeur Sans FlammeDocument2 pagesEffets Thermiques D'une Transformation Chimique: Document 1: Un Réchauffeur Sans Flammeaxel artusPas encore d'évaluation
- TD Melanges 2014 Lsll-Wahab DiopDocument2 pagesTD Melanges 2014 Lsll-Wahab DiopMamadou Thioye100% (1)
- CatalaseDocument7 pagesCatalaseLeila MolnarPas encore d'évaluation
- Entropie Et Deuxième PrincipeDocument65 pagesEntropie Et Deuxième Principemehdielamra123Pas encore d'évaluation
- Les Cahiers de La Luciole CE2 - La Matiere CorrigesDocument10 pagesLes Cahiers de La Luciole CE2 - La Matiere CorrigesSelena Hamiche100% (2)
- TP S2 ChimieDocument13 pagesTP S2 ChimieLeï IaPas encore d'évaluation
- Plan de Travail - Module 2.4Document3 pagesPlan de Travail - Module 2.4edikola1Pas encore d'évaluation
- Nogesba TD 3émeDocument7 pagesNogesba TD 3émeEric SonaPas encore d'évaluation
- Questions Calcul Pratique Debits VapeurDocument10 pagesQuestions Calcul Pratique Debits Vapeurdallagi mohamedPas encore d'évaluation
- DS1 Chap1Document3 pagesDS1 Chap1Sassi LassaadPas encore d'évaluation
- TP Chimie N° 1Document2 pagesTP Chimie N° 1MERi B100% (1)
- Devoir 4 20142015Document5 pagesDevoir 4 20142015Amadou Makhtar SeckPas encore d'évaluation
- 2 I-07 EtatsDocument5 pages2 I-07 EtatsssgPas encore d'évaluation
- Chimie 2 - Introduction Aux LaboratoiresDocument59 pagesChimie 2 - Introduction Aux LaboratoireslesliePas encore d'évaluation
- Questions-Calcul Pratique Debits Eau Air Partie 2Document13 pagesQuestions-Calcul Pratique Debits Eau Air Partie 2Meryem BarnyPas encore d'évaluation
- Poly TP Réact en Sol 31 007Document32 pagesPoly TP Réact en Sol 31 007Laurent KeletaonaPas encore d'évaluation
- Exercices Post-Examen 2 - FDocument8 pagesExercices Post-Examen 2 - FSarah Taibi El KettaniPas encore d'évaluation
- P 46 50 Metrologie Dany VertDocument5 pagesP 46 50 Metrologie Dany VertnabilaPas encore d'évaluation
- Compte Rendu TP2 Chimie 2Document9 pagesCompte Rendu TP2 Chimie 2soumiagpoPas encore d'évaluation
- Leçon Re - Solution - de - PB - 1e - Re - S - Synthe - Se - Savon - ReluDocument2 pagesLeçon Re - Solution - de - PB - 1e - Re - S - Synthe - Se - Savon - ReluVolanirina RaharintsoaPas encore d'évaluation
- 14TPO Le Bioethanol 1Document4 pages14TPO Le Bioethanol 1TshisolaPas encore d'évaluation
- TD 2 de ThermochimieDocument4 pagesTD 2 de ThermochimieCARDI BPas encore d'évaluation
- ds1 Chap1 CorrigeDocument3 pagesds1 Chap1 CorrigeMagatte DiopPas encore d'évaluation
- Cours de Production de Froid PDFDocument158 pagesCours de Production de Froid PDFKouakou Khan100% (1)
- Exercice N°1: Exercice Sur 6,5 PointsDocument2 pagesExercice N°1: Exercice Sur 6,5 PointschironiPas encore d'évaluation
- TD2 Isa 2 2022Document2 pagesTD2 Isa 2 2022Hassan ChehouaniPas encore d'évaluation
- Guide Redaction RapportDocument10 pagesGuide Redaction RapportBlain HailePas encore d'évaluation
- Laboratoire: Essais de Gel-DégelDocument10 pagesLaboratoire: Essais de Gel-DégelAdil ALAOUIPas encore d'évaluation
- Cours Partie N°2 Chimie Des Eaux (M1-GPE 2021-2022)Document15 pagesCours Partie N°2 Chimie Des Eaux (M1-GPE 2021-2022)Boudjaoui100% (1)
- TD Melanges 2020 LSLL - Wahab DiopDocument2 pagesTD Melanges 2020 LSLL - Wahab DiopBilel BelhajamorPas encore d'évaluation
- Cahier Des Laboratoires NYA2023Document73 pagesCahier Des Laboratoires NYA2023Lucas BulméPas encore d'évaluation
- Plan de Travail - Module 1.2Document3 pagesPlan de Travail - Module 1.2edikola1Pas encore d'évaluation
- Gaz MédicauxDocument10 pagesGaz MédicauxMerieme SafaaPas encore d'évaluation
- 16 1 Cinetique Et Catalyse A6Document17 pages16 1 Cinetique Et Catalyse A6Rafik DraPas encore d'évaluation
- TPP2-1Spe-Sujet-Loi de MariotteDocument2 pagesTPP2-1Spe-Sujet-Loi de MariotteceliabenayPas encore d'évaluation
- AE2 Facteurs Cinétiques Et Catalyse Correction EleveDocument3 pagesAE2 Facteurs Cinétiques Et Catalyse Correction ElevekandedianissyPas encore d'évaluation
- Copie de HM Module 2 Gammes de Maintenance PreventiveDocument95 pagesCopie de HM Module 2 Gammes de Maintenance PreventiveMakki ABDELLATIFPas encore d'évaluation
- Dece 45061Document51 pagesDece 45061Chawki ZerroukiPas encore d'évaluation
- Détermination Du Coefficient de Porosité Ouverte D'après La Poussée D'archimèdeDocument4 pagesDétermination Du Coefficient de Porosité Ouverte D'après La Poussée D'archimèdeChannel FormePas encore d'évaluation
- Wek 2017-11 2Document281 pagesWek 2017-11 2Sofiane Ait MebroukPas encore d'évaluation
- 10 SD FRDocument4 pages10 SD FRabbes ben hemanaPas encore d'évaluation
- Rapport de Stage Étude D'assainissement Du Centre de Bouderbala 2021 Réaliser Par Walide Bakka Étudiant ITSAZ-BERKANDocument61 pagesRapport de Stage Étude D'assainissement Du Centre de Bouderbala 2021 Réaliser Par Walide Bakka Étudiant ITSAZ-BERKANBRDAHM TVPas encore d'évaluation
- Note de Calcul Reseau GazDocument1 pageNote de Calcul Reseau GazDjamal Mohammedi100% (1)
- Chapitre 7Document10 pagesChapitre 7Ludovic LeroyPas encore d'évaluation
- Pocan B3235000000Document4 pagesPocan B3235000000OumaimaPas encore d'évaluation
- Les EcransDocument6 pagesLes EcransKhadija ED DAHBYPas encore d'évaluation
- Guide Pratique Daménagement Des PEIDocument37 pagesGuide Pratique Daménagement Des PEICarmel ADEBIAYEPas encore d'évaluation
- Danfoss DHP-AQ Service VMGFJ104 FRDocument41 pagesDanfoss DHP-AQ Service VMGFJ104 FRBoubaker YoussefPas encore d'évaluation
- HazopDocument5 pagesHazopSagacious IvejutenPas encore d'évaluation
- Profil Des PalesDocument4 pagesProfil Des PalesazizkhouribgaPas encore d'évaluation
- Chapitre 3 Pré-DimensionnementDocument9 pagesChapitre 3 Pré-Dimensionnementfarouk kennichePas encore d'évaluation
- Liebherr Pompes A Beton Stationnaires FRDocument20 pagesLiebherr Pompes A Beton Stationnaires FRatek hacenePas encore d'évaluation
- CiatDocument7 pagesCiatlahcen_bahassouPas encore d'évaluation
- BTS CPI 1 CH 9 Méca FluidesDocument3 pagesBTS CPI 1 CH 9 Méca FluidesLucas Filipuzzi100% (1)
- NC 0105Document6 pagesNC 0105Hocine ChekrounPas encore d'évaluation
- DocumentDocument5 pagesDocumentAbdoulaye AbdourahamanePas encore d'évaluation
- Calcul Flexibilité Pomperie IncendieDocument77 pagesCalcul Flexibilité Pomperie IncendieHédi HammamiPas encore d'évaluation
- STEP ProjetDocument41 pagesSTEP Projetyoussef hachimiPas encore d'évaluation
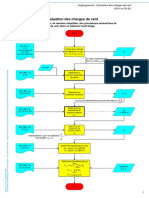
- Organigramme: Evaluation Des Charges de VentDocument4 pagesOrganigramme: Evaluation Des Charges de Vent3 éme infraPas encore d'évaluation
- Chapitre - EscaliersDocument9 pagesChapitre - EscaliersMohamed AmeurPas encore d'évaluation
- 553-2 S - Procédure D'utilisation d'ET Pour Les Pelles C PDFDocument28 pages553-2 S - Procédure D'utilisation d'ET Pour Les Pelles C PDFChakrounePas encore d'évaluation
- Les Composantes Hydrauliques PDFDocument10 pagesLes Composantes Hydrauliques PDFHamza LiberadosPas encore d'évaluation
- CoursDocument39 pagesCoursxe.pav12Pas encore d'évaluation
- Ex de Calcul Pont Roulant PDFDocument61 pagesEx de Calcul Pont Roulant PDFBourafa Salim100% (1)
- Colmatage Et Nettoyage Des Membranes D'osmose Inverse de DessalementDocument14 pagesColmatage Et Nettoyage Des Membranes D'osmose Inverse de Dessalementyoussef hachimiPas encore d'évaluation
- TD Plomberie2023Document3 pagesTD Plomberie2023terifrancois4Pas encore d'évaluation