Académique Documents
Professionnel Documents
Culture Documents
Sujet PCT 3e
Transféré par
arsene BATAWUILA0 évaluation0% ont trouvé ce document utile (0 vote)
5 vues1 pageCopyright
© © All Rights Reserved
Formats disponibles
PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
5 vues1 pageSujet PCT 3e
Transféré par
arsene BATAWUILADroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 1
Année scolaire : 2022-2023 COMPOSITION DU PREMIER TRIMESTRE Classe : 3e
DRE GRAND-LOME ÉPREUVE DE PHYSIQUE CHIMIE ET TECHNOLOGIE Durée : 2 H Coef : 2
Exercice 1 : (08 points)
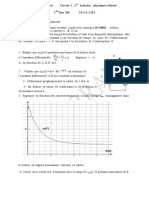
Aurélia réalise l’expérience ci-dessous dont le but est de déterminer la nature du liquide dans lequel est
plongé l’objet. Après l’expérience elle a des difficultés pour atteindre son objectif.
A partir de tes connaissances et des données de l’expérience, aide Aurélia en recherchant la nature du
liquide utilisé.
1,44 N
1,5 N
V2 = 25 cm3
3
V1 = 20 cm
Liquide
On donne : g = 10 N/kg
Liquide Eau Alcool Eau salée Miel
Masse volumique 1 kg/dm3 0,82 kg/dm3 1,2 kg/dm3 1,4 kg/dm3
Pertinence 2,5 pts ; Cohérence 2,5 pts ; Correction 2 pts ; Perfectionnement 1pt
Exercice 2 : (06 points)
1. Réponds par vrai ou faux. (2 pts)
a) Tous les hydrocarbures sont des alcanes.
b) Les alcanes sont des sources d’énergie.
c) Un alcane à 8 atomes d’hydrogène contient 3 atomes de carbone.
d) La synthèse de l’eau est sa décomposition en dihydrogène et en dioxygène.
2. Voici l’équation bilan de la combustion complète d’un alcane :
𝑥C4 H10 + 𝑦O2 ⟶ 𝑧CO2 + 𝑤H2 O
Choisis parmi les propositions suivantes les valeurs des coefficients x, y, z et w qui permettent
d’équilibrer cette équation : (0,5 pt)
a) x = 2 ; y = 13 ; z = 4 ; w = 10. C2H6
b) x = 2 ; y = 13 ; z = 8 ; w = 10. Butane
13 C4H10
c) x = 2 ; y = 2 ; z = 8 ; w = 10. Méthane
3. Reproduis les deux diagrammes ci-contre puis relie le nom de chaque alcane Éthane CH4
à sa formule brute. (1,5 pt)
C2H4
4. Remplace les chiffres par les mots manquants sans recopier le texte. (2 pts)
Dans un montage de détecteur de lumière, la ---1--- joue le rôle de capteur et le ---2--- joue
le rôle de dispositif électronique. Dans le transistor de type NPN, le courant électrique ---3--- par l’émetteur
E. en régime linéaire le transistor joue le rôle d’un ---4--- de courant.
Exercice 3 : (06 points)
On réalise l’électrolyse de 180 g d’eau.
1. Écris l’équation bilan de cette réaction chimique. (0,5 pt)
2. On recueille à la cathode 224 dm3 d’un gaz. De quel gaz s’agit-il ? (0,5 pt)
3. Quel gaz recueille-t-on à l’autre électrode ? Quel est son volume ? (1 pt)
4. Comment peut-on identifier ces gaz ? (1 pt)
5. Sachant que la masse du gaz recueilli à la cathode est de 20 g, calcule la masse de l’autre gaz. (1 pt)
6. On t’indique que 18 g d’eau contiennent 6 1023 molécules d’eau. Combien de molécules de chacun
des gaz obtient-on ? (2 pts)
Vous aimerez peut-être aussi
- DST PCT 3è Nov 2023Document1 pageDST PCT 3è Nov 2023Narma BakoutarePas encore d'évaluation
- Bepc Blanc-2Document1 pageBepc Blanc-2DATSOMOPas encore d'évaluation
- Chimie 15-22 PTDocument170 pagesChimie 15-22 PTTaha MarweniPas encore d'évaluation
- Epreuve de Chimie: Données: Volume Molaire VDocument2 pagesEpreuve de Chimie: Données: Volume Molaire VDonaldPas encore d'évaluation
- Sujet SciencesDocument6 pagesSujet SciencesLina LamouchiPas encore d'évaluation
- Annatut UE1 Chimie Générale 2012 2013 PDFDocument27 pagesAnnatut UE1 Chimie Générale 2012 2013 PDFÏk Râm0% (1)
- Devoir Corrigé de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2015-2016) MR TRAYIA NABILDocument9 pagesDevoir Corrigé de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2015-2016) MR TRAYIA NABILwalidPas encore d'évaluation
- Devoir de Controle n1 2022bac MathDocument5 pagesDevoir de Controle n1 2022bac MathNour NessahPas encore d'évaluation
- 4 Liaison ChimiqueDocument8 pages4 Liaison ChimiqueAzumi ChanPas encore d'évaluation
- Bac Blanc Et Sa Correction Pour 2 BAC Mai 2022 MR SabourDocument26 pagesBac Blanc Et Sa Correction Pour 2 BAC Mai 2022 MR SabourHiba LaaraichiPas encore d'évaluation
- Devoir Corrigé de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2015-2016) MR TRAYIA NABILDocument10 pagesDevoir Corrigé de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2015-2016) MR TRAYIA NABILMouhamed Ali SahbaniPas encore d'évaluation
- C PT 2020 PDFDocument16 pagesC PT 2020 PDFHammouda ChebbiPas encore d'évaluation
- Phy ChiDocument6 pagesPhy ChiPaul Hervé Zanga ZangaPas encore d'évaluation
- E ph2mp2021Document8 pagesE ph2mp2021Siham JiwooPas encore d'évaluation
- PCT 3è-1Document1 pagePCT 3è-1arsene BATAWUILAPas encore d'évaluation
- EXAMEN SVITU SESSION Rattrapage 2019-2020Document6 pagesEXAMEN SVITU SESSION Rattrapage 2019-2020cherki hiPas encore d'évaluation
- H PG OXoo 5 ZB 4 BDD Pje TJ YPP43 WW 1 FQ0 Hii UURn GOqDocument5 pagesH PG OXoo 5 ZB 4 BDD Pje TJ YPP43 WW 1 FQ0 Hii UURn GOqOusmane BorePas encore d'évaluation
- Epreuve de PCT 3eme - Evaluation de BaseDocument1 pageEpreuve de PCT 3eme - Evaluation de BaseLAWSON NICOLASPas encore d'évaluation
- Bac Blanc 2021bisDocument7 pagesBac Blanc 2021bisSahbi Mabrouki YamenPas encore d'évaluation
- Épreuve Sciences Physiques Classe 4ème Sciences 1 Prof: Chebbi RachidDocument4 pagesÉpreuve Sciences Physiques Classe 4ème Sciences 1 Prof: Chebbi RachidMohamed SaidiPas encore d'évaluation
- CO1 TS1 2024 Ialg - WahabdiopDocument4 pagesCO1 TS1 2024 Ialg - Wahabdioppapa samba sarrPas encore d'évaluation
- 1ères CD - CH REVISION N°02Document2 pages1ères CD - CH REVISION N°02NDE0% (1)
- DS1 (11 12 09)Document8 pagesDS1 (11 12 09)Seif Souid100% (5)
- ds1 2013 PDFDocument5 pagesds1 2013 PDFMustapha ElhafiPas encore d'évaluation
- Correction DC1 19 20Document3 pagesCorrection DC1 19 20amir bougachaPas encore d'évaluation
- Bac Blanc Série D Avril 2023Document4 pagesBac Blanc Série D Avril 2023gracemboa5Pas encore d'évaluation
- Bepc-Blanc N°2Document2 pagesBepc-Blanc N°2eliazamedePas encore d'évaluation
- Bepc Jec BepcDocument3 pagesBepc Jec BepcAntoine SawadogoPas encore d'évaluation
- U C A D D: Exercice 1Document5 pagesU C A D D: Exercice 1Lindeltaylor DioufPas encore d'évaluation
- مواضيع البكالوريا ل موريطانيا من 2002إلى 2012 PDFDocument177 pagesمواضيع البكالوريا ل موريطانيا من 2002إلى 2012 PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Prop TSDocument3 pagesProp TSAly NDAOPas encore d'évaluation
- Composition 1er Semestre - Sciences Physiques - 3 Heures: Cours À Domicile: 775136349Document2 pagesComposition 1er Semestre - Sciences Physiques - 3 Heures: Cours À Domicile: 775136349Spotify SpotifyPas encore d'évaluation
- Devoir de Contrôle N°1 2013 2014 (Kallel Chiheb)Document4 pagesDevoir de Contrôle N°1 2013 2014 (Kallel Chiheb)Sou HaPas encore d'évaluation
- UntitledDocument4 pagesUntitledMohamed SaidiPas encore d'évaluation
- Série 3 2021Document5 pagesSérie 3 2021Rafael EscobarPas encore d'évaluation
- Chimie Des Solutions Aqueuses TD 5Document6 pagesChimie Des Solutions Aqueuses TD 5WIJDANEPas encore d'évaluation
- Chimie 2nde C DSN 2Document2 pagesChimie 2nde C DSN 2TCHUINDJO NYAMSIPas encore d'évaluation
- SC - Physiques Bac Blanc - Maths-2021 (Jlali Ammar)Document5 pagesSC - Physiques Bac Blanc - Maths-2021 (Jlali Ammar)Ali SkimaPas encore d'évaluation
- DC1 4SC 2022 2023 Boussada - AtefDocument4 pagesDC1 4SC 2022 2023 Boussada - Atefabderrazek0% (1)
- Examen Blanc 2021 Physique Chimie SMDocument9 pagesExamen Blanc 2021 Physique Chimie SMTesteur Mohammedia100% (1)
- Devoir Controle 1 2024Document5 pagesDevoir Controle 1 2024rayentmar0Pas encore d'évaluation
- Concours Epss Chimie G 2018-2019 Version A CorrDocument3 pagesConcours Epss Chimie G 2018-2019 Version A CorrohoureginaPas encore d'évaluation
- Devoir 3Document4 pagesDevoir 3Mehdi BnmssdPas encore d'évaluation
- PCT Tle DDocument4 pagesPCT Tle DalladayewildinePas encore d'évaluation
- Pages de Bac Blanc 2Document5 pagesPages de Bac Blanc 2Khaouda Driss100% (2)
- 628bcf3af06f4 - Sujet1 - Bac2022-Sujet N°1-EnoncéDocument9 pages628bcf3af06f4 - Sujet1 - Bac2022-Sujet N°1-EnoncéWael Hajji0% (1)
- Devoir de Contrôle N°1 Lycée Pilote - Physique - Bac Mathématiques (2011-2012) MR FekiriDocument5 pagesDevoir de Contrôle N°1 Lycée Pilote - Physique - Bac Mathématiques (2011-2012) MR FekiriDeadly TokyoPas encore d'évaluation
- Devoir de Revision HediDocument5 pagesDevoir de Revision HediAmine AlaoUii AlaouiPas encore d'évaluation
- Correction de DSN2 Bac 2020..Document3 pagesCorrection de DSN2 Bac 2020..dahnenanisPas encore d'évaluation
- Devoir Synthèse-1 - 4 ScTech-2022Document6 pagesDevoir Synthèse-1 - 4 ScTech-2022Riadh BesbesPas encore d'évaluation
- SEQ1 Maths TleCDocument1 pageSEQ1 Maths TleCYannick NantiaPas encore d'évaluation
- DS 7 430 2020-2021 34-27Document4 pagesDS 7 430 2020-2021 34-27Armel Marc KouchoewanouPas encore d'évaluation
- Devoir 2 20182019Document3 pagesDevoir 2 20182019Amadou Makhtar SeckPas encore d'évaluation
- DC N°1 4 EME 2023 Lycée OkbaDocument3 pagesDC N°1 4 EME 2023 Lycée OkbaSalah ZahouaniPas encore d'évaluation
- Examen 2er Semestre Mai 2017version Finale Enone Et CorrigeeDocument8 pagesExamen 2er Semestre Mai 2017version Finale Enone Et CorrigeeAziz JridiPas encore d'évaluation
- Devoir de Synthèse N°1 - Sciences Physiques - Bac Mathématiques (2015-2016) MR Maalej Med HabibDocument6 pagesDevoir de Synthèse N°1 - Sciences Physiques - Bac Mathématiques (2015-2016) MR Maalej Med HabibMustapha ElhafiPas encore d'évaluation
- Fiche de TD N°2 PDFDocument15 pagesFiche de TD N°2 PDFPaola DjeugaPas encore d'évaluation
- Document de prépa bepc 2024 Provincial (maths,Pc,Fr,Svt,Ang,All,Esp)Document115 pagesDocument de prépa bepc 2024 Provincial (maths,Pc,Fr,Svt,Ang,All,Esp)arsene BATAWUILAPas encore d'évaluation
- CHIMIE 2nde C EVA 5Document2 pagesCHIMIE 2nde C EVA 5vincenzo essomba100% (3)
- IESG DEVOIRS 2024Document1 pageIESG DEVOIRS 2024arsene BATAWUILAPas encore d'évaluation
- Fiche Professeur - 1ère Technique Option STIDocument61 pagesFiche Professeur - 1ère Technique Option STIarsene BATAWUILAPas encore d'évaluation
- Fiche Pedagogique SVT 6eme 2019-2020Document105 pagesFiche Pedagogique SVT 6eme 2019-2020arsene BATAWUILAPas encore d'évaluation
- PC 1D 1a Ta S2 2024Document4 pagesPC 1D 1a Ta S2 2024arsene BATAWUILAPas encore d'évaluation
- Gea Prepa Bepc 2023Document74 pagesGea Prepa Bepc 2023angry toura100% (1)
- Maths 1ère A4 Du 14.03.24Document2 pagesMaths 1ère A4 Du 14.03.24arsene BATAWUILAPas encore d'évaluation
- Bepc Blanc 2024 SVT Local Gagnoa (Nouveau)Document3 pagesBepc Blanc 2024 SVT Local Gagnoa (Nouveau)arsene BATAWUILAPas encore d'évaluation
- Physique 6è Les Propriétés Physiques de La Matière Doc 2Document1 pagePhysique 6è Les Propriétés Physiques de La Matière Doc 2arsene BATAWUILAPas encore d'évaluation
- MATHS 4e BON - CopieDocument1 pageMATHS 4e BON - Copiearsene BATAWUILAPas encore d'évaluation
- Devoir PC 5eme Trimestre 3Document2 pagesDevoir PC 5eme Trimestre 3arsene BATAWUILAPas encore d'évaluation
- Revision Generale Tle D N°2Document2 pagesRevision Generale Tle D N°2arsene BATAWUILAPas encore d'évaluation
- SC Phys Seconde CD Bon2Document1 pageSC Phys Seconde CD Bon2arsene BATAWUILAPas encore d'évaluation
- Intro Generale À L'informatiqueDocument53 pagesIntro Generale À L'informatiquearsene BATAWUILAPas encore d'évaluation
- SP 2CDDocument2 pagesSP 2CDarsene BATAWUILAPas encore d'évaluation
- Cours Langage CDocument114 pagesCours Langage Carsene BATAWUILAPas encore d'évaluation
- Scnphys Seconde A4Document1 pageScnphys Seconde A4arsene BATAWUILAPas encore d'évaluation
- Concours Miss Maths 2018 Niveau Tle CDocument1 pageConcours Miss Maths 2018 Niveau Tle Carsene BATAWUILAPas encore d'évaluation
- Fiche Devoir N°2 Deuxieme Trimestre 3ieme Février 2024Document2 pagesFiche Devoir N°2 Deuxieme Trimestre 3ieme Février 2024arsene BATAWUILAPas encore d'évaluation
- Maths 3èmeDocument1 pageMaths 3èmearsene BATAWUILAPas encore d'évaluation
- DST 2 Eme T MATHS 4èmeDocument1 pageDST 2 Eme T MATHS 4èmearsene BATAWUILAPas encore d'évaluation
- TROISIEMEDocument2 pagesTROISIEMEarsene BATAWUILAPas encore d'évaluation
- Épreuve de Mathématiques - Durée: 4 Heures: 2 Bac Blanc (Décembre 2022)Document2 pagesÉpreuve de Mathématiques - Durée: 4 Heures: 2 Bac Blanc (Décembre 2022)arsene BATAWUILAPas encore d'évaluation
- Ceg Sagbiebou Bepc BlancDocument2 pagesCeg Sagbiebou Bepc Blancarsene BATAWUILAPas encore d'évaluation
- PCT 5eDocument1 pagePCT 5earsene BATAWUILAPas encore d'évaluation
- DST 2 Eme T PCT 4èmeDocument2 pagesDST 2 Eme T PCT 4èmearsene BATAWUILAPas encore d'évaluation
- Exercices Divers Sur Le Thème OxydoréductionDocument12 pagesExercices Divers Sur Le Thème Oxydoréductionissaradjab13Pas encore d'évaluation
- TP DcoDocument6 pagesTP Dcobigloser865Pas encore d'évaluation
- Contrôle 16 (PR Hammou Mouna)Document4 pagesContrôle 16 (PR Hammou Mouna)Mohamed ElouakilPas encore d'évaluation
- TelechargezDocument25 pagesTelechargezOussema SKPas encore d'évaluation
- Travaux DirigésDocument9 pagesTravaux Dirigéssad girlPas encore d'évaluation
- SEQ 5 - Stabilité Des Entités ChimiquesDocument4 pagesSEQ 5 - Stabilité Des Entités ChimiquesSpectre UnPas encore d'évaluation
- Epreuve U32 Elements de Correction Bts Fed 2023Document2 pagesEpreuve U32 Elements de Correction Bts Fed 2023Je suis Je suisPas encore d'évaluation
- C7A2 Activité Corrigé 2023Document12 pagesC7A2 Activité Corrigé 2023raphideneboudePas encore d'évaluation
- Eval CE1 - États de Leau LBDocument2 pagesEval CE1 - États de Leau LBlariechoupoPas encore d'évaluation
- COURS 2 Membrane PlasmiqueDocument109 pagesCOURS 2 Membrane Plasmiqueautre.compte.02468Pas encore d'évaluation
- TP N° 1 (Détermination Des Enthalpies de Réaction)Document4 pagesTP N° 1 (Détermination Des Enthalpies de Réaction)Ahmed Ben YoussefPas encore d'évaluation
- Série D'exercices N°10 Avec Correction - Sciences Physiques - Révision - Bac Sciences Exp (2019-2020) MR Amine TouatiDocument9 pagesSérie D'exercices N°10 Avec Correction - Sciences Physiques - Révision - Bac Sciences Exp (2019-2020) MR Amine TouatihermessimedPas encore d'évaluation
- C Exercices - Chapitre 1Document8 pagesC Exercices - Chapitre 1hassanrachsmpPas encore d'évaluation
- Notion PH EXOSDocument2 pagesNotion PH EXOSAbel MalléPas encore d'évaluation
- Quantité de MatièreDocument4 pagesQuantité de MatièreMaxime SadouPas encore d'évaluation
- Chimie Générale - Zumdahl, Steven S - 1998 - Anjou (Québec) - CEC - 9782761714549 - Anna's ArchiveDocument516 pagesChimie Générale - Zumdahl, Steven S - 1998 - Anjou (Québec) - CEC - 9782761714549 - Anna's ArchiveetidyanfakiltePas encore d'évaluation
- Almg4,5Mn0,7 (Ag4,5Mc)Document5 pagesAlmg4,5Mn0,7 (Ag4,5Mc)michael.tujague14Pas encore d'évaluation
- Exercice Photochimie CorrigéDocument12 pagesExercice Photochimie CorrigéchemputicPas encore d'évaluation
- Cours de Gestion Et Traitement Des Rejets IndustrielsDocument68 pagesCours de Gestion Et Traitement Des Rejets IndustrielsPrince ndjatePas encore d'évaluation
- BOUAKRIF ZahirDocument47 pagesBOUAKRIF ZahirhakimPas encore d'évaluation
- 101f - 2023-1 - Guide A Lintention Des La Certification Aux Normes Csa w47.1 w47.2 w55.3 Et w186Document15 pages101f - 2023-1 - Guide A Lintention Des La Certification Aux Normes Csa w47.1 w47.2 w55.3 Et w186Smith FrankPas encore d'évaluation
- Corrige Examen M1 2018 2019Document6 pagesCorrige Examen M1 2018 2019aida062023Pas encore d'évaluation
- Série c4Document3 pagesSérie c4ANTOINE THIAREPas encore d'évaluation
- Cours PV - Chap3 - 2023-2024Document93 pagesCours PV - Chap3 - 2023-2024Omar AssouPas encore d'évaluation
- Chapitre 7Document59 pagesChapitre 7Imade MassaiPas encore d'évaluation
- SVI (S2) 2019-2020 Chimie II Chimie Organique Pr. Oussaid Adyl1Document80 pagesSVI (S2) 2019-2020 Chimie II Chimie Organique Pr. Oussaid Adyl1abb32214Pas encore d'évaluation
- Poids Et MasseDocument1 pagePoids Et Massebabacar mbayePas encore d'évaluation
- Devoir 1 (2h)Document5 pagesDevoir 1 (2h)guigui farmeurPas encore d'évaluation
- BrevetDocument6 pagesBrevetdadimarwane59Pas encore d'évaluation
- Devoir de Synthèse N°2 Avec Correction - Sciences Physiques - 3ème Sciences Exp (2019-2020) MR Amine TouatiDocument8 pagesDevoir de Synthèse N°2 Avec Correction - Sciences Physiques - 3ème Sciences Exp (2019-2020) MR Amine TouatiBouzid Hadj AliPas encore d'évaluation