Académique Documents
Professionnel Documents
Culture Documents
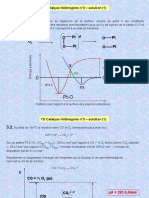
Exercices Divers Sur Le Thème Oxydoréduction
Transféré par
issaradjab13Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Exercices Divers Sur Le Thème Oxydoréduction
Transféré par
issaradjab13Droits d'auteur :
Formats disponibles
http://www.accesmad.
org
Exercices divers sur le thème de l'oxydoréduction
URL source du document
http://www.chimix.net/
exercice 1 zinc (Zn) et acide chlorhydrique(HCl)
A une masse m=2 g de zinc, on ajoute V=600 mL d'une
solution d'acide chlorhydrique telle que la concentration
soit C=0,5 mol L-1.
Zn=65,4; H=1 ;Cl=35,5 g mol-1.
volume molaire 22,4 L mol-1.
Quelles sont les quantité de matière initiale de chaque
réactif?
En déduire qui est en excès et de combien?
Quels sont les concentrations finales des ions?
Vérifier que la solution est électriquement neutre.
Quels sont la masse et le volume de dihydrogéne
formé ?
Quelle est la quantité d'électricité mise en jeu ?
corrigé
couples en présence:
H3O+ / H2
Zn2+ /Zn
ion ion
Zn métal H2
H3O+ Zn2+
Une réaction naturelle a lieu entre le réducteur le plus
Qté matière 0,5*0,6
2 / 65,4
fort Zn et l'oxydant le plus fort H3O+ mol = 0 0
=3,06 10-2
au départ 0,3
Zn + 2 H3O+ donne Zn2+ + H2+ 2H2O
à partir de
0,0306 mol
de zinc, il donc H3O+
faut 0,0612 en excès
mol H3 O+
lors de la -6,12 3,06 3,06
-3,06 10-2
réaction 10-2 10-2 10-2
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 1/12
http://www.accesmad.org
3,06 3,06
bilan 0 0,2388
10-2 10-2
concentration des ions en solution:
les ions
ion H3O+ ion Zn2+ ion Cl-
présents
concentration 0,2388/0,6=
0,0306/0,6=0,051 inchangée 0,5
mol L-1 0,398
la solution reste électriquement neutre
[H3O+] + 2[Zn2+]= [Cl-]
volume de dihydrogène:
3,06 .10-2 .22,4 = 0,685 L
Quantité d'électricité mise en jeu
Zn s'oxyde et donne Zn2+ + 2 électrons
la quantité de matière d'électrons (mol)est deux fois plus
grande que celle de zinc
2.3,06. 10-2=6,12. 10-2 mol
la charge d'une mole d'électrons est 96500 coulombs ou
1 faraday
96500.6,12 .10-2=5906 C
exercice 2 aluminium (Al) et acide sulfurique(H2SO4)
A une masse m=2 g d'aluminium, on ajoute V=50 mL
d'une solution d'acide sulfurique telle que la
concentration en ion hydronium soit C=0,4 mol L-1.
Al=27; H=1 ;S=32 ; O=16 g mol-1.
volume molaire 22,4 L mol-1.
Danger !! 0,4 mol H3O+ mais 0,2 mol SO42-
Quelles sont les quantité de matière initiale de chaque
réactif?
En déduire qui est en excès et de combien?
Quels sont les concentrations finales des ions?
Vérifier que la solution est électriquement neutre.
Quels sont la masse et le volume de dihydrogéne
formé ?
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 2/12
http://www.accesmad.org
Quelle est la quantité d'électricité mise en jeu ?
corrigé
couples en présence:
H3O+ / H2
Al3+ /Al
Al ion ion
H2
métal H3O+ Al3+
Une réaction naturelle a lieu entre le réducteur le plus 2 / 27
Qté matière mol 0,05*0,4
fort Al et l'oxydant le plus fort H3O+ =7,41 0 0
au départ =0,02
10-2
Al + 3 H3O+ donne Al3+ + 1,5H2+ 3H2O
à partir de 6,67 10-3 donc
mol de métal il faut métal
en
0,02 mol H3O+
excès
-6,67 6,67
lors de la réaction -0,02 10-2
10-3 10-3
6,74 6,67
bilan 0 10-2
10-2 10-3
concentration des ions en solution:
les ions présents ion Al3+ ion SO42-
concentration mol L-1 6,67 10-3 / 0,05=0,133 inchangée 0,2
la solution reste électriquement neutre
3[Al3+]= 2[SO42-]
volume de dihydrogène:
10-2 .22,4 =0,224 L
Quantité d'électricité mise en jeu
Al s'oxyde et donne Al3+ + 3 électrons
la quantité de matière d'électrons (mol)est trois fois plus
grande que celle d'aluminium ayant réagi
3.6,67. 10-3=2. 10-2 mol
la charge d'une mole d'électrons est 96500 coulombs ou
1 faraday
96500.2. 10-2=1930 C
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 3/12
http://www.accesmad.org
d'autre données m=1 g; V=100 mL; C= 1 mol L-1....
réponses: ion hydronium excés de 8,9. 10-2 mol;
[Al3+]=0,37 mol L-1 ; gaz 5,56 .10-2 mol ; 10700 C
mélange cuivre aluminium +ac sulfurique
exercice 3 H2SO4
A une masse m=10 g d'un mélange aluminium et cuivre
on ajoute une solution diluée d'acide sulfurique en
excès. On recueille V=3,36 L de dihydrogène .
Al=27; H=1 ;S=32 ; O=16 ; Cu=63,5 g mol -1. volume
molaire 22,4 L mol-1.
Danger !! le cuivre n'est pas attaqué par l'acide
Quelle est la quantité de matière de dihydrogéne?
Ecrire l'équation bilan
En déduire la qté de matière d'aluminium ayant réagi
En déduire la masse d'aluminium
Quelle est la composition du mélange en % massique.
corrigé
Une réaction naturelle a lieu entre le réducteur le plus couples en présence:
fort Al et l'oxydant le plus fort H3O+ le cuivre n'est pas Cu2+ / Cu
attaqué H3O+ / H2
Al + 3 H3O+ donne Al3+ + 1,5H2+ 3H2O
Al3+ /Al
Al métal H2
Qté matière mol 0,15 /1,5= 0,1 3,36 / 22,4 = 0,15
masse de métal aluminium
masse molaire fois qté de matière en mol =27.0,1 =2,7 g
je déduis la masse de cuivre : 10-2,7 =7,3 g
% massique
2,7 /10 .100= 27 % aluminium
7,3 /10 .100= 73 % cuivre
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 4/12
http://www.accesmad.org
autre données : m=20 g; V=2,016 L …
réponses: 0,09 mol H2 ; 8,1 % Al
exercice 4 mélange fer + aluminium + acide sulfurique
A une masse m=8,2 g d'un mélange aluminium et fer on
ajoute une solution diluée d'acide sulfurique en excès.
On recueille V=7,84 L de dihydrogène . On notera x la
quantité de matière de fer en mol et y celle d'aluminium.
(Al=27; H=1 ;S=32 ; O=16 ; Fe=56 g mol-1.)
volume molaire 22,4 L mol-1.
Danger !! les deux métaux sont attaqués par l'acide
Quelle est la quantité de matière de dihydrogéne?
Ecrire les équations bilan
En déduire une 1 ère relation entre x et y et la quantité de
dihydrogéne en mol.
Ecrire une autre relation entre x et y et la masse du
mélange
Quelle est la composition du mélange en % massique.
corrigé
Une réaction naturelle a lieu entre les réducteurs les plus couples en présence:
forts Al et Fe et l'oxydant le plus fort H3 O+
H3O+ / H2
Al + 3 H3O+ donne Al3+ + 1,5H2+ 3H2O
Fe2+ / Fe
Fe + 2 H3O+ donne Fe2+ + 1H2+ 2H2O Al3+ /Al
Qté de matière de dihydrogène en mol
volume du gaz divisé par le volume molaire
soit: 7,84 /22,4 =0,35 mol
Qté de dihydrogéne issue de la 1ère réaction : 1,5 y mol
Qté de dihydrogéne issue de la 2ème réaction : x mol
d'où x + 1,5 y = 0,35
masse du mélange = somme des masses de fer et
d'aluminium
masse = masse molaire fois qté de matière en mol
masse de fer :56 x
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 5/12
http://www.accesmad.org
masse d'aluminium : 27 y
d'où 56 x + 27 y = 8,2
la résolution du système de 2 équations à 2 inconnues
donne:
aluminium 5,4 g ou 0,2 mol ou 65,9 % en masse
fer 2,8 g ou 0,05 mol ou 34,1 % en masse
d'autre données m=13,7 ; V=12,32 L....…
réponses: 5,6 g fer 8,1 g Al
exercice 5 cuivre et acide nitrique HNO3
A une masse m=12,7 g de cuivre, on ajoute V=0,3 L
d'une solution d'acide nitrique (C=2 mol L-1) .
(Cu=63,5; H=1 ;N=14 ; O=16 g mol-1. )
volume molaire 22,4 L mol-1.
Quelles sont les quantité de matière initiale de chaque
réactif?
Ecrire l'équation bilan
En déduire qui est en excès et de combien?
Quels sont les concentrations finales des ions?
Vérifier que la solution est électriquement neutre.
Quels sont la masse et le volume de monoxyde d'azote
formé ?
Quelle est la quantité d'électricité mise en jeu ?
corrigé
Une réaction naturelle a lieu entre les réducteurs les plus couples en présence:
forts Cu et l'oxydant le plus fort NO3 -
NO3- / NO
2 fois{ NO3- + 4 H++ 3 électrons donne NO + 4 H2O } Cu2+ / Cu
3 fois{ Cu donne Cu2+ +2 électrons } Cu ion ion ion
NO
métal H3O+ Cu2+ NO3-
dans le bilan les électrons n'apparaissent pas
2NO3- + 8 H++ 3Cu donne 3 Cu2++2NO + 8 H2O Qté matière 12,7/
0,3*2=
0,3*2
mol 63,5= 0 = 0
0,6
au départ 0,2 0,6
à partir de donc
0,2 mol de H3O+
métal il faut
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 6/12
http://www.accesmad.org
0,533 mol en
H3O+ excès
lors de la -
-0,2 -0,533 0,2 0,133
réaction 0,133
bilan 0 0,067 0,2 0,467 0,133
concentration des ions en solution:
les ions présents ion Cu2+ ion NO3- ion H3O+
concentration mol 0,467/0,3=
0,2/0,3=0,667 0,067/0,3=0,223
L-1 1,556
la solution reste électriquement neutre
2[Cu2+] + [H3O+]=[NO3-]
volume de monoxyde d'azote:
0,133.22,4 =2,98 L
Quantité d'électricité mise en jeu
Cu s'oxyde et donne Cu2+ + 2 électrons
la quantité de matière d'électrons (mol) est deux fois
plus grande que celle de cuivre ayant réagi
2.0,2=0,4 mol
la charge d'une mole d'électrons est 96500 coulombs ou
1 faraday
96500.0,4=38600 C
d'autre données.....m=6,35 g ; V=100 mL ; C=2 mol L-1 ;
réponses:
Cu en excès de 0,025 mol ; Cu 2+ 0,75 mol L-1 ; 1,12 L
de gaz ; 0,15 mol électrons
exercice 6 composition d'un mélange de 3 métaux
On a un mélange sous forme de poudre de cuivre, de
zinc et d'aluminium. On ajoute de l'acide chlorhydrique
en excès à 10,5 g de ce mélange. Après réaction, il reste
un résidu solide de 2,4 g et le gaz qui s'est dégagé lors
de l'attaque par l'acide occupe un volume de 5,66 L.
Calculer la composition du mélange en pourcentage
massique. (Cu=63,5 ; Al=27 ; Zn=65,4 g mol-1 .)
volume molaire : 22,4 L mol-1.
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 7/12
http://www.accesmad.org
corrigé
Le cuivre n'est pas attaqué dans ces conditions: les 2,4
g résiduels correspondent à la masse de cuivre soit
2,4.100/10,5 = 22,8%
Zn + 2 H3O+ donne Zn2+ + H2 + 2H2O
Al + 3 H3O+ donne Al3+ + 1,5 H2 + 3H2O
a mol de zinc et b mol d'aluminium
masse (g) = qté de matière (mol).masse molaire (gmol-1)
masse mélange(10,5-2,4)= masse zinc + masse
aluminium
8,1 = a .65,4 + b .27 (1)
qté de matière (mol)= volume (L) / volume molaire
(L.mol-1)
5,66/22,4 =0,253 = a + 1,5 b (2)
la résolution du système de 2 équations donne
a=0,076 mol et b=0,118 mol
soit en masse: 4,97 g de zinc ou 47,2% et 3,18 g Al ou
30,8%
exercice 7 un alliage utilisé dans les fusibles
Un alliage contient du bismuth, de l'étain et du plomb. Il
fond à 95°C. Une masse m=5 g de cet alliage est traité
avec V=100 mL d'acide chlorhydrique à C=3 mol L-1. Le
résidu solide a une masse de 2,4 g et on recueille 0,372
de gaz.
On recueille 10 mL de la solution décantée dans laquelle
on ajoute un excès d'ion iodure: On obtient un précipité
jaune PbI2 de masse 0,345 g
masse atomique molaire en g mol -1 : Pb=207 ; I= 127 ;
Sn=118,7 ;
volume molaire 22,4 L mol-1
Ecrire les équations bilan
exprimer les quantités de matière initiales en mol
interpreter les équations bilan et en déduire la
composition massique de cet alliage.
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 8/12
http://www.accesmad.org
corrigé
couples en présence:
Une réaction naturelle a lieu entre les réducteurs les plus
forts Pb etSn et l'oxydant le plus fort H3O+ Bi3+ / Bi
H3O+ / H2
Pb + 2 H3O+ donne Pb2+ + H2+ 2H2O
Pb2+ /Pb
Sn + 2 H3O+ donne Sn2+ + 1H2+ 2H2O
Sn2+ /Sn
le résidu solide est du bismuth 2,4g soit 48% en masse
Pb 2++ 2 I- donne Pb I2 solide
masse molaire Pb I2: 207+2.127=461 g mol-1.
Qté de matière Pb I2: 0,345/ 461=7,48. 10-4 mol
7,48 .10-4 mol dans le dixième de la solution
j'en déduis donc 7,48.10-3mol de plomb où
7,48. 10-3.207=1,55g de plomb ..31%
à partir de 7,48.10-3 mol de plomb j'obtiens
7,48. 10-3 mol de dihydrogène
soit 7,48 .10-3.22,4 =0,1675 L
le volume de dihydrogène issu de l'attaque due l'étain
est donc :
0,372-0,1675=0,204 L
soit 0,204 / 22,4 =9,12 .10-3 mol H2.
9,12.10-3 mol H2 proviennent de l'attaque de
9,12 .10-3 mol d'étain
soit en masse 9,12 .10-3 .118,7=1,07 g ou 21,5% étain
je vérifie que la somme des pourcentages est voisine de
100%.
révisions oxydo-réduction
exercice 8
On plonge une lame de zinc dans 50 mL d'une solution
de sulfate de cuivre de concentration 0,02 mol.L-1.
Zn = 65,4 ; Cu = 63.5 ; Ag=108 g.mol-1
Qu'observe-t-on ?Ecrire l'équation bilan de la réaction .
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 9/12
http://www.accesmad.org
Quelle est la masse de zinc qui a été oxydée ?
Quelle est la masse du dépot métallique ?
De la tournure de cuivre est immergée dans 200mL
d'une solution de nitrate d'argent de concentration
5.10-3 mol.L-1 .Un dépot métallique se forme ; sa
masse est de 45mg.
Ecrire l'équation bilan de la réaction ?
La réaction est-elle totale ?Si elle ne l'est pas calculer
la concentration des ions dans la solution à la fin de
l'expérience.
vérifier que la solution est électriquement neutre.
corrigé
Zn (réducteur) ---> Zn2+ + 2e- oxydation
Cu2+ (oxydant) + 2e- ---> Cu réduction
Zn + Cu2+ --->Zn2+ + Cu oxydoréduction
à partir de (0,02.0,05= 10-3 mol) Cu2+ , 10-3 mol de
zinc est oxydé soit 65,4 mg.
10-3 mol de cuivre se dépose soit 63,5 mg.
Cu (réducteur) ---> Cu2+ + 2e- oxydation
2Ag+ (oxydant) + 2e- ---> 2Ag réduction
Cu + 2Ag+ --->Cu2+ + 2Ag oxydoréduction
à partir de (0,005.0,2= 10-3 mol) Ag+ , 10-3 mol d'argent
métal peut être réduit soit 108 mg. Donc le cuivre est
en défaut.
0,045/108= 4,16 10-4 mol d'argent se dépose
soit 2,08 10-4 mol de cuivre et d'ion Cu2+.
[Cu2+]=2,08. 10-4 /0,2= 1,04. 10-3 molL-1
[Ag+]= (10-3- 4,16 .10-4 )/0,2= 2,92. 10-3 molL-1
[NO3-]= 5.10-3 mol.L-1
[NO3-] = [Ag+] + 2 [Cu2+]
5.10-3 =2,92 .10-3 +2.1,04.10-3 vrai
fabrication Cl2 au laboratoire
exercice 9
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 10/12
http://www.accesmad.org
Un moyen commode de préparer rapidement une
petite quantité de dichlore gazeux consiste à verser
une solution concentrée d'acide chlorhydrique sur des
cristaux de permanganate de potassium KMnO4.
Mn=55; K=39; O=16 gmol-1. V=22,4 Lmol-1.
Ecrire séparément les deux demi-équations de
réduction des ions permanganate et d'oxydation des
ions chlorure.
En déduire l'équation bilan de la réaction observée.
Le manipulateur utilise 25 g de KMnO4. (solide). Quel
est le volume maximal de dichlore qu'il peut obtenir ?
Quel est le volume minimal d'une solution commerciale
à 12 molL-1 qu'il doit utiliser s'il veut employer tout le
permanganate ?
Quelle sera, dans la solution obtenue, la concentration
en ions Mn2+ ?
corrigé
2 fois { MnO4- + 8H+ +5 e- ---> Mn2+ + 4H2O }
réduction
5 fois { 2 Cl- ---> Cl2 + 2e- } oxydation
2 MnO4- + 16 H+ + 10 Cl- ---> 5Cl2 + 2Mn2+ + 8H2O
oxydo-réduction
volume maxi de Cl2
Qté de matière KMnO4. 25/(39+55+4.16)= 0,158 mol
2,5 mol de dichlore à partir d'une mole KMnO4.
2,5.0,158 = 0,395 mol Cl2 ou 0,395 .22,4 = 8,8 L
volume solution acide
8 mol d'ion H+ à partir d'une mole KMnO4.
8.0,158 = 1,27 mol d'ion H+
1,27 = volume (L)*12
V= 0,105 L
concentration [Mn2+]
1 mol d'ion Mn2+ à partir d'une mole KMnO4
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 11/12
http://www.accesmad.org
0,158 mol dans 0,105 litre
[Mn2+] = 0,158/0,105= 1,5 mol L-1
Auteur : Equipe Physique d’EDUCMAD
Date de version : 13/10/18 12/12
Vous aimerez peut-être aussi
- Chap 3 Diagrammes EpHDocument4 pagesChap 3 Diagrammes EpHcours importantPas encore d'évaluation
- Chimie en Solution @Document48 pagesChimie en Solution @Ambroise DadjaPas encore d'évaluation
- DHETCatahetero TD3 SolutionsDocument3 pagesDHETCatahetero TD3 SolutionsYves-donald MakoumbouPas encore d'évaluation
- DHETCatahetero TD3 SolutionsDocument3 pagesDHETCatahetero TD3 SolutionsYves-donald MakoumbouPas encore d'évaluation
- Potentiometrie BtsDocument31 pagesPotentiometrie BtsOmar AbdellaouiPas encore d'évaluation
- Corrigé TD2 CSDocument5 pagesCorrigé TD2 CSSimo MaroPas encore d'évaluation
- Fich PC SP 3mDocument2 pagesFich PC SP 3mNemir MimirPas encore d'évaluation
- Les Réactions D'oxydoréductionDocument30 pagesLes Réactions D'oxydoréductionMeryem MaatallahPas encore d'évaluation
- Fiche de Revision DNB PDFDocument19 pagesFiche de Revision DNB PDFMohamed MeatiPas encore d'évaluation
- 1 C/ D Ép Reuve de Chi M I E: 1 Séquence / Octobre 2006Document2 pages1 C/ D Ép Reuve de Chi M I E: 1 Séquence / Octobre 2006Steve MbosopPas encore d'évaluation
- Chimie Des Solution 1Document10 pagesChimie Des Solution 1Moussa TabbaiPas encore d'évaluation
- Nombre D'oxydation Cours N°2Document4 pagesNombre D'oxydation Cours N°2Amine NouarPas encore d'évaluation
- smc3 Descriptive Metaux Alcalino Terreux 2017 18Document14 pagessmc3 Descriptive Metaux Alcalino Terreux 2017 18assane100% (1)
- Serie 1 Electrochimie Avec CorrectionDocument14 pagesSerie 1 Electrochimie Avec Correctionimad sahliPas encore d'évaluation
- Expose - Classification QuantitatifDocument8 pagesExpose - Classification Quantitatifpaul gbedjiPas encore d'évaluation
- Les - Reactions - Oxydoreduction-1Document10 pagesLes - Reactions - Oxydoreduction-1TeriitauPas encore d'évaluation
- Les Reactions OxydoreductionDocument11 pagesLes Reactions OxydoreductionagabuskasepaPas encore d'évaluation
- 1-Applications de L'équation de Nernst 2020Document10 pages1-Applications de L'équation de Nernst 2020Ines BoudjahemPas encore d'évaluation
- Oxydant ReducteurDocument27 pagesOxydant ReducteurFaissal FariaaPas encore d'évaluation
- 5 TD React Oxydoreduction SolutionDocument3 pages5 TD React Oxydoreduction SolutionJosé Ernest RamarosandratanaPas encore d'évaluation
- Hydrometallurgie Du ZincDocument8 pagesHydrometallurgie Du Zincimane bakassi100% (1)
- Chapitre 4 Ensa 2021-22Document23 pagesChapitre 4 Ensa 2021-223freefire 3gamePas encore d'évaluation
- Chimie Des Solutions Mpsi-1Document9 pagesChimie Des Solutions Mpsi-1mounirPas encore d'évaluation
- Ts Chi 1 CorrectionexocoursDocument3 pagesTs Chi 1 CorrectionexocoursfePas encore d'évaluation
- Equilibrage Des Reactions RedoxDocument21 pagesEquilibrage Des Reactions RedoxАли ИбрагимPas encore d'évaluation
- C PB03 Saq CaDocument3 pagesC PB03 Saq CaZineb ZahimPas encore d'évaluation
- 12 ReactionsDocument26 pages12 ReactionsfayePas encore d'évaluation
- Serie 3 PDFDocument13 pagesSerie 3 PDFMoha T OmpPas encore d'évaluation
- Electrochimie - Exercices - Eleves - Correction - Rappel 2OS - 2020bDocument6 pagesElectrochimie - Exercices - Eleves - Correction - Rappel 2OS - 2020bmoh mohPas encore d'évaluation
- Chapitre VDocument14 pagesChapitre VHåmēd Bën MåkhtārįPas encore d'évaluation
- Winkler DiagrammeDocument3 pagesWinkler Diagrammedemoiselle motivationPas encore d'évaluation
- Chap 3 Diagrammes EpHDocument7 pagesChap 3 Diagrammes EpHayoub echraaPas encore d'évaluation
- Se - Rie 4 - Les Re - Actions D'oxydo-Re - DuctionsDocument2 pagesSe - Rie 4 - Les Re - Actions D'oxydo-Re - Ductionssakouvogui100% (1)
- 1année S2 Chimie II OxydoréductionDocument9 pages1année S2 Chimie II OxydoréductionDenis KaldjobPas encore d'évaluation
- Cours Oxydoréduction en Solution AqueuseDocument4 pagesCours Oxydoréduction en Solution AqueuseFleuretta FleurePas encore d'évaluation
- Janvier 1999 BG CorDocument7 pagesJanvier 1999 BG CorAshraf Ouro-adohiPas encore d'évaluation
- Correction TD Série 4-20-21Document13 pagesCorrection TD Série 4-20-21ZouikrPas encore d'évaluation
- Electrochimie - Exercices - Eleves - Correction - 2018Document12 pagesElectrochimie - Exercices - Eleves - Correction - 2018IbtiPas encore d'évaluation
- Série 2 PH (1) - 2021-07-20T143107.674Document30 pagesSérie 2 PH (1) - 2021-07-20T143107.674Abdel OihabPas encore d'évaluation
- 6 Electrochimie Exercices Eleves CorrectionDocument13 pages6 Electrochimie Exercices Eleves CorrectionNikiemaPas encore d'évaluation
- D Equilibres Oxyred PowerDocument45 pagesD Equilibres Oxyred Powermenin noorPas encore d'évaluation
- Risa 3Document42 pagesRisa 3Sa Majesté David100% (2)
- Corrigé Centrale 2010 Acide OxaliqueDocument6 pagesCorrigé Centrale 2010 Acide OxaliquePascal FrajmanPas encore d'évaluation
- Serie 3 Electrochimie Avec CorrectionDocument16 pagesSerie 3 Electrochimie Avec Correctionimad sahliPas encore d'évaluation
- Chapitre 2 Version IntégraleDocument56 pagesChapitre 2 Version Intégraledyhp2pswsrPas encore d'évaluation
- Cours5 - OxydoreductionDocument54 pagesCours5 - OxydoreductionBONNEHPas encore d'évaluation
- COURS Equilibre OxredDocument19 pagesCOURS Equilibre Oxredsembei1Pas encore d'évaluation
- Chimie Des SolutionsDocument17 pagesChimie Des SolutionsamaghchichePas encore d'évaluation
- Cours de DavidDocument5 pagesCours de DavidmboumbamboumbadavidjephetePas encore d'évaluation
- TP N° 5 - Oxydo-Réduction - PDFDocument7 pagesTP N° 5 - Oxydo-Réduction - PDFleilalargate_37809290% (1)
- Serie 1 Oxydo RedDocument6 pagesSerie 1 Oxydo Redseib72400Pas encore d'évaluation
- Oxydo ReductionDocument55 pagesOxydo ReductionMeryem MaatallahPas encore d'évaluation
- Corrige: Brevet de Technicien Superieur Traitements Des MateriauxDocument6 pagesCorrige: Brevet de Technicien Superieur Traitements Des Materiauxpedro66Pas encore d'évaluation
- Oxydoreduction Cours 01Document19 pagesOxydoreduction Cours 01Sa LimPas encore d'évaluation
- Resume AtomeDocument3 pagesResume Atomehitachi hadiPas encore d'évaluation
- Cours Ox RedDocument42 pagesCours Ox RedFRANCK ARMAND JOSIAS BONKOUNGOU WENDBENEDOPas encore d'évaluation
- 1S-T1.2Modélisation Et Suivi D'une Transformation Chimique Et Titrage ColorimétriqueDocument4 pages1S-T1.2Modélisation Et Suivi D'une Transformation Chimique Et Titrage ColorimétriqueAlejandra Lorite AbadPas encore d'évaluation
- C5-Réaction D'oxydoréductionDocument6 pagesC5-Réaction D'oxydoréductionaymane el hachimiPas encore d'évaluation
- 8 Anticoccidiens SbyDocument59 pages8 Anticoccidiens Sbyamamùra maamarPas encore d'évaluation
- Azurite - Vertus de La Pierre, Propriétés Et BienfaitsDocument11 pagesAzurite - Vertus de La Pierre, Propriétés Et Bienfaitsmarieange3584Pas encore d'évaluation
- Plantes Et CancerDocument14 pagesPlantes Et Cancer1harmonie100% (1)
- Derbietanche Etancheite v5 2018Document2 pagesDerbietanche Etancheite v5 2018Yahya KhadhraPas encore d'évaluation
- Cours TitragesDocument6 pagesCours TitragesKira BeatboxPas encore d'évaluation
- La Fabrication Des Huiles Végétales: Une Activité À RisquesDocument30 pagesLa Fabrication Des Huiles Végétales: Une Activité À RisquesBouchedda YassinePas encore d'évaluation
- TD 1Document2 pagesTD 1forio_23Pas encore d'évaluation
- Sé Rie TD N°2 LCDocument2 pagesSé Rie TD N°2 LCRazan KhPas encore d'évaluation
- Algal+ AbdoDocument19 pagesAlgal+ AbdoIMADCHEMMAMEPas encore d'évaluation
- 01 Etude GeotechniqueDocument15 pages01 Etude GeotechniqueKKDPPas encore d'évaluation
- Daftar Harga E Catalog 2023 (Obat Program Jaminan Kesehatan Tahun 2023)Document250 pagesDaftar Harga E Catalog 2023 (Obat Program Jaminan Kesehatan Tahun 2023)RikoPas encore d'évaluation
- Les Symboles de SoudageDocument41 pagesLes Symboles de SoudageAyoub El'100% (1)
- T.D Geochimie 1Document4 pagesT.D Geochimie 1Theophile IZEREPas encore d'évaluation
- Annales Exercices 1Document3 pagesAnnales Exercices 1Linda KoundziPas encore d'évaluation
- Fiche Méthode - Synthèse PeptidiqueDocument2 pagesFiche Méthode - Synthèse PeptidiqueTaleen PekerPas encore d'évaluation
- Cours de GéochimieDocument69 pagesCours de GéochimiedanielPas encore d'évaluation
- Les VolcansDocument5 pagesLes VolcansGoumidi MohamedPas encore d'évaluation
- Cours Propriétés Colligatives Des Solutions 2.0Document12 pagesCours Propriétés Colligatives Des Solutions 2.0Modo HecatePas encore d'évaluation
- PGC-Composition Du Béton FinaleDocument124 pagesPGC-Composition Du Béton FinaleMarioPas encore d'évaluation
- Davoine 1970-3Document350 pagesDavoine 1970-3massac.chPas encore d'évaluation
- Sem17 Meca Flu KDDocument18 pagesSem17 Meca Flu KDalan benjamenPas encore d'évaluation
- Mémoire Master IIDocument85 pagesMémoire Master IInadjet polyPas encore d'évaluation
- Eau de GachageDocument10 pagesEau de GachageIS AA100% (2)
- Bouchon Stérilisateur LakhovskyDocument8 pagesBouchon Stérilisateur LakhovskyfullinaPas encore d'évaluation
- Min ClassDocument36 pagesMin ClassprvalencPas encore d'évaluation
- Tta 601 BisDocument211 pagesTta 601 BisNicolas Martin100% (3)
- Détergents VFDocument35 pagesDétergents VFmohammed yassine mouhsinePas encore d'évaluation
- CH 5 Solutions Electrolytiques-1 ImpDocument155 pagesCH 5 Solutions Electrolytiques-1 ImpAbdelhakim BailalPas encore d'évaluation
- Etude Dangers Dae Vert DeshyDocument86 pagesEtude Dangers Dae Vert Deshymohammed OuardiPas encore d'évaluation
- Identification Des Difficultes DesDocument21 pagesIdentification Des Difficultes DesNour SayediPas encore d'évaluation