Académique Documents
Professionnel Documents
Culture Documents
Corrige: Brevet de Technicien Superieur Traitements Des Materiaux
Transféré par
pedro66Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Corrige: Brevet de Technicien Superieur Traitements Des Materiaux
Transféré par
pedro66Droits d'auteur :
Formats disponibles
BREVET DE TECHNICIEN SUPERIEUR
TRAITEMENTS DES MATERIAUX
SCIENCES PHYSIQUES APPLIQUEES
Sous-épreuve spécifique à chaque option
Option B : Traitements de surface
- U4.3B -
SESSION 2016
DUREE : 2 HEURES
COEFFICIENT : 2
CORRIGE
BTS TRAITEMENTS DES MATERIAUX Sciences Physiques et Chimiques Session 2016
Sous-épreuve spécifique à chaque option – U4.3 B Code : TMPC B Page 1 sur 6
Partie A - Gamme de préparation - 3,5 points
A.1. Dégraissage
A.1.1. Les bains de dégraissage peuvent être montés à la soude ou à
0,5
la potasse.
A.1.2. Réaction chimique de dégraissage.
triester + 3 (Na+ + HO- ) → glycérol + 3 (Na+ + R-COO-)
Avec triester du glycérol.
CH2-O-CO-R
CH-O-CO-R 2
1
CH2-O-CO-R
Et glycérol :
CH2-OH
CH-OH
CH2-OH
A.1.3. L’ajout de tensio-actifs permet de maximiser l’effet du
0,5
dégraissage par ultrasons.
A.2 Démétallisation
A.2.1. En milieu acide l’eau et le cuivre ont des domaines communs
donc il n’y aura pas d’action de l’acide chlorhydrique. Le cuivre et
1
les ions NO3 ayant des domaines disjoints, l’acide nitrique
1,5
permettra d’enlever la couche de cuivre sur le substrat.
A.2.2. L’acide nitrique étant corrosif et le dioxyde d’azote étant un gaz
toxique, la manipulation se fera sous hotte, le technicien étant 0,5
équipé des EPI usuels.
BTS TRAITEMENTS DES MATERIAUX Sciences Physiques et Chimiques Session 2016
Sous-épreuve spécifique à chaque option – U4.3 B Code : TMPC B Page 2 sur 6
Partie B : Etude du bain - 12 points
B.1. Etude thermodynamique
B.1.1. CuSO4, 5H2O(s) → Cu2+(aq) + SO42-(aq)+ 5H2O
0,5
Donc Cu 2 CCuSO4 ,5 H 2O
75
249,7
0,30 mol / L 0,25
0,25
Cette valeur est cohérente avec la convention de tracé
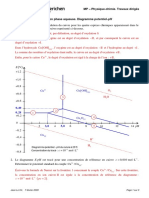
B.1.2. Domaines correctement placés (0,75) + définitions (0,75)
Immunité (Cu(s)) : La réaction de corrosion est thermodynamiquement
impossible.
0,75
Passivation (Cu2O(s) et Cu(OH)2(s)) : Le métal est oxydé en un oxyde
0,75
solide protecteur.
Corrosion (Cu2+(aq)): le métal passe à un degré d’oxydation supérieur
et des composés solubles sont formés.
B.1.3. Degrés d’oxydation.
espèce n.o.
Cu(s) 0
Cu2O(s) +I
1
2+
Cu (aq) +II (4 X 0,25)
6
Cu(OH)2(s) +II
0,25 si aucune justification
B.1.4. Pour le couple Cu 2 O(s) / Cu(s) :
Cu2O(s) 2e 2H (aq) 2Cu(s) H 2O
1
E E
0,06
2
2
log H E 0,06 log H 0,46 0,06 pH
B.1.5. Calcul du pH de début de précipitation : 1
H 3O Ke
HO
Ke
Ks
Cu
2
A.N. H3O 1,1.105 mol.L1 et pH = 5,0 0,25
0 si uniquement lecture graphique
Donc Cu(OH)2 ne précipite pas dans le bain à pH = 0.
Qr = [Cu2+].[HO-]2 = 0,30.(10-14)2 = 3,0.10-29 < 1,0.10-18,6 accepté
comme justification pour conclure. 0,25
BTS TRAITEMENTS DES MATERIAUX Sciences Physiques et Chimiques Session 2016
Sous-épreuve spécifique à chaque option – U4.3 B Code : TMPC B Page 3 sur 6
B.2. Etude cinétique
B.2.1. Montage à 3 électrodes :
G
I A
V
I I
Electrode de
référence (ESM) Contre-
électrode (Pt)
Electrode de
travail (Cu)
B.2.2. Réductions possibles : les demi-équations électroniques sont
attendues 0,5
2
SO4 H 2 O 2e SO32 2HO sulfate
0,5 les 2 6
2H 2e H 2 autres
Cu 2 2e Cu
B.2.3. Expérimentalement on observe seulement le dépôt de cuivre et
la réduction de l’eau. Réactions bien placées.
5
0
-1,6 -1,4 -1,2 -1 -0,8 -0,6 -0,4 -0,2 0
Cu Cu2+ -5
-10
j(en mA/cm2)
0,25
-15 0,25
H2 H+ -20
-25
-30
-35
E/ESM (enV)
B.2.4. Si les ions sulfate avaient été électroactifs, vu leur
concentration, on aurait observé une augmentation de la ddc 0,25
cathodique au lieu d’un palier
B.2.5. Le palier observé correspond à une limitation par la diffusion.
Augmenter le potentiel ne permet donc pas de déposer plus vite
0,5
parce que les espèces électroactives ne sont pas
réapprovisionnées au voisinage de l’électrode.
BTS TRAITEMENTS DES MATERIAUX Sciences Physiques et Chimiques Session 2016
Sous-épreuve spécifique à chaque option – U4.3 B Code : TMPC B Page 4 sur 6
B.2.6. Au pH du bain, si le système était rapide, la réduction de l’eau
démarre à E/ESH = 0,0 V donc à E/ESM = - 0,65 V. Mais il existe une
0,5
surtension sur l’électrode de cuivre d’où le démarrage à un
potentiel proche de -1 V.
B.2.7. Calcul du temps de dépôt : 1
La quantité d’électricité mise en jeu est Q I .t 2.n.F avec
mCu Cu .e.S I
n et j
M Cu M Cu S
2. Cu .e.S .F 2. Cu .e.S .F 2. Cu .e.F
D’où I .t et par suite t
M Cu M Cu .I M Cu . j
8900.150.10 6.96500.2
A.N. t 16230 s 270 min
63,5.10 3.2,5.10 2
0,25
B.2.8. On dépose 150 µm en 270 minutes soit 0,55 µm/min ce qui est
1
cohérent avec la donnée de la fiche technique
BTS TRAITEMENTS DES MATERIAUX Sciences Physiques et Chimiques Session 2016
Sous-épreuve spécifique à chaque option – U4.3 B Code : TMPC B Page 5 sur 6
Partie C - Perspective de développement : métallisation de plastiques -
4,5 points
C.1. Les trois grandes classes de polymères sont les
0,75
thermoplastiques, les thermodurcissables et les élastomères.
C.2. C’est le palladium libéré du colloïde qui servira à la catalyse. 0,5
C.3.
Calculons d’abord la concentration en Ni2+ : Ni 2
6,0
58,7
0,10 mol / L 1
Calculons ensuite la concentration en ions hypophosphite H 2 PO2 :
H 2 PO2
30
106
0,28 mol / L
Ni 2
0,35 .
D’où
H PO
2
2
0,25 4,5
Le bain est bien monté à l’optimum.
C.4.
Ni 2 2e Ni
H 2 PO2 H 2O H 2 PO3 2 H 2e 1
Ni 2 H 2 PO2 H 2O H 2 PO3 2 H Ni
C.5. Selon l’équation de réaction, il faut 3 moles d’ions
hypophosphite pour 1 mole de Ni consommée.
On doit avoir :
Ni 2 1
0,33 .
H 2 PO2
3 1
La composition du bain à l’optimum est bien en accord avec ce
rapport.
BTS TRAITEMENTS DES MATERIAUX Sciences Physiques et Chimiques Session 2016
Sous-épreuve spécifique à chaque option – U4.3 B Code : TMPC B Page 6 sur 6
Vous aimerez peut-être aussi
- 9 - Diagram E-pHDocument11 pages9 - Diagram E-pHadnanPas encore d'évaluation
- Q - Révision - ZM Oxydoreduction - EnoncéDocument4 pagesQ - Révision - ZM Oxydoreduction - EnoncéOut Of (Order)Pas encore d'évaluation
- 08 CCP TSI Ellingham E-pH Cuivre CorrigeDocument6 pages08 CCP TSI Ellingham E-pH Cuivre CorrigeMeryem Lamri ZeggarPas encore d'évaluation
- TP Chimie #09C Oxydant-Réducteur. Correction, Première SDocument12 pagesTP Chimie #09C Oxydant-Réducteur. Correction, Première SKouassi Alain KoffiPas encore d'évaluation
- 8206 E4 U43 B Bts TM 2013 Partie 2 CorrectionDocument4 pages8206 E4 U43 B Bts TM 2013 Partie 2 CorrectionYoussef AkrPas encore d'évaluation
- Corrige TPC8 PDFDocument4 pagesCorrige TPC8 PDFSaraa Papillon100% (1)
- TD29Document2 pagesTD29Anis SouissiPas encore d'évaluation
- Métallurgie Du Cobalt KziDocument48 pagesMétallurgie Du Cobalt KziLandry50% (2)
- Chap6 TD Diagrammes EpHDocument5 pagesChap6 TD Diagrammes EpHlahcen elamraouiPas encore d'évaluation
- Chap 3 TD Diagrammes EpHDocument4 pagesChap 3 TD Diagrammes EpHdimaPas encore d'évaluation
- Série Courbe Intensité PotentielDocument9 pagesSérie Courbe Intensité PotentielWael Zid100% (2)
- Correction TD Série 4-20-21Document13 pagesCorrection TD Série 4-20-21ZouikrPas encore d'évaluation
- EMD - Travail Personnel Corrosion L3 - GP - 2021 - COVID 19Document4 pagesEMD - Travail Personnel Corrosion L3 - GP - 2021 - COVID 19Meafa abd rahmanPas encore d'évaluation
- TD20Document7 pagesTD20Frejeanferd EssangaPas encore d'évaluation
- Serie 1 Electrochimie Avec CorrectionDocument14 pagesSerie 1 Electrochimie Avec Correctionimad sahliPas encore d'évaluation
- TD3 Réaction D'oxydoréduction (1) 1bac SMDocument4 pagesTD3 Réaction D'oxydoréduction (1) 1bac SMmaroua gainouPas encore d'évaluation
- TD: Exercices Avec Solution: Méthodes Instrumentales D'analyse/ ElectrochimieDocument24 pagesTD: Exercices Avec Solution: Méthodes Instrumentales D'analyse/ ElectrochimieHamza YahyaouiPas encore d'évaluation
- TP6-Conservation Element Cuivre-Correction 2Document2 pagesTP6-Conservation Element Cuivre-Correction 2Zakaria ElhammoumiPas encore d'évaluation
- TDN 5: Oxydo-Réduction Exercice 1:: Lame de Zinc Lame de Cuivre Lame D'aluminiumDocument2 pagesTDN 5: Oxydo-Réduction Exercice 1:: Lame de Zinc Lame de Cuivre Lame D'aluminiummoustafa soudani0% (2)
- Electrochimie GP Ef 2017correctionDocument4 pagesElectrochimie GP Ef 2017correctionAbdelatif100% (2)
- Diagramas de PourbaixDocument57 pagesDiagramas de PourbaixLuis MaldonadoPas encore d'évaluation
- chp4 s3 PDFDocument18 pageschp4 s3 PDFAbdelhakim Bailal50% (2)
- Sujet de Chimie: Le Sujet Est Constitué de Trois Parties Largement IndépendantesDocument7 pagesSujet de Chimie: Le Sujet Est Constitué de Trois Parties Largement Indépendanteshala shooowPas encore d'évaluation
- Risa Exercices CH IV TC 2020Document2 pagesRisa Exercices CH IV TC 2020Gnaly KpazaiPas encore d'évaluation
- Potentiometrie BtsDocument31 pagesPotentiometrie BtsOmar AbdellaouiPas encore d'évaluation
- CorrosionDocument11 pagesCorrosionMohamed Amine ChalhyPas encore d'évaluation
- Les Phenomenes Doxydoreduction - Theorie - 2020Document18 pagesLes Phenomenes Doxydoreduction - Theorie - 2020Lawrence Mundene-timotheePas encore d'évaluation
- Hydrometallurgie Du ZincDocument8 pagesHydrometallurgie Du Zincimane bakassi100% (1)
- Examen de Chimie MinéraleDocument7 pagesExamen de Chimie Minéraleranaater008Pas encore d'évaluation
- TD12 Redox 1516Document6 pagesTD12 Redox 1516Raouf RamoulPas encore d'évaluation
- Série 3 Chimie Solutions 2022-2023Document2 pagesSérie 3 Chimie Solutions 2022-2023hamzaelm802Pas encore d'évaluation
- Série N°1 2020-2021Document2 pagesSérie N°1 2020-2021Abdo AiaichePas encore d'évaluation
- 5 TD React Oxydoreduction SolutionDocument3 pages5 TD React Oxydoreduction SolutionJosé Ernest RamarosandratanaPas encore d'évaluation
- Série 3 Chimie Solutions 2022-2023Document2 pagesSérie 3 Chimie Solutions 2022-2023hamzaelm802Pas encore d'évaluation
- DS01 CDocument12 pagesDS01 CbaatoutmbPas encore d'évaluation
- MP CHIMIE CCP 1 2013.enonceDocument7 pagesMP CHIMIE CCP 1 2013.enonceMohssine ElaissaouiPas encore d'évaluation
- Cours Electrolyse ElouardeDocument6 pagesCours Electrolyse Elouarderihab100% (1)
- td3 redoxE-pHDocument6 pagestd3 redoxE-pHEl Mounchit AyoubPas encore d'évaluation
- Série TD 1 FinalDocument2 pagesSérie TD 1 FinalZakia MedadPas encore d'évaluation
- Exo Redox CompletDocument10 pagesExo Redox CompletMira insaf MekkiPas encore d'évaluation
- C PB03 Saq CaDocument3 pagesC PB03 Saq CaZineb ZahimPas encore d'évaluation
- Expose - Classification QuantitatifDocument8 pagesExpose - Classification Quantitatifpaul gbedjiPas encore d'évaluation
- Chap 10 ElectrolyseDocument4 pagesChap 10 Electrolysetoto TOTOROTOPas encore d'évaluation
- Cours Oxydoréduction en Solution AqueuseDocument4 pagesCours Oxydoréduction en Solution AqueuseFleuretta FleurePas encore d'évaluation
- Lecon2 Et 3 Competence 2 Classification Qualificative Des Couples Oxydant ReducteursDocument6 pagesLecon2 Et 3 Competence 2 Classification Qualificative Des Couples Oxydant ReducteursFrançois-jo YaoPas encore d'évaluation
- TD3 Chimie en Solution 2021Document7 pagesTD3 Chimie en Solution 2021chairimanal017Pas encore d'évaluation
- Planche 3è PCTDocument41 pagesPlanche 3è PCTdupontvania822Pas encore d'évaluation
- Chimie-1ereC D TI-Eval4Document13 pagesChimie-1ereC D TI-Eval4paulfrancoisngnintedemPas encore d'évaluation
- psi-2018-TD Reactions de Dissolution Ou de PrecipitationDocument3 pagespsi-2018-TD Reactions de Dissolution Ou de PrecipitationMetyPas encore d'évaluation
- Compte Rendu Chimie Des SolutionDocument12 pagesCompte Rendu Chimie Des Solutionmeriem.bouaouda7102100% (1)
- DS07 Moments Kepler Redox CorrigeDocument12 pagesDS07 Moments Kepler Redox Corrigedidier denisPas encore d'évaluation
- C1 Diagrammes Potentiel PH TD PDFDocument12 pagesC1 Diagrammes Potentiel PH TD PDFNourchaine MadiouniPas encore d'évaluation
- TP Corrosion OlympiadesDocument7 pagesTP Corrosion OlympiadesmariaPas encore d'évaluation
- TD25 Diagramme Potentiel-pH Du Cuivre CorrigeDocument3 pagesTD25 Diagramme Potentiel-pH Du Cuivre Corrigesarah jiji100% (2)
- DS01Document11 pagesDS01baatoutmbPas encore d'évaluation
- TD5 Chimie3 Corrigé (2014 2015)Document2 pagesTD5 Chimie3 Corrigé (2014 2015)moustafa soudaniPas encore d'évaluation
- Exos CH 12Document2 pagesExos CH 12lol testPas encore d'évaluation
- Recueil Chimie 3Document8 pagesRecueil Chimie 3Safae RezzoukPas encore d'évaluation
- Chimie Des Solutions: Bts EecDocument5 pagesChimie Des Solutions: Bts Eecpedro66Pas encore d'évaluation
- I) Réalisation Et Interprétation Qualitative D'une Réaction ÉlectrochimiqueDocument3 pagesI) Réalisation Et Interprétation Qualitative D'une Réaction Électrochimiquepedro66Pas encore d'évaluation
- Fragilisation Par Hydrogene For - b4 Lfor2Document2 pagesFragilisation Par Hydrogene For - b4 Lfor2pedro66Pas encore d'évaluation
- Tp13 Dosage Sel de Mohr Corrige 2010-2011Document3 pagesTp13 Dosage Sel de Mohr Corrige 2010-2011pedro66100% (3)
- 3 Chimie Chap2 PDFDocument8 pages3 Chimie Chap2 PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- ProgrammeDocument6 pagesProgrammepedro66Pas encore d'évaluation
- BTS ESF 1ère Année Devoir Surveillé: H O H O + H H O / H O OH H O H O / HoDocument4 pagesBTS ESF 1ère Année Devoir Surveillé: H O H O + H H O / H O OH H O H O / Hopedro66Pas encore d'évaluation
- Organisation Des Espaces de TravailDocument20 pagesOrganisation Des Espaces de Travailpedro66Pas encore d'évaluation
- DESCRIPTIF LUS PI GP2020 CopieDocument1 pageDESCRIPTIF LUS PI GP2020 Copiepedro66Pas encore d'évaluation
- Affiche LUS PI GP Aout2020 1Document1 pageAffiche LUS PI GP Aout2020 1pedro66Pas encore d'évaluation
- I) Réalisation Et Interprétation Qualitative D'une Réaction ÉlectrochimiqueDocument3 pagesI) Réalisation Et Interprétation Qualitative D'une Réaction Électrochimiquepedro66Pas encore d'évaluation
- cm6 td24Document2 pagescm6 td24pedro66Pas encore d'évaluation
- TD 34 Corrigé - Systèmes Séquentiels - GRAFCET - Structure de Base OU Et ETDocument4 pagesTD 34 Corrigé - Systèmes Séquentiels - GRAFCET - Structure de Base OU Et ETYassino Wick0% (2)
- Expériences Illustrant L'application de L'électrolyse À L'électroplastieDocument7 pagesExpériences Illustrant L'application de L'électrolyse À L'électroplastiepedro66Pas encore d'évaluation
- 2 - Propriétés Des Surfaces Industrielles: D D (A) (B)Document1 page2 - Propriétés Des Surfaces Industrielles: D D (A) (B)pedro66Pas encore d'évaluation
- C 04-02 PDFDocument8 pagesC 04-02 PDFkharrat samirPas encore d'évaluation
- 3 Chimie Chap2 PDFDocument8 pages3 Chimie Chap2 PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- 02 P Gousselot Prepa Surface AcierDocument15 pages02 P Gousselot Prepa Surface Acierpedro66Pas encore d'évaluation
- 14 - Les Traitements Par Transformation: 14.2.4 Aspects Métallurgiques Du Durcissement SuperficielDocument1 page14 - Les Traitements Par Transformation: 14.2.4 Aspects Métallurgiques Du Durcissement Superficielpedro66Pas encore d'évaluation
- Degraissage ElectrochimiqueDocument22 pagesDegraissage Electrochimiquepedro66Pas encore d'évaluation
- 6 - L'opération de DécapageDocument1 page6 - L'opération de Décapagepedro66Pas encore d'évaluation
- 5 - L'opération de DégraissageDocument1 page5 - L'opération de Dégraissagepedro66Pas encore d'évaluation
- L'Opération de DécapageDocument1 pageL'Opération de Décapagepedro66Pas encore d'évaluation
- 4 - Évaluation de La Propreté de SurfaceDocument1 page4 - Évaluation de La Propreté de Surfacepedro66Pas encore d'évaluation
- L'Opération de DégraissageDocument1 pageL'Opération de Dégraissagepedro66Pas encore d'évaluation
- 1 - Définition Et Critères Fonctionnels Des SurfacesDocument1 page1 - Définition Et Critères Fonctionnels Des Surfacespedro66Pas encore d'évaluation
- 12 - Revêtements Obtenus en Phase GazeuseDocument1 page12 - Revêtements Obtenus en Phase Gazeusepedro66Pas encore d'évaluation
- 14 - Les Traitements Par Transformation: 14.2.4 Aspects Métallurgiques Du Durcissement SuperficielDocument1 page14 - Les Traitements Par Transformation: 14.2.4 Aspects Métallurgiques Du Durcissement Superficielpedro66Pas encore d'évaluation
- 3.1 Rappel de La Définition D'une Surface IndustrielleDocument1 page3.1 Rappel de La Définition D'une Surface Industriellepedro66Pas encore d'évaluation
- 2 - Propriétés Des Surfaces Industrielles: I Fe Fe + 2Document1 page2 - Propriétés Des Surfaces Industrielles: I Fe Fe + 2pedro66Pas encore d'évaluation
- 2 Generalites ChausseeDocument126 pages2 Generalites Chausseekhalidboutahri100% (2)
- Technique Du Froid Cours de BaseDocument196 pagesTechnique Du Froid Cours de Baseيزيد عبد الحميد منصور50% (2)
- TD Eq - CHMQ L1-S2 (CPGE)Document5 pagesTD Eq - CHMQ L1-S2 (CPGE)Btn Princii IsraëlPas encore d'évaluation
- AMDECDocument33 pagesAMDECNour BouAfouraPas encore d'évaluation
- Different Cour de SoudageDocument37 pagesDifferent Cour de SoudageTRAOREPas encore d'évaluation
- BaryteDocument0 pageBarytemohamedouffaPas encore d'évaluation
- Construction Traditionnelle en Bas DauphineDocument31 pagesConstruction Traditionnelle en Bas DauphineromPas encore d'évaluation
- Nouveau Document Microsoft Office WordDocument13 pagesNouveau Document Microsoft Office WordluyfgjPas encore d'évaluation
- Transistor MOSFET A Appauvrissement Canal PDocument6 pagesTransistor MOSFET A Appauvrissement Canal PNardjes BenPas encore d'évaluation
- Cours Calcul de SoudureDocument3 pagesCours Calcul de SoudureKorichiKarimPas encore d'évaluation
- Cours GeluleDocument4 pagesCours GeluleHalima ZaghbibPas encore d'évaluation
- Colles Et AdhesifsDocument45 pagesColles Et AdhesifsSaphoSpiritPas encore d'évaluation
- Exam Ratt Forge 18 MinDocument2 pagesExam Ratt Forge 18 Minfsd vxxsPas encore d'évaluation
- Cours de Géologie PétrolièreDocument53 pagesCours de Géologie PétrolièreMick TotyPas encore d'évaluation
- Amélioration Performance EnvironnementaleDocument220 pagesAmélioration Performance EnvironnementaleMourad EzzPas encore d'évaluation
- Site 164 332650830Document68 pagesSite 164 332650830adn1234100% (1)
- 5 ch1 Cours2Document2 pages5 ch1 Cours2Houcem B HsnPas encore d'évaluation
- Controle 1 - 4 S1 3AC InterDocument3 pagesControle 1 - 4 S1 3AC InterallounimanePas encore d'évaluation
- IKEA Catalogue 2012 FR FRDocument193 pagesIKEA Catalogue 2012 FR FRDavid Da CostaPas encore d'évaluation
- 07-RA16 C3 SCTE 1 Diversite Matiere 635282Document10 pages07-RA16 C3 SCTE 1 Diversite Matiere 635282Go RikanPas encore d'évaluation
- TD FasciculeDocument35 pagesTD FasciculeRawda Kh100% (2)
- EmballageDocument12 pagesEmballageRaid YaSsinePas encore d'évaluation
- CHAP II COURBES TTT Et TRCDocument19 pagesCHAP II COURBES TTT Et TRCbenchallalhaitamPas encore d'évaluation
- Cours Partie 3 Et 4 FI GMQE - Verres Et Céramiques - S3-07-11-2022Document30 pagesCours Partie 3 Et 4 FI GMQE - Verres Et Céramiques - S3-07-11-2022Fadwa Asri100% (1)
- TP JarDocument4 pagesTP JarAY YàPas encore d'évaluation
- P4 Bordereau de Prix Lot 3 Equipement TighirtDocument13 pagesP4 Bordereau de Prix Lot 3 Equipement TighirtMustapha NajemPas encore d'évaluation
- Cours 3Document151 pagesCours 3Ahlem MansourPas encore d'évaluation
- Descriptif 02ss+rdc+1Document21 pagesDescriptif 02ss+rdc+1nanfackPas encore d'évaluation
- Tajan Design Et ArchitectureDocument180 pagesTajan Design Et ArchitectureNary Radoniaina RazafindratsifaPas encore d'évaluation
- ProjetDocument6 pagesProjetHamza AzzaariPas encore d'évaluation