Académique Documents
Professionnel Documents
Culture Documents
Sujet Physique Chimie
Transféré par
myriamdibbTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Sujet Physique Chimie
Transféré par
myriamdibbDroits d'auteur :
Formats disponibles
Bac Spécialité Physique-Chimie Asie 2022 https://labolycee.
org
EXERCICE C - DISSOLUTION D’UNE COQUILLE D’ŒUF (5 points)
Pour permettre aux enfants de découvrir les sciences, certains sites internet proposent des expériences
simples et réalisables chez soi, comme la dissolution d’une coquille d’œuf dans du vinaigre blanc.
Dans cet exercice, on se propose de vérifier le titre d’un vinaigre blanc et d’étudier l’action de ce vinaigre
sur une coquille d’œuf.
A – Vérification du degré d’un vinaigre blanc
Le vinaigre blanc est une solution aqueuse d’un acide faible appelé acide éthanoïque dont la formule
chimique est CH3COOH (aq). Le vinaigre blanc a une acidité de 8 ° en acide éthanoïque. La valeur de son
pH est d’environ 3.
Données :
➢ Couples acide / base : CH3COOH (aq) / CH3COO– (aq) ;
H2O (ℓ) / HO– (aq)
➢ pKA du couple (acide éthanoïque / ion éthanoate) : 4,8 ;
➢ Masses molaires atomiques : M(H) = 1,0 g·mol–1 ; M(C) = 12,0 g·mol–1 ;
M(O) = 16,0 g·mol–1 ; M(Ca) = 40,0 g·mol–1.
➢ Le titre ou l’acidité d’un vinaigre est donné en degré (°) : 1,00° correspond à 1,00 g d'acide
éthanoïque pur pour 100 g de vinaigre ;
➢ La valeur de la masse volumique du vinaigre est : = 1010 g·L–1.
1. Tracer le diagramme de prédominance du couple acide éthanoïque / ion éthanoate. Indiquer quelle
espèce prédomine dans la solution de vinaigre.
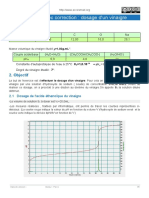
Pour vérifier le titre en degré du vinaigre, on réalise un titrage avec suivi pH-métrique d’un volume de
vinaigre Vvinaigre égal à 5,0 mL par une solution de soude (Na+ (aq) + HO– (aq)) de concentration
cb = 5,0·10–1 mol·L–1 . La valeur du volume relevé à l’équivalence est : Véq = 13,4 mL.
2. Faire un schéma annoté du montage expérimental nécessaire à la mise en œuvre du titrage.
3. Écrire la réaction support du titrage qui a lieu entre la solution de soude et le vinaigre.
4. Déterminer la concentration en mol·L–1 de l’acide éthanoïque, notée ca , présent dans ce vinaigre.
5. En détaillant le raisonnement, vérifier que le titre de ce vinaigre est bien de 8°.
Pour répondre à cette question, le candidat est invité à prendre des initiatives et à présenter la démarche
suivie, même si elle n’a pas abouti. La démarche est évaluée et nécessite d’être correctement présentée.
B – Action du vinaigre sur une coquille d’œuf
La coquille d’œuf des oiseaux est constituée en majorité (95 %) d’une substance minérale appelée
carbonate de calcium dont la formule chimique est CaCO3 (s).
Le processus est lent, mais en immergeant un œuf dans du vinaigre, on voit apparaître de petites bulles
de gaz qui se forment à la surface de la coquille qui se dissout.
Données :
➢ Principales bandes d’absorption IR :
O–H alcool : 3200 à 3400 cm–1 (bande forte et large)
O–H acide carboxylique : 2600 à 3100 cm–1 (bande forte et très large)
C=O : 1700 à 1760 cm–1 (bande forte et fine)
➢ Couples acide / base : CO2 (g),H2O (ℓ) / HCO3– (aq) ; HCO3– (aq) / CO32– (aq)
6. Représenter le schéma de Lewis de l’acide éthanoïque CH3COOH.
7. À l’aide des principales bandes d’absorption données, identifier le spectre infrarouge correspondant
à l’acide éthanoïque parmi ceux proposés dans la figure 1 ci-dessous.
Spectre IR 1 :
Spectre IR 2 :
Figure 1. Spectres infrarouges de deux substances
Source : https://webbook.nist.gov/
En solution aqueuse, le carbonate de calcium CaCO3 (s) se dissout, selon l’équation :
CaCO3 (s) → Ca2+ (aq) + CO32– (aq)
8. L’ion carbonate CO32– (aq) réagit avec l’acide éthanoïque introduit en large excès. Écrire l’équation
de la réaction acido-basique qui se produit entre ces deux espèces chimiques.
9. L’ion hydrogénocarbonate HCO3– (aq) ainsi formé réagit avec l’acide éthanoïque. Écrire l’équation
de la réaction acido-basique qui se produit entre ces deux espèces chimiques.
10. Montrer que l’équation de la réaction qui modélise l’action du vinaigre sur le carbonate de calcium
s’écrit :
CaCO3 (s) + 2 CH3COOH (aq) → Ca2+ (aq) + CO2 (g) + H2O (ℓ) + 2 CH3COO– (aq)
11. Indiquer, en le justifiant, le caractère acide-base de l’ion hydrogénocarbonate HCO3– (aq).
Vous aimerez peut-être aussi
- 2022 Asie J2 ExoC Sujet DissolutionCoquille 5pts PDFDocument3 pages2022 Asie J2 ExoC Sujet DissolutionCoquille 5pts PDFsara msouigPas encore d'évaluation
- 2011 Liban Exo3 Sujet AciditeVin 4ptsDocument3 pages2011 Liban Exo3 Sujet AciditeVin 4ptsgrajzgrPas encore d'évaluation
- DM Nâ°1Document8 pagesDM Nâ°1grégoire beraudPas encore d'évaluation
- Cours de VirologieDocument5 pagesCours de VirologieFrancisca AgboviPas encore d'évaluation
- Chapitre Acide BaseDocument23 pagesChapitre Acide BaseFakoro Abdul Aziz Doumbia100% (1)
- Dosages Acide ConvertiDocument6 pagesDosages Acide ConvertiAbir SoujaaPas encore d'évaluation
- Transformations Liees A Des Reactions Acide Base Exercices Non Corriges 1 1Document6 pagesTransformations Liees A Des Reactions Acide Base Exercices Non Corriges 1 1boufdili100% (2)
- Exercice Corrigé Sur DosageDocument5 pagesExercice Corrigé Sur DosageIkram MgPas encore d'évaluation
- Epreuve Chimie 1 Preparation Au CNC 2021Document7 pagesEpreuve Chimie 1 Preparation Au CNC 2021Meriem El AbzazePas encore d'évaluation
- TD2 Chimie en Solution 2021-1Document6 pagesTD2 Chimie en Solution 2021-1chairimanal017Pas encore d'évaluation
- TD4 - Réaction Acido BasiqueDocument8 pagesTD4 - Réaction Acido Basiquemelo.lasserrePas encore d'évaluation
- Acice Fort Base Forte Exercice 1Document8 pagesAcice Fort Base Forte Exercice 1Hamidou Diatta100% (1)
- Acide Base +dosage1Document2 pagesAcide Base +dosage1hamzacrypto080Pas encore d'évaluation
- Serie 5 Et 6 Solution Aqueuse Acide Fort Base ForteDocument7 pagesSerie 5 Et 6 Solution Aqueuse Acide Fort Base ForteCheujeu chaldouPas encore d'évaluation
- Le Vin Et Ses Composants Exercice 1 Obligatoire 10 Points Asie Sujet 1 2022 Specialite Physique ChimieDocument6 pagesLe Vin Et Ses Composants Exercice 1 Obligatoire 10 Points Asie Sujet 1 2022 Specialite Physique Chimienoha Abdel bassetPas encore d'évaluation
- 2018 NelleCaledo Exo1 Correction Vinaigre 4ptsDocument2 pages2018 NelleCaledo Exo1 Correction Vinaigre 4ptsElie KapouPas encore d'évaluation
- 2022 Asie J1 Exo1 Sujet BeerVin Ester Titrage 10pts - 0Document6 pages2022 Asie J1 Exo1 Sujet BeerVin Ester Titrage 10pts - 0GabrielPas encore d'évaluation
- TD Acide Faible Base Faible Constante Dacidite TS2 2023 2024Document12 pagesTD Acide Faible Base Faible Constante Dacidite TS2 2023 2024fallccheikhPas encore d'évaluation
- Série N°8Document2 pagesSérie N°8Jihad ELPas encore d'évaluation
- TD Tampon 2013 lsll-WahabDiopDocument4 pagesTD Tampon 2013 lsll-WahabDiopFy EzahanaPas encore d'évaluation
- C7 Af BF WahabDiopDocument5 pagesC7 Af BF WahabDiopGaye BachirPas encore d'évaluation
- TD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - MonobaseDocument5 pagesTD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - MonobaseLOUkmen Bel100% (1)
- 1cm3jftoi 866968Document2 pages1cm3jftoi 866968bipPas encore d'évaluation
- Chimie - Bière Brune AromatiséeDocument6 pagesChimie - Bière Brune AromatiséeAbdel ElouaerPas encore d'évaluation
- TP Dosage Ions HydrogenocarbonateDocument3 pagesTP Dosage Ions Hydrogenocarbonatefszkd2mgg9Pas encore d'évaluation
- 6 Exercices Réactions Acido-Basique 1Document1 page6 Exercices Réactions Acido-Basique 1RIDA SAMIPas encore d'évaluation
- Using Fruit Fly Larvae To Shine Further Light On Neurological Diseases - InriaDocument3 pagesUsing Fruit Fly Larvae To Shine Further Light On Neurological Diseases - Inriapietro.pendePas encore d'évaluation
- Exercice 1 (7 Points) Cinétique de La Décomposition de L'eau OxygénéeDocument8 pagesExercice 1 (7 Points) Cinétique de La Décomposition de L'eau Oxygénéeأمال بلقاسم100% (1)
- Exercice 1 (7 Points) Cinétique de La Décomposition de L'eau OxygénéeDocument8 pagesExercice 1 (7 Points) Cinétique de La Décomposition de L'eau OxygénéefatimazahraPas encore d'évaluation
- Acides Faibles Et Bases Faibles Couples Acide-Base & Constante D'AciditeDocument5 pagesAcides Faibles Et Bases Faibles Couples Acide-Base & Constante D'AciditeNjuga Sene100% (1)
- 5 Reactions Acido BasiquesDocument3 pages5 Reactions Acido BasiquesYouness SinePas encore d'évaluation
- Exercices Corriges Chimie en SolutionDocument157 pagesExercices Corriges Chimie en SolutionKhalid Zeg83% (23)
- Spe Physique Chimie 2022 1 PDFDocument18 pagesSpe Physique Chimie 2022 1 PDFabdallah kheirallahPas encore d'évaluation
- Série de TD N°2 - Équilibres Acido-BasiquesDocument2 pagesSérie de TD N°2 - Équilibres Acido-Basiqueskim namjoon100% (1)
- 2005 Polynesie Sujet Exo3 Ammoniac 4ptsDocument2 pages2005 Polynesie Sujet Exo3 Ammoniac 4ptskhamis faridPas encore d'évaluation
- TD PH COUPLE-ACIDE-BASE 2016Document13 pagesTD PH COUPLE-ACIDE-BASE 2016Oumar TraoréPas encore d'évaluation
- Exercices Sur Les Ions en SolutionDocument7 pagesExercices Sur Les Ions en Solutionmustapha zaamPas encore d'évaluation
- Serie 7 8 Acides Faibles Bases Faibles Solutions TamponsDocument10 pagesSerie 7 8 Acides Faibles Bases Faibles Solutions TamponsBrahim DahaiPas encore d'évaluation
- TD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - MonobaseDocument5 pagesTD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - Monobaseel hazbi fadilaPas encore d'évaluation
- DS2 Tspé 2020-2021-5Document5 pagesDS2 Tspé 2020-2021-5hanaemaaroufPas encore d'évaluation
- Acide Base PDFDocument2 pagesAcide Base PDFabdelkrim salemPas encore d'évaluation
- 2006 Pondichery Exo1 Sujet Acide Base 7ptsDocument4 pages2006 Pondichery Exo1 Sujet Acide Base 7ptsasakuma2006Pas encore d'évaluation
- TD Tampon 2019 LSLL WahabdiopDocument2 pagesTD Tampon 2019 LSLL WahabdiopOumou Khaïry DiopPas encore d'évaluation
- 2015 Polynesie Exo3 Sujet MedicamentDocument4 pages2015 Polynesie Exo3 Sujet Medicamentl.mayerPas encore d'évaluation
- 2023 Liban J1 Exo2 Correction Assouplissant 5ptsDocument3 pages2023 Liban J1 Exo2 Correction Assouplissant 5ptsfatimazahramadanialaoui983Pas encore d'évaluation
- Couple Acide - Base: ExercicesDocument16 pagesCouple Acide - Base: ExercicesAhamadi ElhouyounPas encore d'évaluation
- Exercices Réactions Acido-BasiquesDocument4 pagesExercices Réactions Acido-Basiquesayyoub dhbPas encore d'évaluation
- Exercice 1 (7 Points) Propriétés D'un AlcoolDocument7 pagesExercice 1 (7 Points) Propriétés D'un AlcoolKeys of H.A.Pas encore d'évaluation
- Serie 9 CHIMIE DES SOLUTIONS AQUEUSES 2Document2 pagesSerie 9 CHIMIE DES SOLUTIONS AQUEUSES 2deyinPas encore d'évaluation
- TD Acide Faible-2024-Lsll - WahabdiopDocument2 pagesTD Acide Faible-2024-Lsll - Wahabdiopxydj5wh2wb100% (1)
- TD Exercices-Corrigés PDFDocument21 pagesTD Exercices-Corrigés PDFabdelouahed.rhaouiPas encore d'évaluation
- TD CG - 01 Acides BasesDocument5 pagesTD CG - 01 Acides BasesMed BriniPas encore d'évaluation
- Chapitre VI Réaction ABDocument6 pagesChapitre VI Réaction ABSarah DiomandePas encore d'évaluation
- Tle CD PCTDocument57 pagesTle CD PCTdupontvania822Pas encore d'évaluation
- Degré Alcoolique Vin - CPF0708 PDFDocument4 pagesDegré Alcoolique Vin - CPF0708 PDFalphonse19880% (1)
- Livre Vers Le Bacc T2Document27 pagesLivre Vers Le Bacc T2Hanine Hmida50% (2)
- Détermination Du Degré Alcoolique Dun Vin DépinesDocument4 pagesDétermination Du Degré Alcoolique Dun Vin DépinesDina DalilPas encore d'évaluation
- PH Des Solutions Aqueuses 023 0Document10 pagesPH Des Solutions Aqueuses 023 0km.aouadiPas encore d'évaluation
- Équilibres en solution: Les Grands Articles d'UniversalisD'EverandÉquilibres en solution: Les Grands Articles d'UniversalisPas encore d'évaluation
- Glucides: Les Grands Articles d'UniversalisD'EverandGlucides: Les Grands Articles d'UniversalisPas encore d'évaluation
- A Smyrne PDF Explication TexteDocument3 pagesA Smyrne PDF Explication TextemyriamdibbPas encore d'évaluation
- Dali Exposé Français Sur Un TableauDocument8 pagesDali Exposé Français Sur Un TableaumyriamdibbPas encore d'évaluation
- Diaporama TiktokDocument7 pagesDiaporama TiktokmyriamdibbPas encore d'évaluation
- Philosophie Montaigne "Philosopher, C'est Apprendre À Mourir" Explication de CitationDocument1 pagePhilosophie Montaigne "Philosopher, C'est Apprendre À Mourir" Explication de CitationmyriamdibbPas encore d'évaluation
- Guide Des Protocoles Gynecologie-ObstetriqueDocument159 pagesGuide Des Protocoles Gynecologie-Obstetriquejeannette bonivhe100% (1)
- Electromag c13 SiteDocument36 pagesElectromag c13 Siteabdelilah.hassounePas encore d'évaluation
- 1 Cours Catenaire Date Inconnue FraDocument130 pages1 Cours Catenaire Date Inconnue Frasnoofsnoof100% (5)
- Accessoire Pour Distributeurs A Commande Electrique Connecteurs BobinesDocument5 pagesAccessoire Pour Distributeurs A Commande Electrique Connecteurs Bobinesfcbarca2020ifyPas encore d'évaluation
- 30ème FOIRE DE LA PRODUCTION ALGÉRIENNE - SAFEXDocument5 pages30ème FOIRE DE LA PRODUCTION ALGÉRIENNE - SAFEXnabil heddadPas encore d'évaluation
- 200 Questions Isolées en QCM-Orthopédie TraumatologieDocument222 pages200 Questions Isolées en QCM-Orthopédie TraumatologieZohra Targui67% (3)
- Le Renouveau Rural (Algérie - 2006)Document435 pagesLe Renouveau Rural (Algérie - 2006)cissmaroc100% (3)
- 8 French Werber Bernard Le Livre Du Voyage PDFDocument83 pages8 French Werber Bernard Le Livre Du Voyage PDFmariaPas encore d'évaluation
- 2020 01 15 Liste OFDocument4 pages2020 01 15 Liste OFREHAZPas encore d'évaluation
- FT 10 Dénombrement CSRDocument2 pagesFT 10 Dénombrement CSRihab hentourPas encore d'évaluation
- Livre Secourisme GénéralDocument91 pagesLivre Secourisme GénéralAmalia Dragan-SuciuPas encore d'évaluation
- Rapport Revue Processus Production Septembre 2023 (2) ADocument16 pagesRapport Revue Processus Production Septembre 2023 (2) AKOUAMEPas encore d'évaluation
- Tpe Seminaire Et ConferenceDocument19 pagesTpe Seminaire Et ConferenceErickPas encore d'évaluation
- Chap 1Document14 pagesChap 1NoussaPas encore d'évaluation
- Transmission Puissance 1ere Doc ÉlèveDocument5 pagesTransmission Puissance 1ere Doc ÉlèveMarouen Mekki100% (1)
- Sites Potentiels en Substances Utiles (Tunis°Document112 pagesSites Potentiels en Substances Utiles (Tunis°Ons Ben Abdallah Kalai100% (1)
- Environnement Et Changement Climatique Au MarocDocument90 pagesEnvironnement Et Changement Climatique Au MarocHichamLahbil100% (1)
- 2013 - Audit EnergetiqueDocument58 pages2013 - Audit EnergetiqueMouhcine HajjoujePas encore d'évaluation
- InvestissementsDocument2 pagesInvestissementsMOUSSA DIABATEPas encore d'évaluation
- ZAP05 Pages SimplesDocument68 pagesZAP05 Pages SimplesFourier MakambioPas encore d'évaluation
- Croquis Quartier Batignolles ParisDocument23 pagesCroquis Quartier Batignolles ParisBruno BROCHARDPas encore d'évaluation
- Developpement Dun Systeme de Production Du Biodiesel A Partir Dhuile UtiliseDocument59 pagesDeveloppement Dun Systeme de Production Du Biodiesel A Partir Dhuile UtiliseyveseonePas encore d'évaluation
- 6180Document827 pages6180Justyna Podlecka67% (3)
- Texte 3 - "Les Colchiques" (Apollinaire, Alcools Extrait N°1)Document2 pagesTexte 3 - "Les Colchiques" (Apollinaire, Alcools Extrait N°1)Florence MauriesPas encore d'évaluation
- Corrigé DS01 2014 PDFDocument6 pagesCorrigé DS01 2014 PDFEssaidi AliPas encore d'évaluation
- Epreuve Pratique CGM Chaudronnerie 2021Document34 pagesEpreuve Pratique CGM Chaudronnerie 2021ben ayed bouraouiPas encore d'évaluation
- Département de Génie Mécanique Option - Génie Des Matériaux Mémoire de Fin D Étude en Vue de L Obtention Du Diplôme de Master en Génie Des MatériauxDocument120 pagesDépartement de Génie Mécanique Option - Génie Des Matériaux Mémoire de Fin D Étude en Vue de L Obtention Du Diplôme de Master en Génie Des MatériauxmoummouPas encore d'évaluation
- StatiqueDocument4 pagesStatiqueMounire BenmoussaPas encore d'évaluation
- 5géologie StructuraleDocument27 pages5géologie StructuraleChakib SafarPas encore d'évaluation
- Ondes Sonores Fluides 1Document7 pagesOndes Sonores Fluides 1SaraIdrissiPas encore d'évaluation