Académique Documents
Professionnel Documents
Culture Documents
Bac C 2019
Transféré par
eveabagheTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Bac C 2019
Transféré par
eveabagheDroits d'auteur :
Formats disponibles
CORRIGE DU BAC C 2019
CHIMIE
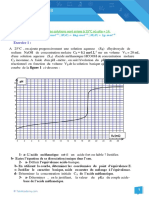
Au cours d’une séance de travaux pratiques (T.P), un élève, d’une classe de ITEMS Pondération
terminale scientifique, se propose de préparer une solution tampon à partir d’une
solution d’acide carboxylique AH de volume 𝑉 = 500 𝑚𝐿. ENONCE 1 (36 points)
1. Il réalise , à cet effet, un dosage pH-métrique d’un volume 𝑉𝑎 = 10 𝑚𝐿 de la 1.1. L’équivalence acido-basique est l’état pour lequel les réactifs 4 pts
solution d’acide carboxylique AH de concentration molaire inconnue 𝐶𝑎 avec sont mélangés dans les proportions stœchiométriques ou
une solution d’hydroxyde de sodium (soude) de concentration molaire 𝐶𝑏 = atteinte lorsque la quantité de matière de l’acide est égale à
1,0 × 10−1 𝑚𝑜𝑙. 𝐿−1 . Les résultats obtenus lui ont permis de tracer la courbe la quantité de base apportée.
𝑝𝐻 = 𝑓(𝑉𝑏 ) en annexe. 1.2. 𝐴𝐻 + 𝑂𝐻 − ⟶ 𝐴− + 𝐻2 𝑂 4 pts
1.1. Définir l’équivalence acido-basique. 𝐶𝑏 𝑉𝑏𝐸
4pts
A L’équivalence on a : 𝐶𝑎 𝑉𝑎 = 𝐶𝑏 𝑉𝑏𝐸 ⟹ 𝐶𝑎 = (a)
𝑉𝑎
1.2. Ecrire l’équation-bilan simplifiée de la réaction de dosage. (a)2pt
E(𝑉𝑏𝐸 = 10 𝑚𝐿; 𝑝𝐻𝐸 = 8,3). (voir graphe) (b)
1.3. Déterminer la concentration 𝐶𝑎 de cette solution d’acide. 1,0×10−1 ×10 (b)1pt
A.N : Ca = 10 (c) 1pt
1.3. Ca = 1,0 × 10−1 𝑚𝑜𝑙. 𝐿−1 (c)
2. La masse 𝑚 d’acide carboxylique dissoute dans les 500 𝑚𝐿 a pour valeur 𝑚 =
6,1 𝑔.
2.1. 𝑅 − 𝐶𝑂𝑂𝐻 R étant un radical alkyle ou aryle 4pts
2.1. Donner la formule générale d’un acide carboxylique.
NB : tolérer si le candidat ne précise pas la nature du radical
2.2. Ecrire l’équation de la réaction de cet acide avec l’eau en tenant compte de
2 𝑅 − 𝐶𝑂𝑂𝐻 + 𝐻2 𝑂 ⇄ 𝑅 − 𝐶𝑂𝑂− + 𝐻3 𝑂+ 4pts
la formule générale.
2.3. Déterminer la formule semi-développée 𝐴𝐻 de l’acide sachant que sa 𝑛 𝑚
Ca=𝑉 = 𝑀𝑉 ⟹
𝑚
M= 122g.mol-1 (a)
2.3. 𝐶𝐴 𝑉
4pts
molécule possède un noyau benzénique. On prendra molaire 𝐶𝑎 = 1,0 × (a)1+1pts et
Calculons la masse molaire de 𝐶6 𝐻5 - ⟹
10−1 𝑚𝑜𝑙. 𝐿−1 . (b) 2pt
M(𝐶6 𝐻5 -)=77g.mol-1 et –COOH ⟹ M( -COOH) = 45g.mol-1
77 +45 = 122 d’où la formule semi-développée est
3. Cet élève se propose de préparer une solution tampon de 𝑝𝐻 = 4,2 et de 𝐶6 𝐻5 – COOH (b)
volume 𝑉𝑇 = 500 𝑚𝐿 à partir de la solution d’acide carboxylique 𝐴𝐻
précédente. Pour cela, il mélange 𝑛1 = 2,0 × 10−2 𝑚𝑜𝑙 d’acide AH et 𝑛2 = Toute autre méthode cohérente sera acceptée.
1,0 × 10−2 𝑚𝑜𝑙 de soude.
3.1. Donner les propriétés d’une solution tampon.
3.2. Montrer que le mélange réalisé par cet élève est adéquat pour préparer cette 3.1. Caractéristiques d’une solution tampon : le pH 4pts
solution tampon. ne varie pas lors d’une dilution modérée ;
varie peu lors d’une addition modérée d’acide ou de
base.
CORRIGE BAC C 2019 Page 1
3.3. Déterminer les volumes d’acide 𝑉𝐴 et de soude 𝑉𝐵 à mélanger pour obtenir 3.2. On nB =n1 = 1,0.10-2 mol 4pts
nA= n1 = 2,0.10-2 mol on constate que nB= (a)
𝑛𝐴
cette solution tampon. (a)2pts
2
Données : Masses atomiques molaires en 𝑔. 𝑚𝑜𝑙−1 : 𝑀 ( 𝐶) = 12,0 ; 𝑀(𝐻) = il s’agit d’un mélange de nB mole de base forte avec nA mole (b)2pts
𝑛𝐴
1,0 ; 𝑀(𝑂) = 16,0 d’acide faible tel que nB= 2 . Le mélange est adéquat pour
préparer cette solution tampon. (b)
3.3. 4pts
𝑛1
n1= 𝐶𝐴 𝑉𝐴 ⟹ VA = (a) (a) 1
𝐶𝐴
(b) 1
A.N : VA = 2,0.10-1 L VA= 200mL. (b)
(c) 1
Par conséquent
(d) 1
VB = 500 – VA (c) VB= 500 – 200 = 300mL (d)
CHIMIE
Lors d’une séance de travaux pratiques, les élèves d’une classe de terminale ITEMS Pondération
scientifique se proposent de préparer un savon dont ils vont déterminer la masse.
La préparation d’un savon nécessite de faire réagir un corps gras avec une base forte. ENONCE 2 (36 points)
Dans le laboratoire, les élèves disposent de l’acide palmitique de formule
1.1. Ion hydraté est un ion entouré des molécules d’eau. 4pts
𝐶15 𝐻31 𝐶𝑂𝑂𝐻 et du glycérol. −
1. Les élèves cherchent à comprendre, dans un premier temps, comment le savon 1.2. Partie hydrophile −𝐶𝑂𝑂 ; Partie lipophile : 𝐶15 𝐻31 − 2x2pts
arrive à extraire une tache d’huile d’un linge trempé dans l’eau savonneuse. La 1.3. Le savon par sa partie lipophile attrape la tâche d’huile du
recherche documentaire leur fournit comme information : « Un savon permet linge et par sa partie hydrophile est hydratée de telle sorte 4pts
« la dissolution » dans l’eau des espèces organiques normalement insolubles. que la tâche d’huile se détache du linge.
L’ion carboxylate d’un savon possède une partie hydrophile et une partie
lipophile. Un composé hydrophile a des affinités avec des molécules polaires 2.1. Propan-1,2,3-triol 4pts
comme l’eu. Un composé lipophile a des affinités avec les graisses. »
1.1. Définir un ion hydraté. 2.2. 4pts
1.2. Indiquer les parties hydrophile et lipophile de l’ion carboxylate.
1.3. Expliquer à partir du texte, le mode d’action d’un savon sur une tache
d’huile.
2. Les élèves se proposent de synthétiser le corps gras en faisant réagir du glycérol
en excès et une masse 𝑚 = 200 𝑔 d’acide palmitique.
2.1. Donner en nomenclature officielle, le nom du glycérol. 2.3. 2x2pts
2.2. Ecrire l’équation bilan de la réaction qui se produit. 3A + B 3C + D
2.3. Déterminer la masse 𝑚1 du corps gras obtenue sachant que le rendement 3mol 1mol 3xr mol 1xr mol
𝑛𝐴 𝑛 𝑚 𝑚1
= 𝐷 ⟹ = ⟹ 𝒓𝒙 𝒎𝒙 𝑴𝟏
de la réaction est 𝑟 = 70%. 3 𝑟 3𝑀 𝑟𝑀1 m1 =
AN : m1 = 147g 𝟑𝑴
CORRIGE BAC C 2019 Page 2
3. Les élèves font réagir, ensuite une masse 𝑚’ = 100 𝑔 du corps gras obtenu
avec une solution d’hydroxyde de sodium (soude) concentrée et en excès.
3.1. Nommer cette réaction. 3.1. Saponification 4pts
3.2. Ecrire l’équation-bilan de la réaction qui se produit sachant que le corps
gras a pour formule semi-développée : 3.2. 4pts
3.3. Déterminer la masse 𝑚2 de savon obtenue.
3.3. 4pts
Données : Masses molaires en 𝑔. 𝑚𝑜𝑙−1 : 𝑀 ( 𝐶) = 12,0 ; 𝑀(𝐻) 1,0 ; 𝑀(𝑂) = 3A + B 3C + D
𝑛 𝑚2 𝑚′
16,0 ; 𝑀(𝑐𝑜𝑟𝑝𝑠 𝑔𝑟𝑎𝑠) = 806 nA= 3𝐶 ⟹ = m2 = 3m’
𝑴𝟐
3𝑀 2 𝑀 𝑴
(absence de la masse molaire du sodium)
PHYSIQUE
Les satellites artificiels existent depuis, seulement ,une cinquantaine d’années. Le ITEMS Pondération
premier, SPOUTNIK 1, a été lancé le 4 octobre 1957.
Les satellites sont devenus nécessaires dans de nombreux domaines comme la ENONCE 3 (36 points)
science, la défense, les télécommunications, la prévision du temps.
1.1. Dans un référentiel Galiléen, la somme vectorielle des forces 4pts
Pour placer un satellite sur une orbite, on le met, d’abord sur l’orbite intermédiaire appliquées à un solide est égale au produit de sa masse par le
1 à une altitude ℎ1 au dessus du sol. Le satellite utilise, alors ses moteurs pour se vecteur accélération de son centre d’inertie
placer sur l’orbite 2 considéré comme orbite définitive. On se propose de 1.2. TCI : 𝐹⃗ = m𝑎⃗ 4pts
déterminer l’énergie fournie par les moteurs du satellite pour le faire passer de Dans la base de Frenet on a :
𝑣2
l’orbite 1 vers l’orbite 2. 𝐹⃗ = F 𝑛⃗⃗ ⟹ a=an =
A 𝑟
1 Suivant ԏ
𝑑𝑣
⃗⃗ m𝑑𝑡 =0 soit
𝑑𝑣
=0 et v =cste le mouvement est
𝑑𝑡
uniforme.
Sur 𝑛⃗⃗ on a :
1. Le satellite se trouve en un point de l’orbite 1. Terr
Terre 𝑣2 𝑣2
1.3. F = m𝑟 = m𝑅
1.1. Enoncer le théorème du centre d’inertie. P 𝑇 + ℎ1 𝐺𝑥 𝑀𝑇 2x2pts
v1 = √𝑅
1.2. Montrer que le mouvement circulaire du satellite est uniforme. 𝑇 + ℎ1
1.3. Déterminer la valeur de la vitesse 𝑉1 du satellite sur l’orbite 1. V1 = 7,6.103 m.s-1
CORRIGE BAC C 2019 Page 3
2. Pour faire passer le satellite de l’orbite 1 à l’orbite 2, les moteurs du satellite, lui 2.1. Autour d’un axe, les carrés de la période de révolution du 4pts
communiquent, au point P, une vitesse. Le satellite décrit, alors, l’orbite de transfert (en satellite en orbite circulaire sont proportionnels aux cubes
pointillée) dite orbite de Hohmann. des rayons des orbites.
2.1. Enoncer la troisième loi de Kepler. 2.2. 2x2pts
2.2. Montrer que la distance AP qui représente la longueur du grand axe de l’ellipse AP= 𝟐𝑹𝑻 + h1 + h2
vaut 49300 𝑘𝑚. A.N
2.3. Déterminer le temps t que met le satellite pour partir du point P au point A. AP= 2x6,4.103 + 500 +36000
3. Arrivé au point A de l’orbite de transfert, on augmente, à nouveau, la vitesse du satellite AP= 49300 Km
pour qu’il soit en orbite à l’altitude ℎ2 . 2.3. 𝑇2
=
4𝜋2
T=√
4𝜋2 𝑟3
or t=
𝑇
donc
2x2pts
3.1. Définir l’énergie mécanique d’un système mécanique. 𝑟3 𝐺𝑀𝑇 𝐺𝑀𝑇 2
3.2. Montrer que l’énergie mécanique du satellite à une altitude h est donnée
𝐺𝑚𝑀𝑇 1 4𝜋2 𝐴𝑃 3
par la relation : 𝐸 = − t= √ ⟹ t= √
𝟏 𝑨𝑷𝟑
2(𝑅𝑇 +ℎ) 2 8𝐺𝑀𝑇 𝟐 𝟖𝑮𝑴𝑻
On considérera que l’énergie potentielle de pesanteur est donnée par l’expression : AN : t= 1,9.104 s
𝐸𝑃 = −𝑚𝑔(𝑅𝑇 + ℎ)
3.3. Déterminer l’énergie 𝜺 fournie, par les moteurs du satellite, pour l’amener de 3.1. La somme de l’énergie cinétique et de l’énergie potentielle 4 pts
l’orbite 1 à l’orbite 2. du système mécanique. Ou 𝐸𝑚 = 𝐸𝐶 + 𝐸𝑝 avec
𝐸𝑚 : 𝑒𝑛𝑒𝑟𝑔𝑖𝑒𝑚𝑒𝑐𝑎𝑛𝑖𝑞𝑢𝑒, 𝐸𝐶 : 𝑒𝑛𝑒𝑟𝑔𝑖𝑒 𝑐𝑖𝑛𝑒𝑡𝑖𝑞𝑢𝑒; 𝐸𝑝 : 𝑒𝑛𝑒𝑟𝑔𝑖𝑒 𝑝𝑜𝑡𝑒𝑛𝑡𝑖𝑒𝑙𝑙𝑒
Données : masse de la terre 𝑀𝑇 = 6,0. 1024 𝑘𝑔 ; rayon de la terre 𝑅𝑇 = 6,4. 103 𝑘𝑚 ; 3.2. 1 1 𝑚𝐺𝑀𝑇
𝐸 = 𝑚𝑣 2 − 𝑚𝑔(𝑅𝑇 + ℎ) = − 𝑚𝑔(𝑅𝑇 + ℎ)
constante gravitationnelle 𝐺 = 6,67. 10 −11
𝑆𝐼 ; masse du satellite 𝑚 = 1500 𝑘𝑔 ; ℎ1 = 2
𝐺𝑀𝑇 1 𝑚𝐺𝑀𝑇
2 (𝑅𝑇 + ℎ)
𝑚𝐺𝑀𝑇 1 𝑚𝐺𝑀𝑇
4pts
Or 𝑔 = (𝑅 +ℎ) 2 ⇒ 𝐸 = 2 (𝑅 +ℎ) − (𝑅 +ℎ) ⇒ 𝐸 = − 2 (𝑅 +ℎ)
500 𝑘𝑚; ℎ2 = 36000 𝑘𝑚 ; le grand axe (AP) de l’ellipse passe par le centre de la terre. 𝑇 𝑇 𝑇 𝑇
3.3. 𝑚𝐺𝑀𝑇 1 1 4pts
𝜀 = 𝐸2 − 𝐸1 = − ( − )
2 𝑅𝑇 + ℎ2 (𝑅𝑇 + ℎ1 2+2
𝑚𝐺𝑀𝑇 1 1
𝜀= ( − )
2 𝑅𝑇 + ℎ1 (𝑅𝑇 + ℎ2
𝜀=3,6. 1010 𝐽
PHYSIQUE
La protonthérapie est une technique médicale utilisée pour le traitement des cellules ITEMS Pondération
cancéreuses. Les protons sont accélérés dans un cyclotron, qui est un accélérateur
de particules, puis, dirigés sur les cellules cancéreuses. ENONCE 4 (36 points)
On se propose de déterminer le nombre de tours 𝑛 necessaires que doivent 4pts
1.1. 𝐹 𝑚 = e𝑣
⃗⃗⃗⃗⃗ ⃗⃗
⃗ⴷ𝐵
effectuer les protons dans le cyclotron pourqu’ils acquièrent l’énergie nécessaire afin
de détruire les cellules cancéreuses. 1.2. P( 𝐹 𝑚 ) = 𝐹𝑚 . 𝑣
⃗⃗⃗⃗⃗ ⃗⃗⃗⃗⃗ ⃗ or 𝐹 𝑚 = e𝑣
⃗⃗⃗⃗⃗ ⃗⃗
⃗ⴷ𝐵 4pts
Un cyclotron est constitué de deux demi-cylindres métalliques creux appelés P( 𝐹 𝑚 ) =e(𝑣
⃗⃗⃗⃗⃗ ⃗ⴷ𝐵⃗⃗).𝑣⃗= 0
Si P( 𝐹 ⃗⃗⃗⃗⃗
𝑚 )=0 alors ∆𝐸𝐶 = 0 ⇒ v= cste le movement est
« dees » (figure ci-dessous) placés, horizontalement, dans un champ magnétique
uniforme
CORRIGE BAC C 2019 Page 4
𝑒 𝑒𝑣0 𝐵
𝑚 = e𝑣
uniforme 𝐵 ⃗⃗, perpendiculaire au plan de la figure. On négligera le poids des protons ⃗⃗⃗⃗⃗
𝐹 ⃗⃗ = m𝑎⃗ ⇒ 𝑎⃗ =
⃗ⴷ𝐵 ⃗⃗ ⇒ a=
𝑣⃗ⴷ𝐵 𝑡⃗ⴷ𝑘⃗⃗
𝑚 𝑚
devant les autres forces. 𝑒𝑣0 𝐵 𝑣02 2x2pts
𝑎⃗ = 𝑚
𝑛⃗⃗ or 𝑎⃗ = 𝑅
𝑛⃗⃗
𝑣02 𝑒𝑣0 𝐵
= ⇒ R=
𝒆𝒗𝟎
A.N: R=5,2cm
1.3. 𝑅 𝑚 𝒎𝑩
2.1. La période est la durée au bout de laquelle le proton fait un 4pts
tour complet.(ou toute définition)
1. Des protons pénètrent dans le dee (D1) avec une vitesse initiale 𝑣0 . 2.2. Le proton est accéléré, il est soumis à la force 4pts
électrostatique vers le bas. Or 𝐹⃗⃗⃗⃗𝑒 = e 𝐸⃗⃗ ⇒ 𝐸⃗⃗ est dirigé vers
1.1. Donner l’expression vectorielle de la force magnétique ⃗⃗⃗⃗⃗
𝐹𝑚 qui s’exerce sur
le bas.(toute autre démarche cohérente)
les protons à l’intérieur du dee (D1).
2.3. 2x2 pts
1 2𝜋𝑅 2𝜋𝑚
f= or T= = donc 𝒆𝒃
1.2. Montrer, en utilisant la puissance de la force magnétique, que le 𝑇 𝑉 𝑒𝐵 f=
7
f= 3,05.10 Hz 𝟐𝝅𝒎
mouvement des protons est uniforme.
3.1. L’énergie cinétique d’un mobile est l’énergie qu’il possède 4pts
1.3. Déterminer le rayon R de la trajectoire des protons dans le dee (D 1). 1
du fait de sa vitesse. ( ou Ec = 2 m𝑣 2 en précisant les
2. Entre les deux demi-cylindres, les protons sont soumis à une tension électrique
grandeurs)
u(t) alternative de fréquence 𝑓, qui crée un champ électrique 𝐸⃗⃗ de sorte qu’à
3.2. 1 2x2pts
chaque passage dans cette région, les protons soient accélérés. On négligera ma E0 = = 2 m𝑣02
durée du trajet dans cette région.
2.1. Définir une période. E0 = 8,4.10-14 J
2.2. Donner, en justifiant, l’orientation du champ électrique 𝐸⃗⃗ lorsque le proton 3.3. 2x2pts
passe du dee (D1) au dee (D2). 𝐸−𝐸0
𝑛= avec 𝛿𝐸, énergie gagnée par tour et 𝛿𝐸 = 2∆𝐸𝐶
𝛿𝐸
2.3. Déterminer la fréquence 𝑓 de cette tension électrique. avec ∆𝐸𝐶 = 𝑒𝑈 ⇒ 𝑛 =
𝐸−𝐸0
2𝑒𝑈
3. Les protons sont accélérés pour acquérir une énergie de 150 MeV, nécessaire
pour atteindre les cellules malades. 𝑛 = 374 𝑡𝑟𝑠
3.1. Définir l’énergie cinétique d’un mobile.
3.2. Donner, en justifiant, l’énergie cinétique 𝐸0 d’un proton à l’instant où il
pénètre dans le dee (D1).
3.3. Déterminer le nombre de tours 𝑛 nécessaire pour que les protons
acquièrent l’énergie de 150 𝑀𝑒𝑉.
Données : Charge du proton 𝑞 = 1,60 × 10−19 𝐶 ; 𝑈 = 200 𝑘𝑉 ; masse du proton
𝑚 = 1,67 × 10−27 𝑘𝑔 ; 𝐵 = 2,00 𝑇 ; 1𝑒𝑉 = 1,60 × 10−19 𝐽 ; 𝑣0 = 1,0 × 107
CORRIGE BAC C 2019 Page 5
PHYSIQUE
Une masse M est soudée à un ressort fixé à l’une de ses extrémités. L’autre extrémité ITEMS Pondération
du ressort est fixée à un support horizontal (voir figure ② ci-dessous). Un groupe
d’élèves se propose de déterminer la longueur à vide 𝑙0 du ressort. ENONCE 5 (36 points)
1.1. Dans un référentiel galiléen, le centre d’inertie d’un système 4pts
isolé ou pseudo isolé est soit immobile ou soit en
mouvement rectiligne uniforme.
1.2. D’après la figure 2 4pts
T=(m +M)g
En position 1 : Mg=k (l1 + l0) (1) 2x2pts
1.3. En position 2 : (M +m) g = k( l2 – l0) (2)
(2) – (1) mg= k (l2 – l0 – l1 – l0 )
𝒎𝒈
k = 𝒍 −𝒍
𝟐 𝟏
k= 100N.m-1
2.1. Dans un référentiel Galiléen, la somme vectorielle des forces 4pts
appliquées à un solide est égale au produit de sa masse par le
vecteur accélération de son centre d’inertie.
1. Un élève accroche une masse 𝑚 = 500 𝑔 à la masse 𝑀. Le système se met,
2.2. Solution sous la forme x= xm cos (ωt +ℓ) 4pts
alors en équilibre (voire figure ②). 2𝜋
D’après la courbe, xm=5,0cm et ω0= 𝑇 = 4𝜋 ⇒ 1pt x 4
1.1. Enoncer le principe de l’inertie. 0
1.2. Exprimer la tension T du ressort en fonction de 𝑀, 𝑚 et 𝑔. ω0= 4𝜋 𝑟𝑎𝑑/𝑠
1.3. Déterminer la raideur k du ressort. A t=0, x= xm ⇒ cos𝜌 =1 et 𝜌 =0
L’équation est: X(t) = 5,0 cos (4𝜋t ) en cm ou
𝜋
2. Un autre élève décroche la masse 𝑚. Le ressort se met à osciller, sans X (t)= 5,0 sin (4𝜋t + 2 ) en cm
frottement, autour de sa première position d’équilibre. L’équation différentielle 2.3.
𝑘
𝜔02 = 𝑚 alors 2x2 pts
qui régit le mouvement est de la forme :𝑥̈ + 𝜔02 𝑥 = 0. On prendra, comme 𝒌
M = 𝝎𝟐
𝟎
origine des date, l’instant où la masse 𝑚 est décrochée et comme origine des M= 0,633kg
espaces la position du point 𝑂. 3.1. E = EC + EPP + Epc 4pts
2.1. Enoncer le théorème du centre d’inertie.
2.2. Donner en justifiant, l’expression numérique de la solution de l’équation
différentielle du mouvement. 3.2. Absence de forces de frottements entraine conservation de 4pts
2.3. Déterminer la masse 𝑀 du solide. On prendra 𝑘 = 100 𝑁. 𝑚 −1 et comme l’énergie mécanique
origine des énergies potentielles la position du point 𝑂.
3.3. A la position d’élongation maximale Ec=0 2x2pts
E= Epp + Epc
3. Le groupe d’élèves veut maintenant déterminer la longueur à vide 𝑙0 du ressort.
E = -mgxm + k( l1 – l0 +xm)2 ⇒
1
2
CORRIGE BAC C 2019 Page 6
3.1. Donner la formule de l’énergie mécanique du système. On prendra comme
origine des énergies potentielles la position du point 𝑂.
2(𝐸+𝑀𝑔𝑥𝑚)
l0 = xm +l1 - √ 𝑘
3.2. Expliquer pourquoi il y a conservation de l’énergie mécanique du système.
3.3. Déterminer la longueur à vide 𝑙0 du ressort sachant que l’énergie mécanique
du système vaut 𝐸 = 0,305 𝐽. On prendra à nouveau 𝑘 = 100 𝑁. 𝑚 −1 l0 = 0,19cm
Données : 𝑙1 = 25,0 𝑐𝑚 ; 𝑙2 = 30,0 𝑐𝑚 ; 𝑔 = 10,0 𝑚. 𝑠 −2 .
CORRIGE BAC C 2019 Page 7
Vous aimerez peut-être aussi
- CHimie Terminale S Tome 1Document49 pagesCHimie Terminale S Tome 1Anna Guéye89% (9)
- Apprendre L'hypnose Pour Une Ut - M Muzamal NaveedDocument71 pagesApprendre L'hypnose Pour Une Ut - M Muzamal NaveedAina Hery100% (4)
- ANALYSE FILMIQUE SyllabusDocument3 pagesANALYSE FILMIQUE SyllabusAgnès Prisca MIGANPas encore d'évaluation
- Équilibres en solution: Les Grands Articles d'UniversalisD'EverandÉquilibres en solution: Les Grands Articles d'UniversalisPas encore d'évaluation
- QCM RéseauDocument28 pagesQCM RéseauSamira El Margae60% (5)
- DossierGrammaireContrastive JOSÉ ROMERODocument134 pagesDossierGrammaireContrastive JOSÉ ROMEROAnibal RomeroPas encore d'évaluation
- 2022 Amsud J1 Exo1 Sujet AcideLactique 10pts - 0Document5 pages2022 Amsud J1 Exo1 Sujet AcideLactique 10pts - 0Louis VincentPas encore d'évaluation
- Bac Math Pysh Acide Base Serie 4Document1 pageBac Math Pysh Acide Base Serie 4Nourhene Jlassi33% (3)
- Série Acide Base DosageDocument5 pagesSérie Acide Base DosageBac TechniquePas encore d'évaluation
- Chap09 ExercicesDocument3 pagesChap09 ExercicesR VMPas encore d'évaluation
- 2022 Examen 2 Chimie Solutions Corrigé LDDocument7 pages2022 Examen 2 Chimie Solutions Corrigé LDLaurent KeletaonaPas encore d'évaluation
- TD Acide Faible-2024-Lsll - WahabdiopDocument4 pagesTD Acide Faible-2024-Lsll - WahabdiopAmadou Oury DialloPas encore d'évaluation
- Chapitre 3-Transformations Chimiques S'effectuée Deux SensDocument2 pagesChapitre 3-Transformations Chimiques S'effectuée Deux SensMoulham KhalidPas encore d'évaluation
- Bac Blanc (Chimie) GSFADocument3 pagesBac Blanc (Chimie) GSFAahmed amilPas encore d'évaluation
- 18 Acide-Base 1Document3 pages18 Acide-Base 1Ilyes Ben JemaaPas encore d'évaluation
- TD Acide Faible-2024-Lsll - WahabdiopDocument2 pagesTD Acide Faible-2024-Lsll - Wahabdiopxydj5wh2wb100% (1)
- Acide Base TakiDocument4 pagesAcide Base Takiaziz bensaid2Pas encore d'évaluation
- Acide BaseDocument19 pagesAcide Basehamzi0% (1)
- Série 1Document7 pagesSérie 1chadaPas encore d'évaluation
- 01-SA1 Réactions Acido-BasiquesDocument12 pages01-SA1 Réactions Acido-BasiquesberthouPas encore d'évaluation
- Force Relative Des Acides Et BasesDocument5 pagesForce Relative Des Acides Et BasesBabacar NdiayePas encore d'évaluation
- 1cm3jftoi 866968Document2 pages1cm3jftoi 866968bipPas encore d'évaluation
- PH Avec CorrectionDocument7 pagesPH Avec Correctionaminamaaloul09Pas encore d'évaluation
- No1 03 Jan 2024 Sujetexa - ComDocument2 pagesNo1 03 Jan 2024 Sujetexa - ComstonesilverteurPas encore d'évaluation
- Chimie TleCD Mini Session3 College Retraite Janvier 2022Document3 pagesChimie TleCD Mini Session3 College Retraite Janvier 2022Bodrin KuelangPas encore d'évaluation
- DST TS 2022Document26 pagesDST TS 2022dexiya94Pas encore d'évaluation
- 2023 Reunion J2 Exo2 Correction AcideButyrique 5ptsDocument2 pages2023 Reunion J2 Exo2 Correction AcideButyrique 5ptsgrajzgrPas encore d'évaluation
- TD Acide Faible Classification 2019 LSLL WahabDocument2 pagesTD Acide Faible Classification 2019 LSLL WahabOumou Khaïry DiopPas encore d'évaluation
- 2011 - Etudes de L'alcool AmyliqueDocument1 page2011 - Etudes de L'alcool AmyliqueEzéchiel HandjemedjiPas encore d'évaluation
- ACIDE BASE Equilibre D'un Systeme Janvier 2004Document3 pagesACIDE BASE Equilibre D'un Systeme Janvier 2004David BéliardPas encore d'évaluation
- C17 Resolu2Document1 pageC17 Resolu2Imene ImenePas encore d'évaluation
- TD MD ChimieDocument2 pagesTD MD ChimieMatthias KingPas encore d'évaluation
- Serie CoronaDocument15 pagesSerie CoronaJoséphine NancassePas encore d'évaluation
- NEW EVAL CHIMIE TC, D CrucialDocument3 pagesNEW EVAL CHIMIE TC, D Crucialb60032595Pas encore d'évaluation
- Bac 2Document2 pagesBac 2Marie-Luc BlaiPas encore d'évaluation
- Lycee de Bahouan........ Controle Chimie N°4 (Repet) FinalDocument2 pagesLycee de Bahouan........ Controle Chimie N°4 (Repet) FinalIlias Mounde100% (1)
- Série 5 Transformations Associées À Des Réactions Acido-Basiques en Solution AqueuseDocument6 pagesSérie 5 Transformations Associées À Des Réactions Acido-Basiques en Solution AqueuseFATIMA fatiii100% (1)
- Corrige s2 2014Document7 pagesCorrige s2 2014GueyePas encore d'évaluation
- Revision Generale Tle D N°2Document2 pagesRevision Generale Tle D N°2arsene BATAWUILAPas encore d'évaluation
- Epreuve Bac 2022 Chimie Série C D e Cameroun PDFDocument2 pagesEpreuve Bac 2022 Chimie Série C D e Cameroun PDFAmza Farel100% (2)
- 26 Dosage 3Document3 pages26 Dosage 3Ilyes Ben Jemaa0% (1)
- NarutoDocument10 pagesNarutosmkskyrozPas encore d'évaluation
- Baccalauréat Blanc Science Physique Avril 2022Document2 pagesBaccalauréat Blanc Science Physique Avril 2022pemejosuePas encore d'évaluation
- Les Transf Chimiq S'effectuant Ds Les Deux Sens - Série 2 - Soutien À Distance - Prof OTHMANEDocument11 pagesLes Transf Chimiq S'effectuant Ds Les Deux Sens - Série 2 - Soutien À Distance - Prof OTHMANEAyoub LatifPas encore d'évaluation
- Exercice Corrigé - Dosage D'un Acide Fort Avec Une Base Faible (Allure de La Courbe PH F (Va)Document5 pagesExercice Corrigé - Dosage D'un Acide Fort Avec Une Base Faible (Allure de La Courbe PH F (Va)Baye ModouPas encore d'évaluation
- Chimie Premiere CD Mars 2023Document2 pagesChimie Premiere CD Mars 2023Aubin TcheunouPas encore d'évaluation
- TR Acidobasiques PCDocument11 pagesTR Acidobasiques PCalaeddinePas encore d'évaluation
- Exos21 Acides BasesDocument4 pagesExos21 Acides BasesSohaib LaminePas encore d'évaluation
- Bac CDE Zéro Chimie 2022Document3 pagesBac CDE Zéro Chimie 2022hitmanPas encore d'évaluation
- Compo Du 2ème Trim Tle DDocument5 pagesCompo Du 2ème Trim Tle DMohamed MOUSSEPas encore d'évaluation
- Cours PCT A TIRERDocument60 pagesCours PCT A TIRERJoy TowendoPas encore d'évaluation
- DL 3: Chimie en Solution: Problème 1: Quelques Aspects Des Réactions Acidobasiques en Solution AqueusesDocument6 pagesDL 3: Chimie en Solution: Problème 1: Quelques Aspects Des Réactions Acidobasiques en Solution Aqueusesistudy43Pas encore d'évaluation
- Serie 9 CHIMIE DES SOLUTIONS AQUEUSES 2Document2 pagesSerie 9 CHIMIE DES SOLUTIONS AQUEUSES 2deyinPas encore d'évaluation
- Epreuve-CHIMIE-1ere-C, D-E-&TICOLLEGE-PRIVE-MADELEINE-EVALUATION N°1Document2 pagesEpreuve-CHIMIE-1ere-C, D-E-&TICOLLEGE-PRIVE-MADELEINE-EVALUATION N°1lemarwat3Pas encore d'évaluation
- Acides Carboxyliques - SalaneDocument2 pagesAcides Carboxyliques - SalaneSokhna penda KanePas encore d'évaluation
- Compilation Chimie Bac C, D, Ti 1998-2023Document147 pagesCompilation Chimie Bac C, D, Ti 1998-2023essarnaud1Pas encore d'évaluation
- Bac CH 2000Document2 pagesBac CH 2000Haman Bello OumarouPas encore d'évaluation
- Chimie Exemple 2 SGDocument9 pagesChimie Exemple 2 SGSerge DemirdjianPas encore d'évaluation
- Exercices C7 TSDocument2 pagesExercices C7 TSkondemamadousaidouPas encore d'évaluation
- Acides Faibles Et Bases Faibles Couples Acide-Base & Constante D'AciditeDocument5 pagesAcides Faibles Et Bases Faibles Couples Acide-Base & Constante D'AciditeNjuga Sene100% (1)
- SOLUTIONS AQUEUSES AU BAC TSE-STI-TSExpDocument6 pagesSOLUTIONS AQUEUSES AU BAC TSE-STI-TSExpModibo CoulibalyPas encore d'évaluation
- Chimie TCD N4Document2 pagesChimie TCD N4Häm's Ham'sPas encore d'évaluation
- Chimie BAC&D 2014Document3 pagesChimie BAC&D 2014enamaalexandre5Pas encore d'évaluation
- Fiche de Progression 2ème AnnéeDocument5 pagesFiche de Progression 2ème AnnéeOscard KanaPas encore d'évaluation
- But Gaco-Tc Upf BdeDocument7 pagesBut Gaco-Tc Upf BdeCompte SecoursPas encore d'évaluation
- Base de DonneesDocument6 pagesBase de Donneeshouda BaghdadiPas encore d'évaluation
- Accès Distant Aux RE - Univ CarthageDocument2 pagesAccès Distant Aux RE - Univ Carthagecshelter98Pas encore d'évaluation
- Guertin-Baril Thais 2018 Memoire PDFDocument131 pagesGuertin-Baril Thais 2018 Memoire PDFkiolioPas encore d'évaluation
- Evaluation Canada - DIALLO Mamadou FelaDocument1 pageEvaluation Canada - DIALLO Mamadou FelaFella DialloPas encore d'évaluation
- Hassaine, SlimaneDocument59 pagesHassaine, Slimanesghoul795Pas encore d'évaluation
- TPOL1 InitProteus TPSE1Document9 pagesTPOL1 InitProteus TPSE1Lukombo AfonsoPas encore d'évaluation
- Modèles de CV de Téléconseiller (Centre D'appel)Document1 pageModèles de CV de Téléconseiller (Centre D'appel)nadia kouryaniPas encore d'évaluation
- Pratiques 2220Document207 pagesPratiques 2220kmllina07Pas encore d'évaluation
- Operation Pack DivisionDocument12 pagesOperation Pack DivisionAnifaPas encore d'évaluation
- Cher Directeur Des Ressources HumaineDocument1 pageCher Directeur Des Ressources HumaineAnas RahmouniPas encore d'évaluation
- Integral de CheminDocument112 pagesIntegral de CheminLouani NadjibPas encore d'évaluation
- Ghislain Personnel 2019Document12 pagesGhislain Personnel 2019Patience OkembaPas encore d'évaluation
- 5 Projet DidactiqueDocument2 pages5 Projet DidactiqueLacramioara DeliuPas encore d'évaluation
- References BibliographiquesDocument20 pagesReferences BibliographiquesAmel HydPas encore d'évaluation
- 25anais ADMEE 2016Document232 pages25anais ADMEE 2016natvlimaPas encore d'évaluation
- Admis Def2022 Ae BandiagaraDocument39 pagesAdmis Def2022 Ae BandiagaraDaniokoPas encore d'évaluation
- 7086 s2016 Agreg Interne Sii Electrique 2Document43 pages7086 s2016 Agreg Interne Sii Electrique 2Tsito RTnPas encore d'évaluation
- Laadimi Hafsa: ProfilDocument1 pageLaadimi Hafsa: Profilhopephotographer12Pas encore d'évaluation
- Perspective ActionnelleDocument12 pagesPerspective Actionnellesunan100% (1)