Académique Documents
Professionnel Documents
Culture Documents
ds1 Corrige
Transféré par
mourad.mustaphaTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
ds1 Corrige
Transféré par
mourad.mustaphaDroits d'auteur :
Formats disponibles
Physique – Chimie DS n°1 - corrigé Classe : 1S
la
Exercice 1 : Le verre à saké
1. Schéma à l'échelle 5 signifie que 5 mm dans la réalité correspond à 5 x 5 = 25 mm sur le schéma.
L'image est réelle car elle se trouve à droite de la lentille.
2. L'image est cette fois-ci virtuelle car située à gauche de la lentille. On ne voit donc la
photographie à l'intérieur du verre, uniquement lorsque celui-ci est plein.
Exercice 2 : Où est la lentille et quelles sont ses caractéristiques ?
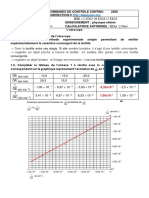
1. On trace le rayon qui relie le
sommet de l'objet au sommet
de l'image (1). Il coupe l'axe
optique en O : centre optique
de la lentille. On peut alors
placer la lentille (2)
2. On trace le rayon (3) qui passe
par le sommet de l'objet et qui
arrive parallèlement à l'axe
optique. Il passe également par
le sommet de l'image et coupe l'axe optique au point focal image : F' (4). La distance focale f' est
de 3,3 cm.
3. C = 1 / f' = 1 / (3,3 x 10-2) = 30 δ. La valeur de la vergence est de 30 dioptries.
Exercice 3 : Comparer le fonctionnement de l’œil et l'appareil photographique
1. Rôle Constituant de l'appareil
Constituant de l’œil
photographique
Fait converger les rayons sur la rétine ou le capteur cristallin objectif
Là où se forme l'image rétine Pellicule ou capteur
Empêche la lumière d'entrer paupière obturateur
Permet de régler la quantité de lumière qui entre iris diaphragme
2. Lors de la mise au point, l'objectif qui s'apparente à une lentille mince convergente de vergence
fixe, est mobile et s'approche plus ou moins de la pellicule ou du capteur.
3. Ce n'est pas le même processus mis en œuvre pour l’œil. En effet, la distance cristallin-rétine est
fixe. C'est le cristallin qui se bombe plus ou moins afin de faire varier sa vergence.
4. Lorsque le photographe rapproche son appareil de l'objet,
l'objectif s'éloigne de la pellicule. En effet, l'image se
déplace toujours dans le même sens que l'objet.
5. La forme du cristallin du photographe est plus bombée
lorsqu'il se rapproche de l'objet, car il accommode
davantage.
6. Un paysage très lointain est considéré comme à l'infini.
Donc l'objet est à l'infini, donc OA = - ∞. Donc 1/OA = 0.
1/OA' – 1/OA = 1/f' . Donc 1/OA' = 1/f' donc OA' = f '. La distance objectif-pellicule est donc égale à
la distance focale de l'objectif.
Exercice 4 : La loupe de l'enquêteur
1. L'enquêteur observe le détail d'une empreinte digitale de taille 1,0 mm placé à 10 cm de la loupe.
1 1
a) On utilise la formule de conjugaison grâce à laquelle on déterminera OA'. ̄ ' − OA
̄ =C
OA
1 1
Avec OA = - 10 cm = - 10 x 10-2 m. ̄ = +5,0=−5,0 . donc OA' = - 0,20 m.
OA ' −10 x 10−2
L'image se trouve à 20 cm à gauche de la lentille.
b) On cherche A'B'. On utilise cette fois-ci la relation de grandissement :
̄ ' A ̄' B'
OA OA ̄ −0,20×1,0 x 10−3
̄ '× AB −3
γ= ̄ = ̄ donc A ̄'B '= ̄ = =2,0 x 10 m=2 mm. La taille de
OA ' AB OA ' −10 x 10
−2
l'image vue à travers la loupe est de 2 mm.
c) OA' < 0 donc l'image est virtuelle. γ > 0 donc l'image est droite.
2. L'enquêteur voudrait que l'image fasse 1,0 cm donc A'B' = 1,0 cm.
A ̄'B' 1 cm 10−2
a) γ= ̄ = = =10 Le grandissement doit être égal à 10.
AB 1 mm 10−3
b) On recherche OA. On ne connaît que le grandissement et C. Il faut résoudre un système
d'équations à 2 inconnues :
̄ '
OA 1 1 1 1 ̄ 1−γ 1−10
γ= ̄ et ̄ − ̄ =C ̄ '=γ×OA
OA ̄ ; − =C OA= = =0,18m
OA OA ' OA ; γ×OĀ ̄
OA γ×C 10×5,0
L'enquêteur doit donc placer la loupe à 18 cm de l'indice.
Exercice 5 : « Superglue® »
1. Structure 2.a) Nombre d'électrons de 2.b) Nombre de liaisons 2.c) Nombre de
Atome
électronique valence covalentes doublets non liants
Carbone (K)2(L)4 4 4 (octet) 0
oxygène (K)2(L)6 6 2 (octet) 2
1
hydrogène (K) 1 1 (duet) 0
azote (K)2(L)5 5 3 (octet) 1
Chaque atome établit au sein d'une molécule, un nombre de liaisons covalentes qu'il lui permettra
d'être entouré soit de huit électrons (règle de l'octet) soit de deux électrons (règle du duet pour l'atome
d'hydrogène). Ce sont les règles de stabilité.
3. Pour établir la formule de Lewis, il faut vérifier que chaque atome établisse
le nombre de liaisons covalentes indiqué dans le tableau précédent et
qu'il soit entouré du nombre de doublets non liants (tableau). On peut
ensuite vérifier que chaque atome est entouré de 1 doublet pour H ou de
4 doublets pour les autres atomes.
Vous aimerez peut-être aussi
- Annales de Mathématiques, Baccalauréat C et E, Cameroun, 2008 - 2018: Sujets et CorrigésD'EverandAnnales de Mathématiques, Baccalauréat C et E, Cameroun, 2008 - 2018: Sujets et CorrigésÉvaluation : 4.5 sur 5 étoiles4.5/5 (4)
- Dev1 CorrectionDocument2 pagesDev1 CorrectionFédyHamdiPas encore d'évaluation
- ch1 ds30pt Complet DM CDocument6 pagesch1 ds30pt Complet DM CDaniel Trujillo MarinPas encore d'évaluation
- Ds1 CorrectionDocument5 pagesDs1 CorrectionFédyHamdiPas encore d'évaluation
- Série de TD N3Document2 pagesSérie de TD N3Ayoub AmazalPas encore d'évaluation
- FICHE DE TD DE PHYSIQUE PD& TI Décembre 2023Document5 pagesFICHE DE TD DE PHYSIQUE PD& TI Décembre 2023zhen ntangPas encore d'évaluation
- Colle 5 ExercicesDocument7 pagesColle 5 ExercicesAdil JaouahirPas encore d'évaluation
- Appareil Photographique PDFDocument0 pageAppareil Photographique PDFWarrior of the lightPas encore d'évaluation
- Physique 2011Document2 pagesPhysique 2011koryanahirislinePas encore d'évaluation
- Proprietes Dune Lentille CorrigeesDocument5 pagesProprietes Dune Lentille CorrigeesAndré KassoguePas encore d'évaluation
- TD N°4 - PHYSIQUES - Classe: 1 C - Mois: Janvier 2023: TD Sur Optique GeometriqueDocument10 pagesTD N°4 - PHYSIQUES - Classe: 1 C - Mois: Janvier 2023: TD Sur Optique GeometriquePauline DaissoPas encore d'évaluation
- MP18 Instruments Doptique BESSONARTDocument7 pagesMP18 Instruments Doptique BESSONARTnellynguedia7Pas encore d'évaluation
- 04 Lentilles ConvergentesDocument15 pages04 Lentilles ConvergentesEboro1997Pas encore d'évaluation
- Optique Optique Geometrique Cours TD4-Corrige AP1Document9 pagesOptique Optique Geometrique Cours TD4-Corrige AP1Kha OulaPas encore d'évaluation
- TDoptiquegeometriquev1 05Document14 pagesTDoptiquegeometriquev1 05Yannick Bakale OmaPas encore d'évaluation
- Correction Série 8 - Les Lentilles MincesDocument4 pagesCorrection Série 8 - Les Lentilles Mincessarah nabilPas encore d'évaluation
- Miroir Et Images: Travaux Dirigés D'optique N°2Document4 pagesMiroir Et Images: Travaux Dirigés D'optique N°2Faical BharPas encore d'évaluation
- 2018 Ep1 CorrectionDocument13 pages2018 Ep1 CorrectionLilia BennaceurPas encore d'évaluation
- 01 PhyspeDocument4 pages01 PhyspeHasangi Mohamed AhmedPas encore d'évaluation
- TP02 - Cours - Lentilles Minces Et Miroirs - CorrigeDocument4 pagesTP02 - Cours - Lentilles Minces Et Miroirs - Corrigehamza gamePas encore d'évaluation
- Examen OPT GEO 2019 2020Document2 pagesExamen OPT GEO 2019 2020Phú KhổngPas encore d'évaluation
- PC Gene 100 Correction Exo2 Phy Chi PhotoargentiqueDocument3 pagesPC Gene 100 Correction Exo2 Phy Chi PhotoargentiqueLiz BembenPas encore d'évaluation
- TD Modèles de Quelques Dispositifs OptiquesDocument4 pagesTD Modèles de Quelques Dispositifs OptiquesYounes JaaidaniPas encore d'évaluation
- P5 - ExercicesDocument8 pagesP5 - ExercicesazertyPas encore d'évaluation
- 2021 Asie Sujet2 ExoC Correction Lunette 5ptsDocument5 pages2021 Asie Sujet2 ExoC Correction Lunette 5ptsWilfried BonyPas encore d'évaluation
- MGT TD Lunette Terrestre - Correction - Exo 1Document1 pageMGT TD Lunette Terrestre - Correction - Exo 1ΛLT.ƧPas encore d'évaluation
- Tdo Tdo Tdo TdoDocument1 pageTdo Tdo Tdo TdoPINGO xXxMOaDPas encore d'évaluation
- TD Optique Ondulatoire PC RibiereDocument28 pagesTD Optique Ondulatoire PC RibieremPas encore d'évaluation
- 1 PC 2020 Sujet0 Correction Hypermetropie 10ptsDocument3 pages1 PC 2020 Sujet0 Correction Hypermetropie 10ptsilyessbg41Pas encore d'évaluation
- FR - GE - Op.2 - EXP3 - Geometrical Optics - ExercisesDocument12 pagesFR - GE - Op.2 - EXP3 - Geometrical Optics - ExercisesHortelio MOUBEPas encore d'évaluation
- 1TSI1 - DL12 - Instruments OptiquesDocument5 pages1TSI1 - DL12 - Instruments Optiquestaoufyk.lydex.2024Pas encore d'évaluation
- TD2e Lentilles 2017Document4 pagesTD2e Lentilles 2017Holy BiblePas encore d'évaluation
- Chapitre 7 Les Lentilles Format EcritDocument7 pagesChapitre 7 Les Lentilles Format EcritLAYNA LAYNAPas encore d'évaluation
- TP OptiqueGeometriqueL1S2Document8 pagesTP OptiqueGeometriqueL1S2Simo AchaàlPas encore d'évaluation
- ENAC-PHY 2022 Q25-30 Lunette AstroDocument2 pagesENAC-PHY 2022 Q25-30 Lunette Astroayakhalifa251Pas encore d'évaluation
- Ds Lentilles Ds Lentilles 1664528521Document2 pagesDs Lentilles Ds Lentilles 1664528521comebichardPas encore d'évaluation
- Exercices de Spécialité TSDocument126 pagesExercices de Spécialité TSghziale100% (1)
- 1eres DS1Document3 pages1eres DS1FédyHamdiPas encore d'évaluation
- Compte Rendue FocométrieDocument9 pagesCompte Rendue FocométrieMagdalenaEL33% (3)
- 1ère D - PHYSIQUE SEQ N°03 2010 - 2011Document2 pages1ère D - PHYSIQUE SEQ N°03 2010 - 2011Boris NguetaPas encore d'évaluation
- 1) Principe de La Loupe: TD7: Optique GéométriqueDocument2 pages1) Principe de La Loupe: TD7: Optique Géométriquesafia ouyPas encore d'évaluation
- Optique VisionDocument4 pagesOptique VisionenimaPas encore d'évaluation
- TD Optique PCM1 2020-2021Document1 pageTD Optique PCM1 2020-2021Siaka YodaPas encore d'évaluation
- 11-Méthode de Badal Sliberman Bessel .Document6 pages11-Méthode de Badal Sliberman Bessel .Aziz Benamor0% (1)
- Seance 5Document4 pagesSeance 5aliahmadalinePas encore d'évaluation
- Oral Phys2Document16 pagesOral Phys2Alexandre Dacosta BastosPas encore d'évaluation
- SMPC S2 Optique1 TDs - BenaissaDocument21 pagesSMPC S2 Optique1 TDs - BenaissahanhedaPas encore d'évaluation
- Physique 1ered Eval4 Lycee Bilingue Yabassi 2019 2020Document2 pagesPhysique 1ered Eval4 Lycee Bilingue Yabassi 2019 2020brice mouadjePas encore d'évaluation
- Sans TitreDocument7 pagesSans Titreqh7ps6r4b8Pas encore d'évaluation
- PC Gene 014 Correction Exo2 Phy OtoscopeDocument3 pagesPC Gene 014 Correction Exo2 Phy Otoscopemaxime dplPas encore d'évaluation
- Exercice 1 Exam Sem1 2019-20 MP1 (Teams)Document2 pagesExercice 1 Exam Sem1 2019-20 MP1 (Teams)lina hkl officialPas encore d'évaluation
- P PB06 40 CM PDFDocument7 pagesP PB06 40 CM PDFYoussef CoulibalyPas encore d'évaluation
- Optique (Ex)Document21 pagesOptique (Ex)Youssef FarjallahPas encore d'évaluation
- TP 2 La Découverte Des Lentilles MincesDocument7 pagesTP 2 La Découverte Des Lentilles MincesDalia FeddaPas encore d'évaluation
- BAC Optique Et Physico Chimie 2009 STL PhysiqueDocument6 pagesBAC Optique Et Physico Chimie 2009 STL PhysiqueLetudiant.frPas encore d'évaluation
- Photographie de Létoile Albiréo Au Télescope 20 - 221123 - 115304Document3 pagesPhotographie de Létoile Albiréo Au Télescope 20 - 221123 - 115304fan ClubPas encore d'évaluation
- Cours+exos Introduction l' ÉnergieDocument3 pagesCours+exos Introduction l' Énergiemourad.mustaphaPas encore d'évaluation
- Chimie Chapitre3 III - ApplicationDocument1 pageChimie Chapitre3 III - Applicationmourad.mustaphaPas encore d'évaluation
- La Fusion - 2021862182 - 03 11 2023Document1 pageLa Fusion - 2021862182 - 03 11 2023mourad.mustaphaPas encore d'évaluation
- Adolescence PolyhandicapDocument158 pagesAdolescence Polyhandicapmourad.mustaphaPas encore d'évaluation
- 2bex 01 Continuité Ctr3Fr AmmariDocument1 page2bex 01 Continuité Ctr3Fr AmmariAbd Elmooti HijaziPas encore d'évaluation
- Cours Trc6Document70 pagesCours Trc6Mohamed CHARIFPas encore d'évaluation
- Université Des Sciences Et Département de Chimie Techniques de Masuku Faculté Des SciencesDocument19 pagesUniversité Des Sciences Et Département de Chimie Techniques de Masuku Faculté Des SciencesRene VoumaPas encore d'évaluation
- DIAMETRES EQUIVALENCE Pouces DN Clim FroidDocument1 pageDIAMETRES EQUIVALENCE Pouces DN Clim FroidMarco BahierPas encore d'évaluation
- Tomographie ÉlectriqueDocument8 pagesTomographie ÉlectriqueJean Daniel NgohPas encore d'évaluation
- TP 4 Centrale D'acquisition Sysam-SP5Document3 pagesTP 4 Centrale D'acquisition Sysam-SP5koitaabdoulaye12.ma100% (1)
- NF En-13286-52Document10 pagesNF En-13286-52Zaineb Ben AbdallahPas encore d'évaluation
- DérivabilitéDocument4 pagesDérivabilitécoucou89Pas encore d'évaluation
- Notice - 1byone - Sonnettes TelecommandeesDocument5 pagesNotice - 1byone - Sonnettes TelecommandeesPICARDPas encore d'évaluation
- Chapitre RelevementDocument19 pagesChapitre RelevementMultiple ContentPas encore d'évaluation
- TPN-1 Réalisation Dun Pile Éléctrochimie GPDocument3 pagesTPN-1 Réalisation Dun Pile Éléctrochimie GPعبدالسلام ارفيس75% (4)
- Les Économies D'énergie Électrique en Dessalement D'eau Mer Par Osmose Inverse: Possibilités Et LimitesDocument6 pagesLes Économies D'énergie Électrique en Dessalement D'eau Mer Par Osmose Inverse: Possibilités Et LimitesHafsa MajentaPas encore d'évaluation
- Mie Tcer Psim 3Document4 pagesMie Tcer Psim 3mouaadh0% (1)
- 2023 Polynesie SI Exo2 Sujet DiffractionHematologie 10pts 30min 0Document3 pages2023 Polynesie SI Exo2 Sujet DiffractionHematologie 10pts 30min 055crtbdtdvPas encore d'évaluation
- DistributionsDocument37 pagesDistributionsDavit HarutyunyanPas encore d'évaluation
- CSTC-2009-Bétons Ultra Hautes PerformancesDocument8 pagesCSTC-2009-Bétons Ultra Hautes PerformancesJoseph KanaanPas encore d'évaluation
- REACTIONS D'addition ÉléctrophileDocument7 pagesREACTIONS D'addition Éléctrophilewarda MaPas encore d'évaluation
- Devoir Surveillé de Physique N°8: Les Calculatrices Sont InterditesDocument6 pagesDevoir Surveillé de Physique N°8: Les Calculatrices Sont InterditesSaliou SENEPas encore d'évaluation
- Brevet 2020 MathsDocument57 pagesBrevet 2020 MathsgaripipokPas encore d'évaluation
- Cours 2 MDFDocument61 pagesCours 2 MDFColombe KouamePas encore d'évaluation
- TP 05 Co-2022-2023Document3 pagesTP 05 Co-2022-2023Yazid ZitouniPas encore d'évaluation
- Lot 2Document22 pagesLot 2Vijay JamadarPas encore d'évaluation
- Fiche Technique Du Groupe Electrogene HMW 605 t5 Insonorisandeacute Franandccedil AisDocument6 pagesFiche Technique Du Groupe Electrogene HMW 605 t5 Insonorisandeacute Franandccedil AisYoughorta TirPas encore d'évaluation
- Etude Et Comparaison Entre Un Concentrateur Solaire Parabolique Et Cylindro-Parabolique.Document100 pagesEtude Et Comparaison Entre Un Concentrateur Solaire Parabolique Et Cylindro-Parabolique.Oumayma ElkanouniPas encore d'évaluation
- Série Produit Scalaire La ParitéeDocument2 pagesSérie Produit Scalaire La Paritéehamada ahmedPas encore d'évaluation
- L ' Essai de TractionDocument9 pagesL ' Essai de TractionTahar ADJOUDJPas encore d'évaluation
- 3 - Pertes de ChargeDocument12 pages3 - Pertes de ChargeMarieme Boutraih100% (1)
- Résumé DTR c3-4 (Calcul Des Apports) PDFDocument26 pagesRésumé DTR c3-4 (Calcul Des Apports) PDFPFEPas encore d'évaluation
- Notion de Tension SuperficielleDocument9 pagesNotion de Tension SuperficielleNoureddine FrhPas encore d'évaluation
- Agrégation Des Sciences Mathématiques (Session de 1927) - Mathematiques SpécialesDocument17 pagesAgrégation Des Sciences Mathématiques (Session de 1927) - Mathematiques SpécialesAlex DumortierPas encore d'évaluation