Académique Documents
Professionnel Documents
Culture Documents
Cours - Chimie - Piles Électrochimiques - Bac Sciences Exp (2019-2020) MR Barhoumi Mourad
Transféré par
CHEMLI YoucefTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Cours - Chimie - Piles Électrochimiques - Bac Sciences Exp (2019-2020) MR Barhoumi Mourad
Transféré par
CHEMLI YoucefDroits d'auteur :
Formats disponibles
Cours chimie :
Piles électrochimiques
BARHOUMI. Mourad Section : 4M-4Sc.Exp
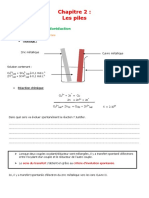
I- La pile Daniell
1- Transfert indirect d’électrons d’un réducteur à un un oxydant
Dispositif expérimental
K
A R
Lame de Cu
Lame de Zn
Pont salin
Solution (Zn2++SO42-) Solution (Cu2+ +SO42-)
Lorsqu’on ferme l’interrupteur k
Passage d’un courant électrique de la lame de cuivre (Cu) vers la lame de zinc (Zn)
Sur la lame de cuivre il apparait un dépôt de cuivre
BARHOUMI MOURAD Page 1 sur 14
Cu2+ + 2è Cu (Sd) (Réduction : gain d’électrons)
Cette électrode (lame de cuivre) est appelé cathode
La lame de zinc s’amincît
Zn(Sd) Zn2+ + 2è (oxydation : perte d’électrons).
Cette électrode (lame de zinc) est appelé anode
La réaction d’oxydoréduction qui se produit dans ce dispositif est alors
Zn (Sd) + Cu2+ Zn2+ + Cu (Sd)
Conclusion
Au cours de cette réaction il ya transfert indirect d’électrons de la lame de zinc vers (Cu2+ )
Ce dispositif qui permet d’obtenir du courant électrique grâce à une réaction chimique
spontanée est appelé pile électrochimique
Une pile est constituée de deux demi-piles reliées par une jonction électrochimique ou
pont salin.
Une demi-pile correspond à un couple redox. Elle est formée d’un conducteur électrique
(métal, graphite ….) en contact avec un conducteur ionique (électrolyte)
Le pont salin ou jonction électrochimique :
Le pont salin ou jonction électrochimique est obtenu soit :
- par une bande de papier filtre imbibée de nitrate de potassium.
- un tube en U qui contient une solution de KCl ou de KNO3 gélifiée.
Son rôle est
D’assurer la neutralité électrique des deux solutions
D’assurer la continuité électrique du circuit entre les deux compartiments
D’empêcher le mélange des deux solutions
BARHOUMI MOURAD Page 2 sur 14
2- Représentation de la pile Daniell
Par un schéma
Lame de Zn Lame de Cu
Pont salin
Solution
(Zn2++SO42-) Solution
(Cu2+ +SO42-)
[ Zn 2+] = C1 [ Cu2+] = C2
Par un symbole
Zn│ Zn2+ (C1) ║ Cu2+ (C2)│Cu
3- Equation associée
Zn + Cu2+ Zn2+ + Cu
4- Force électromotrice de la pile
E = Vborne Droite - VborneGauch
= VbCu - VbZn
5- Signe de la F.é.m. et sens de la réaction chimique :
E>0 la réaction directe se produit spontanément.
E<0 la réaction inverse se produit spontanément.
E=0 il n’y a pa de réaction possible spontanément
(Équilibre dynamique)
BARHOUMI MOURAD Page 3 sur 14
II- Autres exemples de pile de type Daniell : Pile zinc-Plomb
Lame de Pb
Lame de Zn
Pont salin
Solution (Zn2++SO42-) Solution (Pb2+ +SO42-)
([ Zn 2+] = C1 ) ([ Pb 2+] = C2 )
Zn│ Zn2+ (C1) ║ Pb2+ (C2)│Pb
Zn + Pb2+ Zn2+ + Pb
III- Etude de l’influence des concentrations sur la f.e.m d’une pile
Cu
Dispositif expérimental Zn
Pont salin
Solution (Zn2++SO42-) Solution (Cu2+ +SO42-)
([ Zn 2+] = C1 ) ([ Cu 2+] = C2 )
On fait varier les concentrations C1 et C2 et on mesure chaque fois la f.é.m. E de la pile réalisée
La courbe représentant la fonction E=f(log) est donnée par la figure ci-dessous
BARHOUMI MOURAD Page 4 sur 14
1180
1160
1140
1120
E (mV)
1100
1080
1060
1040
1020
-2.5 -2 -1.5 -1 -0.5 0 0.5 1 1.5 2 2.5
log (P)
Interprétation
La courbe ainsi obtenue montre, qu’a température constante, la f.é.m.
E de la pile dépend des concentrations réalisées dans les deux
compartiments et qu’elle est une fonction affine du logarithme décimal
de la fonction des concentrations Π de l’équation chimique associée :
E = a log Π + b
Ou b est la valeur de E lorsque Π = 1 dite "f.e.m. standard" de la pile
notée conventionnellement par E° et a est une constante qui dépend de
la température et qui vaut -0,03 V a 25°C.
E peut donc s’écrire sous la forme :
[Zn 2+ ]
E = E° - 0,03 log Π = E° - 0,03 log .
[Cu 2+ ]
Généralisation
Aune température donnée, pour toute pile formée par les couples redox
M1n+ /M1 et M2n+/M2,
La f.é.m. est une fonction affine du logarithme décimal de la fonction des
concentrations A 25°C
BARHOUMI MOURAD Page 5 sur 14
E=E° - 0.06
log
n
E° est la force électromotrice standard ;
[𝐌𝟐𝐧+ ]
• Π= est la fonction des concentrations relative a l’équation
[𝐌𝟏𝐧+ ]
chimique
M2 + M1n+ M2n+ + M1 ;
• n représente le nombre d’électrons qui apparait dans les équations
formelles permettant d’écrire l’équation chimique associée à la pile.
Attention : Pour donner l’expression de la fonction des concentrations , on doit utiliser
l’équation chimique associée à la pile et non l’équation de la réaction possible
spontanément
IV- Constante d’équilibre K associée à une pile
On dit qu’une pile est usée ( à rejeter) lorsque sa f.e.m est nulle (E=0) : il n’y aura plus
de circulation de courant ( c'est-à-dire d’électrons) dans le circuit, la réaction aboutit à un
état d’équilibre dynamique ( = K).
Pile usée f.e.m E =0 =K
nE0
0
0 E0
0,06
logK d’où logK
nE
K 10 0,06
n 0,06
E0
Pour n=2, on a K 10 0,03
E0 0,03logK
V- Comparaison des forces de couples redox d’apres la valeur de
f.e.m standard E° de la pile correspondante
Aune température donnée, pour toute pile formée par les couples
redox M1n+ /M1 et M2n+/M2,
La réaction associée à cette pile
M2 + M1n+ M2n+ + M1
À l’équilibre dynamique
nE0
[𝐌𝟐𝐧+ ]
K 10
0,06
K=
[𝐌𝟏𝐧+ ]
BARHOUMI MOURAD Page 6 sur 14
Si E° > 0 K >1 M1n+ est un oxydant plus fort que M2n+
M2 est un réducteur plus fort que M1
Si E° < 0 K <1 M2n+ est un oxydant plus fort que M1n+
M1 est un réducteur plus fort que M2
VI- Le potentiel standard d’oxydoréduction
1- L’électrode normale à hydrogène ( E.N.H)
Tige en platine
H2
Solution d’acide de
concentration molaire Plaque en platine
C=1 mol.L-1 platinée
Le potentiel de l’électrode normale à hydrogène (ENH) est pris, par convention, nul
donc E°(H3O+ / H2 ) = 0 V.
2- Le potentiel d’électrode d’un couple rédox
Le potentiel d’un couple Ox/Red, symbolisé par E(Ox/Red) est par définition la f.e.m
de la pile formée par l’ENH placée à gauche et le couple Ox/Red placé à droite
Tige en platine Pt
Pression = 1 atm
H2 Pont salin M
Solution d’acide de
concentration molaire
C=1 mol.L-1
Solution contenant
M2+ avec
[Mn+]=C mol.L-1
Plaque en platine Demi-pile contenant le
platinée couple Mn+/M
BARHOUMI MOURAD Page 7 sur 14
Symbole de la pile :
Pt(H2) │ H3O (1 mol.L )
+ -1
║ Mn+ (1 mol.L-1)│M
La f.e.m de cette pile est E= E(Mn+/M) – E0(ENH) = E(Mn+/M) – 0 = E(Mn+/M).
3- Le potentiel normal d’électrode d’un couple redox
Lorsque la concentration des ions Mn+ est égale à 1 mol.L-1 le potentiel d’électrode
est dit potentiel normal d’électrode et symbolisé par E°( Mn+/M).
V
Tige en platine Pt
H2 Pont salin M
Solution d’acide de
concentration molaire
C=1 mol.L-1 Solution contenant
Mn+ avec [Mn+]=1
mol.L-1
Plaque en platine
platinée
La f.e.m de cette pile est E= E0(Mn+/M) – E0(ENH) = E0(Mn+/M) – 0 = E0(Mn+/M).
Exemples de potentiel normal d’électrode :
Couple Ox/Red Fe2+/Fe H+/H2 Zn2+/Zn Sn2+/Sn Cu2+/Cu
E°(Ox/Red) (V) - 0,44 0 - 0,76 - 0,14 0,34
VII- Classification électrochimique des métaux
1- Comparaison d’un couple Mn+/M au couple H3O+/H2
Connaissons la f.é.m. E0(oxi/redi) du couple redox oxi/redi
a oxi + H2 +H2O b redi +H3O+
𝑛 𝐸 0 𝑜𝑥𝑖 /𝑟𝑒𝑑𝑖
K= 10 0.06
0 𝑜𝑥𝑖 𝑝𝑙𝑢𝑠 𝑓𝑜𝑟𝑡 𝑞𝑢𝑒 𝐻3 𝑂+
𝐸 𝑜𝑥𝑖 /𝑟𝑒𝑑𝑖 > 0 K >1
𝐻2 𝑝𝑙𝑢𝑠 𝑓𝑜𝑟𝑡 𝑞𝑢𝑒 𝑟𝑒𝑑𝑖
𝑜𝑥𝑖 𝑚𝑜𝑖𝑛𝑠 𝑓𝑜𝑟𝑡 𝑞𝑢𝑒 𝐻3 𝑂+
𝐸 0 𝑜𝑥𝑖 /𝑟𝑒𝑑𝑖 <0K<1
𝐻2 𝑚𝑜𝑖𝑛𝑠 𝑓𝑜𝑟𝑡 𝑞𝑢𝑒 𝑟𝑒𝑑𝑖
BARHOUMI MOURAD Page 8 sur 14
2- Détermination de la f.é.m. standard d’une pile
Soit la pile symbolisée par M2│ M2
n+
║ M1n+ │M
E = E(couple de droite) - E(couple de gauche) = E (M1/M1n+)- E(M2/M2n+)
Quand =1
E0 = E0(couple de droite) - E0(couple de gauche) = E0(M1/M1n+) - E0(M2/M2n+)= E0D - E0G
Exemple :
La pile Daniell Zn Zn2+ Cu2+ Cu
E°(Cu2+/Cu)=0,34 V et E°(Zn2+/Zn) = -0,76 V.
E° = E°(Cu2+/Cu) - E°(Zn2+/Zn ) = 0,34 – (-0,76)= 1,1 V.
3- Classification électrochimique des couples redox
Le couple redox qui a le potentiel normal le plus grand est le couple qui a le
pouvoir oxydant le plus important (donc le pouvoir réducteur le plus faible).
Zn/Zn2+ Fe2+/Fe Sn2+/Sn H+/H2 Cu2+/Cu couple
-0,76 -0,44 -0,14 0 0,34 E°(V)
Pouvoir oxydant croissant
Pouvoir réducteur décroissant
BARHOUMI MOURAD Page 9 sur 14
Exercice
A 20°C , on se propose d’étudier une pile électrochimique (P) schématisée par
Lame de Co Lame de Ni
Pont salin
Solution
(Co2++SO42-) Solution
(Ni2+ +SO42-)
[ Co 2+] = C1 [ Ni2+] = C2
=0.01 mol. L-1 =0.01 mol. L-1
1- Donner le symbole de cette pile (p)
2- Ecrire l’équation de la réaction chimique associée à cette pile
3- On fixe [ Co2+] = C1=0.01 mol.L-1 et on fait varier [ Ni2+] = X mol.L-1
On mesure à chaque fois la force électromotrice (f.é.m) E de la pile. Le graphe de la
figure-1 représente les variations de la force électromotrice E de la pile en
fonction de ( -logX )
E (V)
0.08
Figure-1
- log (X)
0 2.66
a- Exprimer la fonction des concentrations P de la pile en fonction de X
b- Exprimer la force électromotrice E en fonction de sa force électromotrice
standard E° et des concentrations [ Ni2+] et [ Co2+]
c- Montrer que la force électromotrice E de la pile peut s’exprimer par la relation
suivante
E= E°+0.06 + 0.03 logX
d- En déduire, à partir du graphe, la f.é.m. standard E° de la pile (p)
e- Calculer la constante d’équilibre K correspondant à la réaction associée à la pile (p)
f- Ecrire, en le justifiant, l’équation de la réaction spontanée qui se produit dans la
pile en circuit fermé
g- Pour quelle valeur de [ Ni2+] la pile se trouve épuisée (ne débite pas du courant) ?
BARHOUMI MOURAD Page 10 sur 14
4- A partir de l’état d’équilibre, on dilue 20 fois, par ajout de l’eau distillée, la solution
contenant les ions Ni2+
a. Calculer la nouvelle valeur de la f.e.m de la pile ( P ), juste après la dilution
b. En déduire l’effet de cette dilution sur le déplacement de l’équilibre chimique
Dans la pile (P)
5- La mesure de la f.é.m. E de la pile schématisée par la figure ci-dessous donne
E= -0.28 V
V
Tige en platine Pt
H2 Pont salin Co
Solution d’acide de
concentration molaire
C=1 mol.L-1 Solution contenant
Co2+ avec
[Co2+]=1 mol.L-1
Plaque en platine
platinée
a- Ecrire l’équation chimique associée à cette pile
b- Indiquer ce que représente E pour le couple Co2+/ Co
c- Déduire alors le potentiel normal du couple ( Ni2+/Ni ) : E° (Ni2+/ Ni)
d- Comparer les pouvoirs réducteurs des deux couples redox (Co2+/Co) et ( Ni2+/Ni )
Correction
1- Co│ Co2+ (C1) ║ Ni2+ ( C2)│Ni
2- Co + Ni2+ Co2+ + Ni
3-
𝑪𝒐𝟐+ 𝑪𝟏
a- P 𝑵𝒊𝟐+ 𝑿
b- La f.e.m E de la pile est donnée par l’expression suivante
𝟎.𝟎𝟔
E=E- 𝒏 log π
𝟎.𝟎𝟔 𝑪𝟏
c- E =E°- 𝟐 log 𝑿
= E°-0.03 ( log C1 – log X )
= E°-0.03 (log 0.01 –log X)
= E°-0.03 (-2 –log X)
= E°+0.06 + 0.03 log X (1)
BARHOUMI MOURAD Page 11 sur 14
d- La courbe E=f(-logX) est un segment de droite
D’équation E= b+ a (-logX)
b= 0.08 v (d’après la courbe ordonné à l’origine )
𝟎.𝟎𝟖−𝟎
a=pente de la courbe= 𝟎−𝟐.𝟔𝟔 =- 0.03
E= 0.08 +0.03 logX
Par identification avec l’expression théorique (1)
E°+0.09=0.08
E°=0.08- 0.06=0.02 V
𝑛 𝐸0 2𝑥 0.02
e- K= 10 0.06 = 10 0.06 = 4.64
f- K>1 E>0 la réaction qui a lieu spontanément est la réaction directe
Co + Ni2+ Co2+ + Ni
g- La pile ne débite plus : E=0 et P =K
Pile épuisé E=0 v 0.08+0.03 logX = 0
(0.08)
=> logX= - = -2.66 => [ Ni2+]eq =X= 2.15 10-3 mol.L-1
0.03
4-
a- On dilution 20 fois de la solution contenant Ni2+
[ Ni2+]=[ Ni2+]eq /20 = 1,075.10-4 mol.L-1
Cherchons [ Co2+]eq = ?
Tableau d’avancement volumique :
Equation chimique de la
Co + Ni2+ Co2+ + Ni
réaction
Etat du Avancement
Concentration molaire en mol.L-1
système volumique
Initial 0 C2 C1
final yf C2-yf C1+yf
A l’équilibre on a
C2-yf = 2.15.10-3 mol.L-1 yf = C2- 2.15.10-3 = 0.01- 2.15.10-3=7.85 x10-3
[ Co2+]eq= C2-yf = 0.01- 7.85x10-3= 2.15x10-3mol.L-1
𝑪𝒐𝟐+ 𝟎.𝟎𝟎𝟐𝟏𝟓
E= E°- 0.03 log P =E°- 0.03 log = 0.02-0.03𝒍𝒐𝒈 𝟏.𝟎𝟕𝟓𝒙𝟏𝟎−𝟒 = -0.02
𝑵𝒊𝟐+
b- E < 0 l’évolution du système se fait dans le sens de la formation de Ni 2+
Ni + Co2+ Ni2++ Co
5-
a- Co2+ + H2 + 2H2O Co + 2H3O+
b- Cette valeur correspond la f.é.m. standard du couple redox Co2+ /Co
E = E°(Co2+/Co) =-0.28 v
BARHOUMI MOURAD Page 12 sur 14
c- E° = E°(Co2+/Co) - E°(Ni2+/Ni ) E°(Ni2+/Ni ) = E° - E°(Co2+/Co) =0.02- (-0.28) = 0.3 V
d- E°(Ni2+/Ni ) > E°(Co2+/Co) le couple Ni2+/Ni à le pouvoir réducteur le plus faible
PILES ALCALINES
I : Introduction
Les piles de type Daniell utilisent des solutions aqueuses salines , ces piles ne sont pas
commodes pour un usage dans les appareils domestique parce que :
Ont une capacité électrique faible
Ne sont pas adoptées aux positions aléatoires de ces appareils
Donc il faut penser à d’autres types de piles : les piles sèches telles que les piles
alcalines
L’électrolyte dans ce type de pile est l’hydroxyde de potassium KOH. La solution
de KOH est gélifiée pour éviter son écoulement (la pile est dite sèche)
L’hydroxyde de potassium contient l’élément chimique K est un alcalin
appartient 1ere colonne du tableau périodique ( Li, Na, K)
Les piles alcalines se diffèrent l’une de l’autre par la nature des couples redox mis en jeu
et de leurs formes (cylindrique, plates , cylindrique plate (pile bouton))
II : Description et fonctionnement de quelques piles alcalines
1- Pile à oxyde de manganèse
Possède une f.e.m nominale de 1.5 V
- La cathode limitée e par un boîtier en acier constituée du dioxyde de manganèse MnO2 et du
graphite en poudre
- les compartiments anodique et cathodique de la pile sont séparés par une feuille en
fibres plastiques imbibée d’hydroxyde de potassium joue le rôle de jonction électrique
(échange ionique)
Boîtier en acier
Zinc en poudre
amalgamé
Solution de KOH
Poudre de graphite et
Fibres dioxyde de manganèse
plastiques
imbibées de Clou en acier
potasse
Les couples redox mis en jeu dans cette pile sont Zn(OH)42-/ Zn et MnO2/ MnOOH
BARHOUMI MOURAD Page 13 sur 14
L’équation de réaction qui se produit dans la pile lorsqu’elle débite un courant électrique
est :
Zn +2OH- + 2MnO2 + 2H2O Zn(OH)42- + 2MnOOH
2- Pile à oxyde d’argent (pile bouton)
Possède une f.e.m nominale de 1.55 V
Dans le compartiment on dispose d’une plaque de zinc Zn en contact direct avec un
électrolyte (KOH gélifiée ) joue le rôle de pont conducteur entre les deux compartiments
de la pile . l’électrode de zinc constitue le pole négatif
Dans le deuxième compartiment on une tige en argent Ag en contact direct avec un
mélange de (Ag2O + graphite en poudre ) l’électrode d’argent constitue le pole positif
Les couples redox mis en jeu dans cette pile sont Zn(OH)42- / Zn et Ag2O/ Ag
L’équation de réaction qui se produit dans la pile lorsqu’elle débite un courant électrique
est :
Zn +2OH- +Ag2O + 2OH-+ H2O Zn(OH)42- + 2Ag
3- Pile à oxyde de mercure (pile bouton)
Possède une f.e.m nominale de 1.35 V
Dans le compartiment on dispose d’une plaque de zinc Zn en contact direct avec un
électrolyte (KOH gélifiée ) joue le rôle de pont conducteur entre les deux compartiments
de la pile . l’électrode de zinc constitue le pole négatif
Dans le deuxième compartiment on a de l’oxyde de mercure HgO et du graphite en poudre
imbibées d’hydroxyde de potassium l’électrode de graphite constitue le pole positif
Les couples redox mis en jeu dans cette pile sont Zn(OH)42- / Zn et HgO/ Hg
L’équation de réaction qui se produit dans la pile lorsqu’elle débite un courant électrique
est :
Zn +2OH- +HgO + 2OH-+ H2O Zn(OH)42- + Hg
BARHOUMI MOURAD Page 14 sur 14
Vous aimerez peut-être aussi
- 1 - Transformation Spontanées Dans Le Piles Et Production D'énergieDocument7 pages1 - Transformation Spontanées Dans Le Piles Et Production D'énergieTaha BoulmanePas encore d'évaluation
- Cours PilesDocument5 pagesCours PilesLotfi Ben MalekPas encore d'évaluation
- Bac D PCDocument118 pagesBac D PCtanjiaPas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences PhysiquesDocument3 pagesDevoir de Contrôle N°2 - Sciences Physiqueskougfst ldhd100% (1)
- Série+d'exercices - Sciences Physiques Préparation Bac+2011 - Bac+Mathématiques (2010-2011) MR Benaich PDFDocument21 pagesSérie+d'exercices - Sciences Physiques Préparation Bac+2011 - Bac+Mathématiques (2010-2011) MR Benaich PDFBen Salem Noureddine0% (2)
- Devoir Corrigé de Synthèse N°3 - Physique - Bac Mathématiques (2010-2011) Elève SindaDocument7 pagesDevoir Corrigé de Synthèse N°3 - Physique - Bac Mathématiques (2010-2011) Elève SindaTawfiq Weld EL ArbiPas encore d'évaluation
- Devoir de Synthèse N°1 - Sciences Physiques - Bac Mathématiques (2015-2016) MR Maalej Med HabibDocument6 pagesDevoir de Synthèse N°1 - Sciences Physiques - Bac Mathématiques (2015-2016) MR Maalej Med HabibMustapha ElhafiPas encore d'évaluation
- Lecon Exercice PC 1ere SDocument5 pagesLecon Exercice PC 1ere SKevin RajaonarivonyPas encore d'évaluation
- 4 Exercice Suivi D'une Transformation ChimiqueDocument2 pages4 Exercice Suivi D'une Transformation Chimiquenabil echerrarPas encore d'évaluation
- Acide BaseDocument10 pagesAcide BaseAmeni Slimen100% (1)
- Suites Numeriques Resume de Cours 1 13Document2 pagesSuites Numeriques Resume de Cours 1 13anuom20100% (1)
- c2 1bac Biof - Les Grandeurs Liées À La Quantité de Matière Prof - Sbiro (WWW - Pc1.ma) PDFDocument2 pagesc2 1bac Biof - Les Grandeurs Liées À La Quantité de Matière Prof - Sbiro (WWW - Pc1.ma) PDFHAMADA1972100% (2)
- Transformations Liees A Des Reactions Acide Base Cours 3 2Document4 pagesTransformations Liees A Des Reactions Acide Base Cours 3 2assad saisPas encore d'évaluation
- RCI 2017 BAC Serie D Physique ChimieDocument4 pagesRCI 2017 BAC Serie D Physique ChimieJunior RaymondPas encore d'évaluation
- Sciences Physiques - Cinetique Chimique-Gazzah MahmoudDocument3 pagesSciences Physiques - Cinetique Chimique-Gazzah MahmoudMahmoud GazzahPas encore d'évaluation
- Devoir 2 Modele 5 Mathematiques 2 Bac SPC Semestre 1Document1 pageDevoir 2 Modele 5 Mathematiques 2 Bac SPC Semestre 1Zakaria AjichePas encore d'évaluation
- 0607DM2 PDFDocument3 pages0607DM2 PDFFoudil Laouici100% (1)
- Transformations Lentes Et Transformations Rapides Exercices Non Corriges 1 2Document2 pagesTransformations Lentes Et Transformations Rapides Exercices Non Corriges 1 2Med RTPas encore d'évaluation
- Dipole RC (Serie1+2) +correctionDocument7 pagesDipole RC (Serie1+2) +correctionSamir JemniPas encore d'évaluation
- Technique de Suivi Temporel D'une TransformationDocument8 pagesTechnique de Suivi Temporel D'une TransformationJosé Ahanda NguiniPas encore d'évaluation
- Chute Libre Verticale D Un Solide Exercices Non Corriges 4Document5 pagesChute Libre Verticale D Un Solide Exercices Non Corriges 4S Bouhmid100% (1)
- C9Chim Transformations Forcees PDFDocument2 pagesC9Chim Transformations Forcees PDFAzizElheni100% (1)
- Manuel - Résumés de Cours, Séries D'exercies, Examens Blancs Et Nationaux-ELBEHRI Et AITRAISS-2021-2022 - 220611 - 131342Document231 pagesManuel - Résumés de Cours, Séries D'exercies, Examens Blancs Et Nationaux-ELBEHRI Et AITRAISS-2021-2022 - 220611 - 131342ghalibouhlal16Pas encore d'évaluation
- Série D'exercices N°2 - Sciences Physiques Série de Revision 2eme Trimestre - Bac Toutes Sections (2012-2013) Mme Titouhi ImenDocument3 pagesSérie D'exercices N°2 - Sciences Physiques Série de Revision 2eme Trimestre - Bac Toutes Sections (2012-2013) Mme Titouhi ImenTawfiq Weld EL ArbiPas encore d'évaluation
- 2006 Antilles Exo1 Correction Bobine 5 5ptsDocument3 pages2006 Antilles Exo1 Correction Bobine 5 5ptsVincent PHANPas encore d'évaluation
- DS2 (06 03 09)Document7 pagesDS2 (06 03 09)Seif Souid100% (3)
- Extrait de Cours Sciences Physiques TerminaleDocument15 pagesExtrait de Cours Sciences Physiques TerminaleAmine schoolPas encore d'évaluation
- Derives D Ac CarbDocument1 pageDerives D Ac CarbMoufida Zouaghi100% (1)
- Oscillations Libres Dans Un Circuit RLC PDFDocument8 pagesOscillations Libres Dans Un Circuit RLC PDFMarøøen Bouabid100% (1)
- Acides Et Bases de BronstedDocument2 pagesAcides Et Bases de BronstedSmaali Faouzi Smaali100% (1)
- Devoir 2 Modele 1 Physique Chimie 2 Bac SPC Semestre 1 Corrige 1Document2 pagesDevoir 2 Modele 1 Physique Chimie 2 Bac SPC Semestre 1 Corrige 1Marouane AkkaPas encore d'évaluation
- Exercice 4 Réactions Destérification Et Dhydrolyse LAHLALI PDFDocument5 pagesExercice 4 Réactions Destérification Et Dhydrolyse LAHLALI PDFBouba KhedherPas encore d'évaluation
- Série D'exercices N°2 - Sciences Physiques LA BOBINE ET LE DIPOLE RL - Bac Sciences Exp (2015-2016) MR Daghsni Sahbi PDFDocument5 pagesSérie D'exercices N°2 - Sciences Physiques LA BOBINE ET LE DIPOLE RL - Bac Sciences Exp (2015-2016) MR Daghsni Sahbi PDFMahmoud Essahbi Sahbi DaghsniPas encore d'évaluation
- TP Physique ImportantDocument286 pagesTP Physique ImportantZakari YaePas encore d'évaluation
- 1 - Cinétique ProfDocument16 pages1 - Cinétique Profyahya chbaniPas encore d'évaluation
- 2-Examens BAC Nucleaire PC FRDocument4 pages2-Examens BAC Nucleaire PC FRMouad Driouch SMIA-TD4100% (1)
- Devoir Maison 01-2bac-BIOFDocument1 pageDevoir Maison 01-2bac-BIOFFatima EssalhiPas encore d'évaluation
- Cinetique Chimique 12233Document3 pagesCinetique Chimique 12233sdirianisPas encore d'évaluation
- DS1 (11 12 09)Document8 pagesDS1 (11 12 09)Seif Souid100% (5)
- Resume Acide Base1 Final 1Document2 pagesResume Acide Base1 Final 1MazingaPas encore d'évaluation
- 2004-Polynesie QCM OndesDocument2 pages2004-Polynesie QCM OndesanasronaldoPas encore d'évaluation
- Cours - Chimie - Cinétique Chimique - Vitesse D'une Réaction - Bac Sciences Exp (2018-2019) MR Sfaxi Salah PDFDocument6 pagesCours - Chimie - Cinétique Chimique - Vitesse D'une Réaction - Bac Sciences Exp (2018-2019) MR Sfaxi Salah PDFmohamed amine hattayPas encore d'évaluation
- Série Acide BaseDocument5 pagesSérie Acide BaseMohamed Helmi ChebbiPas encore d'évaluation
- Résumé-FonCtions - 2BAC-SCDocument1 pageRésumé-FonCtions - 2BAC-SCAbde Aitoutbib100% (1)
- Phenomene Physique de Équation DifferentielleDocument14 pagesPhenomene Physique de Équation Differentielleelmourri hayfaPas encore d'évaluation
- Série D'exercices N°8 Avec Correction - Sciences Physiques - Révision - Bac Sciences Exp (2019-2020) MR Amine Touati PDFDocument7 pagesSérie D'exercices N°8 Avec Correction - Sciences Physiques - Révision - Bac Sciences Exp (2019-2020) MR Amine Touati PDFsiwar kokoPas encore d'évaluation
- Sa. Dev3 TS3 13-14 PDFDocument10 pagesSa. Dev3 TS3 13-14 PDFaittaliPas encore d'évaluation
- Contrôle 2Document3 pagesContrôle 2Mery EmPas encore d'évaluation
- Equilibre Esterification-Hydrolyse PDFDocument7 pagesEquilibre Esterification-Hydrolyse PDFAzizElheniPas encore d'évaluation
- DM16 1112 - Dosage PH Metrique Es PDFDocument6 pagesDM16 1112 - Dosage PH Metrique Es PDFEmma LovaPas encore d'évaluation
- Controle N1 2BAC PC BIOF 22 OmarDocument4 pagesControle N1 2BAC PC BIOF 22 Omarassad saisPas encore d'évaluation
- Cours Et Exercices Corrigés Maths 2 Bac SM Prof Zakaria Bouicha FinalDocument144 pagesCours Et Exercices Corrigés Maths 2 Bac SM Prof Zakaria Bouicha FinalAbderrahmane El OuafyPas encore d'évaluation
- C2Chim Vitesse Reaction Exercices PDFDocument8 pagesC2Chim Vitesse Reaction Exercices PDFAzizElheniPas encore d'évaluation
- Pile Électrochimique2024Document15 pagesPile Électrochimique2024Barhoumi MouradPas encore d'évaluation
- Pile TunisieDocument14 pagesPile TunisieMohamed ElouakilPas encore d'évaluation
- Série N°11 Chimie Les Piles 2013 2014)Document4 pagesSérie N°11 Chimie Les Piles 2013 2014)Amen RouissiPas encore d'évaluation
- Pile de DanielleDocument3 pagesPile de DanielleAnis NissouPas encore d'évaluation
- Chap Piles CouleurDocument4 pagesChap Piles CouleurIsmail ait talebPas encore d'évaluation
- Hea 400 - Hea 360Document21 pagesHea 400 - Hea 360YassineElabdPas encore d'évaluation
- 08-MC-3x50 Et 2x50 - CalculsDocument49 pages08-MC-3x50 Et 2x50 - CalculspompelargeurPas encore d'évaluation
- F - Remaline 50 Fiche CommercialeDocument2 pagesF - Remaline 50 Fiche CommercialeAlexandre RogerPas encore d'évaluation
- TD Chimie OrganiqueDocument9 pagesTD Chimie Organiqueass mohPas encore d'évaluation
- FR Fiche Technique - Flooring Systems - Hourdis - Feb 2023Document11 pagesFR Fiche Technique - Flooring Systems - Hourdis - Feb 2023djantoine16Pas encore d'évaluation
- Soudage À La Flamme PDFDocument8 pagesSoudage À La Flamme PDFGOUAREF SAMIRPas encore d'évaluation
- SKILLS M08F Portiques Batiments Simple RDC v3 PDFDocument79 pagesSKILLS M08F Portiques Batiments Simple RDC v3 PDFHammadi TaharPas encore d'évaluation
- Poly ETSHER Béton Armé LEGRAND 1996Document144 pagesPoly ETSHER Béton Armé LEGRAND 1996Morci Mnejja83% (6)
- ThermodynamiqueDocument2 pagesThermodynamiqueAli WardiPas encore d'évaluation
- 31-Reprises D'humidité Dans Les Coins DoucheDocument2 pages31-Reprises D'humidité Dans Les Coins DouchemezouedPas encore d'évaluation
- These Renoux jennifer-VFDocument179 pagesThese Renoux jennifer-VFstive.gouch99Pas encore d'évaluation
- Chap 2Document38 pagesChap 2Salas gamerPas encore d'évaluation
- Alucobond at 2 16 1730 k7 PDFDocument34 pagesAlucobond at 2 16 1730 k7 PDFSifou MegdoudPas encore d'évaluation
- TP MineralogieDocument40 pagesTP MineralogieSamir MoussPas encore d'évaluation
- Korzerter Straße 21-25 D-42349 Wuppertal Germany WWW - Wera.De WWW - Wera-Tools - Co.Uk Wera Werkzeuge GMBHDocument2 pagesKorzerter Straße 21-25 D-42349 Wuppertal Germany WWW - Wera.De WWW - Wera-Tools - Co.Uk Wera Werkzeuge GMBHWilliam ZuñigaPas encore d'évaluation
- Extr Etancheite ToitureDocument8 pagesExtr Etancheite ToitureAbdelhak Guetti50% (2)
- Essai Sur Mortier Normaldnc DDocument7 pagesEssai Sur Mortier Normaldnc Dأيوب طويلPas encore d'évaluation
- TP Masse Volumique Humide Et SècheDocument10 pagesTP Masse Volumique Humide Et Sèchekhaled sioud100% (1)
- BARRAGEDocument18 pagesBARRAGEAnas HamdiPas encore d'évaluation
- Volume 3 CPTDocument178 pagesVolume 3 CPTRazak SeonePas encore d'évaluation
- Manuel Technique Pour La Formation Des Formateurs en GDMA PDFDocument114 pagesManuel Technique Pour La Formation Des Formateurs en GDMA PDFHakim Maguiri100% (2)
- Cor12 3Document1 pageCor12 3fafoulolPas encore d'évaluation
- Les ExplosifsDocument136 pagesLes ExplosifsMourad Chouaf100% (1)
- Correspondance Norme Din Iso Nfen Nfe BV Ldoc36 1Document10 pagesCorrespondance Norme Din Iso Nfen Nfe BV Ldoc36 1ناريمان ابو السعودPas encore d'évaluation
- Travaux Diriges de Biomasse EnergieDocument27 pagesTravaux Diriges de Biomasse Energiehamza kadim100% (1)
- TP1 Electochimie 3émé AnnéeDocument10 pagesTP1 Electochimie 3émé AnnéeLïnâ ExØtîc DõlĽPas encore d'évaluation
- 07 Ph-MetrieDocument13 pages07 Ph-MetrieJeff HardyPas encore d'évaluation
- Etude de La Precipitation Des Asphaltenes Dans La Zone1 de Hassi MessaoudDocument82 pagesEtude de La Precipitation Des Asphaltenes Dans La Zone1 de Hassi MessaoudRihab khPas encore d'évaluation
- Oxydation Des Colorants Par Les Procedes Doxydation Avancee Sur Des Catalyseurs A Base de La Montmorillonite Modifiee PDFDocument48 pagesOxydation Des Colorants Par Les Procedes Doxydation Avancee Sur Des Catalyseurs A Base de La Montmorillonite Modifiee PDFBibi BibaPas encore d'évaluation
- Materiaux de Construction Chap 1Document13 pagesMateriaux de Construction Chap 1YounessElKhattabiPas encore d'évaluation