Académique Documents
Professionnel Documents
Culture Documents
Cours - Physique - Spectre Atomique - Bac Sciences Exp (2019-2020) MR Barhoumi Mourad
Transféré par
Bassouma KhmasTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Cours - Physique - Spectre Atomique - Bac Sciences Exp (2019-2020) MR Barhoumi Mourad
Transféré par
Bassouma KhmasDroits d'auteur :
Formats disponibles
BARHOUMI. Mourad Section : 4M-4Sc.
Exp
I- La quantification de l'énergie transférée à un atome
1- Expérience de Franck et Hertz (1914)
a- Dispositif expérimental simplifié
Un canon à électrons : permettant d'obtenir des électrons de même énergie cinétique.
Un capteur analyseur : permettant de compter les électrons qui l'atteignent avec la même énergie
cinétique initiale.
Atome de mercure
Capteur
analyseur
𝐸𝑐
Canon à électrons -
Électron
Vapeur de mercure à faible
pression
b- Principe
Les atomes de vapeur de mercure à faible pression sont bombardés avec des électrons
d’énergie cinétique Ec variables.
Le capteur est réglé de sorte à compter le nombre d’électrons qui l’atteignent avec la
même ECi initiale et de la comparer leurs ECf à la sortie de la chambre à gaz.
c- Résultats de l’expérience et interprétation:
Ne : nombre d’électrons par unité de temps
initialement émis par le canon
Nc : nombre d’électrons par unité de temps
comptés par le capteur
1 e.v =1.6x10-19 J
BARHOUMI MOURAD Page 1 sur 14
𝑁𝑐
Ec < 4,9 ev 𝑁𝑒 = 1 Nc= Ne
Donc tous le électrons arrivent au capteur avec la même énergie Ec
Pour certains électrons émis peuvent entrer en collision avec les atomes
de mercure mais sans céder leur énergie Il se produit un choc
élastique entre l’électron et l’atome de mercure
𝑁𝑐
Ec ≥4,9 ev 𝑁𝑒 < 1 Nc < Ne
Un certain nombre des ces électrons n’atteignent pas le capteur avec leur
vitesse initiale. Ces électrons entrent en collision avec les atomes de mercure
et leur cèdent une énergie de valeur 4.9 e.v il s’agit d’un choc inélastique
entre l’électron et l’atome de mercure donc ces électrons n’arrivent ne sont
plus comptés
d- Conclusion :
Lors de la collision d’un atome avec un électron d’énergie cinétique Ec, l’électron peut lui
céder de l’énergie. Cette énergie transférée ne peut prendre que des valeurs particulières.
L’expérience de Franck et Hertz met en évidence la quantification du transfert
d’énergie entre un atome et le milieu extérieur.
2- Niveaux d'énergie d’un atome
a- Hypothèses de Bohr (1855-1962)
* Les variations d'énergie de l'atome sont quantifiées.
* L'atome ne peut se trouver que dans certains états d'énergie bien définis.
b- Niveaux d'énergie
* L'énergie d'un atome donné ne peut prendre que certaines valeurs particulières appelées
niveaux d'énergie
* L'ensemble des niveaux d'énergie associés à un atome est unique.
On schématise les niveaux d'énergie d'un atome par des paliers sous forme de traits
définis par E = cte sur un axe choisi comme axe des énergies
Dans son état le plus stable, un atome est au niveau d'énergie le plus bas : on dit qu'il est
dans son état fondamental
Lorsqu'un atome est dans un état autre que son état fondamental, on dit qu'il est dans
un état excité
Les niveaux d'énergie supérieurs sont appelés des états excités.
Le passage de l'atome d'un état de niveau d'énergie Ep a un état d'énergie En est appelé
un transition, p et n étant des entiers désignant les numéros des états considères.
BARHOUMI MOURAD Page 2 sur 14
Lorsqu'un atome passe d’un état plus bas vers un autre état plus haut il absorbe de
l’énergie
Lorsqu'un atome passe d’un état plus haut vers un autre état plus bas il cède de
l’énergie
II- SPECTRES LUMINEUX
1- Spectre de la lumière blanche
On appelle lumière blanche toute lumière dont la décomposition par un prisme (ou un
réseau) donne une figure colorée qui contient toutes les couleurs de l’arc en ciel.
La lumière blanche est composée d’une infinité de radiations colorées (ou lumières
colorées) dont la décomposition (par un prisme ou un réseau) donne une figure colorée
contenant une infinité de couleurs.
BARHOUMI MOURAD Page 3 sur 14
2- Spectre d’émission
Lampe à vapeur de mercure
La lumière émise par une lampe spectrale (lampe a vapeur de mercure) analysée par un réseau
donne lieu a un spectre discontinu, constitue de bandes fines multicolores sur fond sombre,
appelé spectre de raies.
Etant le résultat de la dispersion du faisceau lumineux émis par une lampe à vapeur d’atomes
identiques, le spectre de raies est appelé spectre d’émission.
Le spectre d’émission caractérise l’élément chimique qui le produit
BARHOUMI MOURAD Page 4 sur 14
3- Spectre d’absorption
On appelle spectre d’absorption d’une substance le spectre de la lumière obtenue
après traversée de cette substance par la lumière blanche ;
On appelle spectre de raies d’absorption, un spectre qui contient des raies sombres
(appelées raies d’absorption) sur le fond coloré d’un spectre continu ;
On appelle spectre de bandes d’absorption, un spectre qui contient des bandes
sombres (appelées bandes d’absorption) sur le fond coloré d’un spectre continu.
Lorsque des radiations lumineuses traversent un gaz froid sous faible pression ou une solution
colorée, certaines radiations peuvent être absorbées. Si le spectre du rayonnement incident est
continu, alors il est amputé de certaines raies après le passage au travers du gaz ou de la
solution.
Exemples
Spectre de raie d’absorption du sodium (en lumière blanche)
Spectre de bandes d’absorption du permanganate de potassium
(En lumière blanche)
Remarque
Un élément chimique n’absorbe que les radiations qu'il est capable d'émettre : les raies
d'absorption et d'émission de l’élément se situent donc à la même longueur d’onde ( au
même endroit) sur les spectres (émission et absorption).
BARHOUMI MOURAD Page 5 sur 14
Pour un atome A donné, les longueurs d’onde des raies qu’il émet sont identiques à
celles des raies qu’il absorbe
Spectre de raie d’émission d’un élément chimique A
Spectre de raie d’absorption d’un élément chimique A
Conclusion
- Le spectre de la lumière qui a traversé un gaz, constitué d’atomes ou d’ions simples
(sous faible pression et à basse température), est un spectre de raies d’absorption ;
- Chaque entité chimique (atome ou ion) possède un spectre de raies d’émission
spécifique, ce qui permet de l’identifier ;
- Un élément chimique n’absorbe, lorsqu’il est éclairé, que les radiations (les couleurs)
qu'il émet lorsqu’il rayonne. Un gaz absorbe les mêmes radiations (couleurs) qu'il
émettrait s'il était chaud.
III- SPECTRES DE L’ATOME D’HYDROGENE
1- NOTION DE PHOTON
On admet qu’une radiation lumineuse de longueur d’onde λ est constituée d’un flux
de particules non chargées et sans masse appelées photons. Chaque photon transporte
l’énergie :
𝑪
w = h = h
𝝀
Ou
- h est une constante appelée la constante de Planck. h = 6,62.10-34 J.s.
- fréquence de la radiation (en Hertz )
- 𝛌 longueur d’onde (en mètre)
- 𝐂 : vitesse de la lumière ( m.s-1 )
BARHOUMI MOURAD Page 6 sur 14
Remarque
L’énergie d’un photon est appelée quantum d’énergie
2- MODELE DE BOHR DE L’ATOME D’HYDROGENE
Pour interpréter le spectre d'émission de l'atome d'hydrogène, Niels Bohr à été amène à
conférer à l’atome d’hydrogène un modèle basé sur les postulats suivants :
Le noyau est suppose fixe dans l’atome car sa masse est
1836 fois plus grande que celle de l'électron.
L’électron ne peut graviter autour du noyau que sur des
Orbites circulaires bien déterminées. Ces orbites quantifiées sont
Dites stationnaires
.
L’électron n’échange de l’énergie avec l’extérieur que lors de
son passage d’une orbite stationnaire a une autre.
3- ENERGIE DE L’ATOME D’HYDROGENE
En se basant sur ses postulats, Bohr établit l’expression de l’énergie de l’atome d’hydrogène
pour un niveau d’énergie En en fonction de l’énergie Eo de l’état fondamental
𝑬𝟎
En =-
𝒏𝟐
Avec
- Eo = 13,6 eV et n un entier naturel non nul
- En est exprime en eV.
- n ϵ N*
1 eV = 1,6.10-19 J.
Pour n = 1, E1 = - 13,6 eV ; c’est le niveau d’énergie minimale ou niveau
fondamental. Il correspond a l’état le plus stable de l’atome d’hydrogène.
Pour n > 1 : - 13,6 eV < En < 0 : l’atome est dans l’un des états excites.
Pour n→∞, En(∞) = 0 : l’atome est ionise, le proton et l’électron sont sépares.
ionisé
exicités
fondamental
BARHOUMI MOURAD Page 7 sur 14
4- INTERPRETATION DES RAIES D’EMISSION
Grace a un apport extérieur d’énergie, par exemple sous l’effet d’un rayonnement ou par
collision avec un atome ou une autre particule matérielle, l’atome peut passer d’un niveau n a
un niveau p (p > n). Dans ce cas, l’atome absorbe juste l’énergie nécessaire au changement
de niveau :
𝟏𝟑.𝟔 𝟏𝟑.𝟔 𝟏 𝟏 𝟏 𝟏
ΔEn,p= Ep – En= - -(- ) = 13.6 x ( - ) = E0 x ( - )
𝒑𝟐 𝒏𝟐 𝒏𝟐 𝒑𝟐 𝒏𝟐 𝒑𝟐
• Lorsqu’un atome se désexcite en passant d’un niveau p vers un niveau n (p > n), il restitue
l’énergie : ΔEp,n = En - Ep en émettant un photon d’énergie hν = - ΔEp,n.
𝟏 𝟏
hν = - ΔEp,n= ΔEn,p = (Ep-En) = E0 x ( - )
𝒏𝟐 𝒑𝟐
𝑪 𝟏 𝟏 𝒉 .𝑪
h = E0 x ( 𝒏𝟐 - ) = En-Ep 𝛌 p,n=
𝝀 𝒑𝟐 𝟏 𝟏
𝑬𝟎 ( 𝟐 − 𝟐 )
𝒏 𝒑
BARHOUMI MOURAD Page 8 sur 14
Pour les transitions aboutissant au niveau excite n = 1
ΔEp,1 = En – Ep = E1-Ep
𝟏 𝟏 𝟏 𝟏
hνp,1 = - ΔEp,1= ΔE1,p= E0 x ( - ) = E0 x ( - )
𝟏𝟐 𝒑𝟐 𝟏𝟐 𝒑𝟐
𝒉 .𝑪
𝛌 p,1= 𝟏 𝟏
𝑬𝟎 ( 𝟐 − 𝟐 )
𝟏 𝒑
Pour n = 1 et p = 2, ΔE2,1 = E2 - E1 = 10,2 eV = 16,32.10-19J,
or ΔE2,1 = hν2,1, d’où
ν2,1 = 2,4.1015 Hz : fréquence de la radiation
et
𝑪
λ2,1 = = 121x10-9 m = 121 nm : longueur d’onde de la radiation
𝝂𝟐,𝟏
Pour tout p > 2, ΔEp,1 = hνp,1 > ΔE2,1 , d’ou νp,1 > ν2,1.
Donc, il en est de même pour toutes les transitions aboutissant au niveau
fondamental n = 1.
Ces transitions constituent une série de raies invisibles appelée série de Lyman.
Pour les transitions aboutissant au niveau excite n = 2 :
ΔEp,2 = E2-Ep
𝟏 𝟏
hνp,2 = - ΔEp,2 = ΔE2,p= E0 x ( - )
𝟐𝟐 𝒑𝟐
𝒉 .𝑪
𝛌 p,2= 𝟏 𝟏
𝑬𝟎 ( 𝟐 − 𝟐 )
𝟐 𝒑
Les raies correspondant aux transitions qui aboutissent au niveau
excite n = 2 constituent la série de Balmer.
Pour les transitions aboutissant au niveau excite n = 3 :
ΔEp,3 = E3-Ep
𝟏 𝟏
hνp,3 = - ΔEp,3 = ΔE2,p= E0 x ( - )
𝟑𝟐 𝒑𝟐
𝒉 .𝑪
𝛌 p,3= 𝟏 𝟏
𝑬𝟎 ( 𝟐 − 𝟐 )
𝟑 𝒑
BARHOUMI MOURAD Page 9 sur 14
Les raies correspondant aux transitions qui aboutissent au niveau
excité n =3 constituent la série de Paschen .
Les raies correspondant aux transitions qui aboutissent au niveau
excité n =4 constituent la série de Brackett
Les raies correspondant aux transitions qui aboutissent au niveau
excité n =5 constituent la série de Pfund
5- INTERPRETATION DES RAIES D’ABSORPTION
Considérons un atome d’hydrogène dans l’état d’énergie En.
Quand il reçoit un photon d’énergie hν deux éventualités se présentent :
L’énergie du photon est insuffisante pour ioniser l’atome.
- Si l’énergie du photon correspond exactement a une transition possible entre le niveau
d’énergie En et un niveau excite d’énergie Ep, avec p > n, la radiation de fréquence ν est
absorbée ; la conservation de l’energie conduit a la relation :
ΔEn,p = Ep – En = hν .
Le spectre d’absorption présente alors une raie noire correspondant a la fréquence ν.
- Si l’énergie du photon ne correspond pas a une transition électronique possible, le
photon n’est pas absorbe, mais diffuse, c'est-a-dire renvoyé avec la même énergie dans
une direction a priori quelconque.
BARHOUMI MOURAD Page 10 sur 14
L’énergie du photon est supérieure ou égale à l’énergie d’ionisation de l’atome.
Si l’énergie hν du photon est supérieure a l’énergie d’ionisation Ei, le photon peut être absorbe : une
partie de son énergie permet l’ionisation de l’atome ; le reste est transfère sous forme d’énergie
cinétique a l’électron éjecte.
hν = Ei +Ec
Ainsi, un photon d’énergie quelconque peut être absorbe par l’atome d’hydrogène pourvu
que cette energie soit au minimum égale a l’énergie d’ionisation.
IV- Application à l’astrophysique
Quelles informations l’étude des spectres des étoiles peut-elle nous
fournir ?
On a dit que plus un corps est chauffé à une température élevée, plus le spectre de la lumière
qu’il émet est enrichi en radiations de courtes longueurs d’onde (bleu – violet) :
Le spectre des étoiles que l’on reçoit sur Terre est un spectre d’absorption. En
l’analysant, on peut retrouver les éléments responsables de cette absorption
BARHOUMI MOURAD Page 11 sur 14
La lumière d’une étoile est émise par sa surface (gaz chaud sous forte pression).
Cette lumière traverse l’atmosphère de l’étoile composée de plusieurs gaz sous
faible pression.
==> absorption de radiations,
==> raies noires d’absorption sur le spectre continu de l’étoile.
La position des raies sombres permet de déterminer les entités chimiques
présentes dans l’atmosphère
==> détermination de sa composition chimique.
Ex : Le Soleil est essentiellement composé d’hydrogène H et d’hélium He (92 % et 7,8 %)
Exercice
L’énergie d’un atome d’hydrogène est quantifiée ces valeurs discrètes
vérifient la relation et ne peut prendre que les valeurs suivantes
Eo
En avec n Є N *
n2
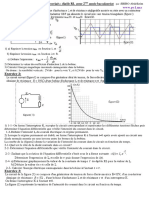
Sur le diagramme de la figure-1 on représente trois niveaux d’énergie de l’atome
d’hydrogène
E (eV)
0 Etat ionisé
Figure-1
-3.4 n=2
-Eo n=1
1-
a- En justifiant , déduire en électron –volts la valeur de Eo
b- Définir l’état fondamental de l’atome d’hydrogène ; quelle est sa valeur
2- La figure -2 représente le spectre de l’atome d’hydrogène
Figure-2
Violet Bleu Vert Rouge
a- S’agit-il d’un spectre d’émission ou d’absorption ?
b- En s’aidant du diagramme d’énergie de la figure-2 justifier le caractère
discontinu du spectre de l’atome d’hydrogène
BARHOUMI MOURAD Page 12 sur 14
3- Sachant que l’atome d’hydrogène passe du niveau d’énergie correspondant à p au
niveau n ( p > n)
a- Préciser si l’atome absorbe ou perd de l’énergie au cours de cette transition
b- Montrer que la longueur d’onde de la radiation associée à cette transition
est donnée par la relation suivante
( n2 x p2 )
9.12x10- 8 x 2 en (mètre) ; n , p Є N * (p>n)
( p - n2 )
c- Calculer pour n=2 et p=3
4- L’atome d’hydrogène étant dans un état correspondant au niveau n=3 , il est
éclairé par une lumière monochromatique de longueur d’onde = 1.28 m
Sachant que l’atome d’hydrogène absorbe cette radiation dans quel nouvel état se
trouve l’atome
5- L’atome d’hydrogène étant dans un état correspondant au niveau n=3 , il reçoit un
photon d’énergie E1= 2.5 eV
a- Calculer l’énergie nécessaire pour ioniser l’atome d’hydrogène se trouvant à
l’état n=3
b- En déduire que le photon d’énergie E1 peut arracher un électron
c- Calculer son énergie cinétique
1eV= 1.6x10-19 J, h=6.62 x10-34 J.s-1 ; C=3.108 m.s-1
Correction
1-
Eo
a- E 2 => Eo= - 4xE2=-4 x (-3.4)=13.6 eV
22
b- C’est l’état le plus stable correspondant au niveau d’énergie le plus
bas E1=-Eo=-13.6 eV
2-
a- Il s’agit d’un spectre d’émission : c’est le résultat de la dispersion du
faisceau lumineux émis par l’atome d’hydrogène
b- Chaque raie d’un spectre est associée à l’émission ou l’absorption
d’un photon lors d’une transition atomique donc les échanges
d’énergies entre la matière et la lumière se font de manière
discontinue
3-
Eo Eo
a- p > n p2 > n2 - p2 < -n2 - 2
p2 n
Ep > En => Ep,n= En-Ep < 0
=> l’atome perdre de l’énergie sous forme d’un rayonnement
BARHOUMI MOURAD Page 13 sur 14
b- hνp,n = - ΔEp,n=En,p
= Ep-En
hxC Eo Eo 1 1 p 2 n2
- 2 - (- 2 ) Eo( 2 2 ) Eo( 2 2 )
p n n p p xn
hxC p 2 xn2 6.62x1034 x3.108 p 2 xn2 2
8 p xn
2
( ) 9.12 x10 en mètre)
Eo p 2 n2 13.6 x1.6 x1019 p 2 n2 p 2 n2
p 2 xn2 32 x 2 2
c- n=2 et p=3 = 9.12x108 9.12x108 x10-6 m
p 2 n2 32 2 2
p 2 x32 p 2 x9
x= 9.12x108
9
4- n=3 et p= ? = 92
p 2 32 p 9
2
14 p
5 14
92 p2= ( ) x9 p=5
14 p 5
13.6
5- a- Ei= Ei- E3= 1.51 eV
32
b- E1>Ei l’énergie du photon est supérieure à Ei donc ce photon
ionise l’atome d’hydrogène initialement à l’état excité n=3
c- Ec= E1-Ei =2.5-1.51=0.99 eV
BARHOUMI MOURAD Page 14 sur 14
Vous aimerez peut-être aussi
- Exercices d'optique et d'électromagnétismeD'EverandExercices d'optique et d'électromagnétismeÉvaluation : 5 sur 5 étoiles5/5 (1)
- Séries D'exercices N°1 Et 2 - Le Champ Magnétique Créé Par Un Courant Électrique - Dr. Karam OuharouDocument3 pagesSéries D'exercices N°1 Et 2 - Le Champ Magnétique Créé Par Un Courant Électrique - Dr. Karam Ouharouأكاديمية التأكدم - Taakdom Academy100% (4)
- Correction Série #15 PhysiqueDocument6 pagesCorrection Série #15 PhysiqueSiham Darif100% (4)
- Série de 11 Exercices Circuit RCDocument14 pagesSérie de 11 Exercices Circuit RCben zayed aliPas encore d'évaluation
- Resume Du Cours Avec Serie Corrigees RLC LIBRE Lycee Pilote Sfax MR Boussarsar HediDocument6 pagesResume Du Cours Avec Serie Corrigees RLC LIBRE Lycee Pilote Sfax MR Boussarsar HediEmna Träad88% (8)
- 1 Exercices Les Ondes Mecaniques ProgressivesDocument7 pages1 Exercices Les Ondes Mecaniques ProgressivesHAMADA197270% (10)
- Physique Des Particules - MarleauDocument282 pagesPhysique Des Particules - MarleauFils100% (1)
- Exercices Corrigés: Le Dipôle RLDocument4 pagesExercices Corrigés: Le Dipôle RLحميد خلفاوي100% (5)
- Cours de Renforcement: Série D'exercices Champ MagnétiqueDocument2 pagesCours de Renforcement: Série D'exercices Champ Magnétiquealphonse100% (1)
- TD Oscillations Mécaniques LibresDocument2 pagesTD Oscillations Mécaniques LibresMohieddine Khaili100% (3)
- Acide Et Base - DosageDocument33 pagesAcide Et Base - Dosagemohamed saidi50% (2)
- Examen Blanc Physique Chimie Bac DDocument4 pagesExamen Blanc Physique Chimie Bac Dkouassi hermann ulrich koffi100% (1)
- BAC BLANC - V FDocument7 pagesBAC BLANC - V FHAMADA1972100% (1)
- Cours Mécanique Quantique by RayDocument62 pagesCours Mécanique Quantique by RayHousseini Dan BouzouaPas encore d'évaluation
- Dipole RL Exercices Non Corriges 4 2Document5 pagesDipole RL Exercices Non Corriges 4 2Marouane Zakir100% (1)
- Travaux Dirigés D'induction N°3: Exercice 1: Rails de Laplace VerticauxDocument4 pagesTravaux Dirigés D'induction N°3: Exercice 1: Rails de Laplace VerticauxEL Ansari Jalal100% (1)
- Devoir N 1SII 2021 Bac BiofDocument4 pagesDevoir N 1SII 2021 Bac Biofالغزيزال الحسن EL GHZIZAL Hassane100% (1)
- 7-Equilibre D'un Solide en Rotation Autour D'un Axe FixeDocument7 pages7-Equilibre D'un Solide en Rotation Autour D'un Axe FixeMed Elyoubi83% (6)
- Chimie (07 Points) : SujetDocument3 pagesChimie (07 Points) : SujetSarah Sara50% (2)
- Série D'exercices 6, Dipôle RC, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHID PDFDocument9 pagesSérie D'exercices 6, Dipôle RC, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHID PDFFadwa KouhraPas encore d'évaluation
- 6 Spectre Atomique 4sc 1Document9 pages6 Spectre Atomique 4sc 1Mohsen Arfaoui0% (1)
- Exercices 3 Dipôle RC Non CorrigeDocument7 pagesExercices 3 Dipôle RC Non CorrigeIsmail Aboutabit0% (1)
- Série de Révision (++corrigé) N°11 ..Spectres Atomiques PDFDocument7 pagesSérie de Révision (++corrigé) N°11 ..Spectres Atomiques PDFMoufida Zouaghi100% (1)
- Spectre CoursDocument7 pagesSpectre CoursJerbi Ines0% (1)
- Série D'exercices - Physique RLC Amortie - Bac Sciences Exp (2012-2013) MR Barhoumi Ezedine PDFDocument4 pagesSérie D'exercices - Physique RLC Amortie - Bac Sciences Exp (2012-2013) MR Barhoumi Ezedine PDFAzizElheniPas encore d'évaluation
- Série 2 Chimie Structure de La Matière À L'échelle MicroscopiqueDocument3 pagesSérie 2 Chimie Structure de La Matière À L'échelle MicroscopiqueSamou_haa100% (2)
- 1er DS - 2bsmbiof-2018-2019Document3 pages1er DS - 2bsmbiof-2018-2019khalid71% (7)
- ' ' Premier Exercice (7 Points) Pendule Élastique HorizontalDocument6 pages' ' Premier Exercice (7 Points) Pendule Élastique HorizontalAli Rammal50% (2)
- Noyaux Masse Et EnergieDocument6 pagesNoyaux Masse Et EnergieDadati Sou100% (1)
- Cours-1 - Un Modèle de L'atome PDFDocument4 pagesCours-1 - Un Modèle de L'atome PDFAyoub Ben MlahPas encore d'évaluation
- Interaction Onde MatièreDocument6 pagesInteraction Onde Matièreأسماء النخليPas encore d'évaluation
- PH9 (Spectre Atomique)Document8 pagesPH9 (Spectre Atomique)Seif Souid91% (11)
- Cours - Sciences Physiques - Modele de L'atome - 2ème Sciences (2016-2017) MR Ghouili MondherDocument2 pagesCours - Sciences Physiques - Modele de L'atome - 2ème Sciences (2016-2017) MR Ghouili MondherRAY EVOLUTION100% (3)
- Serie-Onde Mécanique ProgressiveDocument4 pagesSerie-Onde Mécanique ProgressiveBarhoumi MouradPas encore d'évaluation
- C1Phy Ondes Mecaniques ProgressivesDocument2 pagesC1Phy Ondes Mecaniques Progressiveskarimzid100% (1)
- Série 1 - Les Réactions D'oxydo-RéductionsDocument20 pagesSérie 1 - Les Réactions D'oxydo-RéductionsMed Amine Hattaki100% (3)
- Cours Bobine Dipole RLDocument17 pagesCours Bobine Dipole RLMoufida Zouaghi0% (1)
- Modèle 21 PR ISMAIL ARAIBACHDocument3 pagesModèle 21 PR ISMAIL ARAIBACHaya yami100% (6)
- Cours Lycée Pilote - Physique Intéraction Onde-Matière - Bac Sciences Exp (2010-2011) MR Sfaxi SalahDocument8 pagesCours Lycée Pilote - Physique Intéraction Onde-Matière - Bac Sciences Exp (2010-2011) MR Sfaxi SalahAmel Ben Yahia67% (3)
- Le Courant Electrique Continu Exercices Non Corriges 1Document3 pagesLe Courant Electrique Continu Exercices Non Corriges 1maryam zagriri100% (1)
- تمارين حول التكهرب 4م مع الحل بالفرنسيةDocument22 pagesتمارين حول التكهرب 4م مع الحل بالفرنسيةRayane MarmiPas encore d'évaluation
- Cours 5 PR Pr. Hicham Mahajar Pr. Youssef TabitDocument6 pagesCours 5 PR Pr. Hicham Mahajar Pr. Youssef TabitKratus ATREUS100% (1)
- Exercices Dipole RLDocument2 pagesExercices Dipole RLMajed GharibPas encore d'évaluation
- Série D'exercices - Physique Oscillations Libres Amorties Et Non Amorties - Bac Sciences Exp (2010-2011) MR Baccari. Anis PDFDocument8 pagesSérie D'exercices - Physique Oscillations Libres Amorties Et Non Amorties - Bac Sciences Exp (2010-2011) MR Baccari. Anis PDFAzizElheni100% (2)
- 1bac SX-SM L'energie Electrique Cours ExercicesDocument12 pages1bac SX-SM L'energie Electrique Cours ExercicesAmine AlaoUii Alaoui50% (2)
- Série 8 Physique Mouvement D'un SolideDocument4 pagesSérie 8 Physique Mouvement D'un SolideSamou_haa100% (2)
- OMPPBIOFDocument3 pagesOMPPBIOFYassir Ksakass25% (4)
- Activité 1: Charge Et Décharge D'un Condensateur: ExploitationDocument5 pagesActivité 1: Charge Et Décharge D'un Condensateur: ExploitationFATIMA fatiii100% (2)
- La Pile AlcalineDocument5 pagesLa Pile Alcalinechada100% (1)
- TP Esterification 2015Document2 pagesTP Esterification 2015Daghsni Said100% (8)
- Devoir Examen de TP N°1 - Sciences Physiques - 2ème Sciences Exp (2015-2016) MR Galaï AbdelhamidDocument2 pagesDevoir Examen de TP N°1 - Sciences Physiques - 2ème Sciences Exp (2015-2016) MR Galaï AbdelhamidNadia NadiaPas encore d'évaluation
- Série D'exercices Corrigés Dipole RL 2ème A Bac p.SBIRO Abdelkrim (WWW - Pc1.ma)Document15 pagesSérie D'exercices Corrigés Dipole RL 2ème A Bac p.SBIRO Abdelkrim (WWW - Pc1.ma)moustapha00100% (3)
- Chapitre 9, Oscillations Forcées Dans Un Circuit RLC Série, Cours, Acivités, Exercices D'application, 2BAC BIOF, PR JENKAL RACHID, ChtoukaphysiqueDocument12 pagesChapitre 9, Oscillations Forcées Dans Un Circuit RLC Série, Cours, Acivités, Exercices D'application, 2BAC BIOF, PR JENKAL RACHID, ChtoukaphysiqueSamir JemniPas encore d'évaluation
- Série D'exercices - Sciences Physiques Dipôle RC - Bac Technique (2011-2012) MR FRADIDocument2 pagesSérie D'exercices - Sciences Physiques Dipôle RC - Bac Technique (2011-2012) MR FRADIWiem Benchahboun0% (1)
- Caracteristiques de Quelque Dipoles Passifs Corrige Serie D ExercicesDocument7 pagesCaracteristiques de Quelque Dipoles Passifs Corrige Serie D ExercicesWougens Vincent100% (2)
- Ondes Mecaniques Progressives Serie D Exercices 1 2Document5 pagesOndes Mecaniques Progressives Serie D Exercices 1 2Ťăhã Êìî67% (3)
- NUCLEDocument11 pagesNUCLEEL Omrani SaidPas encore d'évaluation
- Ultrasons MétalDocument4 pagesUltrasons MétalAicha Daou100% (6)
- I - Spectres Atomiques: Sources LumineusesDocument6 pagesI - Spectres Atomiques: Sources Lumineusesmabroukanas69Pas encore d'évaluation
- Les Spectres Atomiques (2) XDocument7 pagesLes Spectres Atomiques (2) Xbbea59bb19Pas encore d'évaluation
- Chapitre III Partie 1Document26 pagesChapitre III Partie 1EzadoraPas encore d'évaluation
- Chimie 1 Chap3 (2) - 1Document8 pagesChimie 1 Chap3 (2) - 1Zehnouni AbderezakPas encore d'évaluation
- Cours Lycée Pilote - Physique Puissance Et Energie Électrique - 2ème Sciences Exp (2013-2014) MR Djebbi Ahmed PDFDocument3 pagesCours Lycée Pilote - Physique Puissance Et Energie Électrique - 2ème Sciences Exp (2013-2014) MR Djebbi Ahmed PDFBassouma Khmas100% (1)
- Cours Lycée Pilote - Physique Puissance Et Energie Électrique - 2ème Sciences Exp (2013-2014) MR Djebbi Ahmed PDFDocument3 pagesCours Lycée Pilote - Physique Puissance Et Energie Électrique - 2ème Sciences Exp (2013-2014) MR Djebbi Ahmed PDFBassouma Khmas100% (1)
- Cinétique Chimique 2010 2011 (Becha Adel)Document1 pageCinétique Chimique 2010 2011 (Becha Adel)Bassouma KhmasPas encore d'évaluation
- Cours - Chimie - Dosage Acido-Basique - Bac Toutes Sections (2019-2020) MR Sfaxi SalahDocument3 pagesCours - Chimie - Dosage Acido-Basique - Bac Toutes Sections (2019-2020) MR Sfaxi SalahBassouma Khmas75% (4)
- Les 7 Merveilles de La MécaniqueDocument10 pagesLes 7 Merveilles de La MécaniqueHassan BelqaidPas encore d'évaluation
- Théorie de La Fonctionnelle de La Densité - Iramis - CEADocument35 pagesThéorie de La Fonctionnelle de La Densité - Iramis - CEAbmalki68Pas encore d'évaluation
- CH3 - Introduction À La Mécanique Quantique-1 PDFDocument27 pagesCH3 - Introduction À La Mécanique Quantique-1 PDFYoussoufa Hamadou babaPas encore d'évaluation
- Elemchim CC2 2014 Corr PDFDocument2 pagesElemchim CC2 2014 Corr PDFNour TaboubiPas encore d'évaluation
- Theorie Wien2kDocument26 pagesTheorie Wien2kMounia75% (4)
- CoursMaster1 PDFDocument17 pagesCoursMaster1 PDFouijdane marocPas encore d'évaluation
- Photon 2Document17 pagesPhoton 2Ahmed BahPas encore d'évaluation
- Cours INM2Document36 pagesCours INM2Yves-donald MakoumbouPas encore d'évaluation
- L Atome CoursDocument2 pagesL Atome CoursMohamed OOPas encore d'évaluation
- Controle 6Document2 pagesControle 6Khalid ZegPas encore d'évaluation
- Action Fantôme À DistanceDocument3 pagesAction Fantôme À DistanceFranckPas encore d'évaluation
- Atmol PDFDocument9 pagesAtmol PDFfaslaPas encore d'évaluation
- Cours 02 Interactions Lumière-Matière (Semi-Conducteur)Document4 pagesCours 02 Interactions Lumière-Matière (Semi-Conducteur)Khettab100% (1)
- O2 PDFDocument28 pagesO2 PDFmokhtarkanPas encore d'évaluation
- Atomistique PSIDocument28 pagesAtomistique PSIRebecca Jackson100% (1)
- Plan PHQ 637Document4 pagesPlan PHQ 637Abdelbassit Abdessamed SenhadjiPas encore d'évaluation
- 2017-Liban-Exo3-Sujet-Atomes Froids-5ptsDocument3 pages2017-Liban-Exo3-Sujet-Atomes Froids-5ptsYasmine BenrahhalPas encore d'évaluation
- CHAPITRE 3 Le Modèle QuantiqueDocument16 pagesCHAPITRE 3 Le Modèle QuantiqueFred MazoyerPas encore d'évaluation
- Einstein DamourDocument9 pagesEinstein Damourwawaou412Pas encore d'évaluation
- Theorie Quantique Des Champs IIDocument181 pagesTheorie Quantique Des Champs IIdani_cirig100% (1)
- Regle FermiDocument2 pagesRegle FermiAhlem MalaouiPas encore d'évaluation
- Chimie QuantiqueDocument145 pagesChimie QuantiqueAbdelhakim BailalPas encore d'évaluation
- Cours Liaisons Chimique SMPC s2 Faculte Des Science FesDocument28 pagesCours Liaisons Chimique SMPC s2 Faculte Des Science FesOussama Maacha100% (4)
- Controle1 1011 PDFDocument2 pagesControle1 1011 PDFKhlidPas encore d'évaluation
- Laruelle Philosophie Non Standard IndiceDocument9 pagesLaruelle Philosophie Non Standard Indicefrederickarias100% (1)
- Module 1.4 1 Sous TitresDocument4 pagesModule 1.4 1 Sous TitresAllal ChafiaPas encore d'évaluation
- ch1 Configurations ElectroniquesDocument10 pagesch1 Configurations ElectroniquesFarouk ZeaniPas encore d'évaluation