Académique Documents
Professionnel Documents
Culture Documents
Os Chimie ch2 Ex Suppl Corr 1694611968
Transféré par
Hajar LferdTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Os Chimie ch2 Ex Suppl Corr 1694611968
Transféré par
Hajar LferdDroits d'auteur :
Formats disponibles
Nom : Groupe : Date :
Exercices supplémentaires CORRIGÉ
CHAPITRE 2 :
LE COMPORTEMENT DES GAZ
2.1 LES LOIS SIMPLES DES GAZ
1. Lequel des énoncés suivants est vrai ?
A. Si le volume d’un gaz double, le mouvement des particules de gaz sera nécessairement
deux fois plus grand.
B. Si le volume d’un gaz double, le nombre de collisions subies par les particules de gaz
sera nécessairement deux fois moins grand.
C. Si le volume d’un gaz double, le nombre de particules de gaz sera nécessairement
deux fois plus grand.
X D. Si le volume d’un gaz double, l’espace occupé par les particules de gaz sera nécessairement
deux fois plus grand.
2. Un gaz occupe un volume de 250,0 ml à une pression de 750 mm Hg et à une température
de 27,0 °C. Si la température demeure constante, quel sera le volume de ce gaz à une pression
de 915 mm Hg ?
1. V2 = ?
2. V1 = 250,0 ml
P1 = 750 mm Hg
T1 = 27,0 °C
P2 = 915 mm Hg
T2 = 27,0 °C
P1 V1
3. P1V1 = P2V2, d’où V2 =
P2
750 mm Hg × 250,0 ml
4. V2 = = 204,9 ml
915 mm Hg
Réponse :
Le volume de ce gaz sera de 205 ml.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
1
Nom : Groupe : Date :
3. Gracia introduit 3,0 L de diazote dans un ballon à une température de 22,0 °C. Quel sera le volume
du gaz s’il est chauffé jusqu’à 85,5 °C, mais que sa pression est maintenue constante ?
1. V2 = ?
2. V1 = 3,0 L
T1 = 22,0 °C + 273 = 295,0 K
T2 = 85,5 °C + 273 = 358,5 K
V1 V2 V1 × T 2
3. = , d’où V2 =
T1 T2 T1
3,0 L × 358,5 K
4. V2 = = 3,6 L
295,0 K
Réponse :
Le volume du gaz sera de 3,6 L.
4. Une certaine quantité d’air est introduite aux conditions ambiantes dans un cylindre métallique.
Quelle sera la pression si le cylindre est chauffé jusqu’à 300 °C ?
1. P2 = ?
2. P1 = 101,3 kPa
T1 = 25 °C + 273 = 298 K
T2 = 300 °C + 273 = 573 K
P1 P2 P1 × T 2
3. = , d’où P2 =
T1 T2 T1
101,3 kPa × 573 K
4. P2 = = 194,8 kPa
298 K
Réponse :
La pression sera de 195 kPa.
5. Deux contenants identiques renferment chacun un gaz à la même température et à la même pression.
Lequel des énoncés suivants décrit le mieux leur contenu ?
A. Les deux contenants renferment la même masse de gaz.
B. Les deux contenants renferment le même nombre d’atomes.
X C. Les deux contenants renferment le même nombre de particules de gaz.
D. Les deux contenants renferment le même gaz.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
2
Nom : Groupe : Date :
6. Deux ballons identiques sont soumis aux mêmes conditions de température et de pression.
Le premier contient 2,43 g de dihydrogène, tandis que le deuxième contient 76,82 g d’un gaz inconnu.
Parmi les choix suivants, lequel est probablement ce gaz inconnu ?
SO2, O2, N2O4, Cu.
1. Mx = ?
2. mH2 = 2,43 g
mx = 76,82 g
m m
3. M = , d’où n =
n M
4. Calcul du nombre de moles de H2
mH2 2,43 g
nH2 = = = 1,20 mol
MH2 2,02 g/mol
Selon l’hypothèse d’Avogadro
nx = nH2 = 1,20 mol
Calcul de la masse molaire du gaz inconnu
mx 76,82 g
Mx = = = 64,0 g/mol
nx 1,20 mol
Réponse :
Le gaz inconnu est probablement du SO2 (dioxyde de soufre).
7. Un ballon contient 0,25 g de dioxyde de carbone (CO2) à une température de 25 °C et à une pression
de 760 mm Hg. Quel est le volume occupé par le gaz ?
1. V = ?
2. m = 0,25 g
T = 25 °C
P = 760 mm Hg
3. À TAPN, 1 mol de gaz occupe un volume de 24,5 L.
m m
M = , d’où n =
n M
4. Calcul du nombre de moles de CO2
0,25 g
n= = 5,68 × 10-3 mol
44,01 g/mol
Calcul du volume de CO2
24,5 L ?L
=
1 mol 5,68 × 10-3 mol
24,5 L × 5,68 × 10-3 mol
= 0,139 L
1 mol
Réponse :
Le gaz occupe un volume de 0,14 L.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
3
Nom : Groupe : Date :
8. Pour réaliser une expérience, vous disposez du protocole suivant :
Matériel
1 seringue
1 bécher rempli d’eau
1 thermomètre
1 plaque chauffante
1 manomètre
1 bonbonne de gaz
Manipulations
Introduire une certaine quantité de gaz dans la seringue.
Relier la seringue au manomètre.
Plonger la seringue dans l’eau.
Déposer le bécher contenant la seringue sur la plaque chauffante.
Chauffer le bécher. À intervalles réguliers de température, faire varier le volume de gaz
dans la seringue de manière à maintenir la pression constante.
Noter les résultats.
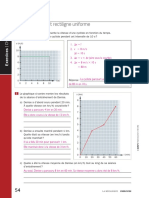
Quel graphique représente le mieux la relation mathématique étudiée au cours
de cette expérimentation ?
A. X B.
C. D.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
4
Nom : Groupe : Date :
2.2 LA LOI GÉNÉRALE DES GAZ
1. Un contenant de 2,0 L renferme du dioxygène à une température de 20 °C et une pression
de 100 kPa. Un second contenant de 2,0 L renferme du dihydrogène aux mêmes conditions
de température et de pression. Lequel des énoncés suivants est vrai ?
A. La vitesse moyenne des molécules de dihydrogène est égale à la vitesse moyenne
des molécules de dioxygène.
B. Le nombre de collisions que subissent les molécules de dihydrogène est le même que celui
que subissent les molécules de dioxygène.
X C. L’énergie cinétique moyenne des molécules de dihydrogène est égale à l’énergie cinétique
moyenne des molécules de dioxygène.
D. La distance entre les molécules de dihydrogène est plus grande que celle entre les molécules
de dioxygène.
2. Une seringue contient une mole de diazote. Si on désire quadrupler la pression de cet échantillon
de gaz, on peut :
A. doubler la température absolue et doubler le volume.
X B. doubler la température absolue et diminuer le volume de moitié.
C. quadrupler la température tout en maintenant le volume constant.
D. quadrupler le volume tout en maintenant la température constante.
3. Une certaine quantité de gaz, soit 4,50 mol, occupe un volume de 15,0 L et exerce une pression de
456 kPa à une température de 26,0 °C. Quel sera le volume de ce gaz si on augmente la température
jusqu’à 78,0 °C, qu’on diminue la pression de 100 kPa et qu’on ajoute 2,00 mol de gaz ?
1. V2 = ?
2. V1 = 15,0 L
P1 = 456 kPa
P2 = 356 kPa
T1 = 26,0 °C + 273 = 299,0 K
T2 = 78,0 °C + 273 = 351,0 K
n1 = 4,50 mol
n2 = 4,50 mol + 2,00 mol = 6,50 mol
P1 V1 P2 V2 P1V1n2T2
3. = , d’où V2 =
n1T1 n2T2 n1T1P2
456 kPa × 15,0 L × 6,50 mol × 351,0 K
4. V2 = = 32,579 L
4,50 mol × 299,0 K × 356 kPa
Réponse :
Le volume sera de 32,6 L.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
5
Nom : Groupe : Date :
4. Un gaz exerce une pression de 1126 kPa. Quelle sera la nouvelle pression exercée si on triple
le volume du gaz, qu’on diminue sa température absolue de moitié et qu’on laisse échapper le tiers
de ses particules ?
1. P2 = ?
2. P1 = 1126 kPa
V1 = x
V2 = 3x
T1 = y
y
T2 =
2
n1 = z
2
n2 = z
3
P1 V1 P2 V2 P1V1n2T2
3. = , d’où P2 =
n1T1 n2T2 n1T1V2
2 y
1126 kPa × x × z ×
3 2
4. P2 = = 125,1 kPa
z × y × 3x
Réponse :
La nouvelle pression exercée sera de 125,1 kPa.
5. On enferme une certaine quantité de gaz dans un ballon. Quel devrait être son volume initial,
aux conditions ambiantes, pour que ce volume soit de 5,0 L à une pression de 245 kPa
et à une température de 115 °C?
1. V1 = ?
2. P1 = 101,3 kPa
P2 = 245 kPa
V2 = 5,0 L
T1 = 25 °C + 273 = 298 K
T2 = 115 °C + 273 = 388 K
P1 V1 P2 V2 P2V2T1
3. = , d’où V1 =
T1 T2 T 2 P1
245 kPa × 5,0 L × 298 K
4. V1 = = 9,29 L
388 K × 101,3 kPa
Réponse :
Le volume initial de ce gaz devrait être de 9,3 L.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
6
Nom : Groupe : Date :
2.3 LA LOI DES GAZ PARFAITS
1. Lequel des énoncés suivants permet de définir un gaz parfait ?
A. Un gaz qui a une masse volumique de 22,4 g/L à TPN.
X B. Un gaz qui frappe les obstacles sans aucune perte d’énergie.
C. Un gaz qui n’a aucune réactivité chimique.
D. Un gaz qui n’a aucun effet néfaste sur l’environnement.
2. Sous quelles conditions le comportement d’un gaz réel se rapproche-t-il le plus de celui
d’un gaz parfait ?
A. À basse température et à basse pression.
B. À basse température et à haute pression.
X C. À haute température et à basse pression.
D. À haute température et à haute pression.
3. Quelle quantité de gaz devrait-on mettre dans un ballon de 10,0 L pour que sa pression soit
de 880 mm Hg à une température de 10,0 °C ?
1. n = ?
2. V = 10,0 L
880 mm Hg × 101,3 kPa
P= = 117,3 kPa
760 mm Hg
T = 10,0 °C + 273 = 283 K
R = 8,314 kPa•L/mol•K
PV
3. PV = nRT, d’où n =
RT
117,3 kPa × 10,0 L
4. n = = 0,499 mol
8,314 kPa•L/mol•K × 283 K
Réponse :
On devrait mettre 0,499 mol de gaz dans le ballon.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
7
Nom : Groupe : Date :
4. Quel est le volume de 48,15 g de méthane (CH4) à TPN ?
Exemple de démarche.
1. V = ?
2. m = 48,15 g
P = 101,3 kPa
T = 0 °C + 273 = 273 K
R = 8,314 kPa•L/mol•K
nRT
3. PV = nRT, d’où V =
m m P
M = , d’où n =
n M
48,15 g
4. n = = 3,000 mol
16,05 g/mol
3,000 mol × 8,314 kPa•L/mol•K × 273 K
V= = 67,2 L
101,3 kPa
Réponse :
Le volume du méthane est de 67,2 L.
5. Une bouteille de 60,00 L contient 800,0 g de dioxygène à une température de 20,0 °C.
Quelle est la pression indiquée sur le manomètre de la bouteille ?
1. P = ?
2. V = 60,00 L
m = 800,0 g
T = 20,0 °C + 273 = 293,0 K
R = 8,314 kPa•L/mol•K
nRT
3. PV = nRT, d’où P =
V
m m
M = , d’où n =
n M
800,0 g
4. n = = 25,00 mol
32,00 g/mol
25,00 mol × 8,314 kPa•L/mol•K × 293,0 K
P= = 1015 kPa
60,00 L
Réponse :
La pression indiquée est de 1015 kPa.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
8
Nom : Groupe : Date :
2.4 LA LOI DES PRESSIONS PARTIELLES
1. Un ballon contient un nombre égal d’atomes d’hélium et d’atomes d’argon. La pression totale
est de 150 kPa. Lequel des énoncés suivants est vrai ?
A. Si l’on retire tout l’hélium du ballon, la pression demeurera inchangée.
B. Si l’on ajoute le même nombre d’atomes de krypton qu’il y a d’atomes d’hélium, la pression
sera trois fois plus grande.
C. Les atomes d'hélium frappent avec la même force que les atomes d’argon.
X D. La pression exercée par l’ensemble des atomes d’hélium est la même que celle exercée
par l’ensemble des atomes d’argon.
2. Un ballon de 10,0 L contient 50,45 g de néon, 12,00 g d’hélium, 79,90 g d’argon et 125,70 g
de krypton. Si la pression partielle de l’hélium est de 75,0 kPa, quelle est la pression totale
dans le ballon ?
Calcul du nombre de moles de chaque gaz
m m
M = , d’où n =
n M
50,45 g
nNe = = 2,500 mol
20,18 g/mol
12,00 g
nHe = = 3,00 mol
4,00 g/mol
79,90 g
nAr = = 2,000 mol0
39,95 g/mol
125,70 g
nKr = = 1,500 mol
83,80 g/mol
g/mol
Calcul de la pression totale
1. PT = ?
2. PpHe = 75,0 kPa
nHe = 3,00 mol
nT = 2,500 mol + 3,00 mol + 2,000 mol + 1,500 mol = 9,00 mol
nA PpHenT
3. PpA = PT , d’où PT =
nT nHe
75,0 kPa × 9,00 mol
4. PT = = 225 kPa
3,00 mol
Réponse :
La pression totale est de 225 kPa.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
9
Nom : Groupe : Date :
3. Du dioxygène est recueilli par déplacement d’eau à une pression de 102,50 kPa et à une température
de 30,0 °C. Quelle est la pression partielle du dioxygène ?
1. PpO2 = ?
2. PT = 102,50 kPa
T = 30,0 °C
PpH2O = 4,24 kPa
3. PT = PpO2 + PpH2O, d’où PpO2 = PT − PpH2O
4. PpO2 = 102,50 kPa − 4,24 kPa = 98,26 kPa
Réponse :
La pression partielle du dioxygène est de 98,26 kPa.
4. Au garage, on gonfle un pneu avec de l’air comprimé composée de 95,0 % de diazote, de 4,0 %
de dioxygène et de traces de plusieurs autres gaz. Si la pression dans le pneu est de 240 kPa,
quelle est la pression partielle du diazote ?
1. PpN2 = ?
2. PT = 240 kPa
nN2 95,0
=
nT 100
nN
3. PpN2 = PT 2
nT
95,0
4. PpN2 = 240 kPa × = 228 kPa
100
Réponse :
La pression partielle du diazote est de 228 kPa.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
10
Nom : Groupe : Date :
SYNTHÈSE DU CHAPITRE 2
1. Un ballon qui contient 3,20 g de dioxygène occupe un volume de 12,0 L. Quel sera son nouveau
volume si on y ajoute 3,50 g d’hélium ?
1. V2 = ?
2. V1 = 12,0 L
mO2 = 3,20 g
mHe = 3,50 g
V1 V2 V1n2
3. = 2, d’où V2 =
n1 n2 n1
m m
M = , d’où n =
n M
3,20 g
4. nO2 = = 0,100 mol
32,00 g/mol
3,50 g
nHe = = 0,875 mol
4,00 g/mol
n2 = 0,100 mol + 0,875 mol = 0,975 mol
12,0 L × 0,975 mol
V2 = = 117 L
0,100 mol
Réponse :
Le nouveau volume sera de 117 L.
2. À une température de 25,0 °C et une pression de 750 mm Hg, Nicolas remplit un ballon d’hélium
jusqu’à ce que le volume atteigne 4,5 L. Il lâche ensuite le ballon, qui s’élève à une altitude de 2000 m,
où la pression diminue à 510 mm Hg et la température, à 15,0 °C. Quel est le nouveau volume
du ballon ?
1. V2 = ?
2. P1 = 750 mm Hg
P2 = 510 mm Hg
V1 = 4,5 L
T1 = 25,0 °C + 273 = 298,0 K
T2 = 15,0 °C + 273 = 288,0 K
P1 V1 P2 V2 P1V1T2
3. = , d’où V2 =
T1 T2 T 1 P2
750 mm Hg × 4,5 L × 288,0 K
4. V2 = = 6,4 L
298,0 K × 510 mm Hg
Réponse :
Le nouveau volume du ballon est de 6,4 L.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
11
Nom : Groupe : Date :
3. Lequel des énoncés suivants ne correspond pas à la description d’un gaz parfait ?
A. Le volume d’une mole d’un gaz parfait est de 22,4 L à TPN.
X B. Un gaz parfait est un gaz qui ne réagit pas chimiquement.
C. Les particules d’un gaz parfait ont une masse, mais leur volume est négligeable.
D. Les particules d’un gaz parfait n’ont aucune interaction entre elles.
E. Un gaz parfait est un gaz qui ne se liquéfie pas, peu importe les conditions de température
et de pression.
4. Deux ballons de verre identiques sont remplis de gaz à la même pression. Le premier ballon contient
2,00 g d’hélium et le deuxième contient 7,00 g de diazote. Que peut-on conclure à propos de la
température de chacun de ces deux gaz ?
1. nHe = ?
nN2 = ?
2. mHe = 2,00 g
mN2 = 7,00 g
m m
3. M = , d’où n =
n M
2,00 g
4. nHe = = 0,500 mol
4,00 g/mol
7,00 g
nN2 = = 0,250 mol
28,02 g/mol
Réponse :
Il y a plus de particules d’hélium que de particules de diazote. Puisqu’il y a une relation
inversement proportionnelle entre le nombre de particules de gaz et la température, à pression
et volume constants, on peut en conclure que la température de l’hélium est plus petite que celle
du diazote.
5. Quelle quantité de gaz devrait-on mettre dans un ballon de verre de 5,00 L pour que la pression soit
de 1245 kPa à une température de 115 °C.
1. n = ?
2. V = 5,00 L
P = 1245 kPa
T = 115 °C + 273 = 388 K
R = 8,314 kPa•L/mol•K
PV
3. PV = nRT, d’où n =
RT
1245 kPa × 5,00 L
4. n = = 1,93 mol
8,314 kPa•L/mol•K × 388 K
Réponse :
On devrait mettre 1,93 mol de gaz dans le ballon de verre.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
12
Nom : Groupe : Date :
6. Lequel des énoncés suivants correspond à la définition du volume molaire d’un gaz ?
A. C’est le volume occupé par n’importe quel gaz à température et pression normales.
X B. C’est le volume occupé par 6,02 × 1023 particules de n’importe quel gaz à une température
et une pression données.
C. C’est le volume occupé par 1,0 g de gaz à une température et une pression données.
D. C’est le volume occupé par n’importe quel gaz aux conditions ambiantes.
7. Un ballon de 3,00 L a une masse de 102,05 g. Lorsqu’on y fait entrer un gaz aux conditions
ambiantes, on constate que la masse passe à 110,76 g. Quel est ce gaz parmi les suivants ?
Cl2, NO2, F2, HCl.
1. M = ?
n=?
2. m = 110,76 g − 102,05 g = 8,71 g
V = 3,00 L
P = 101,3 kPa
T = 25 °C + 273 = 298 K
R = 8,314 kPa•L/mol•K
PV
3. PV = nRT, d’où n =
m RT
M=
n
101,3 kPa × 3,00 L
4. n = = 0,123 mol
8,314 kPa•L/mol•K × 298 K
8,71 g
M= = 70,8 g/mol
0,123 mol
Réponse :
Ce gaz est probablement du Cl2 (dichlore).
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
13
Nom : Groupe : Date :
8. Une bonbonne, dont le manomètre indique une pression de 1200 kPa, contient 100,0 g de dioxygène
et 100,0 g de diazote. Quelle est la pression partielle du diazote contenu dans la bonbonne ?
1. PpN2 = ?
2. PT = 1200 kPa
mO2 = 100,0 g
mN2 = 100,0 g
nN
3. PpN2 = PT 2
nT
m m
M = , d’où n =
n M
100,0 g
4. nO2 = = 3,125 mol
32,00 g/mol
100,0 g
nN2 = = 3,569 mol
28,02 g/mol
nT = 3,125 mol + 3,569 mol = 6,694 mol
3,569 mol
PpN2 = 1200 kPa × = 639,8 kPa
6,694 mol
Réponse :
La pression partielle du diazote est de 639,8 kPa.
DÉFIS DU CHAPITRE 2
1. La masse volumique d’un gaz dépend de sa température et de sa pression. À l’aide de la loi des gaz
parfaits, déterminez une formule qui permettrait de calculer la masse volumique d’un gaz en fonction
de sa pression et de sa température.
La masse volumique (ρ) correspond à m .
La loi des gaz parfaits est PV = nRT. V
Je remplace le « n » dans la formule des gaz parfaits :
m m
M = , d’où n =
n M
mRT
PV =
M
m
J’isole dans cette formule :
V
m PM
ρ= =
V RT
Réponse :
m PM
On peut calculer la masse volumique d’un gaz grâce à la formule : ρ = = .
V RT
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
14
Nom : Groupe : Date :
2. Il est possible de calculer la masse totale que peut soulever un ballon en calculant la différence entre
la masse de l’air déplacé par le ballon et la masse du gaz que contient le ballon. Pour chacune des
situations suivantes, la température autour du ballon est de 22,0 °C et la pression atmosphérique
est de 100 kPa. (Dans ces conditions, on considère que la masse molaire de l’air est de 29,0 g/mol.)
a) Quelle masse un ballon de 2,50 × 105 L gonflé à l’hélium peut-il soulever aux mêmes conditions
de température et de pression que celles de l’air ambiant ?
1. mHe = ?
mair = ?
Masse que peut soulever le ballon = ?
2. P = 100 kPa
V = 2,50 × 105 L
T = 22,0 °C + 273 = 295 K
PV
3. PV = nRT, d’où n =
RT
m
M = , d’où m = M × n
n
100 kPa × 2,50 × 105 L
4. n =
8,314 kPa•L/mol•K × 295 K
= 1,019 × 104 mol
mHe = 1,019 × 104 mol × 4,00 g/mol
= 4,08 × 104 g
mair = 1,019 × 104 mol × 29,0 g/mol
= 2,96 × 105 g
Masse que peut soulever le ballon = mair – mHe
= 2,96 × 105 g – 4,08 × 104 g
= 2,55 × 105 g
Réponse :
Le ballon peut soulever une masse de 2,55 × 105 g.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
15
Nom : Groupe : Date :
b) Quelle masse peut soulever le même ballon gonflé avec de l’air chauffé et maintenu
à une température de 65,0 °C?
1. mair chaud = ?
mair = ?
Masse que peut soulever le ballon = ?
2. P = 100 kPa
V = 2,50 × 105 L
T = 65,0 °C + 273 = 338 K
PV
3. PV = nRT, d’où n =
RT
m
M = , d’où m = M × n
n
100 kPa × 2,50 × 105 L
4. n =
8,314 kPa•L/mol•K × 338 K
= 8,90 × 103 mol
mair chaud = 8,90 × 103 mol × 29,0 g/mol
= 2,58 × 105 g
mair = 2,96 × 105 g
Masse que peut soulever le ballon = mair – mair chaud
= 2,96 × 105 g – 2,58 × 105 g
= 3,80 × 104 g
Réponse :
Le ballon peut soulever une masse de 3,80 × 104 g.
3. À une température de 22,0 °C, une bombe aérosol contient 325 ml de gaz à 445 kPa de pression.
Quel volume de gaz est utilisable aux conditions ambiantes ?
1. V2 = ?
2. T1 = 22,0 °C + 273 = 295,0 K
P1 = 445 kPa
V1 = 325 ml
T2 = 25 °C + 273 = 298 K
P2 = 101,3 kPa
P1 V1 P2 V2 P1V1T2
3. = , d’où V2 =
T1 T2 T 1 P2
445 kPa × 325 ml × 298 K
4. V2 =
295,0 K × 101,3 kPa
= 1442 ml
Volume utilisable de gaz = 1442 ml – 325 ml = 1117 ml
(puisqu’il restera 325 ml dans la bombe aux conditions ambiantes)
Réponse :
Le volume utilisable de gaz est de 1,12 × 103 ml ou de 1,12 L.
Exercices supplémentaires © ERPI Reproduction et/ou modifications autorisées uniquement dans
les classes où les cahiers OPTIONscience – Chimie sont utilisés. OPTIONscience – Chimie
Chapitre 2 N38327
16
Vous aimerez peut-être aussi
- Os Chimie ch4 Ex SupplDocument13 pagesOs Chimie ch4 Ex SupplSarah Taibi El KettaniPas encore d'évaluation
- Os Chimie ch6 Ex Suppl CorrDocument12 pagesOs Chimie ch6 Ex Suppl CorrSarah Taibi El Kettani100% (1)
- 000 Os - Chimie - ch4 - Ex - Suppl - CorrDocument13 pages000 Os - Chimie - ch4 - Ex - Suppl - CorrKhalil OukebdanePas encore d'évaluation
- Os Chimie ch5 Ex Suppl CorrDocument16 pagesOs Chimie ch5 Ex Suppl CorrSarah Taibi El KettaniPas encore d'évaluation
- CHI5062 Eval ch8Document15 pagesCHI5062 Eval ch8Sarah Taibi El KettaniPas encore d'évaluation
- Cahierch4 CORRIGEDocument30 pagesCahierch4 CORRIGESalim SaoudiPas encore d'évaluation
- Corrigé 6.3 ChimieDocument4 pagesCorrigé 6.3 ChimieMaeva SimPas encore d'évaluation
- Évaluation Des Concepts Chapitre 6Document10 pagesÉvaluation Des Concepts Chapitre 6Robert Breton100% (1)
- Os Chimie Corrige Ch1Document16 pagesOs Chimie Corrige Ch1laura sofia brunelle cyr100% (2)
- Chapitre 3Document29 pagesChapitre 3chiraz biotechPas encore d'évaluation
- CHI5062 Eval ch7Document5 pagesCHI5062 Eval ch7Sarah Taibi El KettaniPas encore d'évaluation
- Exercices: La Réactivité Chimique Des GazDocument12 pagesExercices: La Réactivité Chimique Des GazSarah Taibi El Kettani67% (3)
- Chimie Corrige Ch2 Partie1Document8 pagesChimie Corrige Ch2 Partie1Jimmy NguyenPas encore d'évaluation
- Corrige ManuelDocument9 pagesCorrige Manueleyohi86Pas encore d'évaluation
- Mod2 Corrige ch4 Partie2Document6 pagesMod2 Corrige ch4 Partie2api-278378684Pas encore d'évaluation
- Mécanique ch3Document18 pagesMécanique ch3Tanaj Tahya100% (1)
- 3.cinétique Chimique (DR - Chaal)Document9 pages3.cinétique Chimique (DR - Chaal)Neou Phors SoporsPas encore d'évaluation
- Os Opt Corrige Ch3Document24 pagesOs Opt Corrige Ch3RKT100% (1)
- Chimie Corrige ch7 Partie1Document2 pagesChimie Corrige ch7 Partie1api-278378684100% (2)
- Mod2 Corrige ch4 Partie1Document2 pagesMod2 Corrige ch4 Partie1api-278378684100% (1)
- Exercices: Qu'est-Ce Que La Vitesse de Réaction ?Document27 pagesExercices: Qu'est-Ce Que La Vitesse de Réaction ?Sarah Taibi El KettaniPas encore d'évaluation
- Os Chimie Corrige ch3 PDFDocument24 pagesOs Chimie Corrige ch3 PDFf.B100% (1)
- Mécanique ch5Document24 pagesMécanique ch5Tanaj Tahya100% (1)
- Mod3 Chimie Corrige ch6 Partie3Document2 pagesMod3 Chimie Corrige ch6 Partie3api-278378684100% (1)
- Mécanique ch4Document18 pagesMécanique ch4Tanaj Tahya100% (1)
- Exercices: L'énergie Et Ses FormesDocument29 pagesExercices: L'énergie Et Ses FormesSarah Taibi El Kettani100% (2)
- Mod3 Chimie Corrige ch6 Partie2Document1 pageMod3 Chimie Corrige ch6 Partie2api-278378684100% (1)
- Mécanique ch2Document19 pagesMécanique ch2Tanaj TahyaPas encore d'évaluation
- Mécanique ch1Document18 pagesMécanique ch1Tanaj TahyaPas encore d'évaluation
- Os Chimie Corrige Ch6Document52 pagesOs Chimie Corrige Ch6Said SouhassouPas encore d'évaluation
- Os Chimie Corrige ch3 PDFDocument24 pagesOs Chimie Corrige ch3 PDFFaria Haque0% (1)
- Os Chimie Corrige Ch8Document66 pagesOs Chimie Corrige Ch8Said Souhassou0% (1)
- Mod4 Corrige ch7 Partie3Document1 pageMod4 Corrige ch7 Partie3api-278378684100% (1)
- AlcèneDocument6 pagesAlcènechristophe100% (1)
- CinhDocument8 pagesCinhbeebac2009Pas encore d'évaluation
- Corrigé DevoirDocument9 pagesCorrigé DevoirKevin Beauchamp100% (2)
- Mod3 Chimie Corrige ch6 1Document5 pagesMod3 Chimie Corrige ch6 1api-278378684100% (1)
- Mod4 Corrige ch8 ExerciceDocument5 pagesMod4 Corrige ch8 Exerciceapi-278378684100% (1)
- B5.2 Sujet TP1 - Dosage Par Étalonnage Et IncertitudesDocument2 pagesB5.2 Sujet TP1 - Dosage Par Étalonnage Et Incertitudespenelopeouali2006Pas encore d'évaluation
- Cinetique Chimique CoursDocument50 pagesCinetique Chimique CoursBeenani BeenaniPas encore d'évaluation
- CHAPITRE 1 Partie 2Document14 pagesCHAPITRE 1 Partie 2hamid ibbakhPas encore d'évaluation
- Python Exemple 3Document2 pagesPython Exemple 3Lazhar BOUCHAOURPas encore d'évaluation
- Cours Thermo - Chapitre 7. Solutions Réelles - 2019Document27 pagesCours Thermo - Chapitre 7. Solutions Réelles - 2019ait hssainPas encore d'évaluation
- 2nde Chap 14 Cours Poly CompleteDocument4 pages2nde Chap 14 Cours Poly CompleteNour Bouraoui100% (1)
- Fiche TD 01Document2 pagesFiche TD 01wissoubenaouda2110100% (2)
- M28 - Thermo - TD2 - CorrectionDocument4 pagesM28 - Thermo - TD2 - CorrectionHassan DriouachPas encore d'évaluation
- Labo 2Document7 pagesLabo 2Long LuuPas encore d'évaluation
- CHAPITRE 5 Theorie ExercicesDocument80 pagesCHAPITRE 5 Theorie Exercicesrabah mahdiaPas encore d'évaluation
- Ex QCM 2006Document13 pagesEx QCM 2006130660LYC OMAR BENABDELAZIZ NEDROMAPas encore d'évaluation
- QCM Diriges ThermodynamiqueDocument2 pagesQCM Diriges ThermodynamiquedannPas encore d'évaluation
- Thermo 1Document6 pagesThermo 1Oussama El BouadiPas encore d'évaluation
- CHP 7 La Pile ElectrochimiqueDocument4 pagesCHP 7 La Pile ElectrochimiqueAida Ben ChaabenePas encore d'évaluation
- Cours Électrochimie Et Cinétique PDFDocument44 pagesCours Électrochimie Et Cinétique PDFSa ElPas encore d'évaluation
- Thermodynamique PDFDocument18 pagesThermodynamique PDFKarim MegherfiPas encore d'évaluation
- Chimie SolutionDocument164 pagesChimie SolutionZonta NeoPas encore d'évaluation
- Science Secondaire 3Document8 pagesScience Secondaire 3BteiEv1 BteiEv1Pas encore d'évaluation
- 4ème Devoir 1ère C LMJF-GMK 15-16Document3 pages4ème Devoir 1ère C LMJF-GMK 15-16justsdedePas encore d'évaluation
- corrigerevisionfinannee_2 (1)Document27 pagescorrigerevisionfinannee_2 (1)yoimiya pewpewPas encore d'évaluation
- Os Chimie ch6 Ex SupplDocument12 pagesOs Chimie ch6 Ex SupplSarah Taibi El KettaniPas encore d'évaluation
- ExamenDocument2 pagesExamenKenson DEROSANPas encore d'évaluation
- TD N°1 Grandeurs de RéactionDocument4 pagesTD N°1 Grandeurs de RéactionAbdelhamid Elmadani100% (1)
- TD ThermochimieDocument2 pagesTD ThermochimieYossri SallemPas encore d'évaluation
- Cours 03 Physique Chaleur 3Document22 pagesCours 03 Physique Chaleur 3Abde TamPas encore d'évaluation
- Examens Corrige Thermodynamique 2 Session Rattrapage SMP S3 2018 2019Document6 pagesExamens Corrige Thermodynamique 2 Session Rattrapage SMP S3 2018 2019bihi.102.haytamPas encore d'évaluation
- PC 5ème - L6 - Pression AtmosphériqueDocument9 pagesPC 5ème - L6 - Pression Atmosphériquefranck birbaPas encore d'évaluation
- Chapitre 2 3 Et 4Document64 pagesChapitre 2 3 Et 4manelfarah211Pas encore d'évaluation
- Energetique TD1Document1 pageEnergetique TD1Imrane NACHAT100% (1)
- Mécanique Des Fluides #1 - Résumé 23.05.2021Document11 pagesMécanique Des Fluides #1 - Résumé 23.05.2021Mohamed NadjibPas encore d'évaluation
- Memoire de Fin D'Etudes en Vue de L'Obtention Du Diplome Master Academique en Genie Mecanique Option: Optimisation Des Systèmes ÉnergétiquesDocument118 pagesMemoire de Fin D'Etudes en Vue de L'Obtention Du Diplome Master Academique en Genie Mecanique Option: Optimisation Des Systèmes ÉnergétiquesYahia AiouazPas encore d'évaluation
- Vgues de Chaleur (Très Important) BouderDocument102 pagesVgues de Chaleur (Très Important) BouderSalima BensebaaPas encore d'évaluation
- Étude de Système de Climatisation Par Énergie SolaireDocument93 pagesÉtude de Système de Climatisation Par Énergie SolaireSohaila LakhalPas encore d'évaluation
- E.T. Et Terre en PérilDocument14 pagesE.T. Et Terre en PérilsergeduretPas encore d'évaluation
- Adon These Manuscrit 2011Document290 pagesAdon These Manuscrit 2011mulungula isalimyaPas encore d'évaluation
- TD Dynamic ReelsDocument6 pagesTD Dynamic ReelsamalPas encore d'évaluation
- Généralités Sur Les CompresseursDocument20 pagesGénéralités Sur Les CompresseursRaouf BelamriPas encore d'évaluation
- Livre de 11e SCES, Doc Final 2 CorrDocument224 pagesLivre de 11e SCES, Doc Final 2 Corrmrbalmain99100% (1)
- Serie2+3+solutions Elt 2023 1 5Document5 pagesSerie2+3+solutions Elt 2023 1 5Amna Selsabil MokriPas encore d'évaluation
- CHAPITRE IV - Simulateurs en GP - 2023Document25 pagesCHAPITRE IV - Simulateurs en GP - 2023lamis izukuPas encore d'évaluation
- Corrigé de La Série N°2 ThermoDocument4 pagesCorrigé de La Série N°2 ThermoKacem KacemPas encore d'évaluation
- TD1 Intro ThermodynamiqueDocument3 pagesTD1 Intro ThermodynamiqueAytaç AktuğPas encore d'évaluation
- El NiñoDocument7 pagesEl NiñoNatacha DUROSEPas encore d'évaluation
- L'ATMOSPHEREDocument11 pagesL'ATMOSPHEREBenslimane mahmoud100% (1)
- DM1 T-Fluide 2022Document4 pagesDM1 T-Fluide 2022ghassen Ben hlimaPas encore d'évaluation
- Notice Sepam Serie80 Exploitation FR PDFDocument176 pagesNotice Sepam Serie80 Exploitation FR PDFOmar UrreaPas encore d'évaluation
- Simulation Et Optimisation Des Paramètres D'extraction Des Liquides Des Gaz Associé de Complexe ZCINA Hassi MessaoudDocument143 pagesSimulation Et Optimisation Des Paramètres D'extraction Des Liquides Des Gaz Associé de Complexe ZCINA Hassi MessaoudTul IpePas encore d'évaluation
- Statique Des Fluides: J.M. Perrier-CornetDocument21 pagesStatique Des Fluides: J.M. Perrier-CornetBrahim MouhcinePas encore d'évaluation
- Pfe - CopieDocument26 pagesPfe - CopieŸöùcéf Ch100% (1)
- Physique Chapitre13 Gaz ParfaitDocument2 pagesPhysique Chapitre13 Gaz ParfaitFabricePas encore d'évaluation
- Masse Vol Air HumideDocument3 pagesMasse Vol Air HumidePierre ChoquenetPas encore d'évaluation
- Atmosphère Et ClimatDocument4 pagesAtmosphère Et ClimatSoatoavina RANDRIANOMENJANAHARYPas encore d'évaluation
- Le profilage au service du football: Démarche scientifique pour un recrutement et entraînements optimisésD'EverandLe profilage au service du football: Démarche scientifique pour un recrutement et entraînements optimisésPas encore d'évaluation
- Améliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesD'EverandAméliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesÉvaluation : 5 sur 5 étoiles5/5 (2)
- Secrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieD'EverandSecrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieÉvaluation : 5 sur 5 étoiles5/5 (2)
- L'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)D'EverandL'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)Évaluation : 4 sur 5 étoiles4/5 (3032)
- Transformez votre vie: Utilisez le pouvoir créateur qui est en vous pour construire votre vie à l'image de ce que vous voulez qu'elle soitD'EverandTransformez votre vie: Utilisez le pouvoir créateur qui est en vous pour construire votre vie à l'image de ce que vous voulez qu'elle soitÉvaluation : 4 sur 5 étoiles4/5 (14)
- Harmonisation Energétique des Personnes: Manuel de Curothérapie 2020D'EverandHarmonisation Energétique des Personnes: Manuel de Curothérapie 2020Évaluation : 4 sur 5 étoiles4/5 (8)
- La vie des abeilles: Prix Nobel de littératureD'EverandLa vie des abeilles: Prix Nobel de littératureÉvaluation : 4 sur 5 étoiles4/5 (41)
- Électrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsD'EverandÉlectrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Manuel de fabrication du savon: Je fabrique mes savons facilementD'EverandManuel de fabrication du savon: Je fabrique mes savons facilementÉvaluation : 5 sur 5 étoiles5/5 (4)
- Harmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020D'EverandHarmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020Évaluation : 2.5 sur 5 étoiles2.5/5 (3)
- Approvisionnement et traitement de l’eau: Les Grands Articles d'UniversalisD'EverandApprovisionnement et traitement de l’eau: Les Grands Articles d'UniversalisPas encore d'évaluation
- 160 ressources pour se lancer dans la vidéo quand on n’y connait rienD'Everand160 ressources pour se lancer dans la vidéo quand on n’y connait rienPas encore d'évaluation
- 20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsD'Everand20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Enseigner une Langue Etrangère Par l’Apprentissage HybrideD'EverandEnseigner une Langue Etrangère Par l’Apprentissage HybridePas encore d'évaluation
- Théorie relative de la musique: Maîtriser le mouvement par la logique des intervallesD'EverandThéorie relative de la musique: Maîtriser le mouvement par la logique des intervallesÉvaluation : 4 sur 5 étoiles4/5 (1)
- Anatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursD'EverandAnatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursPas encore d'évaluation
- Cancer - Leucémie: Et autres maladies apparemment incurables, mais guérissables avec des moyens naturelsD'EverandCancer - Leucémie: Et autres maladies apparemment incurables, mais guérissables avec des moyens naturelsPas encore d'évaluation
- Semer avec succès pour rassembler avec abundance. Jardin organique et synergique: Calcul des meilleurs jours pour l'ensemencement de chaque légumeD'EverandSemer avec succès pour rassembler avec abundance. Jardin organique et synergique: Calcul des meilleurs jours pour l'ensemencement de chaque légumePas encore d'évaluation
- Cahier de jeux de stimulation cognitive: Sujets Alzheimer, désorientés, démences, amnésiesD'EverandCahier de jeux de stimulation cognitive: Sujets Alzheimer, désorientés, démences, amnésiesPas encore d'évaluation
- Puissance naturelles - Que faire si votre "meilleure partie" est en grève?: Puissance naturelles-améliorer les recours pour augmenter la virilité de la capacité à obtenir une érection de fermetéD'EverandPuissance naturelles - Que faire si votre "meilleure partie" est en grève?: Puissance naturelles-améliorer les recours pour augmenter la virilité de la capacité à obtenir une érection de fermetéÉvaluation : 3.5 sur 5 étoiles3.5/5 (3)
- Un régime quantiqueD'EverandUn régime quantiqueÉvaluation : 5 sur 5 étoiles5/5 (1)
- Le B.A.-Ba de la communication: Comment convaincre, informer, séduire ?D'EverandLe B.A.-Ba de la communication: Comment convaincre, informer, séduire ?Évaluation : 3 sur 5 étoiles3/5 (1)
- Physique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresD'EverandPhysique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresÉvaluation : 5 sur 5 étoiles5/5 (2)
- L'Art de La Magie au Bougie Wicca: Le Guide du Débutant à la Pratique de la Magie au Bougie de WiccaD'EverandL'Art de La Magie au Bougie Wicca: Le Guide du Débutant à la Pratique de la Magie au Bougie de WiccaÉvaluation : 3 sur 5 étoiles3/5 (1)
- Automatique: Les Grands Articles d'UniversalisD'EverandAutomatique: Les Grands Articles d'UniversalisPas encore d'évaluation