Académique Documents
Professionnel Documents
Culture Documents
Controle2 2
Transféré par
amina oubennaiTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Controle2 2
Transféré par
amina oubennaiDroits d'auteur :
Formats disponibles
Devoir 𝑵𝟒 semestre 𝟏 Niveau: 2BIOF
Lycée qualifiant :
Année scolaire: Prof :
Exercice 𝟏 : Questions du cours
Rependre par vrai ou faux (𝑸𝑪𝑴 ∓ 𝟎, 𝟐𝟓) .
❑ Les noyaux stables de 𝒁 < 𝟐𝟎 se trouvent en dessus du premier médiateur .
❑ Les noyaux lourds de 𝒁 > 𝟏𝟗𝟓 se disposent sur le premier médiateur .
❑ La radioactivité est une désintégration contrôlée .
❑ Les noyaux radioactifs 𝜷+ se disposent au dessous de la vallée de stabilité .
❑ Les transformations nucléaires spontanées sont endoénergétiques .
❑ L’énergie de liaison par nucléon est l’énergie qu’il faut fournir à un noyau pour le dissocier
en ses nucléons .
❑ Le défaut de masse d’un noyau est toujours positif .
❑ Le noyau légère se fissionne pour former un noyau plus lourd donc plus stable .
Définir : La radioactivité , L’activité nucléaire .
Exercice 2: La fusion nucléaire
La fusion nucléaire est une transformation nucléaire dans laquelle deux noyaux légers s’assemblent
pour former un noyaux plus stable .
𝟑𝟎
Cet exercice vise à étudier la réaction de fusion suivante : 𝟐𝟕 𝟒 𝑨
𝟏𝟑𝑨𝒍 + 𝟐𝑯𝒆 → 𝟏𝟓𝑷 + 𝒁𝑿
La réaction de fusion est dite thermonucléaire . Expliquer pourquoi ?
En utilisant les lois de conservation de Soddy , déterminer la particule 𝑨𝒁𝑿.
Calculer en 𝑴𝒆𝒗 ∆𝑬 l’énergie consommée par cette réaction de fusion
Déduire en 𝑴𝒆𝒗 puis en joule (𝑱) , l’énergie 𝑬𝑻 consommée par la fusion de deux moles
d’Aluminium 𝟐𝟕 𝟒
𝟏𝟑𝑨𝒍 avec une quantité suffisante en Hélium 𝟐𝑯𝒆 .
Calculer l’énergie de liaison du 𝟐𝟕 𝟑𝟎
𝟏𝟑𝑨𝒍 et celle du 𝟏𝟓𝑷 et déduire le noyau le plus stable .
Noyau ou particule 𝟐𝟕 𝟒 𝟑𝟎 𝟏 𝟏
𝟏𝟑𝑨𝒍 𝟐𝑯𝒆 𝟏𝟓𝑷 𝟎𝒏 𝟏𝑷
Données Masse en (𝒖) 𝟐𝟔, 𝟗𝟕𝟒𝟒𝟎 𝟒, 𝟎𝟎𝟏𝟓𝟎 𝟐𝟗, 𝟗𝟕𝟎𝟎𝟔 𝟏, 𝟎𝟎𝟖𝟔𝟔 𝟏, 𝟎𝟎𝟕𝟐𝟖
𝑵𝑨 = 𝟔, 𝟎𝟐 × 𝟏𝟎𝟐𝟑𝒎𝒐𝒍−𝟏 ; 𝟏𝒖 = 𝟗𝟑𝟏, 𝟓𝑴𝒆𝒗/𝒄𝟐 ; 𝟏𝑴𝒆𝑽 = 𝟏, 𝟔 × 𝟏𝟎−𝟏𝟑𝑱
Exercice 3 La fission nucléaire
𝟐𝟑𝟓 𝟏 𝟏𝟒𝟐
L’une des réaction de fissions de l’uranium est : 𝟗𝟐𝑼 + 𝟎𝒏 → 𝟓𝟔𝐁𝐚 + 𝟗𝟏𝒂𝑲𝒓 + 𝐛 𝟏𝟎𝒏
Déterminer les deux nombres a et b
Vérifier que le défaut de masse du noyau de krypton 𝟗𝟏𝒂𝑲𝒓 est :
∆𝒎 𝟗𝟏𝒂𝑲𝒓 = 𝟎, 𝟖𝟏𝟒𝟗𝟑𝒖
Déduire la valeur de 𝐸𝑙 𝟗𝟏𝒂𝑲𝒓 l’énergie de liaison du noyau 𝟗𝟏𝒂𝑲𝒓
Comparer la stabilité des noyaux : 𝟐𝟑𝟓 𝟗𝟏 𝟏𝟒𝟐
𝟗𝟐𝑼, 𝒂𝑲𝒓, 𝟓𝟔𝐁𝐚
En exploitant le diagramme énergétique déterminer 𝑬𝑳𝒊𝒃 l’énergie
libérée par la fission d’un gramme d’uranium 235 en 𝑀𝑒𝑉 puis en joule
𝐦 𝟗𝟏𝑲𝒓 = 𝟗𝟎, 𝟗𝟐𝟑𝟒𝟓𝒖
Donnée 𝒂
Exercice 𝟒 : Datation d’une roche marine
Le Radium 𝟐𝟐𝟔 se trouve dans les roches marines , résulte de la désintégration spontanée du
Thorium 𝟐𝟑𝟎 au cour du temps . C’est pourquoi que le Radium et Thorium se trouvent dans toutes
les roches marines en proportions différentes , selon leurs dates de formation .
𝑵
La mesure du rapport 𝒓 = 𝑹𝒂 permet de calculer l'âge de la roche marine .
𝑵𝑻𝒉
Donner la composition du noyau du Thorium 𝟐𝟑𝟎 𝟗𝟎𝑻𝒉 .
Le noyau 𝟗𝟎𝑻𝒉 est radioactif , dont le noyau fils est le
𝟐𝟑𝟎
Radium 𝟐𝟐𝟔 𝟖𝟖𝑹𝒂 . Écrire l’équation de désintégration du
Thorium 𝟐𝟑𝟎 𝟗𝟎𝑻𝒉, en précisant la particule émise .
La courbe ci-contre représente l’évolution de 𝒍𝒏 𝒓 + 𝟏
en fonction du temps
𝒂 − Montrer que : 𝐥𝐧 𝐫 + 𝟏 = 𝝀𝒕
𝒃 − En se basant sur la courbe déterminer 𝝀 et déduire
la valeur du temps de demi-vie .
𝐜 − L’étude d’un échantillon de la roche montre 𝒓 = 𝟎, 𝟐𝟑 .
Déterminer 𝒕𝑹 l'âge de l’échantillon .
Calculer l’activité nucléaire 𝒂(𝒕𝑹 ) à l’instant 𝒕𝑹 sachant que le nombre de noyaux du radium dans
l’échantillon à cet instant est : 𝐍 = 𝟒, 𝟑 × 𝟏𝟎𝟐𝟓
Exercice 𝟓 : Equilibre d’un système chimique
L'acide acétique ou acide éthanoïque est un acide organique. Sa formule chimique est
𝑪𝑯𝟑 𝑪𝑶𝑶𝑯. L'acide acétique pur est un liquide incolore et inflammable .
On prépare , une solution aqueuse (𝑺) d’acide éthanoïque de concentration 𝑪 = 𝟓 × 𝟏𝟎−𝟐 𝒎𝒐𝒍/𝑳 et
de volume 𝑽 = 𝟓𝟎𝐦𝑳 . La mesure de 𝒑𝑯 de la solution (𝑺) donne : 𝒑𝑯 = 𝟑, 𝟎𝟐
Ecrire l’équation de la réaction entre l’acide éthanoïque et l’eau .
Dresser le tableau d’avancement de cette réaction en fonction de 𝑪 , 𝑽 , 𝒙 et 𝒙é𝒒
Trouver l’expression du taux l’avancement final de la réaction en fonction de 𝒑𝑯 et 𝑪 . Calculer
sa valeur . Et conclure .
Trouver l’expression de la conductivité 𝝈é𝒒 de la solution en fonction de 𝝀𝟏 et 𝝀𝟐 et la
concentration 𝒑𝑯 . Calculer 𝝈é𝒒
Trouver l’expression de la constante d’équilibre 𝑲 associée à la réaction d’acide éthanoïque
et l’eau en fonction de 𝑪 et 𝒑𝑯 . Calculer sa valeur .
On dilue 𝒏 fois la solution (𝑺) , et on obtient une solution (𝑺’) d’acide éthanoïque de
Puits
concentration: 𝐂 ′
𝒂 −Donner la nouvelle valeur de la constante d’équilibre 𝑲’ ( une justification est demandée )
𝒃 −Choisir la valeur du 𝝉′ de la solution (S’), parmi les valeurs suivantes : 1,9% , 1,03% , 5,77%
𝑪 − Calculer concentration 𝐂 ′ de la solution (S’), et déduire le coefficient de dilution 𝒏 .
On réalise une autre étude ,en utilisant une solution (S’’) d’acide méthanoïque de concentration
𝐂’’ tel que : 𝐂’’ = 𝑪′ . Soit 𝝉′′ le taux d’avancement final de la réaction d’acide
méthanoïque avec l’eau . Comparer 𝝉′′ avec 𝝉′ (la valeur trouvée en question -𝒃) , justifier votre
réponse . La constante d’équilibre associée à la réaction d’acide méthanoïque avec l’eau est :
𝑲’’ = 𝟏, 𝟖 × 𝟏𝟎−𝟒
Données à 𝟐𝟓°𝑪: 𝝀𝟐 = 𝝀𝑯𝟑 𝑶+ = 𝟑𝟓 × 𝟏𝟎−𝟑 𝑺𝒎𝟐 𝒎𝒐𝒍−𝟏 et 𝝀𝟏 = 𝝀𝑪𝑯𝟑 𝑪𝑶𝑶− = 𝟒, 𝟎𝟗 × 𝟏𝟎−𝟑 𝑺𝒎𝟐 𝒎𝒐𝒍−𝟏
Vous aimerez peut-être aussi
- Série Complete Nucleaire Prof Elmnaouar (WWW - Pc1.ma)Document9 pagesSérie Complete Nucleaire Prof Elmnaouar (WWW - Pc1.ma)fardadi rachidPas encore d'évaluation
- Noyaux, Masse Et Énergie FDocument4 pagesNoyaux, Masse Et Énergie Fsihammouatassim3Pas encore d'évaluation
- Correction Du Devoir de La MaisonDocument5 pagesCorrection Du Devoir de La Maisonkiloral445Pas encore d'évaluation
- Decroissance RadioactiveDocument11 pagesDecroissance Radioactivedawd.bouzaherPas encore d'évaluation
- Contrôle 23 (PR Prof Ahmed)Document2 pagesContrôle 23 (PR Prof Ahmed)Mouhibi AbdellahPas encore d'évaluation
- Série D'exercice 2 Nucleaire Et Etat Equilibre ModéfierDocument11 pagesSérie D'exercice 2 Nucleaire Et Etat Equilibre Modéfierdouaabouab2021Pas encore d'évaluation
- Serie Les Piles PCDocument7 pagesSerie Les Piles PCalaeddinePas encore d'évaluation
- PCMterm FS06 RadioactiviteDocument5 pagesPCMterm FS06 RadioactiviteTop KristiouPas encore d'évaluation
- Noyaux Masse Et Énergie - PCDocument11 pagesNoyaux Masse Et Énergie - PCthefreezerisbroken100% (1)
- 2F NucléaireDocument2 pages2F NucléaireSalma ElfaroukiPas encore d'évaluation
- Résumé. Chap1.Décroissance Radioactive 2022Document2 pagesRésumé. Chap1.Décroissance Radioactive 2022Saad Filali Oujdi50% (2)
- CHAPITRE 2 (Radioactivité)Document6 pagesCHAPITRE 2 (Radioactivité)mariecurie.academy19Pas encore d'évaluation
- 5-Cha5-Energie de Cohesion Des SolidesDocument66 pages5-Cha5-Energie de Cohesion Des SolidesAbdelaziz EdPas encore d'évaluation
- Physique Nucleaire PDF (1) - 1Document15 pagesPhysique Nucleaire PDF (1) - 1alseiny923Pas encore d'évaluation
- CH1 DiélectriquesDocument24 pagesCH1 DiélectriquesOUSSAMA AHAKKARPas encore d'évaluation
- Serie 6 Noyaux, Energie Masse 2023Document4 pagesSerie 6 Noyaux, Energie Masse 2023hamza elkarmiPas encore d'évaluation
- Lycee Qualiant Tha Housseine Devoir 2 2Pcf 2022/2023Document2 pagesLycee Qualiant Tha Housseine Devoir 2 2Pcf 2022/2023yassine wxahdiPas encore d'évaluation
- Décroissance radioactive-cours-FRDocument7 pagesDécroissance radioactive-cours-FRبدر الذهابيPas encore d'évaluation
- Série 2Document9 pagesSérie 2AMJADPas encore d'évaluation
- Chimie: (7 Points) Exercice 1: (4,5 Points) : X Mol.lDocument4 pagesChimie: (7 Points) Exercice 1: (4,5 Points) : X Mol.lMohamed SaidiPas encore d'évaluation
- Gsa 2bac 1819 S1 C2 PCF PCDocument3 pagesGsa 2bac 1819 S1 C2 PCF PCAmine AlaoUii AlaouiPas encore d'évaluation
- Cours 1 - Décroissance Radioactive PDFDocument7 pagesCours 1 - Décroissance Radioactive PDFMoufida ZouaghiPas encore d'évaluation
- Contrôle 27 (PHamza Khaldoune)Document2 pagesContrôle 27 (PHamza Khaldoune)Mouhibi AbdellahPas encore d'évaluation
- CNC MP 2017 Chimie Corrige PDFDocument21 pagesCNC MP 2017 Chimie Corrige PDFYassir Sadiq ElfilaliPas encore d'évaluation
- Cours Noyaux - Masse Et Énergie ModifiéDocument20 pagesCours Noyaux - Masse Et Énergie ModifiéابومحمدطهPas encore d'évaluation
- Le+Dipôle+RL Cours FRDocument8 pagesLe+Dipôle+RL Cours FRالغزيزال الحسن EL GHZIZAL Hassane0% (1)
- CHAP 7 ConducteurDocument14 pagesCHAP 7 ConducteurMaram DhahriPas encore d'évaluation
- Devoir 2 1S 2 SM (22-23)Document10 pagesDevoir 2 1S 2 SM (22-23)Anas TalhiPas encore d'évaluation
- 3 - Energie de LiaisonDocument15 pages3 - Energie de LiaisonTalhi AbdelazizPas encore d'évaluation
- Solutions Exemple 9.4Document126 pagesSolutions Exemple 9.4Yosr Ben SaidPas encore d'évaluation
- Exercices Examens Nucléaire Smp5 FsoDocument21 pagesExercices Examens Nucléaire Smp5 FsoTaalbi Djouher100% (1)
- Devoir Enseignement Scientifique - Première - Avril 2020: Exercice 1: Révisions de SecondeDocument4 pagesDevoir Enseignement Scientifique - Première - Avril 2020: Exercice 1: Révisions de SecondeIrieej PPas encore d'évaluation
- Cours RayonnementDocument103 pagesCours RayonnementYoussef Lazrak100% (2)
- TleD PHY L18 Réactions Nucléires SpontanéesDocument11 pagesTleD PHY L18 Réactions Nucléires SpontanéesYssah SerifouPas encore d'évaluation
- Séances 3 4Document17 pagesSéances 3 4Aristide DOSSOUPas encore d'évaluation
- Présentation 3 - Cellule ÉlectrolytiqueDocument44 pagesPrésentation 3 - Cellule ÉlectrolytiqueAbdou Djelama0% (1)
- Decroissance Nucliere BiofDocument8 pagesDecroissance Nucliere BiofyoussefPas encore d'évaluation
- DS 2 S1 M2 MouslimDocument2 pagesDS 2 S1 M2 MouslimMr. magnetoPas encore d'évaluation
- 6 - Décroissance RadioactiveDocument12 pages6 - Décroissance Radioactivepro alixPas encore d'évaluation
- 5-Cha5-Energie de Cohesion Des Solides PDFDocument66 pages5-Cha5-Energie de Cohesion Des Solides PDFKarimBenA100% (2)
- Correction TD Electricité 3Document27 pagesCorrection TD Electricité 3imenehmida2023Pas encore d'évaluation
- Controle 2 2bac PC Biof 2021Document2 pagesControle 2 2bac PC Biof 2021Laa MeelaPas encore d'évaluation
- Méthodologie: ContexteDocument6 pagesMéthodologie: ContexteAymen Ben BrahimPas encore d'évaluation
- Chap5 Cours MacromoleculesDocument6 pagesChap5 Cours Macromoleculesbob.morane123789Pas encore d'évaluation
- Spe Sciences Ingenieur 2021 Zero 1 Corrige OfficielDocument4 pagesSpe Sciences Ingenieur 2021 Zero 1 Corrige OfficielCompte GooglePas encore d'évaluation
- Devoir À Maison Svt2022 PCDocument4 pagesDevoir À Maison Svt2022 PCKhalid Awtm0% (1)
- Mécanique Quantique RelativisteDocument41 pagesMécanique Quantique RelativisteNathalie DeberghPas encore d'évaluation
- Partie 1Document20 pagesPartie 1بوبي بابيPas encore d'évaluation
- Ch5 Enthalpie Et Energie de LiaisonDocument8 pagesCh5 Enthalpie Et Energie de LiaisonBadre-ezzamen KaddourPas encore d'évaluation
- Proposition Corrigé Bacc C 2023Document5 pagesProposition Corrigé Bacc C 2023Eldin KamgaPas encore d'évaluation
- Epreuve EMR, M2 20-21Document3 pagesEpreuve EMR, M2 20-21Venveslas BALOUBIPas encore d'évaluation
- Physique Chimie 1er Bac Evaluation Diagnostique 1Document4 pagesPhysique Chimie 1er Bac Evaluation Diagnostique 1Azedine AchettouhPas encore d'évaluation
- Résumé Transformations Nucléaires Prof - Sbiro (WWW - Pc1.ma)Document5 pagesRésumé Transformations Nucléaires Prof - Sbiro (WWW - Pc1.ma)med fatPas encore d'évaluation
- Devoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2013-2014) MR Ridha Ben Yahmed PDFDocument4 pagesDevoir de Synthèse N°3 - Sciences Physiques - Bac Sciences Exp (2013-2014) MR Ridha Ben Yahmed PDFMajed GharibPas encore d'évaluation
- Proposition Corrigé Bacc C 2023Document5 pagesProposition Corrigé Bacc C 2023Taffohouo Nwaffeu Yves ValdezPas encore d'évaluation
- Exercices 3 Noyaux-Masse Et ÉnergieDocument2 pagesExercices 3 Noyaux-Masse Et Énergieabdelfattah elmottakyPas encore d'évaluation
- Transformation Nucléaire: ExercicesDocument7 pagesTransformation Nucléaire: ExercicesHamid Ez-zahirPas encore d'évaluation
- CHAPITREIIIL1ST21Document7 pagesCHAPITREIIIL1ST21Aquilo The EaglePas encore d'évaluation
- Analyse Des Corps GrasDocument2 pagesAnalyse Des Corps Graspacome msdevPas encore d'évaluation
- Master Cours Pedologie13Document51 pagesMaster Cours Pedologie13AgrSt Jean Guy-GladsonPas encore d'évaluation
- Fiche Descriptive Traitement de Surface Octobre 2020 CompresseDocument6 pagesFiche Descriptive Traitement de Surface Octobre 2020 CompressepersoazizPas encore d'évaluation
- Chapitre 1 Géneralités Sur Les CompositesDocument17 pagesChapitre 1 Géneralités Sur Les Compositesayoub ayoubPas encore d'évaluation
- Fiche N02 de TD 3èmeDocument9 pagesFiche N02 de TD 3èmebertin kaborePas encore d'évaluation
- PH AcideDocument2 pagesPH AcideRezgui AbderrahimPas encore d'évaluation
- Chap 3Document43 pagesChap 3zahraPas encore d'évaluation
- Configuration Électronique Par Élément Chimique - WikipédiaDocument19 pagesConfiguration Électronique Par Élément Chimique - WikipédiaSamuel LópezPas encore d'évaluation
- L'Activité Anti-Oxydante Des Deux Tissus (Blanc Et Pigmenté) de Quelques Variétés de Datte CommunesDocument66 pagesL'Activité Anti-Oxydante Des Deux Tissus (Blanc Et Pigmenté) de Quelques Variétés de Datte CommunesRanda BenPas encore d'évaluation
- PGReview Removed1Document5 pagesPGReview Removed1Mohamed BouchmiaaPas encore d'évaluation
- Suivi Temporel D'une Transformation ChimiqueDocument10 pagesSuivi Temporel D'une Transformation ChimiqueMhamed LaihemPas encore d'évaluation
- Usine A ProspecterDocument30 pagesUsine A ProspecterFatoumata Soumah100% (1)
- Vinification RoséDocument1 pageVinification RoséMATAR COUMEPas encore d'évaluation
- Compte Rendu Du TP 1 de Chimie Minéral 2Document5 pagesCompte Rendu Du TP 1 de Chimie Minéral 2chaimaa120% (1)
- Cours 5emeDocument84 pagesCours 5emeSuccess SuccessPas encore d'évaluation
- Chap 1-6 Materiaux de ConstructionDocument4 pagesChap 1-6 Materiaux de ConstructionJordan MpeckPas encore d'évaluation
- Article de La Phytochimie Assia CorrigeDocument22 pagesArticle de La Phytochimie Assia CorrigeALL about ALLPas encore d'évaluation
- Corrige SCPH L2 A 01 2020 PDFDocument2 pagesCorrige SCPH L2 A 01 2020 PDFIbrahim InussPas encore d'évaluation
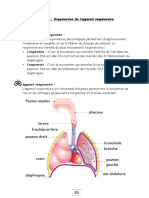
- La Respiration Chez L Homme Cours MaDocument6 pagesLa Respiration Chez L Homme Cours Marabiaa rabPas encore d'évaluation
- CXS 019fDocument5 pagesCXS 019famalgeoPas encore d'évaluation
- CPG HPLCDocument10 pagesCPG HPLCKpabou KpabouPas encore d'évaluation
- TD Chapitre 8 SNDocument4 pagesTD Chapitre 8 SNزيد بخليفةPas encore d'évaluation
- Top 5 Des Sujets de Revision en Physique Chimie Tle DDocument15 pagesTop 5 Des Sujets de Revision en Physique Chimie Tle DzallPas encore d'évaluation
- Guide Roche MarbrièresDocument47 pagesGuide Roche MarbrièresAbdelmalekIsmailiPas encore d'évaluation
- 21chi3e E2Document2 pages21chi3e E2Sassi LassaadPas encore d'évaluation
- Dte 220 Traitement de SurfaceDocument48 pagesDte 220 Traitement de SurfaceKhalil AOUADPas encore d'évaluation
- Rapport MecaniqueDocument98 pagesRapport MecaniqueGhassen Jemaa100% (1)
- Caracterisation ApatiteDocument3 pagesCaracterisation ApatiteFadiliPas encore d'évaluation
- Cours de Chimie HeterocycliqueDocument76 pagesCours de Chimie HeterocycliqueJoris SANTOSPas encore d'évaluation
- PulverisationDocument75 pagesPulverisationALAMIPas encore d'évaluation