Académique Documents
Professionnel Documents
Culture Documents
Os Chimie Corrige ch2 PDF
Transféré par
Faria HaqueTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Os Chimie Corrige ch2 PDF
Transféré par
Faria HaqueDroits d'auteur :
Formats disponibles
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:33 Page75
CHAPITRE
2
2.1
Le brleur au propane
dune montgolfire.
Le comportement
des gaz
Lavnement des montgolfires a marqu le monde de la science.
En effet, le dsir daugmenter la performance de leurs ballons
a pouss les scientifiques et les inventeurs tudier
avec prcision le comportement des gaz.
Quelles sont les lois qui rgissent ce comportement ?
Ces lois sappliquent-elles tous les gaz
et dans nimporte quelles conditions ?
75
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:33 Page76
Dans ce chapitre, nous survolerons les tapes de la dmarche scientifique qui a
men la comprhension du comportement des gaz et la dcouverte de lois
portant sur les variables qui les dcrivent. laide de lois simples, expliquant la
relation entre deux variables, il a t possible de dduire des lois plus complexes,
soit la loi gnrale des gaz et la loi des gaz parfaits. Nous tudierons ces lois, de
mme que celle qui porte sur les pressions partielles dans les mlanges gazeux.
Les lois simples
des gaz
2.1
Pour dfinir les caractristiques dun chantillon de gaz et pour tudier son comportement, quatre variables sont ncessaires: la pression, la temprature, le volume et la
quantit de gaz. Le TABLEAU 2.2 prsente une description de ces quatre variables.
CONCEPTS DJ VUS
o
o
o
2.2
LES VARIABLES DU COMPORTEMENT DES GAZ
Symbole
Variable
Description
Effet
Mesure
Pression
La pression est
directement lie au
nombre de collisions
des particules de gaz
(voir le chapitre 1).
Plus il y a de
collisions, plus il
y a de pression,
et vice versa.
La pression se mesure
laide dun
manomtre ou dune
jauge pression.
Temprature
Comme lindique la
thorie cintique, la
temprature est
directement lie
lnergie cintique
des particules de gaz
(voir le chapitre 1).
Plus la temprature
augmente, plus
les particules de
gaz bougent
rapidement,
et vice versa.
La temprature se
mesure laide dun
thermomtre ou dun
capteur de
temprature.
Volume
Le volume est directement li lespace
entre les particules de
gaz. Comme un gaz
occupe tout lespace
disponible, le volume
dun gaz correspond
au volume du
contenant dans lequel
il se trouve (voir le
chapitre 1).
Plus le volume
augmente, plus
lespace entre
les particules
augmente,
et vice versa.
Le volume dun gaz
se mesure laide
dune seringue ou
dune mthode par
dplacement deau.
Quantit
de gaz
La quantit de gaz
correspond au
nombre de
particules (atomes
ou molcules)
contenues dans
un chantillon.
Plus la quantit
de gaz est
grande, plus il y
a de particules,
et vice versa.
Comme il nexiste pas
dinstrument pour
mesurer le nombre de
particules, on dtermine dabord la masse
de lchantillon, puis
on calcule le nombre
de moles correspondant laide de la
masse molaire.
76
Pression
Temprature
Volume
Masse
Modle particulaire
Notion de mole
LABOS
2 5. LES LOIS SIMPLES
DES GAZ
PARTIE I
L E S GA Z
THORIE
ERPI Reproduction interdite
6. LA MASSE MOLAIRE
DUN GAZ INCONNU
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:33 Page77
On peut comparer le comportement des particules de gaz celui dadolescents et
dadolescentes qui dansent dans un local. La FIGURE 2.3 dfinit les quatre variables
tudier dans cette comparaison. Nous y reviendrons rgulirement dans les
prochaines pages de ce chapitre.
2.3
Une comparaison entre des danseurs et des particules de gaz peut faciliter la comprhension
des lois des gaz.
ERPI Reproduction interdite
CHIMIE
Ds le 17e sicle, les scientifiques ont formul quelques lois simples dcrivant le
comportement des gaz. Pour y parvenir, ils ont ralis des exprimentations en
considrant deux des quatre variables qui caractrisent les gaz, tandis quils
maintenaient constantes les valeurs des deux autres variables. Par exemple, lors de
lanalyse de la relation qui existe entre la pression et le volume, la temprature et
la quantit de gaz ne devaient pas varier. Cest ainsi que les chercheurs ont pu
concevoir des relations mathmatiques et des formules simples deux variables.
tant donn que la temprature et la pression de lair
TYMOLOGIE
varient dun point lautre de la Terre (voir la FIGURE 2.4,
Norme vient du mot
par exemple), les scientifiques ont d tablir des normes
latin norma, qui signifie
quant aux conditions dtude des gaz. Ces normes
querre, rgle, loi.
peuvent savrer utiles pour comparer le comportement
de deux gaz diffrents, pour quantifier des variables dans des conditions prcises,
ou encore pour rsoudre certains problmes concernant les gaz. Ainsi, on
distingue :
les conditions de temprature et de pression normales (TPN) : une temprature
de 0 C et une pression de 101,3 kPa;
les conditions de temprature ambiante et de pression normale (TAPN), quon
peut aussi appeler conditions ambiantes : une temprature de 25 C et une
pression de 101,3 kPa.
2.4
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
THORIE
2
CHAPITRE
T (temprature)
Rythme de la
musique
V (volume)
Taille du local
n (nombre de particules)
Nombre de
danseurs
P (pression)
Collisions entre
les danseurs et
les obstacles
Au sommet du mont
Everest, la pression
moyenne est denviron
31 kPa et la temprature
moyenne, de 36 C.
77
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:33 Page78
Les sections qui suivent montrent la dmarche quont effectue les scientifiques
avant de formuler les lois simples des gaz.
La relation entre la pression et le volume
En 1662, le physicien et chimiste irlandais Robert Boyle (1627-1691) tablit la
relation qui existe entre la pression dun gaz et son volume. Cette relation fut
confirme, en 1676, par le physicien franais Edme Mariotte (1620-1684). Ces
deux scientifiques tudiaient, chacun de leur ct, la compressibilit des gaz.
temprature constante, ils observrent que, lorsque la pression dun chantillon
de gaz diminue, son volume augmente, et vice versa. La mme relation existe si on
tudie leffet dun changement de volume sur la pression : lorsque le volume du
gaz diminue, sa pression augmente, et vice versa. On appelle cette relation la loi
de Boyle-Mariotte.
CONCEPT DJ VU
o
Relation entre la
pression et le
volume
DFINITION
La loi de Boyle-Mariotte indique que, temprature constante, le volume dune
masse de gaz est inversement proportionnel la pression. Si on augmente la
pression, le volume diminue; si on diminue la pression, le volume augmente.
Le graphique de la pression en fonction du volume
(voir la FIGURE 2.5) forme une hyperbole , une courbe
typique dune relation inversement proportionnelle.
Cette relation est confirme par le graphique de la
pression en fonction de linverse mathmatique du
volume, soit 1/V (voir la FIGURE 2.6). Par consquent,
si le volume du contenant double, la pression du gaz
diminue de moiti.
LIEN MATHMATIQUE
Lhyperbole est une
courbe plane deux
branches dont lexpression mathmatique simplifie peut scrire sous
la forme dune fonction
inverse : f(x) = 1 /x.
On peut donc dire que la pression est directement proportionnelle linverse du volume.
Mathmatiquement, cette relation scrit comme
suit (le symbole signifie est directement
proportionnel ) :
P 1
OU
PV = constante
V
LA PRESSION DUN GAZ
EN FONCTION DE SON VOLUME
ERPI Reproduction interdite
Pression (kPa)
Il ne faut pas confondre la constante de cette
formule avec les deux variables qui doivent
demeurer constantes tout au long de lexprimentation, soit ici la temprature et la quantit
de gaz. De ce fait, si on rpte lexprience en
utilisant une autre quantit de gaz ou en leffec tuant une temprature diffrente, on obtiendra
tout de mme une relation inversement propor tionnelle. Toutefois, la constante de la formule
sera diffrente, comme le dmontre la FIGURE 2.7.
La valeur de la constante dpend donc de la
temprature et de la quantit de gaz.
2.5
500
400
300
200
100
0
0
1V
2V
3V
4V
5V
Volume
ANIMATION
78
PARTIE I
L E S GA Z
THORIE
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:33 Page79
2.7
LA PRESSION DUN GAZ EN FONCTION
DE LINVERSE MATHMATIQUE
DE SON VOLUME (1 /V)
LA PRESSION DUN GAZ EN FONCTION
DE SON VOLUME POUR DEUX
QUANTITS DIFFRENTES (n1 ET n2 )
Pression (kPa)
Pression (kPa)
2.6
n2
Volume (ml)
CHIMIE
1/V (1/ml)
CHAPITRE
n1
Comme le produit de la pression par le volume est gal une constante, on peut
comparer des changements de pression et de volume de deux situations diffrentes, pourvu que la quantit de gaz et la temprature ne varient pas de lune
lautre. On obtient la formule suivante :
Relation entre la pression et le volume dun gaz
ERPI Reproduction interdite
P1V1 = P2V2 o P1 reprsente la pression initiale (en kPa ou en mm Hg)
V1 reprsente le volume initial (en ml ou en L)
P2 reprsente la pression finale (en kPa ou en mm Hg)
V2 reprsente le volume final (en ml ou en L)
Une seringue contient 25,0 ml de gaz la pression atmosphrique normale. Quelle sera
la pression de ce gaz si on diminue le volume 20,0 ml tout en gardant la temprature
et le nombre de particules de gaz constants ?
1. Quelle est linformation recherche ?
P2 = ?
2. Quelles sont les donnes du problme ?
V1 = 25,0 ml
P1 = 101,3 kPa
V2 = 20,0 ml
3. Quelle formule contient les variables
dont jai besoin ?
PV
P1V1 = P2V2
Do P2 = 1 1
V2
CHAPITRE 2
MTHO, p. 438
4. Jeffectue les calculs.
P2 = 101,3 kPa 25,0 ml
20,0 ml
= 126,6 kPa
5. Je vrifie ma rponse et je rponds la question.
Puisque la pression est inversement proportionnelle
au volume, il est logique que, lorsquon diminue le
volume, la pression finale soit plus grande que la pression
initiale. La pression du gaz sera donc de 127 kPa.
L E CO M P O RT E M E N T D E S GA Z
THORIE
79
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:33 Page80
EXPLICATION LAIDE DE LA THORIE CINTIQUE
La thorie cintique permet de comprendre la relation qui existe entre la pression
et le volume dun gaz. temprature constante, lorsquon diminue le volume,
lespace entre les particules de gaz diminue. Il en rsulte que le nombre de particules de gaz par unit de volume augmente, ce qui fait augmenter le nombre de
collisions. Cela a pour effet dlever la pression du gaz.
La loi de Boyle-Mariotte permet dexpliquer ce qui se produit au cours de la
respiration (voir la FIGURE 2.8). Lors de la phase dexpiration, les muscles de la
cage thoracique se relchent et le diaphragme slve, ce qui a pour effet de
diminuer le volume des poumons. Il en rsulte une augmentation de la
pression de lair qui sy trouve. Comme un gaz se dplace naturellement dun
milieu o la pression est plus leve vers un milieu o la pression est moins
leve, lair est expuls des poumons. Le phnomne inverse se produit lors de
la phase dinspiration.
INSPIRATION
2.8
EXPIRATION
Air
Air
Volume
plus grand,
pression
plus petite
Volume
plus petit,
pression
plus grande
Lorsque la pression ambiante augmente, par exemple lorsquune personne
fait de la plonge sous-marine, le diazote de lair pntre dans le sang et les
tissus de lorganisme. Il sensuit des picotements, des douleurs aux articulations et des difficults respirer. De plus, si la personne remonte trop vite
la surface, le diazote dissous forme des bulles dans le sang qui ne peuvent tre
limines par la respiration. Ces bulles prennent de lexpansion au fur et
mesure de la remonte, ce qui entrane des complications trs graves. Ces
troubles furent dabord constats au 18e sicle, alors quon utilisait dnormes
cloches de plonge pour la construction de ponts et de tunnels, do leur nom
de mal des caissons. Pour viter ce problme, il faut respecter des paliers de
dcompression au cours de la remonte.
80
La loi de BoyleMariotte explique
le phnomne
de la respiration.
PARTIE I
L E S GA Z
THORIE
ERPI Reproduction interdite
ENRICHISSEMENT
Reprenons la comparaison de la FIGURE 2.3 les adolescents qui dansent pour
illustrer la relation entre la pression dun gaz et son volume. Comme la temprature et le nombre de particules de gaz sont constants, les adolescents dansent au
mme rythme. Toutefois, si on les amne dans un local deux fois plus petit, il y aura
alors deux fois plus de possibilits quils se heurtent, ce qui fera augmenter la
pression.
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:33 Page81
HISTOIRE DE SCIENCE
La plonge sous-marine
ERPI Reproduction interdite
Lonard de Vinci (1452-1519)
imagina le premier scaphandre
casque avec tuyau permettant au
plongeur daspirer lair de la surface. Toutefois, cette technique tait
peu raliste avant lavnement des
pompes air.
En 1690, le physicien et astro nome Edmond Halley (1656-1742)
reprit lide de la cloche de plonge. Il y renouvelait lair grce
des tonneaux quil tranait derrire
lui. Mais ce dispositif tait encombrant et peu pratique.
Larmure de plonge propose
par John Lethbridge (1675-1759)
en 1715 consistait en un tonneau
de bois duquel ne dpassaient que
En 1837, Augustus Siebe (17881872) ajouta des chaussures lestes au scaphandre, do le nom de
scaphandre pieds lourds. La
combinaison de ce scaphandre
tait fabrique dune toile caoutchoute souple et tanche. Le systme dalimentation en air par une
pompe remplaait les soufflets.
La forme actuelle de scaphandre
casque fut essentiellement acheve par Joseph-Martin Cabirol, qui
en obtint le brevet en 1855. Cette
version amliore comportait une
combinaison en toile caoutchoute
et une soupape permettant dvacuer lair vici.
2
CHAPITRE
En 1772, Frminet mit au point
une combinaison de plonge en
cuir agrmente dun casque en
cuivre, quil baptisa machine
hydrostatergatique. Des poids
rpartis sur le plongeur lui permettaient de se maintenir en profondeur et de marcher au fond de
leau. Lair tait pomp grce un
immense soufflet. Ce prototype de
scaphandre casque connut beaucoup de succs et fut amlior au
fil du temps.
Ce membre dune quipe de
secourisme porte un scaphandre
autonome moderne, version
21e sicle.
On raconte quau 4e sicle avant
notre re, Alexandre le Grand
(356, 323) plongea jusqu environ 10 m de profondeur grce
une cloche inverse.
ses deux bras. Une ouverture permettait lalimentation en air
laide dun soufflet; une autre
servait vacuer lair vici.
Grce la collaboration de
Benot Rouquayrol (1826-1875) et
dAuguste Denayrouze (18371883), linvention dun dtendeur
donna naissance au premier scaphandre autonome en 1864. Ce
dispositif servait rguler la pression de lair provenant dun rservoir. Toutefois, les rserves dair
taient limites puisquon ne savait
pas encore comprimer lair efficacement dans une bouteille.
En 1943, lingnieur mile
Gagnan (1900-1979) et le commandant Jacques-Yves Cousteau
(1910-1997) inventrent le scaphandre autonome moderne. Les
nouveaux modles nen sont que
des versions amliores.
LVOLUTION DU SCAPHANDRE AU FIL DU TEMPS
1690
1715
Cloche
de Halley
Tonneau de
Lethbridge
1837
Scaphandre
pieds lourds
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
1864
Scaphandre
autonome
THORIE
1943
Scaphandre
autonome moderne
81
CHIMIE
Lattrait du fond des mers existe
depuis toujours. La plonge en
apne, cest--dire sans appareil
spcialis, est limite par la dure
et la profondeur. En effet, pour
chaque 10 m de descente, la pression augmente denviron 100 kPa.
Cette augmentation de pression
occasionne une diminution du
volume dair dans les poumons et
une difficult respirer.
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:33 Page82
La relation entre le volume
et la temprature
lpoque de linvention des montgolfires, les scientifiques se sont mis sinterroger sur la relation qui existe entre la temprature et le volume dun gaz. En
1787, le physicien franais Jacques Charles (1746-1823) a tabli que, pression
constante, le volume dun gaz dpend de sa temprature. Plus la temprature
augmente, plus le volume augmente, et vice versa.
CONCEPT DJ VU
o
Proprits caractristiques physiques
Cependant, si on trace le graphique du volume en fonction de la temprature en
degrs Celsius, comme la FIGURE 2.10, on constate que la relation entre ces deux
variables nest pas directement proportionnelle. En effet, si la temprature en
degrs Celsius double, le volume du gaz ne double pas. Autrement dit, la droite ne
passe pas par lorigine.
Ce rsultat nest pas vraiment surprenant. Lorsquun volume est gal zro, on
peut dire que lespace occup est vraiment nul ou encore quil ny a pas de volume
mesurer. Dans ces conditions, le gaz nexiste plus. Au contraire, lorsquon note
une temprature de 0 C, lnergie cintique des particules de gaz nest pas nulle.
Si tel tait le cas, on ne pourrait plus respirer en dessous de 0 C, puisquil ny
aurait plus dair ! Cette temprature indique plutt le point de conglation de leau,
tabli de faon arbitraire par le physicien sudois Anders Celsius (1701-1744).
Le physicien franais Guillaume Amontons (1663-1705)
avait suggr, quelques annes plus tt, le concept
dun zro absolu , temprature au-del de laquelle la
matire nexisterait plus. Le zro absolu suggre une
Absolu vient du mot
latin absolutus, qui signifie
dtach, achev, parfait.
LCHELLE DES KELVINS ET LCHELLE DES DEGRS CELSIUS
Conglation
de leau
CHELLE
DES
KELVINS
CHELLE
DES DEGRS
CELSIUS
82
0K
273 C
Zro absolu
Plus haute temprature
terrestre (valle
de la Mort, Californie)
184 K
273 K
310 K
331 K
373 K
89 C
0 C
37 C
58 C
100 C
Plus basse
temprature
terrestre
(Antarctique)
Temprature
normale du corps
humain
PARTIE I
L E S GA Z
THORIE
bullition de leau
ERPI Reproduction interdite
2.9
TYMOLOGIE
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:33 Page83
LE VOLUME DUN GAZ EN FONCTION
DE LA TEMPRATURE
Volume (ml)
100
90
50
80
40
70
30
60
20
50
10
40
273,15 C
20
10
Lchelle des kelvins, aussi appele chelle des
200 100
0
100
200
300
tempratures absolues, est une chelle parallle
Temprature
(C)
celle des degrs Celsius (voir la FIGURE 2.9).
Un intervalle de 1 C quivaut un intervalle de
ANIMATION
1 K, mais les 0 de ces chelles se trouvent un
intervalle de 273 units lun de lautre. Comme
les thermomtres usuels sont gradus en degrs Celsius, pour convertir une
temprature dune chelle lautre, il faut effectuer lopration mathmatique
suivante :
ERPI Reproduction interdite
T (en K) = T (en C) + 273
Fusion des mtaux
933 K
3300 K
14 MILLIONS K
660 C
3027 C
14 MILLIONS C
Combustion
du gaz naturel
Intrieur du Soleil
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
THORIE
83
CHAPITRE
30
la FIGURE 2.10, lextrapolation de la droite (en
pointill) montre un volume qui semble nul une
temprature de 273,15 C. En 1848, le physicien britannique William Thomson (18241907), mieux connu sous le nom de Lord Kelvin,
a choisi ce zro absolu comme point de dpart
dune nouvelle chelle de temprature qui porte
aujourdhui son nom. Le kelvin est lunit de
mesure officielle de la temprature du Systme
international dunits (SI). Il est noter, toutefois,
quaucun gaz ne pourrait atteindre rellement le
zro absolu, puisque tous se liqufient des tempratures plus leves.
2.10
CHIMIE
absence de mouvement des particules de matire
et une nergie cintique nulle. Cette temprature
ne peut donc tre dtermine que thoriquement.
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:34 Page84
Aprs toutes ces considrations, on peut maintenant
noncer la loi de Charles, qui rsume la relation entre le
volume et la temprature lorsque la pression et la quantit
de gaz sont constantes.
DFINITION
La loi de Charles indique que, pression constante, le
volume dune certaine quantit de gaz est directement
proportionnel la temprature absolue. Lorsque la temprature augmente, le volume du gaz augmente; lorsque
la temprature diminue, le volume du gaz diminue.
La loi de Charles permet daffirmer que, pression constante, lorsque la temprature absolue dun gaz double, son
volume double lui aussi. Cette loi fut confirme en 1802
par Louis Joseph Gay-Lussac (1778-1850). Cest pour
cette raison quon lappelle parfois la loi de Gay-Lussac.
2.11
Mathmatiquement, cette relation scrit comme suit :
V = constante
VT
OU
T
La loi de Charles permet de comprendre que, lorsquon
chauffe lair contenu dans une montgolfire, celle-ci se
gonfle parce que lespace entre les particules de gaz
augmente. La masse volumique de lair chaud devient
alors plus petite que celle de lair ambiant. Cette
diffrence permet au ballon de senvoler.
Pour une mme quantit de gaz pression constante, on
peut donc comparer deux situations diffrentes laide de
la formule suivante :
Une seringue contient 75 ml de gaz aux conditions ambiantes de temprature et
de pression. Quel sera le volume de ce gaz si on chauffe la seringue jusqu 50 C
tout en gardant la pression et le nombre de particules de gaz constants ?
1. Quelle est linformation recherche ?
V2 = ?
4. Jeffectue les calculs.
2. Quelles sont les donnes du problme ?
V1 = 75 ml
T1 = 25 C + 273 = 298 K
T2 = 50 C + 273 = 323 K
3. Quelle formule contient les variables dont
jai besoin ?
V1 V2
VT
=
Do V2 = 1 2
T1
T2
T1
84
MTHO, p. 438
PARTIE I
75 ml 323 K
298 K
= 81,3 ml
V2 =
5. Je vrifie ma rponse et je rponds
la question.
Puisque le volume est directement proportionnel
la temprature absolue, il est logique que,
lorsquon augmente la temprature, le volume final
soit plus grand que le volume initial. Le volume du
gaz sera donc de 81 ml.
L E S GA Z
THORIE
ERPI Reproduction interdite
Relation entre le volume et la temprature dun gaz
V1 V2
T1 = T2 o V1 reprsente le volume initial (en ml ou en L)
T1 reprsente la temprature initiale (en K)
V2 reprsente le volume final (en ml ou en L)
T2 reprsente la temprature finale (en K)
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:34 Page85
EXPLICATION LAIDE DE LA THORIE CINTIQUE
Selon la thorie cintique, lorsquon augmente la temprature dun gaz, lnergie
cintique des particules de gaz augmente. Les particules bougent plus vite. Cela a
pour effet daugmenter les possibilits quelles entrent en collision, ce qui entrane
un changement de pression. Le volume augmente en consquence si lon maintient la pression constante.
On peut aussi illustrer la relation avec la comparaison des adolescents qui dansent
(voir la FIGURE 2.3). Par exemple, lorsquon augmente le rythme de la musique (la
temprature), il y a plus de possibilits que les adolescents entrent en collision les
uns avec les autres. Pour maintenir le nombre de collisions (la pression) constant,
il faut alors les amener dans un local plus grand.
La relation entre la pression
et la temprature
CHAPITRE
CHIMIE
2.12
Plusieurs scientifiques, dont Guillaume Amontons, Jacques Charles et Louis Joseph
Gay-Lussac, se sont aussi interrogs sur la relation qui existe entre la pression et la
temprature. Si on augmente la temprature dun chantillon de gaz en maintenant son volume constant, on constate que la pression augmente. Cette relation
est illustre la FIGURE 2.12.
LA PRESSION DUN GAZ EN FONCTION DE LA TEMPRATURE
Pression (kPa)
Vers le manomtre
200
ERPI Reproduction interdite
Vers le manomtre
Bain de
glace
100
Eau
bouillante
273,15 C
200
100
0
Temprature (C)
100
200
300
Si on extrapole la droite obtenue dans ce graphique, on remarque quune pression
nulle correspond une temprature de 273,15 C, ce qui confirme la notion du
zro absolu. Lutilisation de lchelle des tempratures absolues (chelle Kelvin)
est donc de mise pour tablir une relation directement proportionnelle entre la
pression et la temprature dun chantillon de gaz, volume constant.
Mathmatiquement, cette relation scrit comme suit :
P = constante
PT
OU
T
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
THORIE
85
11120_cyr_ch_02-p075-086_Layout 1 2013-06-04 16:34 Page86
2.13
Les fabricants de pneus
recommandent de
mesurer la pression
le matin, puisquelle
est alors son
minimum. Au cours
de la journe, la
temprature augmente,
ce qui augmente la
pression de lair dans
les pneus.
Pour une mme quantit de gaz pression constante, on peut donc comparer deux
situations diffrentes laide de la formule suivante :
Relation entre la pression et la temprature dun gaz
P1 P2
T1 = T2 o P1 reprsente la pression initiale (en kPa ou en mm Hg)
T1 reprsente la temprature initiale (en K)
P2 reprsente la pression finale (en kPa ou en mm Hg)
T2 reprsente la temprature finale (en K)
Un ballon rigide contient 75 ml de gaz aux conditions ambiantes de temprature et de pression.
Quelle sera la pression de ce gaz si on chauffe le ballon jusqu 50,0 C tout en gardant
le volume et le nombre de particules de gaz constants ?
2. Quelles sont les donnes du problme ?
P1 = 101,3 kPa
T1 = 25,0 C + 273 = 298,0 K
T2 = 50,0 C + 273 = 323,0 K
3. Quelle formule contient les variables dont
jai besoin ?
P1
P
= 2
T1
T2
Do P2 =
4. Jeffectue les calculs.
101,3 kPa 323,0 K
P2 =
298,0 K
= 109,798 kPa
5. Je vrifie ma rponse et je rponds
la question.
Puisque la pression est directement proportionnelle
la temprature absolue, il est logique que,
lorsquon augmente la temprature, la pression
finale soit plus grande que la pression initiale.
La pression du gaz sera donc de 109,8 kPa.
P1T2
T1
EXPLICATION LAIDE DE LA THORIE CINTIQUE
Selon la thorie cintique, lorsquon augmente la temprature dun gaz, lnergie
cintique des particules de gaz augmente. Comme elles bougent plus vite, les
possibilits que les particules entrent en collision augmentent, ce qui entrane une
augmentation de pression.
Si lon revient la comparaison avec les adolescents qui dansent (voir la FIGURE 2.3),
lorsque le rythme de la musique (la temprature) augmente, les risques de
collisions (la pression) augmentent galement.
86
PARTIE I
L E S GA Z
THORIE
ERPI Reproduction interdite
1. Quelle est linformation recherche ?
P2 = ?
MTHO, p. 438
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page87
La relation entre le volume
et la quantit de gaz
En se servant de ses observations sur les gaz et du modle atomique de Dalton,
Louis Joseph Gay-Lussac proposa, en 1808, la loi des combinaisons volumtriques. Selon cette loi, lors dune raction chimique, les volumes de ractifs et
de produits gazeux, aux mmes conditions de temprature et de pression, sont
toujours des rapports simples de nombres entiers. La FIGURE 2.14 montre lexemple
de la dcomposition de leau.
Quelques annes aprs lnonc de la loi de
Gay-Lussac, le chimiste et physicien italien Amedeo Avogadro (1776-1856) tenta
dexpliquer les
TYMOLOGIE
bases de cette loi
Hypothse vient du
en
proposant
mot grec hupothesis, qui
l hypothse suisignifie base dun
vante : des voraisonnement, suppolumes gaux de
sition.
gaz, aux mmes
conditions de temprature et de pression,
contiennent le mme nombre de particules.
tant donn que, cette poque, Avogadro
navait pas les ressources ncessaires pour
prouver son hypothse, elle tomba dans
loubli et ne fut accepte comme thorie
quen 1860.
Transformations
chimiques
Masse atomique
relative
La dcomposition de
leau produit toujours
deux fois plus de
dihydrogne que
de dioxygne.
ERPI Reproduction interdite
CHIMIE
Cette thorie est utile, en particulier, pour
dterminer la masse molaire dun gaz
inconnu en la comparant celle dun gaz connu. En effet, si les conditions de
temprature et de pression sont les mmes, le nombre de moles de chacun des gaz
sera le mme. Voyons un exemple.
Un contenant de 1,0 L a une masse de 178,86 g lorsquil est vide. Quand on le remplit de diazote, on mesure
une masse de 179,02 g. Lorsque le contenant contient un gaz inconnu, sa masse est de 179,04 g. Quelle est
la masse molaire du gaz inconnu ?
Calcul de la masse du diazote (mN2 )
179,02 g 178,86 g = 0,16 g
Calcul de la masse molaire du gaz inconnu
m
0,18 g
Mx = n x =
= 31,58 g/mol
0,0057
mol
x
Calcul de la masse du gaz inconnu (mx )
179,04 g 178,86 g = 0,18 g
Calcul du nombre de moles de diazote (MN2 )
mN
mN2
0,16 g
MN2 = n 2 , do nN2 =
= 28,02 g/mol = 0,0057 mol
N2
MN2
La masse molaire du gaz inconnu est de
32 g/mol. Toutefois, cette information
ne suffit pas pour identifier le gaz.
Il faudrait la comparer la masse
molaire des gaz possibles.
cause de lhypothse dAvogadro
nN2 = nx = 0,0057 mol
CHAPITRE 2
2
CHAPITRE
2.14
CONCEPTS DJ VUS
o
L E CO M P O RT E M E N T D E S GA Z
THORIE
87
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page88
Lhypothse que fit Avogadro amena ce dernier
constater que, temprature et pression constantes,
plus la quantit de gaz augmente, plus le volume du
gaz augmente. La relation directement proportionnelle
qui sobserve entre le volume et la quantit de gaz
sappelle la loi dAvogadro. La FIGURE 2.15 illustre
cette relation.
DFINITION
2.15
Volume (L)
La loi dAvogadro indique que, temprature et pression constantes, le volume dun gaz est directement
proportionnel au nombre de moles du gaz. Si on
augmente la quantit de gaz, son volume augmente; si
on diminue la quantit de gaz, son volume diminue.
LE VOLUME DUN GAZ EN FONCTION
DE SA QUANTIT
4
3
2
Mathmatiquement, cette relation scrit comme suit :
V = constante
Vn
OU
n
1
0
0,1
0,2
0,3
Quantit de gaz (mol)
ARTICLE TIR DINTERNET
La bombe mthane est amorce
Une quipe de chercheurs sudois a observ la libration
de millions de tonnes de mthane qui taient jusquici
restes enfouies dans le permafrost sous-marin de
lArctique.
ERPI Reproduction interdite
Sous leffet des eaux trs froides et aux pressions
inimaginables des grandes profondeurs, le mthane se
solidifie au fond des ocans, parfois sous forme
dnormes cristaux. Il suffit toutefois dun lger
rchauffement des eaux de mer pour que ces cristaux
se dstabilisent et pour amorcer le relargage du gaz
dans locan.
Les missions de mthane dtectes par les scientifiques
dans locan taient si intenses que le gaz navait pas le
temps de se dissoudre dans leau de mer. Il atteignait
plutt la surface en grosses bulles.
Cette libration de mthane inquite la communaut
scientifique. En effet, ce gaz est de 20 22 fois plus nocif
comme gaz effet de serre que le dioxyde de carbone.
Les quantits de mthane stockes sous les fonds sousmarins de lArctique dpasseraient en importance la
totalit du carbone contenu dans les rserves mondiales
de charbon.
Adapt de : Le Devoir, La bombe mthane est amorce [en ligne].
(Consult le 11 novembre 2008.)
88
PARTIE I
L E S GA Z
Au-dessus de certaines zones de lArctique,
les concentrations atmosphriques de mthane
dpassent de beaucoup les concentrations
naturelles.
THORIE
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page89
Pour une temprature et une pression donnes, on peut donc comparer deux situations diffrentes laide de la formule suivante :
Relation entre le volume et la quantit dun gaz
V1 V2
=
o V1 reprsente le volume initial (en ml ou en L)
n1
n2
n1 reprsente la quantit de gaz initiale (en mol)
V2 reprsente le volume final (en ml ou en L)
n2 reprsente la quantit de gaz finale (en mol)
3. Quelle formule contient les variables dont
jai besoin ?
V1 V2
=
n1
n2
Do V2 =
4. Jeffectue les calculs.
75 ml 4 mol
V2 =
3 mol
= 100 ml
2. Quelles sont les donnes du problme ?
V1 = 75 ml
n1 = 3 mol
n2 = 3 mol + 1 mol = 4 mol
5. Je vrifie ma rponse et je rponds
la question.
Puisque le volume est directement proportionnel
la quantit de gaz, il est logique que, lorsquon
augmente cette dernire, le volume final soit plus
grand que le volume initial. Le volume sera donc
de 100 ml.
V1 n2
n1
Selon la thorie cintique, lorsquon augmente le nombre de particules de gaz, le
nombre de collisions augmente, ce qui a pour effet daugmenter la pression. Le
volume augmente en consquence si lon maintient la pression constante.
Cest comme si lon invitait une autre classe dtudiants danser dans la comparaison de la FIGURE 2.3. Pour que le nombre daccrochages demeure constant, il faut
choisir un local deux fois plus grand.
ENRICHISSEMENT
ERPI Reproduction interdite
EXPLICATION LAIDE DE LA THORIE CINTIQUE
Il existe aussi une relation entre la quantit et la pression dun gaz. Par
exemple, lorsquon gonfle un pneu de vlo plat, donc compltement vide,
lair quon y insuffle contribue dabord augmenter le volume de la chambre
air, la pression interne tant gale la pression atmosphrique. un certain
moment, la chambre air atteint son volume maximal. Laugmentation de la
quantit de gaz entrane alors une augmentation de la pression de lair dans le
pneu, son volume ne variant pratiquement plus.
Habituellement, la pression recommande est inscrite sur le ct du pneu.
Comme un pneu nest jamais parfaitement tanche, il faut vrifier rgulirement la pression en tenant compte du poids du cycliste et des conditions
routires.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
THORIE
89
CHIMIE
1. Quelle est linformation recherche ?
V2 = ?
MTHO, p. 438
CHAPITRE
Une seringue contient 3 mol de gaz dans un volume de 75 ml, aux conditions ambiantes
de temprature et de pression. Quel sera le volume si on ajoute 1 mol de gaz dans
la seringue tout en gardant la pression et la temprature constantes ?
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page90
LE VOLUME MOLAIRE DUN GAZ
Selon la loi dAvogadro, aux mmes conditions de temprature et de pression, une
mole de gaz, quelle que soit la nature de ce gaz, occupe toujours le mme volume.
Lespace quun gaz occupe ne dpend donc pas de sa nature. De grosses particules
de gaz, comme celles du dioxygne, occupent le mme volume que de petites particules, comme celles du dihydrogne (voir la FIGURE 2.16). Cela est possible parce
que les particules de gaz sont trs loignes les unes des autres. Leur volume est
ngligeable par rapport lespace quelles occupent. Cette constatation a amen
les scientifiques dterminer le volume molaire dun gaz.
2.16
H2
22,4 L
1 mol
6,02 1023 particules
2,02 g
CONCEPT DJ VU
o
Nombre dAvogadro
(STE)
Le volume molaire
dun gaz est de
22,4 L/mol TPN.
O2
22,4 L
1 mol
6,02 1023 particules
32,00 g
DFINITION
Le volume molaire dun gaz est le volume quoccupe une mole de gaz, quelle
que soit la nature de ce gaz, une temprature et une pression donnes. Le
volume molaire sexprime en L/mol.
Le volume molaire dun gaz peut tre utile pour convertir un nombre de moles ou
une masse dun certain gaz en units de volume, ou vice versa, condition que le
gaz soit TPN ou TAPN. Nous verrons aussi, dans le chapitre 3, comment le
volume molaire peut tre utilis pour effectuer des calculs stchiomtriques.
Si un contenant renferme 58,2 L de dioxygne TPN, combien y a-t-il de moles
MTHO, p. 439
de ce gaz dans le contenant ?
1. Quelle est linformation recherche ?
4. Jeffectue les calculs.
? mol 58,2 L
1 mol 58,2 L = 2,598 mol
22,4 L
2. Quelle est la correspondance dont jai
besoin ?
5. Je vrifie ma rponse et je rponds la question.
1 mol 22,4 L ( TPN)
Il y a 2,60 mol de dioxygne dans un volume
de 58,2 L.
3. Jeffectue un produit crois.
22,4 L = 58,2 L
1 mol
? mol
90
PARTIE I
L E S GA Z
THORIE
ERPI Reproduction interdite
Aux conditions de temprature et de pression normales (TPN), il a t dtermin
que le volume molaire dun gaz est denviron 22,4 L/mol, tandis quil est de
24,5 L/mol la temprature ambiante et la pression normale. Comme une mole
comporte 6,02 1023 particules, on peut dire que 22,4 L dun gaz TPN contient
6,02 1023 particules de gaz (voir la FIGURE 2.16). Ce volume correspond un peu
plus de 22 cartons de lait de 1 L, par exemple.
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page91
Nom :
Groupe :
Date :
Exercices
2.1
Les lois simples des gaz
1. Quelle est la variable qui correspond chacune des caractristiques numres ci-dessous ?
a) La vitesse des particules de gaz.
La temprature.
b) Les collisions entre les particules de gaz. La pression.
Le volume.
d) Le nombre de particules de gaz.
La quantit de gaz.
2
CHAPITRE
c) Lespace entre les particules de gaz.
2. Un ballon de 650 ml contient 0,43 g de mthane (CH4 ) aux conditions ambiantes. Quelle est
la valeur de chacune des variables qui caractrisent ce gaz ?
CHIMIE
V = 650 ml ou 0,650 L
T = 25 C ou 298 K
P = 101,3 kPa ou 760 mm Hg
n
m
0,43 g
M = m , do n = M = 16,05 g/mol = 0,027 mol
3. quelle valeur correspond la pression atmosphrique normale en mm Hg ?
Elle correspond 760 mm Hg.
4. Prcisez linstrument qui permettrait de mesurer exprimentalement chacune des variables numres
ERPI Reproduction interdite
ci-dessous.
a) La temprature.
On peut utiliser un thermomtre ou un capteur de temprature.
b) La pression.
On peut utiliser un manomtre ou une jauge de pression.
c) La quantit de gaz.
On peut utiliser une balance et ensuite convertir la masse en moles laide du tableau priodique.
d) Le volume.
On peut utiliser une seringue ou on peut recueillir le gaz par dplacement deau.
5. une temprature donne, un chantillon de diazote exerce une certaine pression dans un contenant
au volume variable. Si on triple le volume tout en gardant la temprature constante, quarrivera-t-il
la valeur de la pression ? Expliquez votre rponse.
Comme la pression est inversement proportionnelle au volume, si on triple le volume de gaz,
la pression sera trois fois plus petite.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
91
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page92
Nom :
Groupe :
Date :
6. Justin gonfle un ballon avec une certaine quantit de gaz jusqu ce que le ballon atteigne un volume
de 550,0 ml 100,8 kPa. Quelle pression devrait-il exercer pour diminuer le volume jusqu 330,0 ml,
tout en gardant la temprature constante ?
1. P2 = ?
100,8 kPa 550,0 ml
330,0 ml
= 168,0 kPa
4. P2 =
2. V1 = 550,0 ml
P1 = 100,8 kPa
V2 = 330,0 ml
3. P1V1 = P2V2
PV
Do P2 = V1 1
2
5. La pression exercer est de 168,0 kPa.
7. Un gaz occupe un volume de 45 ml une pression de 680 mm Hg. temprature constante,
quel sera le volume de ce gaz si on amne la pression 120 kPa ?
1. V2 = ?
90,6 kPa 45 ml
120 kPa
= 34 ml
4. V2 =
2. V1 = 45 ml
680 mm Hg 101,3 kPa
= 90,6 kPa
760 mm Hg
P2 = 120 kPa
ERPI Reproduction interdite
P1 =
3. P1V1 = P2V2
PV
Do V2 = P1 1
2
5. Le volume du gaz sera de 34 ml.
92
PARTIE I
L E S GA Z
EXERCICES
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page93
Nom :
Groupe :
Date :
8. Gabrielle veut gonfler 500 ballons de 1200 ml avec de lhlium, aux conditions ambiantes de
temprature et de pression. Pour ce faire, elle utilise une bouteille dhlium de 20,0 L. Quelle devra
tre la pression minimale dans la bouteille pour que Gabrielle parvienne gonfler tous ses ballons ?
1. P1 = ?
101,3 kPa 600,0 L
20,0 L
= 3039 kPa
4. P1 =
2. V1 = 20,0 L
P2 = 101,3 kPa
V2 = 500 1,200 L
= 600,0 L
5. La pression ncessaire pour gonfler les
ballons est de 3039 kPa.
CHIMIE
Pminimale = 3039 kPa +101,3 kPa = 3140 kPa
2
CHAPITRE
Comme on ne peut vider compltement
une bouteille de gaz sans utiliser de pompe, la
pression finale dans la bouteille sera
quivalente la pression atmosphrique,
soit 101,3 kPa.
3. P1V1 = P2V2
PV
Do P1 = 2V 2
1
La pression minimale dans la bouteille devra tre de 3140 kPa.
9. Les particules de gaz, comme celles de lair ambiant,
possdent-elles encore de lnergie cintique en dessous
de 0 C ? Expliquez votre rponse.
Oui, elles en possdent encore. En effet, lnergie cintique
des particules de gaz ne devient pas nulle 0 C. Sinon,
ERPI Reproduction interdite
il ny aurait plus dair pour respirer en dessous de cette
temprature. Cette valeur de la temprature correspond
plutt au point de conglation de leau.
10. Effectuez la conversion des units de mesure pour les tempratures suivantes :
=
223
c) 180 C =
93
b) 277,0 C =
550,0
d) 318 K
45
a) 50 K
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
93
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page94
Nom :
11.
Groupe :
Date :
Pourquoi une temprature exprime en kelvins ne peut-elle pas tre ngative ?
Lchelle des kelvins est une chelle de temprature absolue, donc 0 K correspond la temprature
la plus basse qui puisse exister.
12. Par une froide journe dhiver, o rgne une temprature de 20 C, Sandrine gonfle un ballon
jusqu ce quil occupe un volume de 2,3 L. Elle dcide damener le ballon lintrieur de la maison,
o il fait 22 C . Si ltiquette du fabricant indique que la capacit maximale du ballon est de 2,5 L,
quarrivera-t-il au ballon dans ces nouvelles conditions ? (On considre que la pression demeure
constante.)
1. V2 = ?
2,3 L 295 K
253 K
= 2,7 L
4. V2 =
2. V1 = 2,3 L
T1 = 20 C + 273 = 253 K
T2 = 22 C + 273 = 295 K
5. Le volume final du ballon sera de 2,7 L.
V
V
3. T 1 = T 2
1
2
VT
Do V2 = T1 2
1
Comme la capacit maximale du ballon est de 2,5 L, il y a de fortes chances que le ballon clate
lorsque Sandrine entrera dans la maison.
13. Carolina effectue une exprience afin dvaluer la relation entre le volume et la temprature dun gaz.
1. T2 = ?
102,4 ml 277,0 K
82,5 ml
= 343,8 K 273 = 70,8 C
4. T2 =
2. V1 = 82,5 ml
T1 = 4,0 C + 273 = 277,0 K
V2 = 102,4 ml
V
V
3. T 1 = T 2
1
2
VT
Do T2 = V2 1
1
5. Le thermomtre indique une temprature de 71 C.
94
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
Elle plonge une seringue contenant du dioxyde de carbone dans un bcher rempli deau glace, dont
la temprature est de 4,0 C. La seringue indique alors 82,5 ml. Aprs avoir chauff le tout pendant
2 minutes, elle note un volume de 102,4 ml. Quelle temprature le thermomtre indique-t-il alors ?
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page95
Nom :
Groupe :
Date :
14. La cryognie est ltude du comportement de la matire trs basse temprature. Grce aux
dcouvertes lies la cryognie, il est maintenant possible de conserver des cellules ou de rcuprer
des gaz nuisibles pour lenvironnement. Quelle est la pression exerce par un gaz 123 C si
on mesure une pression de 92 kPa 27 C ?
1. P2 = ?
92 kPa 150 K
300 K
= 46 kPa
4. P2 =
2. P1 = 92 kPa
T1 = 27 C + 273 = 300 K
T2 = 123 C + 273 = 150 K
P
P
3. T 1 = T 2
1
2
2
CHAPITRE
PT
Do P2 = T1 2
1
CHIMIE
5. La pression exerce par le gaz est de 46 kPa.
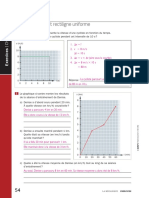
prsente les donnes recueillies par
un tudiant. laide dun diagramme,
dmontrez, dans lespace ci-contre,
quil existe une relation directement
proportionnelle entre la pression
et la temprature.
LA PRESSION DUN GAZ EN FONCTION
DE LA TEMPRATURE
ERPI Reproduction interdite
Temprature
(en C)
Pression (en kPa)
15. Remplissez le tableau ci-dessous, qui
120
100
80
60
Pression
(en kPa)
40
5,0
100,0
20
15,0
103,6
107,2
110,8
114,4
25,0
35,0
45,0
0
0
200
400
Temprature absolue (en K)
Exemple de calcul
PT
100 kPa 288,0 K
= 103,6 kPa
P2 = T1 2 =
278,0 K
1
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
95
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page96
Nom :
Groupe :
Date :
16. Tt le matin, alors que la temprature est de 10 C et la pression atmosphrique, de 101 kPa,
Jean-Sbastien mesure la pression de lair dans les pneus de sa voiture avec une jauge pression
relative. Il note alors une valeur de 240 kPa. Quelle valeur indiquerait la jauge si la temprature
augmentait de 12 C et que la pression atmosphrique demeurait constante ?
1. P2 = ?
341 kPa 295 K
283 K
= 355 kPa
4. P2 =
2. P1 = 240 kPa + 101 kPa = 341 kPa
T1 = 10 C + 273 = 283 K
T2 = 22 C + 273 = 295 K
5. La pression absolue serait de 355 kPa.
355 kPa 101 kPa = 254 kPa
P
P
3. T 1 = T 2
1
2
PT
Do P2 = T1 2
1
La jauge de pression indiquerait une pression relative de 254 kPa.
17.
Un ballon de verre vide de 2,0 L a une masse de 385,3 g. Lorsquil est rempli de dioxygne, on note
alors une masse de 388,0 g. En vidant le ballon et en le remplissant dun gaz inconnu, on note
une masse de 389,0 g.
a) Quelle est la masse molaire du gaz inconnu ?
mO
2,7 g
4. nO2 = M 2 = 32,00 g/mol = 0,084 mol
O2
1. Mx = ?
2. Masse du ballon vide
385,3 g
Masse du O2
388,0 g 385,3 g = 2,7 g
Masse du gaz inconnu
389,0 g 385,3 g = 3,7 g
m
3,7 g
Mx = n x = 0,084 mol = 44 g/mol
x
m
3. M = n
m
Do n = M
5. La masse molaire du gaz inconnu est de 44 g/mol.
b) Quel est le gaz inconnu parmi les gaz suivants : CH4, N2, CO2, SO2 ?
Le gaz inconnu est le CO2 .
96
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
nx = nO2 = 0,084 mol
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page97
Nom :
Groupe :
Date :
18. Une erreur sest glisse lors de la livraison de quatre bouteilles contenant chacune un gaz diffrent :
du CO2, du CH4, du O2 et du N2. Pour les dmler, la technicienne utilise un ballon talon de 3 L,
qui pse exactement 250,0 g. Elle le remplit de dihydrogne et note une masse de 253,6 g.
Elle le vide, puis elle le remplit de nouveau avec lun des gaz inconnus. Le ballon a alors une masse
de 307,2 g. Lequel des gaz inconnus se trouve dans le ballon ?
2. Masse du ballon vide
250,0 g
Masse du H2
253,6 g 250,0 g = 3,6 g
Masse du gaz inconnu
307,2 g 250,0 g = 57,2 g
mH
3,6 g
4. nH2 = M 2 = 2,02 g/mol = 1,78 mol
H2
nx = nH2 = 1,78 mol
m
57,2 g
Mx = n x = 1,78 mol = 32,13 g/mol
x
2
5. La masse molaire du gaz inconnu est de
32,1 g/mol.
CHAPITRE
1. Mx = ?
m
3. M = n
CHIMIE
m
Do n = M
Le gaz inconnu est probablement du dioxygne (O2 ).
19.
Quatre moles de gaz occupent un volume de 2,8 L une temprature de 25 C. Comment devrait-on
modifier la quantit de gaz pour amener le volume 1,2 L ? Prcisez la quantit de gaz quil faudra
ajouter ou enlever et expliquez votre rponse.
ERPI Reproduction interdite
1. n 2 = ?
1,2 L 4,0 mol
2,8 L
= 1,7 mol
4. n 2 =
2. V1 = 2,8 L
n 1 = 4,0 mol
V2 = 1,2 L
5. La quantit de gaz finale sera de 1,7 mol.
4,0 mol 1,7 mol = 2,3 mol
V
V
3. n 1 = n 2
1
2
Vn
Do n 2 = V2 1
1
Il faudra enlever 2,3 mol de gaz.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
97
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page98
Nom :
Groupe :
Date :
20. Un ballon, contenant 7,00 g de N2, occupe un volume de 5,25 L. Quel sera le volume du ballon
si on ajoute 1,75 mol de gaz temprature et pression constantes ?
1. V2 = ?
7,00 g
4. n1 = 28,02 g/mol
= 0,250 mol
n 2 = 0,250 mol + 1,75 mol = 2,00 mol
2. V1 = 5,25 L
m1 = 7,00 g
MN2 = 28,02 g/mol
n2 = n1 + 1,75 mol
5,25 L 2,00 mol
0,250 mol
= 42,0 L
V2 =
V
V
3. n 1 = n 2
1
2
Vn
Do V2 = n1 2
1
m
M= n
m
Do n = M
5. Le volume du ballon sera de 42,0 L.
21. Une seringue, qui indique un volume de 35,0 ml, contient exactement 0,2 mol de gaz. Quel sera le
nouveau volume si on ajoute le double des particules de gaz dans la seringue ?
1. V2 = ?
35,0 ml 0,6 mol
0,2 mol
= 105 ml
4. V2 =
ERPI Reproduction interdite
2. V1 = 35,0 ml
n 1 = 0,2 mol
n 2 = 0,2 mol + 0,4 mol = 0,6 mol
V
V
3. n 1 = n 2
1
2
Vn
Do V2 = n1 2
1
5. Le nouveau volume sera de 105 ml.
98
PARTIE I
L E S GA Z
EXERCICES
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page99
Nom :
Groupe :
Date :
22. Combien de moles de gaz contient un chantillon de 115 L TPN ?
1. ? mol 115 L
2. 1 mol 22,4 L ( TPN)
1 mol ? mol
3. 22,4 L = 115 L
4.
1 mol 115 L
22,4 L = 5,13 mol
CHAPITRE
CHIMIE
5. Cet chantillon contient 5,13 mol de gaz.
23. la temprature ambiante et la pression atmosphrique normale, Cline recueille 20,50 g
de dioxyde de soufre (SO2 ). Quel volume occupe ce gaz ?
24,5 L
?L
3. 1 mol = 0,32 mol
1. ? L 20,50 g
ERPI Reproduction interdite
2. 1 mol 24,5 L ( TAPN)
m
M= n
m
20,50 g
Do n = M = 64,07 g/mol = 0,32 mol
4.
24,5 L x 0,32 mol
= 7,8 L
1 mol
5. Ce gaz occupe un volume de 7,8 L.
24. Mohamed recueille 22,4 L de diazote 0 C et 760 mm Hg. Combien de molcules contient
cet chantillon ? Expliquez votre rponse.
Cet chantillon contient 6,02 1023 molcules, puisque 22,4 L reprsente le volume dune mole
de gaz dans ces conditions (TPN).
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
99
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page100
Nom :
Groupe :
Date :
25. Remplissez le tableau ci-dessous.
Variables en relation
Variables qui ne
doivent pas varier
V et T
P et n
Formule
Graphique
V1 V2
T1 = T2
T (K)
V1 V2
n1 = n2
P et T
V et n
n
T et n
P1V1 = P2V2
V
P et T
P1
P2
T1 = T2
V et n
T (K)
Consulter le Compagnon Web pour dautres exercices en lien avec la section 2.1.
100
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
P et V
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page101
2.2
La loi gnrale des gaz
Les lois simples des gaz permettent de prdire leffet dune variable du comportement gazeux sur une autre. Nanmoins, lorsque plus de deux variables sont en
cause, comme la FIGURE 2.17, il serait utile davoir une formule qui regroupe les
quatre variables. On pourrait alors prvoir quel serait le nouveau volume dun gaz
si on triplait sa temprature absolue, si on quadruplait sa quantit et si on diminuait
de moiti sa pression, par exemple.
2
CHAPITRE
Il faut tenir compte
des variations de
temprature, de volume
et de pression avant le
lancement dun ballon
stratosphrique destin
des observations
scientifiques.
CHIMIE
2.17
Le TABLEAU 2.18 prsente les quatre formules qui rsument les lois simples des gaz.
ERPI Reproduction interdite
2.18
LES FORMULES DES LOIS SIMPLES DES GAZ
Loi
Formule
Relation entre la pression et le volume
P1V1 = P2V2
Relation entre le volume et la temprature
Relation entre la pression et la temprature
Relation entre le volume et la quantit de gaz
V1
V
= 2
T1
T2
P1
P2
=
T1
T2
V1
V
= 2
n1
n2
Comme la pression et le volume sont directement proportionnels la temprature, on peut en dduire que le produit de la pression par le volume serait lui
aussi directement proportionnel la temprature. On peut faire la mme dduc tion avec la quantit de gaz. Ces observations mnent tablir une relation entre
les quatre variables : cest la loi gnrale des gaz.
DFINITION
La loi gnrale des gaz met en relation la pression, le volume, la temprature et
la quantit de gaz en comparant une situation initiale avec une situation finale.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
THORIE
101
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page102
Cette loi sexprime par la formule mathmatique suivante :
Loi gnrale des gaz
P1V1 P2V2
n1 T1 = n2T2 o P1 reprsente la pression initiale (en kPa ou en mm Hg)
V1 reprsente le volume initial (en ml ou en L)
n1 reprsente la quantit de gaz initiale (en mol)
T1 reprsente la temprature initiale (en K)
P2 reprsente la pression finale (en kPa ou en mm Hg)
V2 reprsente le volume final (en ml ou en L)
n2 reprsente la quantit de gaz finale (en mol)
T2 reprsente la temprature finale (en K)
Reprenons lexemple prsent au dbut de la section : quel serait le nouveau volume
dun gaz si on triplait sa temprature absolue, si on quadruplait sa quantit et si on diminuait
de moiti sa pression, en supposant un volume initial de 250 ml ?
1. Quelle est linformation recherche ?
V2 = ?
2. Quelles sont les donnes du problme ?
P1 = x
1
P
=
2
2 x
V1 = 250 ml
n1 = y
n2 = 4y
T1 = z
T2 = 3z
MTHO, p. 438
3. Quelle formule contient les variables dont jai besoin ?
PVnT
P1V1 P2V2
Do V2 = 1 1 2 2
=
n1T1 P2
n1T1
n2T2
4. Jeffectue les calculs.
x 250 ml 4y 3z
V2 =
y z x
= 6000 ml ou 6,00 L
5. Je vrifie ma rponse et je rponds la question.
Le nouveau volume serait de 6000 ml ou 6,00 L.
Aux conditions ambiantes de temprature et de pression, 3,00 mol de gaz occupent
un volume de 75,0 ml. Quelle sera la pression obtenue si on chauffe le tout jusqu 50 C
tout en ajoutant 1,00 mol de gaz et en diminuant le volume jusqu 20,0 ml ?
1. Quelle est linformation recherche ?
P2 = ?
2. Quelles sont les donnes du problme ?
P1 = 101,3 kPa
V1 = 75,0 ml
n1 = 3,00 mol
T1 = 25 C + 273 = 298 K
V2 = 20,0 ml
n2 = 3,00 mol + 1,00 mol = 4,00 mol
T2 = 50 C + 273 = 323 K
102
PARTIE I
MTHO, p. 438
3. Quelle formule contient les variables dont jai besoin ?
PVnT
P1V1 P2V2
Do P2 = 1 1 2 2
=
n1T1 V2
n1T1
n2T2
4. Jeffectue les calculs.
101,3 kPa 75,0 ml 4,00 mol 323 K
P2 =
3,00 mol 298 K 20,0 ml
= 548,99 kPa
5. Je vrifie ma rponse et je rponds la question.
La pression obtenue sera de 549 kPa.
L E S GA Z
THORIE
ERPI Reproduction interdite
Voyons un autre exemple dapplication de la loi gnrale des gaz.
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page103
En se servant de la loi gnrale des gaz, on peut dduire toutes les lois simples dj
tudies, mais aussi plusieurs autres. En effet, si une ou plusieurs caractristiques
demeurent constantes, on simplifie la formule en y liminant les variables correspondantes. Par exemple, si la temprature et la quantit de gaz demeurent constantes, on les limine dans la formule comme ceci :
P1V1 P2V2
=
n 1 T1
n 2T2
On obtient alors la formule suivante : P1V1 = P2V2, qui constitue la loi de BoyleMariotte.
On peut aussi dduire des formules trois variables. Par exemple :
P1V1 P2V2
=
T1
T2
ARTICLE TIR DINTERNET
CHIMIE
Une bouffe doxygne
ERPI Reproduction interdite
Le gouvernement du Qubec a dcid dinvestir
neuf millions de dollars pour la construction
dune chambre hyperbare au-dessus de lurgence
de lHtel-Dieu de Lvis (prs de Qubec). Ces
nouvelles installations feront de lHtel-Dieu le
seul centre de recherche en mdecine hyperbare
au pays.
La mdecine hyperbare consiste faire respirer
de loxygne pur aux patients, une pression
suprieure la pression atmosphrique. Les
chambres hyperbares permettent notamment de
traiter les complications dun accident de
plonge, ou encore des brlures graves. Cette
technique donne galement des rsultats
tonnants lorsquil sagit de soigner
linfection des os.
La conception dune chambre hyperbare sapparente
celle dun sous-marin.
Il y a tellement peu de chambres hyperbares dans
le monde que chaque chambre commande est
faite sur mesure. Il faut deux ans pour la
fabriquer.
LHtel-Dieu estime que la nouvelle chambre
hyperbare rpondra la demande pour les
30 prochaines annes.
Adapt de : Radio-Canada,
Un investissement de 9 millions de dollars [en ligne].
(Consult le 27 octobre 2008.)
Lintrieur dune chambre hyperbare.
CHAPITRE 2
CHAPITRE
Cette dernire formule suppose que la quantit de gaz est demeure constante.
L E CO M P O RT E M E N T D E S GA Z
THORIE
103
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page104
2.3
La loi des gaz parfaits
La formule de la loi gnrale des gaz nest pas trs utile lorsquon veut dterminer
les caractristiques dun gaz un moment prcis (comme la FIGURE 2.19). Pour y
parvenir, on doit modifier la formule de la faon suivante :
PV
= constante
nT
LABO
7. LA CONSTANTE
DES GAZ PARFAITS
La constante se symbolise par la lettre R. Cette nouvelle formule constitue la loi
des gaz parfaits.
DFINITION
La loi des gaz parfaits met en relation la pression, le volume, la temprature
et la quantit de gaz un moment donn. Afin dtablir une galit, on utilise
une constante, symbolise par la lettre R.
La forme la plus courante de cette loi est la suivante :
Loi des gaz parfaits
PV = nRT o P reprsente la pression (en kPa)
V reprsente le volume (en L)
n reprsente la quantit de gaz (en mol)
R reprsente la constante des gaz (en kPaL/molK)
T reprsente la temprature (en K)
Pour dterminer
la quantit de gaz
prsente dans une
bouteille, il faut tenir
compte du volume,
de la temprature
et de la pression.
ERPI Reproduction interdite
2.19
Quentend-on par gaz parfait ? Il sagit dun gaz qui rpond toutes les lois des
gaz de faon rigoureuse et dont le comportement peut tre expliqu par la thorie
cintique, quelles que soient les conditions de temprature et de pression. Cela
signifie que :
les particules dun gaz parfait nont aucune interaction entre elles;
elles rebondissent sans aucune perte dnergie;
leurs collisions avec les obstacles sont parfaitement lastiques;
on peut abaisser la temprature jusqu 0 K sans que le gaz se liqufie.
104
PARTIE I
L E S GA Z
THORIE
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page105
DFINITION
Un gaz parfait est un gaz qui, thoriquement, rpondrait toutes les lois simples
des gaz et dont le comportement pourrait tre expliqu par la thorie cintique.
Un gaz parfait nexiste pas dans la ralit. Toutefois, le comportement des gaz
rels se rapproche de celui dun gaz parfait haute temprature et basse pression. Dans ces conditions, les interactions entre les particules de gaz sont rduites
au minimum. Le TABLEAU 2.20 dmontre que certains gaz se rapprochent plus dun
gaz parfait que dautres, si lon considre leur volume molaire TPN.
2.20 LE VOLUME MOLAIRE DE DIFFRENTS GAZ TPN
Nature du gaz
Volume molaire (en L/mol)
Argon (Ar)
22,09
Diazote (N2 )
22,40
Dioxygne (O2 )
22,40
Hlium (He)
22,41
Dihydrogne (H2 )
22,42
2
CHAPITRE
22,31
Dioxyde de carbone (CO2 )
CHIMIE
On peut calculer la constante dun gaz parfait en utilisant le volume molaire dun
gaz TPN. Ainsi :
101,3 kPa 22,4 L
R=
= 8,31 kPaL/molK
1 mol 273 K
Les scientifiques ont dtermin avec plus de prcision que la constante des gaz
parfaits est de 8,314 kPa L/mol K.
Constante des gaz parfaits : 8,314 kPaL/molK
ERPI Reproduction interdite
Cest cette valeur que nous utiliserons pour la majorit des calculs effectus dans
cet ouvrage. En outre, moins dindications contraires, nous considrerons que
tous les gaz tudis se comportent comme des gaz parfaits.
Quelle est la pression de 0,3000 mol de gaz dans un contenant de 500,0 ml une
temprature de 20,0 C ?
1. Quelle est linformation recherche ?
P=?
2. Quelles sont les donnes du problme ?
V = 500,0 ml 1000 ml/L = 0,5000 L
n = 0,3000 mol
T = 20,0 C + 273 = 293,0 K
R = 8,314 kPa L/mol K
3. Quelle formule contient les variables
dont jai besoin ?
PV = nRT
nRT
Do P = V
CHAPITRE 2
MTHO, p. 438
4. Jeffectue les calculs.
0,3000 mol 8,314 kPa L/mol K 293,0 K
P=
0,5000 L
= 1461,6 kPa
5. Je vrifie ma rponse et je rponds
la question.
Dans ces conditions, la pression du gaz
est de 1462 kPa.
L E CO M P O RT E M E N T D E S GA Z
THORIE
105
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page106
2.4
La loi des pressions partielles
Comme les gaz diffusent facilement, ils forment
souvent des mlanges. Lair en est un exemple. La
FIGURE 2.21 prsente la proportion de ses principaux
constituants.
CONCEPT DJ VU
TYMOLOGIE
Proportion vient du
mot latin proportio, qui
signifie rapport.
Autres gaz
1%
2.21
Mlanges
La proportion des gaz
dans lair.
Dioxygne
(O2)
21 %
Diazote
(N2)
78 %
En tudiant les conditions mtorologiques, le physicien John Dalton (17661844) a observ que, lorsquon mlange deux gaz la mme temprature, la pres sion totale du mlange est gale la somme de la pression de chacun des gaz.
Autrement dit, chaque gaz agit dans un mlange comme sil tait seul occuper
tout lespace disponible dans le contenant. Il conserve ses proprits sans que son
comportement soit influenc par la prsence des autres gaz. Dans ces conditions,
on dit que la pression individuelle de chacun des gaz est une pression partielle,
puisquelle ne reprsente quune fraction de la pression totale du mlange.
DFINITION
La FIGURE 2.22 illustre un exemple de mlange de deux gaz. Selon la thorie cintique, les particules du gaz A (H2) et celles du gaz B (He) exercent un certain
nombre de collisions qui dpend du volume du contenant, de la temprature et de
la quantit de gaz. Lorsque les deux gaz sont mlangs dans le mme contenant,
les collisions de particules du gaz A sadditionnent celles du gaz B. Il en rsulte
une pression quivalant la somme des pressions individuelles de chacun des gaz.
PHe = 730 kPa
PH2 = 290 kPa
5,0 L de H2 20 C
106
Ptotale = 1020 kPa
5,0 L de He 20 C
PARTIE I
2.22
L E S GA Z
Mlange : 5,0 L de gaz 20 C
THORIE
Lorsquon mlange
deux gaz, leurs
pressions sadditionnent.
ERPI Reproduction interdite
La pression partielle dun gaz dans un mlange correspond la pression quil
exercerait sil tait seul dans le volume occup par le mlange.
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page107
Ses observations permirent Dalton dnoncer la loi des pressions partielles.
DFINITION
La loi des pressions partielles indique que, une temprature donne, la
pression totale dun mlange gazeux est gale la somme des pressions partielles exerces par chacun des gaz qui constituent le mlange.
Cette loi sexprime par la formule mathmatique suivante :
Loi des pressions partielles
PT = PpA + PpB + PpC + o PT reprsente la pression totale du mlange
PpA reprsente la pression partielle du gaz A
PpB reprsente la pression partielle du gaz B
PpC reprsente la pression partielle du gaz C
CHAPITRE
Les points de suspension dans la formule indiquent que la pression totale est la
somme de lensemble des pressions partielles, peu importe le nombre de gaz qui
constituent le mlange.
CHIMIE
La loi des pressions partielles est trs utile pour connatre la pression dun gaz
recueilli par dplacement deau. Avec cette mthode, la vapeur deau provenant
de lvaporation se trouve mlange au gaz obtenu. Pour calculer la pression du gaz,
il suffit de soustraire la pression de la vapeur deau. En effet :
PT = Patm = Pgaz + PH2O
Do Pgaz = PT PH2O
La pression de la vapeur deau dpend de la temprature (voir le TABLEAU 2.23).
2.23
LA PRESSION DE LA VAPEUR DEAU POUR DIFFRENTES TEMPRATURES
ERPI Reproduction interdite
Temprature (en C)
Pression (en kPa)
Temprature (en C)
Pression (en kPa)
15
1,71
22
2,64
16
1,81
23
2,81
17
1,93
24
2,99
18
2,07
25
3,17
19
2,20
30
4,24
20
2,33
40
7,37
21
2,49
50
12,33
On peut aussi dterminer la pression partielle de chacun des gaz qui constituent
un mlange en multipliant la pression totale par la proportion que le gaz reprsente dans le mlange. Par exemple, si la pression atmosphrique est de 100 kPa,
la pression partielle du dioxygne sera de 21 kPa, puisque ce gaz reprsente 21 %
de lair. La proportion dun gaz se calcule en effectuant le rapport de son nombre
de moles sur le nombre total de moles du mlange.
Pression partielle dun gaz
n
PpA = PT nA o PpA reprsente la pression partielle du gaz A
T
PT reprsente la pression totale du mlange
nA reprsente la quantit du gaz A (en mol)
nT reprsente la quantit de gaz totale (en mol)
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
THORIE
107
11120_cyr_ch_02-p087-108_Layout 1 2013-06-04 15:46 Page108
Cette formule peut aussi tre utile pour dterminer la pression totale dun mlange,
comme le prsente lexemple suivant.
Dans un contenant de 10 L, on mlange 5,00 mol de dioxygne, 4,00 mol de
dioxyde de carbone et 3,00 mol de diazote. Si la pression partielle du dioxygne
est de 225 kPa, quelle est la pression totale du mlange ?
1. Quelle est linformation recherche ?
PT = ?
MTHO, p. 438
4. Jeffectue les calculs.
225 kPa 12,00 mol
PT =
5,00 mol
= 540 kPa
2. Quelles sont les donnes du problme ?
nO2 = 5,00 mol
nCO2 = 4,00 mol
nN2 = 3,00 mol
PpO2 = 225 kPa
5. Je vrifie ma rponse et je rponds
la question.
La pression totale du mlange est de 540 kPa,
ce qui est suprieur la pression partielle
du dioxygne.
3. Quelle formule contient les variables dont
jai besoin ?
n
P 2nT
PpO2 = PT nO2
Do PT = pO
nO2
T
ARTICLE TIR DINTERNET
La Terre et Vnus: des surs jumelles ?
ERPI Reproduction interdite
Vnus est la plante la plus proche de la Terre. Et pas
seulement en termes de distance. La taille, la densit,
la composition de ces deux plantes sont quasi identiques.
En revanche, avec une temprature au sol dpassant les
450 C, une pression atmosphrique crasante de 92 bars
(9200 kPa) et des pluies dacide sulfurique, Vnus peut tre
qualifie de vritable enfer.
Selon les chercheurs, il nen a pas toujours t ainsi. Peu
de choses distinguaient Vnus de la Terre, il y a 4,5 milliards
dannes. Vnus a probablement mme abrit un ocan !
Les deux plantes possdaient de leau, mais aussi une
grande quantit de CO2.
Vnus est plus proche du Soleil. Son atmosphre tait donc
plus chaude, ce qui a permis lvaporation et la formation
de vapeur deau, un gaz effet de serre encore plus
puissant que le CO2.
La plante Vnus.
En raison de cet effet de serre grandissant, locan primitif de Vnus sest
108
entirement vapor dans latmosphre. Quant au CO , pig sur Terre sous
PARTIE I
L E S GA Z
THORIE
forme de carbonates, il occupe aujourdhui 96,5 % de latmosphre vnusienne.
Adapt de : Journal de lastronomie et de lespace, Science Actualits,
Vnus : une Terre qui aurait mal tourn ? [en ligne]. (Consult le 16 novembre 2008.)
108
PARTIE I
L E S GA Z
THORIE
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page109
Nom :
Groupe :
Date :
Exercices
2.2
La loi gnrale des gaz
1. Nous avons tudi plusieurs lois simples dans ce chapitre. Toutefois, deux dentre elles nont pas t
abordes, comme la relation entre la temprature et la quantit de gaz.
a) Daprs vous, quelle est la relation qui existe entre la temprature et la quantit de gaz, si on garde
la pression et le volume constants ? Expliquez votre rponse en vous basant sur la thorie cintique
des gaz.
La relation entre la temprature et la quantit de gaz est inversement proportionnelle. En effet,
lorsquon augmente la temprature, les particules de gaz bougent plus vite. Il en rsulterait
une augmentation du nombre de collisions si lon ne maintenait pas la pression constante.
CHIMIE
Afin de conserver la mme frquence de collisions, le nombre de particules de gaz doit diminuer.
CHAPITRE
b) Quelle formule reprsente cette relation ?
n 1T1 = n 2T2
ERPI Reproduction interdite
2. Les ballons-sondes, utiliss pour effectuer des
1. V1 = ?
3.
2. P1 = 102,6 kPa
T1 = 22,4 C + 273 = 295,4 K
P2 = 20 kPa
V2 = 120 000 L
T2 = 60 C + 273 = 213 K
60 km
30 C
mesures mtorologiques, sont conus pour
atteindre leur volume maximal et clater une
certaine altitude. Les mtorologues peuvent alors
rcuprer leurs instruments et enregistrer les
mesures effectues. La figure ci-contre montre
la temprature et la pression qui rgnent dans
les premiers kilomtres daltitude de latmosphre.
Si on utilise un ballon ayant un volume maximal
de 120 000 L, et que les conditions au sol sont
de 22,4 C et de 102,6 kPa, quel volume dhlium
faut-il injecter dans le ballon au dpart pour quil
atteigne son volume maximal 10 km daltitude ?
ble
ligea
Ng
50 km
10 C
Pa
0,1 k
20 C
0,3
40 C
60 C
20 km
kPa
10 km
kPa
20
15 C
30 km
a
1 kP
60 C
40 km
kPa
Pa
,3 k
Niveau
de la
mer
101
Temprature
moyenne
Pression moyenne
Altitude
P1V1 P2V2
T1 = T2
Do V1 =
P2V2T1
P1T2
20 kPa 120 000 L 295,4 K
102,6 kPa x 213 K
= 32 441 L
4. V1 =
5. Le volume dhlium injecter dans le ballon est de 32 000 L.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
109
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page110
Nom :
Groupe :
Date :
3. Un ballon, qui contient 0,300 mol de dioxyde de carbone, occupe un volume de 2,50 L une
temprature de 173 C et une pression de 90,0 kPa. Quelle sera la pression si on double la
quantit de gaz, quon augmente le volume de 4,00 L et quon chauffe le tout jusqu 27 C ?
1. P2 = ?
PV P V
3. n1 T 1 = n2 T 2
1 1
2 2
2. P1 = 90,0 kPa
V1 = 2,50 L
n 1 = 0,300 mol
T1 = 173 C + 273 = 100 K
V2 = 6,50 L
n 2 = 0,600 mol
T2 = 27 C + 273 = 300 K
PVn T
Do P2 = n1 T1 V2 2
1 1 2
90,0 kPa x 2,50 L 0,600 mol 300 K
0,300 mol 100 K 6,50 L
= 208 kPa
4. P2 =
5. La pression sera de 208 kPa.
4. Un gaz occupe un volume de 64,2 L une temprature et une pression donnes. Quel sera le volume
de ce gaz si on diminue la temprature absolue de moiti, quon quadruple la pression et quun tiers
des particules schappent du contenant ?
1. V2 = ?
2. P1 = x
V1 = 64,2 L
n1 = y
T1 = z
P2 = 4x
2
n2 = 3 y
1
T2 = 2 z
Do V2 =
4. V2 =
x 64,2 L 2 /3y 1 /2z
y z 4x
= 5,35 L
5. Le volume du gaz sera de 5,35 L.
110
P1 V1 n 2T2
n 1T1P2
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
PV P V
3. n1 T 1 = n2 T 2
1 1
2 2
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page111
Nom :
Groupe :
Date :
5. Un ballon contenant 134,4 g de dioxygne est reli un manomtre qui indique une pression de
85,00 kPa. Quelle sera la pression mesure si on ajoute 207,2 g de diazote, quon double la
temprature absolue et quon diminue le volume au tiers de sa valeur ?
1. P2 = ?
PV P V
3. n1 T 1 = n2 T 2
1 1
2 2
2. P1 = 85,00 kPa
T1 = x
V1 = y
P1 V1 n 2T2
Do P2 = V
2 n 1T1
m
134,4 g
n 1 = 4,200 mol (nO2 = M = 32,00 g/mol ) 4. P = 85,00 kPa y 11,595 mol 2x
2
1 /3y 4,200 mol x
T2 = 2x
= 1408 kPa
1
V2 = 3 y
CHAPITRE
n 2 = 4,200 mol + 7,395 mol
m
207,2 g
= 11,595 mol (nN2 = M = 28,02 g/mol )
CHIMIE
5. La pression mesure sera de 1408 kPa.
6. Les gaz comprims sont trs utiles. Par exemple,
un compresseur air peut actionner certains outils,
comme la cloueuse illustre ci-contre. Quel volume dair
serait-il ncessaire dajouter aux conditions ambiantes, pour
que la pression interne dun rservoir de 20,00 L soit
de 2645 kPa ?
ERPI Reproduction interdite
1. V1 = ?
4. V1 =
2. P1 = 101,3 kPa
T1 = 25 C + 273 = 298 K
P2 = 2645 kPa
V2 = 20,00 L
T2 = 298 K
2645 kPa 20,00 L
101,3 kPa
= 522,2 L
5. Le volume dair ncessaire serait de 522,2 L.
Il y a 20,00 L dair dans le rservoir.
522,2 L 20,00 L = 502,2 L
3. P1V1 = P2V2
Do V1 =
P2V2
P1
Il faudrait ajouter 502,2 L dair.
Consulter le Compagnon Web pour dautres exercices en lien avec la section 2.2.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
111
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page112
Nom :
2.3
Groupe :
Date :
La loi des gaz parfaits
1. On emprisonne un gaz parfait dans une seringue.
a) Quarrivera-t-il aux particules de gaz si on diminue la temprature absolue de moiti ?
Les particules de gaz bougeront quatre fois moins vite. Elles auront deux fois moins dnergie
cintique.
b) Quarrivera-t-il la pression et au volume si on diminue la temprature jusqu 0 K ?
La pression et le volume seront nuls.
c) Si on remplace le gaz parfait par du diazote et quon diminue la temprature jusqu 0 K, le gaz
aura-t-il le mme comportement que le gaz parfait ? Expliquez votre rponse.
Non, le diazote naura pas le mme comportement. En effet, le diazote se liqufiera avant
datteindre 0 K (il se liqufie 196 C).
2. Le volume intrieur du cylindre dune pompe vlo est de 500 ml. Quelle quantit de gaz peut-il
contenir une temprature de 20 C et une pression de 860 kPa ?
1. n = ?
860 kPa 0,500 L
4. n = 8,314 kPa L/mol K 293 K
2. P = 860 kPa
V = 500 ml = 0,500 L
R = 8,314 kPa L/mol K
T = 20 C + 273 = 293 K
ERPI Reproduction interdite
= 0,18 mol
3. PV = nRT
PV
Do n = RT
5. Le cylindre peut contenir 0,18 mol de gaz.
112
PARTIE I
L E S GA Z
EXERCICES
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page113
Nom :
Groupe :
Date :
3. Un scientifique prtend avoir dcouvert un nouveau gaz parfait. Le comit de rvision scientifique
a pris quelques mesures pour sassurer de la vracit de cette dcouverte. Voici quelques rsultats
de son enqute :
une temprature de 100,0 C et une pression de 300,0 kPa, le volume dune mole du nouveau
gaz est de 5,00 L.
Quelle est la conclusion du comit de rvision ? Expliquez votre rponse laide de calculs.
1. R = ?
300,0 kPa 5,00 L
1 mol 173,0 K
= 8,67 kPa L/mol K
4. R =
2. P = 300,0 kPa
V = 5,00 L
T = 100,0 C + 273 = 173,0 K
n = 1 mol
CHAPITRE
CHIMIE
3. PV = nRT
PV
Do R = nT
5. La constante est de 8,67 kPa L/mol K. Le gaz nest pas parfait, puisque la constante nest
pas gale 8,314 kPa L/mol K.
4. Une bouteille de 135 L contient une certaine quantit de dioxyde de soufre (SO2 ) une temprature
de 85 C et une pression de 245 kPa. Quelle masse de gaz cette bouteille contient-elle ?
ERPI Reproduction interdite
1. n = ?
2. P = 245 kPa
V = 135 L
R = 8,314 kPa L/mol K
T = 85 C + 273 = 358 K
245 kPa 135 L
4. n = 8,314 kPa L/mol K 358 K
= 11,1 mol de dioxyde de soufre
Calcul de la masse
m
M= n
Do m = Mn
= 64,07 g/mol 11,1 mol
= 711,2 g
3. PV = nRT
PV
Do n = RT
5. La bouteille contient 711 g de dioxyde de soufre.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
113
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page114
Nom :
Groupe :
Date :
5. Un tube fluorescent de 750 ml contient 1,22 102 g dun gaz. une temprature de 22 C,
la pression dans le tube nest que de 1,00 kPa. Quel est ce gaz parmi les suivants : hlium, non, argon
ou krypton ?
1,00 kPa 0,750 L
4. n = 8,314 kPa L/mol K 295 K = 3,06 104 mol
1. M = ?
2. P = 1,00 kPa
V = 750 ml = 0,750 L
R = 8,314 kPa L/mol K
T = 22 C + 273 = 295 K
m = 1,22 102 g
1,22 102 g
= 39,9 g/mol
3,06 104 mol
5. La masse molaire est de 39,9 g/mol.
M=
3. PV = nRT
PV
Do n = RT
m
M= n
Le gaz contenu dans le tube fluorescent est de largon.
6. Nadia veut emmagasiner 4,5 mol dhlium 205,6 kPa et 22 C. Quel doit tre le volume du
contenant utiliser ?
1. V = ?
4. V =
2. P = 205,6 kPa
n = 4,5 mol
R = 8,314 kPa L/mol K
T = 22 C + 273 = 295 K
4,5 mol 8,314 kPa L/mol K 295 K
205,6 kPa
ERPI Reproduction interdite
= 53,7 L
3. PV = nRT
nRT
Do V = P
5. Le volume du contenant doit tre de 54 L.
Consulter le Compagnon Web pour dautres exercices en lien avec la section 2.3.
114
PARTIE I
L E S GA Z
EXERCICES
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page115
Nom :
2.4
Groupe :
Date :
La loi des pressions partielles
1. Un mlange de dioxyde de carbone et de monoxyde de carbone est recueilli par dplacement deau
une pression de 102,6 kPa et une temprature de 21 C. Si la pression du dioxyde de carbone
est de 80,2 kPa, quelle est la pression du monoxyde de carbone ?
1. PpCO = ?
4. PpCO = 102,6 kPa 80,2 kPa 2,49 kPa
= 19,9 kPa
2. PT = 102,6 kPa
PpCO2 = 80,2 kPa
PpH2O 21 C = 2,49 kPa
3. PT = PpCO2 + PpCO + PpH2O
CHIMIE
CHAPITRE
Do PpCO = PT PpCO2 PpH2O
5. La pression partielle du monoxyde de carbone est de 19,9 kPa.
2. Dans un ballon de 10 L, Ibtissem mlange 5,00 mol de dioxyde de carbone avec 7,00 mol de dioxyde
ERPI Reproduction interdite
de soufre. Elle mesure alors une pression de 260 kPa. Quelle est la pression partielle de chacun
des gaz ?
1. PpCO2 = ?
PpSO2 = ?
2. nCO2 = 5,00 mol
nSO2 = 7,00 mol
PT = 260 kPa
4. PpCO2 =
260 kPa 5,00 mol
= 108 kPa
12,00 mol
PpSO2 =
260 kPa 7,00 mol
= 152 kPa
12,00 mol
n
3. PpA = PT nA
T
5. La pression partielle du CO2 est de 108 kPa et celle du SO2 est de 152 kPa.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
115
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page116
Nom :
Groupe :
Date :
3. Trois bouteilles de 15 L contiennent respectivement du mthane (CH4 ) une pression de 195,4 kPa,
du propane (C3H8 ) une pression de 257,8 kPa et du butane (C4H10 ) une pression de 178,3 kPa.
Si on transfre les trois gaz dans la mme bouteille, quelle sera la pression mesure ?
MTHANE
PROPANE
BUTANE
CH4
C3H8
C4H10
1. PT = ?
4. PT = 195,4 kPa + 257,8 kPa + 178,3 kPa
= 631,5 kPa
2. PpCH4 = 195,4 kPa
PpC3H8 = 257,8 kPa
PpC4H10 = 178,3 kPa
3. PT = PpCH4 + PpC3H8 + PpC4H10
5. La pression totale dans la bouteille sera de 631,5 kPa.
4. Un ballon contient 0,34 g dhlium, 0,68 g de non et 0,34 g de krypton. Quelle est la pression totale
1. PT = ?
m
0,34 g
2. nHe = MHe = 4,00 g/mol = 0,085 mol
He
n
3. PpNe = PT nNe
T
m
0,68 g
NNe = MNe = 20,18 g/mol = 0,034 mol
Ne
m
0,34 g
nKr = MKr = 83,80 g/mol = 0,0041 mol
Kr
Do PT =
4. PT =
PpNe = 260 kPa
PpNenT
nNe
260 kPa 0,1231 mol
0,034 mol
= 941,4 kPa
5. La pression totale du mlange gazeux est de 941,4 kPa.
Consulter le Compagnon Web pour dautres exercices en lien avec la section 2.4.
116
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
si le non exerce une pression de 260 kPa ?
11120_cyr_ch_02-c-c_3.qxd:Layout 1
5/18/10
9:41 AM
Page 117
CHAPITRE
Rsum
Le comportement des gaz
2.1 LES LOIS SIMPLES DES GAZ
Les scientifiques ont tabli des normes quant aux conditions dtude des gaz.
On distingue :
les conditions de temprature et de pression normales (TPN) : une temprature de 0 C et une pression de 101,3 kPa;
les conditions de temprature ambiante et de pression normale (TAPN), ou
conditions ambiantes: une temprature de 25 C et une pression de 101,3 kPa.
La loi de Boyle-Mariotte indique que, temprature constante, le volume dune
masse de gaz est inversement proportionnel la pression. Si on augmente la
pression, le volume diminue, et vice versa. Ainsi :
P 1
OU PV = constante
V
La loi de Charles indique que, pression constante, le volume dune certaine quantit de gaz est directement proportionnel la temprature absolue. Lorsque la
temprature augmente, le volume du gaz augmente, et vice versa. Ainsi :
V T OU V = constante
T
Lchelle des kelvins, ou chelle des tempratures absolues, est une chelle
parallle celle des degrs Celsius. Pour convertir une temprature dune
chelle lautre, il faut effectuer lopration mathmatique suivante :
2
CHAPITRE
Pour dfinir les caractristiques dun chantillon de gaz et pour tudier son comportement, quatre variables sont ncessaires : la pression, la temprature, le
volume et la quantit de gaz.
CHIMIE
ERPI Reproduction interdite
T (en K) = T (en C) + 273
volume constant, la pression dun chantillon de gaz est directement proportionnelle la temprature absolue. Ainsi :
P = constante
P T OU
T
Selon lhypothse dAvogadro, des volumes gaux de gaz, aux mmes conditions
de temprature et de pression, contiennent le mme nombre de particules.
La loi dAvogadro indique que, temprature et pression constantes, le volume
dun gaz est directement proportionnel au nombre de moles du gaz. Si on
augmente la quantit de gaz, son volume augmente, et vice versa. Ainsi :
V n OU V = constante
n
Le volume molaire dun gaz est le volume quoccupe une mole de gaz, quelle
que soit la nature de ce gaz, une temprature et une pression donnes. Le
volume molaire sexprime en L/mol :
TPN, le volume molaire dun gaz est denviron 22,4 L/mol;
TAPN, il est de 24,5 L/mol.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
THORIE
117
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page118
En rsum, voici les lois simples des gaz :
LES FORMULES DES LOIS SIMPLES DES GAZ
Loi
Formule
Relation entre la pression et le volume
P1V1 = P2V2
V1
V
= 2
T1
T2
P1
P
= 2
T1
T2
Relation entre le volume et la temprature
Relation entre la pression et la temprature
V1
V
= 2
n1
n2
Relation entre le volume et la quantit de gaz
2.2 LA LOI GNRALE DES GAZ
La loi gnrale des gaz met en relation la pression, le volume, la temprature et
la quantit de gaz en comparant une situation initiale avec une situation finale.
Cette loi sexprime par la formule mathmatique suivante :
P1V1 P2V2
=
n1T1
n2T2
La loi des gaz parfaits met en relation la pression, le volume, la temprature et
la quantit de gaz un moment donn. Afin dtablir une galit, on utilise une
constante, symbolise par la lettre R.
La forme la plus courante de cette loi est la suivante :
PV = nRT
Un gaz parfait est un gaz qui, thoriquement, rpondrait toutes les lois simples
des gaz et dont le comportement pourrait tre expliqu par la thorie cintique.
haute temprature et basse pression, le comportement des gaz rels se rapproche de celui des gaz parfaits.
Voici la constante R des gaz parfaits :
8,314 kPa L/mol K
2.4 LA LOI DES PRESSIONS PARTIELLES
La pression partielle dun gaz dans un mlange correspond la pression quil
exercerait sil tait seul dans le volume occup par le mlange.
La loi des pressions partielles indique que, une temprature donne, la pression totale dun mlange gazeux est gale la somme des pressions partielles
exerces par chacun des gaz qui constituent le mlange.
Cette loi sexprime par la formule mathmatique suivante :
PT = PpA + PpB + PpC +
On peut aussi dterminer la pression partielle de chacun des gaz qui constituent
un mlange en multipliant la pression totale par la proportion que le gaz reprsente dans le mlange. Ainsi :
nA
PpA = PT
nT
118
PARTIE I
L E S GA Z
THORIE
ERPI Reproduction interdite
2.3 LA LOI DES GAZ PARFAITS
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page119
Nom :
Groupe :
Date :
Exercices sur lensemble du chapitre 2
1. Le volume dun ballon gonfl lhlium augmente au fur
et mesure quil slve dans la troposphre.
Quel nonc explique cette augmentation de volume ?
Encerclez la bonne rponse. Expliquez pourquoi chacun
des noncs correspond ou ne correspond pas la bonne
rponse.
a) Lhlium contenu dans le ballon est plus lger que lair.
Le fait que lhlium soit plus lger que lair explique
le fait quil slve dans la troposphre, mais non que
2
le volume diminue. Donc, la diminution de temprature ne peut expliquer le fait que le volume
augmente.
ERPI Reproduction interdite
c) La pression atmosphrique diminue au fur et mesure que laltitude augmente.
Comme le volume est inversement proportionnel la pression, le fait que la pression diminue
explique le fait que le volume augmente au fur et mesure que le ballon slve.
d) Lhlium contenu dans le ballon diffuse plus rapidement que les gaz de lair.
Comme lhlium est emprisonn dans le ballon, sa vitesse de diffusion ne peut expliquer
laugmentation de volume.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
119
CHIMIE
b) La temprature de lair dans la troposphre diminue au fur et mesure que laltitude augmente.
Comme le volume est directement proportionnel la temprature, si la temprature diminue,
CHAPITRE
son volume augmente.
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page120
Nom :
Groupe :
Date :
2. Un ballon de 2,5 L contient 0,36 mol dhlium la temprature ambiante. Si on veut augmenter
le volume du ballon de 4,0 L sans changer la pression et la temprature, quelle quantit de gaz
devra-t-on ajouter ?
1. n2 = ?
6,5 L 0,36 mol
2,5 L
= 0,94 mol
4. n2 =
2. V1 = 2,5 L
n 1 = 0,36 mol
V2 = 2,5 + 4,0 L = 6,5 L
5. La quantit finale de gaz sera de 0,94 mol.
0,94 mol 0,36 mol = 0,58 mol
V
V
3. n 1 = n 2
1
2
Vn
Do n2 = V2 1
1
On devra ajouter 0,58 mol dhlium.
3. Alexandre veut gonfler le pneu compltement plat de son vlo laide dune petite pompe manuelle.
Le cylindre de cette pompe contient 120 ml dair une pression de 100 kPa. Le pneu peut contenir
environ 2,5 L dair une pression de 360 kPa. Combien de coups de pompe Alexandre devra-t-il
donner pour gonfler ce pneu ?
4. V1 =
2. P1 = 100 kPa
P2 = 360 kPa
V2 = 2,5 L = 2500 ml
360 kPa 2500 ml
= 9000 ml
100 kPa
5. Il faut 9000 ml dair.
9000 ml
120 ml = 75
3. P1V1 = P2V2
PV
Do V1 = 2P 2
1
Alexandre devra donner 75 coups de pompe.
120
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
1. V1 = ?
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page121
Nom :
Groupe :
Date :
4. Au cours dune fte, on gonfle des ballons lhlium jusqu ce quils atteignent un volume de 1,4 L
aux conditions ambiantes. Si un ballon russit schapper, quel sera son volume une altitude
o la pression nest que de 68 kPa et la temprature, de 5 C ?
1. V2 = ?
101,3 kPa 1,4 L 268 K
68 kPa 298 K
= 1,9 L
4. V2 =
2. P1 = 101,3 kPa
T1 = 25 C + 273 = 298 K
V1 = 1,4 L
P2 = 68 kPa
T2 = 5 C + 273 = 268 K
P1V1 P2V2
T1 = T2
CHAPITRE
PVT
Do V2 = P1 T1 2
2 1
5. Le volume du ballon sera de 1,9 L.
5. Un extincteur de 3 L contient 5,000 kg de dioxyde de carbone comprim. Lorsquon vide lextincteur,
le gaz prend de lexpansion, ce qui a la proprit dteindre le feu par touffement.
a) Si le gaz est expuls dun seul coup, quel sera le volume de gaz qui schappera aux conditions
ambiantes ?
1. V =?
4. V =
ERPI Reproduction interdite
2. P = 101,3 kPa
mCO
5 000 g
n = M 2 = 44,01 g/mol = 113,6 mol
CO2
R = 8,314 kPa L/mol K
T = 25 C + 273 = 298 K
113,6 mol 8,314 kPa L / mol K 298 K
101,3 kPa
= 2778,4 L
5. Le volume est de 2778,4 L. Il reste 3 L dans
lextincteur.
Donc, 2778,4 L 3 L = 2775 L
3. PV = nRT
nRT
Do V = P
Le volume du gaz qui schappera sera de 2775 L.
b) Lors dun incendie, obtiendra-t-on le mme volume de gaz expuls ? Expliquez votre rponse.
Non, le volume sera plus grand, puisque le volume est directement proportionnel la temprature.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
121
CHIMIE
3.
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page122
Nom :
Groupe :
Date :
6. une temprature de 20 C, deux bouteilles identiques contiennent chacune la mme masse de gaz.
Une bouteille contient du dihydrogne et lautre contient de lhlium. Quel nonc concernant la
pression dans chacune des bouteilles est vrai ? Expliquez pourquoi.
a) La pression exerce par le dihydrogne est quatre fois plus grande que celle exerce par lhlium.
b) La pression exerce par le dihydrogne est deux fois plus grande que celle exerce par lhlium.
c) La pression exerce par le dihydrogne est gale la pression exerce par lhlium.
d) La pression exerce par le dihydrogne est deux fois plus petite que celle exerce par lhlium.
Lnonc b) est vrai. Comme la masse molaire du dihydrogne est deux fois plus petite que celle
de lhlium, pour une mme masse, il y aura deux fois plus de molcules de dihydrogne que dhlium.
Comme la pression est directement proportionnelle au nombre de particules de gaz, la pression
du dihydrogne sera deux fois plus grande que celle de lhlium.
Alexis a not les donnes rassembles
dans le tableau ci-contre.
Quel est le gaz contenu dans la seringue
parmi les suivants : H2, N2, O2 ou CO2 ?
Expliquez votre rponse.
Variable
Rsultat
Volume de gaz contenu dans la seringue
75 ml
Masse de la seringue vide
76,583 g
Masse de la seringue contenant le gaz
76,670 g
Temprature
22,6 C
Pression du gaz
102,6 kPa
1. M = ?, donc n = ?
2. P = 102,6 kPa
V = 75 ml = 0,075 L
R = 8,314 kPa L/mol K
T = 22,6 C + 273 = 295,6 K
m = 76,670 g 76,583 g = 0,087 g
102,6 kPa 0,075 L
4. n = 8,314 kPa L/mol K 295,6 K
= 0,0031 mol
5. La seringue contient 0,0031 mol.
m
0,087 g
M = n = 0,0031 mol = 28,06 g/mol
3. PV = nRT
PV
Do n = RT
Le gaz contenu dans la seringue est probablement du diazote, puisque sa masse molaire
se rapproche de 28,2 g/mol.
122
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
7. Au cours dune exprience en laboratoire,
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page123
Nom :
Groupe :
Date :
8. Magali recueille un chantillon dargon 100,0 C et 330,0 kPa.
a) Quel est le volume molaire de largon dans ces conditions ?
1. V = ?
2. P = 330,0 kPa
n = 1 mol
R = 8,314 kPa L/mol K
T = 100,0 C + 273 = 373,0 K
3. PV = nRT
nRT
Do V = P
CHAPITRE
1 mol x 8,314 kPa L/mol K x 373,0 K
= 9,397 L
330,0 kPa
CHIMIE
4. V =
5. Le volume molaire de largon est de 9,397 L.
b) Combien datomes dargon contient ce volume ? Expliquez votre rponse.
Ce volume contient 6,02 10 23 atomes dargon, puisque le volume molaire correspond au
volume dune mole de gaz.
c) Si on remplace largon par de lhlium, quel est le volume molaire de ce gaz dans les mmes
conditions ? Expliquez votre rponse.
Le volume molaire de lhlium est de 9,397 L, puisque le volume molaire ne dpend pas de la
ERPI Reproduction interdite
nature du gaz quil contient.
9. En vous appuyant sur la thorie cintique des gaz, expliquez pourquoi la pression augmente
lintrieur dun pneu au cours dune journe chaude.
Lorsque la temprature augmente, lnergie cintique des particules de gaz augmente, donc elles
bougent plus vite. Il en rsulte que le nombre de collisions augmente, ce qui fait augmenter la pression.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
123
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page124
Nom :
Groupe :
Date :
10. Andranne veut gonfler 120 ballons de 20,0 L avec de lhlium. Le fournisseur indique que ce gaz
se vend dans des bouteilles de 25 L dont la pression interne est de 6000 kPa une temprature
de 25 C. Si la temprature dans la pice est de 20 C et que la pression est de 100 kPa au moment
de gonfler les ballons, combien de bouteilles Andranne devra-t-elle acheter ?
1. V2 = ?
100 kPa 2400 L 298 K
6000 kPa 293 K
= 40,7 L
4. V2 =
2. P1 = 100 kPa
T1 = 20 C + 273 = 293 K
V1 = 20,0 L 120 = 2400 L
P2 = 6000 kPa
T2 = 25 C + 273 = 298 K
3.
5. Le volume ncessaire est de 40,7 L.
Calcul du nombre de bouteilles
40,7 L
25 L = 1,6
P1V1 P2V2
T1 = T2
PVT
Do V2 = P1 T1 2
2 1
Andranne devra acheter 2 bouteilles dhlium de 25 L.
Un ballon de verre de 2,5 L contient 3,8 g de mthane (CH4 ). On vide le ballon et on remplace
le mthane par du non (Ne). Si la temprature et la pression nont pas chang durant lchange,
quelle masse de non contient le ballon ?
1. mNe = ?
mCH
3,8 g
4. nCH4 = M 4 = 16,05 g/mol = 0,24 mol
CH4
2. mCH4 = 3,8 g
V, T et P constants
m
3. M = n
mNe = MNenNe = 20,18 g/mol x 0,24 mol = 4,8 g
nCH4 = nNe
5. La masse de non contenu dans le ballon est de 4,8 g.
124
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
11.
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page125
Nom :
Groupe :
Date :
12. Trois ballons identiques de 500 ml contiennent des gaz diffrents aux conditions ambiantes.
Le premier contient du N2, le deuxime du O2 et le troisime du CO2.
a) Lequel des trois ballons contient le plus grand nombre de molcules ? Expliquez votre rponse.
Ils contiennent le mme nombre de molcules, puisquils sont aux mmes conditions de volume,
de pression et de temprature.
b) Quelle masse de gaz est contenu dans chaque ballon ?
PV = nRT
2
CHAPITRE
PV
101,3 kPa 0,500 L
n = RT = 8,314 kPa L/mol K 298 K = 0,0204 mol
mN2 = 28,02 g/mol 0,0204 mol = 0,572 g
mO2 = 32,00 g/mol 0,0204 mol = 0,653 g
CHIMIE
mCO2 = 44,01 g/mol 0,0204 mol = 0,898 g
ERPI Reproduction interdite
Le premier ballon contient 0,572 g de N2. Le deuxime contient 0,653 g de O2. Le troisime
contient 0,898 g de CO2.
c) Lequel des trois gaz possde la plus grande nergie cintique ? Expliquez votre rponse.
Les trois gaz possdent la mme nergie cintique, puisquils sont la mme temprature.
d) Si les ballons sont extensibles, quel effet aura une augmentation de temprature sur la masse
volumique des gaz ?
La masse volumique diminuera, puisque le volume augmente. En effet, le volume est directement
proportionnel la temprature.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
125
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page126
Nom :
Groupe :
Date :
13. Le technicien dun laboratoire remplit un contenant avec 0,90 g de CO2. Il note alors une pression
de 100 kPa et une temprature de 20 C. Il vide le contenant et le remplit de nouveau avec 0,68 g
dun gaz inconnu. Il note alors une pression de 235 kPa et une temprature de 60 C. Quelle est
la masse molaire de ce gaz inconnu ?
Voici une faon de rsoudre ce problme :
1. Mx = ?
nx = ?
4. n2 =
2. P1 = 100 kPa
mCO
0,90 g
n1 = M 2 = 44,01 g/mol = 0,020 mol
CO2
T1 = 20 C + 273 = 293 K
P2 = 235 kPa
T2 = 60 C + 273 = 333 K
235 kPa 0,020 mol 293 K
333 K 100 kPa
= 0,041 mol
5. Le nombre de moles du gaz inconnu
est de 0,041 mol.
m
0,68 g
Mx = n x = 0,041 mol = 16,6 g/mol
x
P
P
3. n T1 = n T2
1 1
2 2
Do n2 =
P2n1T1
T2P1
La masse molaire du gaz inconnu est de 17 g/mol.
14. Un poisson relche des bulles de gaz de 0,80 ml une profondeur de 20 m sous leau, o la
1. T2 = ?
3.
P1V1 P2V2
T1 = T2
2. P1 = 102,3 kPa + 2 100,0 kPa = 302,3 kPa
P2V2T1
V1 = 0,80 ml
Do T2 = P
1V1
T1 = 8,0 C + 273 = 281,0 K
V2 = 0,80 ml 3 = 2,40 ml
102,3 kPa 2,40 ml 281,0 K
4.
T
=
= 285 K
2
P2 = 102,3 kPa
302,3 kPa 0,80 ml
5. La temprature la surface de leau est de 285 K, soit 12 C.
Consulter le Compagnon Web pour dautres exercices sur lensemble du chapitre 2.
126
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
temprature nest que de 8,0 C. Une fois parvenues la surface, juste avant dclater, les bulles
atteignent un volume trois fois plus grand. Si la pression atmosphrique est de 102,3 kPa et que la
pression dans leau augmente de 100,0 kPa chaque 10 m, quelle est la temprature mesure la
surface de leau ?
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page127
Nom :
Groupe :
Date :
Dfis
1. Une tudiante recueille un certain volume de dihydrogne par dplacement deau, une pression
de 102,6 kPa. Elle dtermine que lchantillon contient 2,00 10 3 moles de dihydrogne et
6,0 10 5 moles de vapeur deau. quelle temprature le dihydrogne a-t-il t recueilli ?
1. PpH2O = ?
102,6 kPa 6,0 x 105 mol
2,06 103 mol
= 2,99 kPa
4. PpH2O =
2. nH2 = 2,0 10 3 mol
nH2O = 6,0 10 5 mol
PT = 102,6 kPa
5. La pression de la vapeur deau est de 3 kPa.
2
CHIMIE
CHAPITRE
nH O
3. PpH2O = PT n2
T
Le gaz a t recueilli une temprature de 24 C.
2. Dans un ballon de 10,0 L, 2,00 L dargon ayant une pression de 250 kPa sont mlangs avec 2,50 L
de krypton ayant une pression de 300 kPa. Quelle sera la pression totale dans le ballon aprs
le mlange, si on considre que la temprature est demeure constante ?
ERPI Reproduction interdite
1. PT = ?
2. PAr = 250 kPa avec V = 2,00 L
PKr = 300 kPa avec V = 2,50 L
V du mlange = 10,0 L
P V 250 kPa 2,00 L
4. PpAr = P2 = V1 1 =
= 50,0 kPa
10,0 L
2
PV
300 kPa 2,50 L
PpKr = P2 = V1 1 =
= 75,0 kPa
10,0 L
2
PT = 50,0 kPa + 75,0 kPa = 125 kPa
3. P1V1 = P2V2
PT = PpAr + PpKr
5. La pression totale dans le ballon sera de 125 kPa.
CHAPITRE 2
L E CO M P O RT E M E N T D E S GA Z
EXERCICES
127
11120_cyr_ch_02-p109-128_Layout 1 2013-06-04 16:38 Page128
Nom :
Groupe :
Date :
3. On place 10,0 g de glace sche dans un contenant tanche de 50,0 L dont la temprature est de
22 C et la pression, de 100,0 kPa. La glace sche se transforme directement en gaz, sans passer par
la phase liquide, selon lquation suivante :
CO2(s) CO2(g)
Lorsque la glace sche se sublime, elle absorbe une partie de lnergie environnante, ce qui a pour
effet dabaisser la temprature de lair ambiant. Quelle sera la pression dans le contenant lorsque tout
le CO2 se sera sublim et que la temprature se sera stabilise 4 C ?
1. PT = ?
PV = nRT
2. PAir = 100,0 kPa
T1 = 22 C + 273 = 295 K
T2 = 4 C + 273 = 277 K
V = 50,0 L
mCO
10,0 g
nCO2 = M 2 = 44,01 g/mol
CO2
Do PCO2 =
4. PAir =
nCO2RT
V
100,0 kPa 277 K
295 K
= 93,9 kPa
0,227 mol 8,314 kPa L/mol K 277 K
50,0 L
= 10,5 kPa
= 0,227 mol
PCO2 =
3. PT = PpAir + PpCO2 4,0 C
P1 P2
T1 = T2
PT = 93,9 kPa + 10,5 kPa = 104,4 kPa
PT
Do PAir = T1 2
1
5. La pression totale dans le contenant sera de 104,4 kPa.
La premire exprience se droule une pression constante P1. Avant damorcer la deuxime, Chlo
modifie la pression, jusqu une nouvelle pression, P2. Elle sassure alors de la garder constante tout au
long de la deuxime exprience. Les tableaux suivants contiennent les rsultats que Chlo a obtenus.
LE VOLUME DU GAZ EN FONCTION DE LA
TEMPRATURE P1
LE VOLUME DU GAZ EN FONCTION DE LA
TEMPRATURE P2
Temprature (en K)
Volume (en ml)
Temprature (en K)
Volume (en ml)
100
25
100
50
200
50
200
100
300
75
300
150
400
100
400
200
500
125
500
250
La pression P1 est-elle plus grande ou plus petite que la pression P2? Expliquez votre rponse.
La pression P1 est plus petite que la pression P2 puisque, une temprature donne, le volume P1 est
plus grand que celui P2. Plus le volume est grand, plus la pression est petite.
128
PARTIE I
L E S GA Z
EXERCICES
ERPI Reproduction interdite
4. Chlo effectue deux expriences afin de dmontrer la relation entre le volume et la temprature dun gaz.
Vous aimerez peut-être aussi
- Cours - 4 Gaz Parfait PDFDocument22 pagesCours - 4 Gaz Parfait PDFBilal Bouakrif100% (1)
- Chimie Corrige Ch2 Partie1Document8 pagesChimie Corrige Ch2 Partie1Jimmy NguyenPas encore d'évaluation
- Os Chimie Corrige Ch6Document52 pagesOs Chimie Corrige Ch6Said SouhassouPas encore d'évaluation
- Chimie RappelDocument9 pagesChimie RappelWilliam SabourinPas encore d'évaluation
- Exercices: Qu'est-Ce Que La Vitesse de Réaction ?Document27 pagesExercices: Qu'est-Ce Que La Vitesse de Réaction ?Sarah Taibi El KettaniPas encore d'évaluation
- Exercices: L'énergie Et Ses FormesDocument29 pagesExercices: L'énergie Et Ses FormesSarah Taibi El Kettani100% (2)
- Os Chimie Corrige Ch1Document16 pagesOs Chimie Corrige Ch1laura sofia brunelle cyr100% (2)
- Os Chimie Corrige ch3 PDFDocument24 pagesOs Chimie Corrige ch3 PDFf.B100% (1)
- Os Chimie Corrige Ch8Document66 pagesOs Chimie Corrige Ch8Said Souhassou0% (1)
- Os Chimie Corrige ch3 PDFDocument24 pagesOs Chimie Corrige ch3 PDFFaria Haque0% (1)
- Os Chimie ch5 Ex Suppl CorrDocument16 pagesOs Chimie ch5 Ex Suppl CorrSarah Taibi El KettaniPas encore d'évaluation
- Os Chimie Corrige ch5Document21 pagesOs Chimie Corrige ch5Amellie Gendron100% (7)
- Corrige ManuelDocument9 pagesCorrige Manueleyohi86Pas encore d'évaluation
- Corrigé 6.3 ChimieDocument4 pagesCorrigé 6.3 ChimieMaeva SimPas encore d'évaluation
- Chimie Des Solutions by John W. Hill, Ralph H. Petrucci, Terry W. McCreary, Scott S. Perry, Réal CantinDocument519 pagesChimie Des Solutions by John W. Hill, Ralph H. Petrucci, Terry W. McCreary, Scott S. Perry, Réal CantinjosePas encore d'évaluation
- Os Chimie Chap1 p39-40 ExercicesDocument2 pagesOs Chimie Chap1 p39-40 ExercicesCassandra MaaloufPas encore d'évaluation
- Os Chimie Corrige ch7 PDFDocument38 pagesOs Chimie Corrige ch7 PDFAzizElheniPas encore d'évaluation
- Exercices: Les Lois Simples Des GazDocument29 pagesExercices: Les Lois Simples Des GazSarah Taibi El Kettani100% (1)
- Mécanique ch5Document24 pagesMécanique ch5Tanaj Tahya100% (1)
- Chimie Corrige ch7 Partie1Document2 pagesChimie Corrige ch7 Partie1api-278378684100% (2)
- Mécanique ch2Document19 pagesMécanique ch2Tanaj TahyaPas encore d'évaluation
- Os Chimie ch6 Ex Suppl CorrDocument12 pagesOs Chimie ch6 Ex Suppl CorrSarah Taibi El Kettani100% (1)
- Exercices: La Réactivité Chimique Des GazDocument12 pagesExercices: La Réactivité Chimique Des GazSarah Taibi El Kettani67% (3)
- Mod4 Corrige ch8 Partie2Document8 pagesMod4 Corrige ch8 Partie2api-278378684100% (1)
- Mécanique ch3Document18 pagesMécanique ch3Tanaj Tahya100% (1)
- Cinetique Chimique CoursDocument50 pagesCinetique Chimique CoursBeenani BeenaniPas encore d'évaluation
- 2nd AC - C8 Solutions Aqueuses IoniquesDocument10 pages2nd AC - C8 Solutions Aqueuses IoniquesYoman Arthur verdier Assui100% (1)
- Mécanique ch4Document18 pagesMécanique ch4Tanaj Tahya100% (1)
- Mécanique ch1Document18 pagesMécanique ch1Tanaj TahyaPas encore d'évaluation
- Mod3 Chimie Corrige ch6 1Document5 pagesMod3 Chimie Corrige ch6 1api-278378684100% (1)
- Série de TD de MDF - 2020 2021Document42 pagesSérie de TD de MDF - 2020 2021Boukerche MakhloufPas encore d'évaluation
- Sigma-Wataik 1ac PC Biof Guide-ProfDocument56 pagesSigma-Wataik 1ac PC Biof Guide-ProfYassine AarabPas encore d'évaluation
- Chimie Corrige ch8 1Document8 pagesChimie Corrige ch8 1api-278378684100% (1)
- Cours 13 Équilibres ChimiquesDocument4 pagesCours 13 Équilibres ChimiquesArti80% (5)
- Mathematiques Pour Les Sciences de La Vie Et de La SanteDocument160 pagesMathematiques Pour Les Sciences de La Vie Et de La SanteRakl LoPas encore d'évaluation
- Serien3 ThermochimieDocument2 pagesSerien3 Thermochimieamel100% (2)
- TD Thermochimie SVI1 PDFDocument2 pagesTD Thermochimie SVI1 PDFans1390Pas encore d'évaluation
- TD Chimie MPDocument109 pagesTD Chimie MPMahfoud Zaki75% (4)
- Cours 4-PPT DjaziaDocument25 pagesCours 4-PPT DjaziaLiza Linda DakarPas encore d'évaluation
- Diagrammes Thermodynamiques. GénéralitésDocument13 pagesDiagrammes Thermodynamiques. Généralitéslolph100% (1)
- Correction - TD 6 Acide BaseDocument8 pagesCorrection - TD 6 Acide BaseBILLBOARD TOP AFRICAPas encore d'évaluation
- SP 08 PDFDocument36 pagesSP 08 PDFOlivier Giroud le BâtonnierPas encore d'évaluation
- TD2 ThermochimieDocument2 pagesTD2 Thermochimieno one importantPas encore d'évaluation
- Exercices Chimi IndustrielleDocument7 pagesExercices Chimi IndustrielleMohamed khalido KHNPas encore d'évaluation
- Corrigé Série Thermodynamique ChimiqueDocument5 pagesCorrigé Série Thermodynamique ChimiqueAsdz Bab EzzouarPas encore d'évaluation
- Os Opt Corrige Ch3Document24 pagesOs Opt Corrige Ch3RKT100% (1)
- Tableau Periodique Des ElementsDocument2 pagesTableau Periodique Des Elementsdamien_roule5728Pas encore d'évaluation
- Cinétique Chimique Pour L3 Genie Des Procédés - Genie ChimiqueDocument452 pagesCinétique Chimique Pour L3 Genie Des Procédés - Genie ChimiqueMOUSSADEK Yahia Abdel Illah100% (1)
- Thermo Dy Nami QueDocument224 pagesThermo Dy Nami QueHalim Senhadji100% (2)
- Chimie GénéraleDocument55 pagesChimie Généralenova couliPas encore d'évaluation
- Thermochimie SMPC - TDDocument26 pagesThermochimie SMPC - TDoulaidPas encore d'évaluation
- Phys-Chimie Hachette2014Document16 pagesPhys-Chimie Hachette2014Sidhoum Sid100% (3)
- Fonction Valeur Absolue CoursDocument22 pagesFonction Valeur Absolue CoursCéline Lutti100% (1)
- Résumé de Chimie Organique PDFDocument7 pagesRésumé de Chimie Organique PDFzgazga amirPas encore d'évaluation
- Binaires ExercicesDocument8 pagesBinaires Exercicesfsk100% (1)
- Corrigé+sDocument7 pagesCorrigé+sMOHAMMEDMEJDOUBI100% (2)
- Les Lois Et Les Propriétés de GazDocument21 pagesLes Lois Et Les Propriétés de GazOussama Faratas LainePas encore d'évaluation
- TP N° 2 - La Masse MoléculaireDocument10 pagesTP N° 2 - La Masse MoléculaireNabilDouadiPas encore d'évaluation
- TP N° 2 (La Masse Moléculaire)Document7 pagesTP N° 2 (La Masse Moléculaire)Imene ImiPas encore d'évaluation
- MACHTHERMQDocument125 pagesMACHTHERMQravonantenaina rakotonindrainyPas encore d'évaluation
- Compte RenduDocument6 pagesCompte RenduAbdkrim HPas encore d'évaluation
- EtudCas BOISTECHDocument14 pagesEtudCas BOISTECHKhalil Touri0% (1)
- Exercices Moteur AsynchroneDocument3 pagesExercices Moteur AsynchroneChakib Ka100% (1)
- 300 LT YOURBAN - Remplissage - Purge Installation Des FreinsDocument5 pages300 LT YOURBAN - Remplissage - Purge Installation Des FreinsChristianFacchinettiPas encore d'évaluation
- 4 - Hydrostatique - ComposantsDocument69 pages4 - Hydrostatique - Composantszouhour brahmiPas encore d'évaluation
- Refroidisseurair Sintesis Prime RTAFDocument5 pagesRefroidisseurair Sintesis Prime RTAFstv7gcbg57Pas encore d'évaluation
- Tableau de Bord Social (TBS) 2002: Secteur Eau Et AssainissementDocument83 pagesTableau de Bord Social (TBS) 2002: Secteur Eau Et AssainissementHayZara Madagascar100% (2)
- Vignon Pierre 2020Document161 pagesVignon Pierre 2020Yassine EssertiPas encore d'évaluation
- Intermatic k4321c Instructions PDFDocument4 pagesIntermatic k4321c Instructions PDFJosePas encore d'évaluation
- 08 evaDivCM2Document6 pages08 evaDivCM2Jean-Philippe Solanet-Moulin100% (3)
- Plaquette L'envol VilleurbanneDocument6 pagesPlaquette L'envol VilleurbanneVigo MaestroPas encore d'évaluation
- Soutenance de StageDocument27 pagesSoutenance de StageIlyas BoutouahanPas encore d'évaluation
- Fiche 050-MétéorologieDocument10 pagesFiche 050-MétéorologieHugo GaubertPas encore d'évaluation
- 2015 09 Carel FR EcrbeDocument28 pages2015 09 Carel FR EcrbeDENOUPas encore d'évaluation
- Contrib4 3Document6 pagesContrib4 3hassan khalfiPas encore d'évaluation
- Tube Multicouche en Pex/Al/Pex: Versions Et CodesDocument6 pagesTube Multicouche en Pex/Al/Pex: Versions Et CodesIbra DERPas encore d'évaluation
- Equipements de Positionnement Saf-Fro FRDocument16 pagesEquipements de Positionnement Saf-Fro FRARRAMIPas encore d'évaluation
- Catalogue Imacab 2016Document83 pagesCatalogue Imacab 2016abdelwahad100% (2)
- 2ème Partie Acoubat2Document57 pages2ème Partie Acoubat2saidaPas encore d'évaluation
- ElectrotechniqueDocument5 pagesElectrotechniqueSadrac FILSAINTPas encore d'évaluation
- CCCC PDFDocument14 pagesCCCC PDFHamza El-ghrirPas encore d'évaluation
- 3 Caracteristiques Techniques - Plans D EntretienDocument66 pages3 Caracteristiques Techniques - Plans D EntretienKevine KhaledPas encore d'évaluation
- Notice Gioia 13.1Document52 pagesNotice Gioia 13.1Jessica Bresset-Avena100% (2)
- Manuel PVF PDFDocument52 pagesManuel PVF PDFmiraPas encore d'évaluation
- tp1 Moteur ThermiqueDocument4 pagestp1 Moteur ThermiqueAymen NasrPas encore d'évaluation
- Roulements PréchargésDocument27 pagesRoulements PréchargésYounessElkarkouriPas encore d'évaluation
- Protection Contre Les Surtension PDFDocument53 pagesProtection Contre Les Surtension PDFasa25asabPas encore d'évaluation
- ENGINES DEUTZ 912 913 Section 2Document69 pagesENGINES DEUTZ 912 913 Section 2noucriposPas encore d'évaluation
- TP Initiation Au Logiciel EPANETDocument31 pagesTP Initiation Au Logiciel EPANETSoufiane Ouassou0% (1)
- TD2 Pompes Et Station de PompageDocument5 pagesTD2 Pompes Et Station de Pompagesouheil meghlaouiPas encore d'évaluation