Académique Documents
Professionnel Documents
Culture Documents
2004 Maroc Correction Pile Electrolyse Cuivre
Transféré par
djoudi mouradTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
2004 Maroc Correction Pile Electrolyse Cuivre
Transféré par
djoudi mouradDroits d'auteur :
Formats disponibles
ancien programme
Corrigé
Bac Maroc 2004 Pile et électrolyse avec le cuivre (6,5 pts)
© http://labolycee.org
1. PILE DE CONCENTRATION
1.1.1. Borne positive : Cu(21+) (aq) + 2e– = Cu(1)(s) ; Borne négative : Cu(2) (s) = Cu(22+) (aq) + 2 e–
1.1.2. Borne positive : réduction ; Borne négative : oxydation
1.1.3. : Cu(21+) (aq) + Cu(2) (s) = Cu(1)(s) + Cu(22+) (aq)
Cu(2aq+ ) 1, 0 × 10
−2
1.2.1. Qr, i = 2,i
soit Qr, i = = 1,0 × 10–2
Cu(2aq+ ) 1, 0
1,i
1.2.2. Qr, i < K : le système évolue dans le sens direct, ce qui est cohérent avec la polarité proposée.
1.3.1. et 1.3.2.
Seul le circuit extérieur est représenté : R électrons
I courant
A
+ –
Cu(2aq+ )
1.3.3. Quand l’état d’équilibre est atteint : Qr, éq = K, soit 2+
2,éq
=1 => [Cu2+(aq)]2,éq = [Cu2+(aq)]1, éq
Cu( aq )
1, éq
À l’équilibre, les concentrations en ions cuivre (II) dans les deux compartiments sont égales.
2. DÉPÔT DE CUIVRE PAR ÉLECTROLYSE
2.1.1. Il est nécessaire d’ajouter un générateur dans le circuit extérieur.
2+
2.1.2. On veut déposer du cuivre solide sur la bague, la réaction est : Cu( aq ) + 2 e– = Cu(s) , il s’agit d’une
réduction ayant lieu à la cathode (reliée au pôle – du générateur).
2+
Sur l’autre électrode, il se produit une oxydation (Anode) : Cu(s) = Cu( aq ) + 2 e–
Le générateur force l’évolution du système dans le sens inverse.
Pile et électrolyse avec le cuivre © Production : ABMP&Labolycee.org
ancien programme
2.1.3.
courant
+ - A
électrons
Q
2.2.1. I = => Q = I.∆t soit Q = 400 × 10 –3 × 3600 = 1,44 × 103 C
∆t
1, 44 × 10
3
Q
2.2.2. n(e-) = soit n(e-) = −19
= 1,5 × 10 –2 mol
6, 02 × 10 × 1, 6 × 10
23
N.e
1
2.2.3. ndis(Cu2+) = .n(e-)
2
1 1
2.2.4. ndép(Cu) = ndis(Cu2+) => ndép(Cu) = .n(e-) soit ndép(Cu) = × 1,5 × 10-2 = 7,5 × 10–3 mol
2 2
2.2.5. m(Cu) = ndép(Cu).M(Cu) soit m(Cu) = 7,5 × 10–3 × 63,5 = 4,8 × 10–1 g
3. DÉTERMINATION D’UNE CONCENTRATION EN IONS CUIVRE II
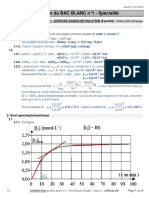
3.1.1. 2 Cu2+(aq) + 4 I–(aq) = 2 CuI(s) + I2 (aq)
Etat initial x=0 n0 excès 0 0
Intermédiaire x n0 – 2x 2x x
Etat final xmax n0 – 2xmax 2xmax n1 = xmax
n0 n
3.1.2. n0 – 2xmax = 0 (réaction totale) => xmax = et n1 = 0
2 2
3.2.1. Le diiode donne une coloration jaune-orange à la solution.
À l’équivalence, tout le diiode est consommé, la solution se décolore.
Remarque : La décoloration n’étant pas forcément bien visible, on peut ajouter quelques gouttes d’empois
d’amidon dans la solution : l’empois d’amidon est bleu en présence de diiode. À l’équivalence, l’empois
d’amidon devient incolore.
3.2.2. À l’équivalence, les réactifs sont mélangés dans les proportions stœchiométriques de l’équation (2) :
nS O 2−
2 3
= n1
2
S 2 O32 − .Véq
3.2.3. [S2O32-].Véq = 2n1 soit n1 =
2
−1 −3
1, 0 ×10 × 10, 0 × 10
soit n1 = = 5,0 × 10 –4 mol
2
3.2.4. D’après 3.1.2. n0 = 2n1 soit n0 = 2 × 5,0×10-4 = 1,0 × 10 –3 mol
n0 1, 0 × 10−3
3.2.5. C0 = soit C0 = = 1,0 × 10 –2 mol.L1
V 100 × 10−3
Pile et électrolyse avec le cuivre © Production : ABMP&Labolycee.org
Vous aimerez peut-être aussi
- Devoir 1 Modele 1 Physique Chimie 2 Bac SPC Semestre 2 Corrige 1Document2 pagesDevoir 1 Modele 1 Physique Chimie 2 Bac SPC Semestre 2 Corrige 1Moukil ÀYoùbPas encore d'évaluation
- 28examen National Physique Chimie SPC 2018 Rattrapage Corrige 2Document8 pages28examen National Physique Chimie SPC 2018 Rattrapage Corrige 2yaasir ouukesoPas encore d'évaluation
- 0607 Core Xo S PilesDocument3 pages0607 Core Xo S PilesChimie ChimiePas encore d'évaluation
- 2010 Polynesie Exo3 Correction Accumulateurs 4ptsDocument2 pages2010 Polynesie Exo3 Correction Accumulateurs 4ptsTom FischerPas encore d'évaluation
- Concours Médecine Dentaire CasaDocument2 pagesConcours Médecine Dentaire Casaateich simohamedPas encore d'évaluation
- TD4 ENSTA CorrigéDocument5 pagesTD4 ENSTA CorrigéSouid GhadaPas encore d'évaluation
- CCP Phys CorrDocument1 pageCCP Phys CorranassesslimaniPas encore d'évaluation
- 2011 CtresEtrangers Exo2 Correction PileCitron Electrolyse 6 5ptsDocument2 pages2011 CtresEtrangers Exo2 Correction PileCitron Electrolyse 6 5ptsgrajzgrPas encore d'évaluation
- 2007 Afrique Spe Correction Piles 4ptsDocument2 pages2007 Afrique Spe Correction Piles 4ptsMartin SALEHPas encore d'évaluation
- Corrige td1 ElectrochimieDocument7 pagesCorrige td1 Electrochimieayoub dahbi100% (1)
- TD: Exercices Avec Solution: Méthodes Instrumentales D'analyse/ ElectrochimieDocument24 pagesTD: Exercices Avec Solution: Méthodes Instrumentales D'analyse/ ElectrochimieHamza YahyaouiPas encore d'évaluation
- Spe Physique Chimie 2021 Zero 1 CorrigeDocument8 pagesSpe Physique Chimie 2021 Zero 1 CorrigeChahid OUAAZIZIPas encore d'évaluation
- 2004 Maroc Sujet Exo1 Pile - Electrolyse - CuDocument3 pages2004 Maroc Sujet Exo1 Pile - Electrolyse - Cudjoudi mouradPas encore d'évaluation
- 2012 Antilles Exo1 Correction EtamageCu 7ptsDocument2 pages2012 Antilles Exo1 Correction EtamageCu 7ptsilinre moPas encore d'évaluation
- Correction DS ExempleDocument4 pagesCorrection DS ExempleAngélique GUAZPas encore d'évaluation
- Solutions Des Exercices - Charges PoctuellesDocument17 pagesSolutions Des Exercices - Charges PoctuellesibrahimaylanePas encore d'évaluation
- 2004 Maroc Sujet Exo1 Pile Electrolyse CuDocument3 pages2004 Maroc Sujet Exo1 Pile Electrolyse Cuhakima032Pas encore d'évaluation
- Corrigà SÃrie NÂ4Document13 pagesCorrigà SÃrie NÂ4Raouia MakhloufPas encore d'évaluation
- 2016 RattDocument6 pages2016 RattCjkbkbkPas encore d'évaluation
- Correction Bac Blanc 4ème MathDocument5 pagesCorrection Bac Blanc 4ème MathMohamed SaidiPas encore d'évaluation
- DS6a CorrectionDocument5 pagesDS6a CorrectionOuu SsaamaPas encore d'évaluation
- EO - Rattrapage - 2016-2017.docx Filename UTF-8''EO Rattrapage 2016-2017-1Document3 pagesEO - Rattrapage - 2016-2017.docx Filename UTF-8''EO Rattrapage 2016-2017-1omayma omaPas encore d'évaluation
- Oxydo - Réduction Sujet Et CorrigéDocument6 pagesOxydo - Réduction Sujet Et Corrigémehdi benmassoudPas encore d'évaluation
- Correction Epreuve de Chimie Des Electrolytes 2014 2015 2Document5 pagesCorrection Epreuve de Chimie Des Electrolytes 2014 2015 2Chimiste ChimistePas encore d'évaluation
- Correction Epreuve de Chimie Des Electrolytes 2014 2015Document5 pagesCorrection Epreuve de Chimie Des Electrolytes 2014 2015عبد الرحيم بشيرPas encore d'évaluation
- Centrale PC Physique 2 2018 Corrigé Thermo Laser Meca EbDocument12 pagesCentrale PC Physique 2 2018 Corrigé Thermo Laser Meca EbjoséPas encore d'évaluation
- Corrige1 Physique 2 CCP PC 2004Document7 pagesCorrige1 Physique 2 CCP PC 2004Crafteur91Pas encore d'évaluation
- 2014 Metro Exo1 Correction BosonLHC 6ptsDocument3 pages2014 Metro Exo1 Correction BosonLHC 6ptsMateus Pimenta CardosoPas encore d'évaluation
- TS - BAC Blanc N°1 Corrigé - Spécialité PDFDocument4 pagesTS - BAC Blanc N°1 Corrigé - Spécialité PDFphytanjaPas encore d'évaluation
- Chapitre 5 - Oxydoréduction - PilesDocument12 pagesChapitre 5 - Oxydoréduction - PilesBeatrice Florin100% (3)
- 2011 Reunion Exo1 Correction Volta 6 5ptsDocument2 pages2011 Reunion Exo1 Correction Volta 6 5ptsgrajzgrPas encore d'évaluation
- AlgebraDocument9 pagesAlgebraHind YahiaouiPas encore d'évaluation
- OxydoréductionDocument6 pagesOxydoréductionMariam ZouhairPas encore d'évaluation
- C Chtsi2021Document8 pagesC Chtsi2021Rose kalvine MougoulaPas encore d'évaluation
- Corr Bac - Pc-Sn-Sp2018-BonDocument6 pagesCorr Bac - Pc-Sn-Sp2018-BonMalak KabbajPas encore d'évaluation
- T - Le Lait Passe Ensuite Dans Le Pasteurisateur Et en Ressort Avec T C TDocument4 pagesT - Le Lait Passe Ensuite Dans Le Pasteurisateur Et en Ressort Avec T C TᎡᎯᏔᎯᏁᎬ ᏰᏚᎻᏞPas encore d'évaluation
- Correction Epreuve de Chimie Des Electrolytes 2013 2014Document5 pagesCorrection Epreuve de Chimie Des Electrolytes 2013 2014Abdelhakim BailalPas encore d'évaluation
- Correction Epreuve de Chimie Des Electrolytes 2013 2014Document5 pagesCorrection Epreuve de Chimie Des Electrolytes 2013 2014Chimiste Chimiste100% (1)
- cm6 td24Document2 pagescm6 td24pedro66Pas encore d'évaluation
- 2014 Polynesie Exo1 Correction AcideCitrique 5 5ptsDocument2 pages2014 Polynesie Exo1 Correction AcideCitrique 5 5ptsHaman Bello OumarouPas encore d'évaluation
- Les PilesDocument17 pagesLes Pilesbrahim_mdPas encore d'évaluation
- Correction Epreuve de Chimie Des Electrolytes 2014 2015Document5 pagesCorrection Epreuve de Chimie Des Electrolytes 2014 2015Imene GhmrPas encore d'évaluation
- Devoir 2 2BACDocument3 pagesDevoir 2 2BACFATIMA fatiiiPas encore d'évaluation
- Examen de Structure de La Matiãre - ST - 2021 2022 Corrigà PDFDocument6 pagesExamen de Structure de La Matiãre - ST - 2021 2022 Corrigà PDFJuanDeagDZPas encore d'évaluation
- 2005 Polynesie Spe Correction Exo3 ConductiDocument2 pages2005 Polynesie Spe Correction Exo3 ConductiChouaib BouhouchPas encore d'évaluation
- Chapitre 4 Electrostatique Cours L2Document16 pagesChapitre 4 Electrostatique Cours L2ait hssainPas encore d'évaluation
- S7 Chapitre 07 ElectrolyseDocument8 pagesS7 Chapitre 07 ElectrolyseHAMADA1972Pas encore d'évaluation
- 1 - Transformation Spontanées Dans Le Piles Et Production D'énergieDocument7 pages1 - Transformation Spontanées Dans Le Piles Et Production D'énergieTaha BoulmanePas encore d'évaluation
- Cu Ag MG Cu Ag MG POCDocument3 pagesCu Ag MG Cu Ag MG POCorsiny clinton TCHAPTCHETPas encore d'évaluation
- Solution Des Exercices Du td-2Document6 pagesSolution Des Exercices Du td-2soumia bouPas encore d'évaluation
- C1Chim Transformations Lentes Rapides Exercices PDFDocument6 pagesC1Chim Transformations Lentes Rapides Exercices PDFAzizElheniPas encore d'évaluation
- Exercices Corrigés Chimie Des Électrolytes SMC s3Document21 pagesExercices Corrigés Chimie Des Électrolytes SMC s3yassine100% (3)
- Dipole RC (Serie1+2) +correctionDocument7 pagesDipole RC (Serie1+2) +correctionSamir JemniPas encore d'évaluation
- NH Ag Ag NH K: Correction Exercices de Revision: Les Reactions de ComplexationDocument3 pagesNH Ag Ag NH K: Correction Exercices de Revision: Les Reactions de ComplexationRitaj-Rayane Karim100% (1)
- C8Chim - Les - Piles - Exos - Alessandro Volta PDFDocument4 pagesC8Chim - Les - Piles - Exos - Alessandro Volta PDFAzizElheniPas encore d'évaluation
- TP - SI N°1Document10 pagesTP - SI N°1Roi AroufPas encore d'évaluation
- Registre-Accessibilite-Cnisam PDF Interactif Sep16Document28 pagesRegistre-Accessibilite-Cnisam PDF Interactif Sep16djoudi mouradPas encore d'évaluation
- Registre Des Entrees Et Sorties Danimaux Despeces Non Domestiques Dans Un Elevage DagrementDocument4 pagesRegistre Des Entrees Et Sorties Danimaux Despeces Non Domestiques Dans Un Elevage Dagrementdjoudi mouradPas encore d'évaluation
- 2004 Maroc Sujet Exo1 Pile - Electrolyse - CuDocument3 pages2004 Maroc Sujet Exo1 Pile - Electrolyse - Cudjoudi mouradPas encore d'évaluation
- 2004 Reunion Correction Exo2 QROC Electrolyse 3ptsDocument1 page2004 Reunion Correction Exo2 QROC Electrolyse 3ptsdjoudi mouradPas encore d'évaluation
- 2003 Reunion Correctionc Exo2 ElectrolyseZincDocument2 pages2003 Reunion Correctionc Exo2 ElectrolyseZincdjoudi mouradPas encore d'évaluation
- 2004 Reunion Sujet Exo2 QROC Electrolyse 3ptsDocument2 pages2004 Reunion Sujet Exo2 QROC Electrolyse 3ptsdjoudi mourad100% (1)
- 2003 Reunion Sujet SSCalc Exo2 ElectrolyseZinc 6 5ptsDocument1 page2003 Reunion Sujet SSCalc Exo2 ElectrolyseZinc 6 5ptsdjoudi mouradPas encore d'évaluation
- D00 Geom SolDocument21 pagesD00 Geom Soldjoudi mouradPas encore d'évaluation
- 2015 09 06 Elec de P1Document21 pages2015 09 06 Elec de P1bilal daoudiPas encore d'évaluation
- S.C. Graduel1Document5 pagesS.C. Graduel1djoudi mouradPas encore d'évaluation
- Sepam40 Notice UtilisationDocument268 pagesSepam40 Notice UtilisationChristian Gilbert100% (2)
- Commande Numerique Et Domensionnement Du Convertisseur Statique DDocument8 pagesCommande Numerique Et Domensionnement Du Convertisseur Statique DdanielPas encore d'évaluation
- RS485Document5 pagesRS485dupond27Pas encore d'évaluation
- Communications AnalogiquesDocument2 pagesCommunications AnalogiquesAl moubarakPas encore d'évaluation
- Regimes de NeutresDocument4 pagesRegimes de NeutresImane El MoussaouiPas encore d'évaluation
- Cal EXAMENS 18 19Document2 pagesCal EXAMENS 18 19Hamdi MahranPas encore d'évaluation
- Conception D'un Sectionneur Haute Tension - Bertrand COHARD-12fev09Document88 pagesConception D'un Sectionneur Haute Tension - Bertrand COHARD-12fev09bertrandPas encore d'évaluation
- Refdp 20088 P 14Document3 pagesRefdp 20088 P 14Aziz TAOUFYQPas encore d'évaluation
- Aky013 4 04Document50 pagesAky013 4 04ggmarcosPas encore d'évaluation
- Fibre OptiqueDocument100 pagesFibre OptiqueAbdelilah AchouriPas encore d'évaluation
- Ds7 Moller - EatonDocument8 pagesDs7 Moller - EatonNilton Campos FernandesPas encore d'évaluation
- Correction - Chapitre I) Le Rayonnement SolaireDocument3 pagesCorrection - Chapitre I) Le Rayonnement SolaireMariaPas encore d'évaluation
- P30 HautefidelitefranceDocument7 pagesP30 HautefidelitefranceHéritier NealPas encore d'évaluation
- La Variation de VitesseDocument6 pagesLa Variation de Vitessenajim68Pas encore d'évaluation
- TP 03 VOM M'hamedDocument8 pagesTP 03 VOM M'hamedabdousouafi59Pas encore d'évaluation
- Le Positionneur de Parabole SG-2100Document33 pagesLe Positionneur de Parabole SG-2100Soulaiman Andahmou100% (1)
- Installations Électriques IndustriellesDocument88 pagesInstallations Électriques Industriellesismail fatihi100% (1)
- Controle 1 - 11 S1 3AC InterDocument2 pagesControle 1 - 11 S1 3AC InteryounesPas encore d'évaluation
- Capteurs À Bres Optiques À Réseaux de BraggDocument4 pagesCapteurs À Bres Optiques À Réseaux de BraggЛюбить ЕннеттPas encore d'évaluation
- Cours Sur Corrosion Et Protection Des MétauxDocument37 pagesCours Sur Corrosion Et Protection Des Métauxnkpebe aliPas encore d'évaluation
- Licence de Base BelgiqueDocument17 pagesLicence de Base BelgiqueEric BriamontPas encore d'évaluation
- Le Transistor CoursDocument4 pagesLe Transistor Coursabdelouahab fartal100% (2)
- Distillerie Industrielle I-Presentation Du Systeme:: Lycée Imam Moslem El Menzah Devoir de Synthese N°3 Le 11/05/2017Document7 pagesDistillerie Industrielle I-Presentation Du Systeme:: Lycée Imam Moslem El Menzah Devoir de Synthese N°3 Le 11/05/2017Amira JebaliPas encore d'évaluation
- Catalogue PT-MT 2019 PDFDocument25 pagesCatalogue PT-MT 2019 PDFMohamed Ait KaddourPas encore d'évaluation
- TD ConvertiDocument4 pagesTD ConvertiNizar FdlPas encore d'évaluation
- Onduleur Nitram Leader 1500 NGA - Line-InteractifDocument2 pagesOnduleur Nitram Leader 1500 NGA - Line-InteractifkoloPas encore d'évaluation
- La Prise de Terre D'une Installation Électrique, Norme NF C 15-100Document7 pagesLa Prise de Terre D'une Installation Électrique, Norme NF C 15-100Tchameni DjinePas encore d'évaluation
- Omron MX2Document64 pagesOmron MX2Mohamed SomaiPas encore d'évaluation
- Devoir de Contrôle N°1 2016 2017 (MR Mejri Chokri)Document3 pagesDevoir de Contrôle N°1 2016 2017 (MR Mejri Chokri)Ghofran NahdiPas encore d'évaluation
- Le livre de la mémoire libérée : Apprenez plus vite, retenez tout avec des techniques de mémorisation simples et puissantesD'EverandLe livre de la mémoire libérée : Apprenez plus vite, retenez tout avec des techniques de mémorisation simples et puissantesÉvaluation : 4 sur 5 étoiles4/5 (6)
- Neuropsychologie: Les bases théoriques et pratiques du domaine d'étude (psychologie pour tous)D'EverandNeuropsychologie: Les bases théoriques et pratiques du domaine d'étude (psychologie pour tous)Pas encore d'évaluation
- Technologie automobile: Les Grands Articles d'UniversalisD'EverandTechnologie automobile: Les Grands Articles d'UniversalisPas encore d'évaluation
- Secrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieD'EverandSecrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieÉvaluation : 5 sur 5 étoiles5/5 (2)
- Hypnotisme et Magnétisme, Somnambulisme, Suggestion et Télépathie, Influence personnelle: Cours Pratique completD'EverandHypnotisme et Magnétisme, Somnambulisme, Suggestion et Télépathie, Influence personnelle: Cours Pratique completÉvaluation : 4.5 sur 5 étoiles4.5/5 (8)
- Manuel pour les débutants Fabriquez des savons naturelsD'EverandManuel pour les débutants Fabriquez des savons naturelsÉvaluation : 3 sur 5 étoiles3/5 (2)
- Améliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesD'EverandAméliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesÉvaluation : 5 sur 5 étoiles5/5 (2)
- Géobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainD'EverandGéobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- Comment développer l’autodiscipline: Résiste aux tentations et atteins tes objectifs à long termeD'EverandComment développer l’autodiscipline: Résiste aux tentations et atteins tes objectifs à long termeÉvaluation : 4.5 sur 5 étoiles4.5/5 (7)
- Aimez-Vous en 12 Étapes Pratiques: Un Manuel pour Améliorer l'Estime de Soi, Prendre Conscience de sa Valeur, se Débarrasser du Doute et Trouver un Bonheur VéritableD'EverandAimez-Vous en 12 Étapes Pratiques: Un Manuel pour Améliorer l'Estime de Soi, Prendre Conscience de sa Valeur, se Débarrasser du Doute et Trouver un Bonheur VéritableÉvaluation : 5 sur 5 étoiles5/5 (4)
- Anatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursD'EverandAnatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursPas encore d'évaluation
- La vie des abeilles: Prix Nobel de littératureD'EverandLa vie des abeilles: Prix Nobel de littératureÉvaluation : 4 sur 5 étoiles4/5 (41)
- Magnétisme Personnel ou Psychique: Éducation de la Pensée, développement de la Volonté, pour être Heureux, Fort, Bien Portant et réussir en tout.D'EverandMagnétisme Personnel ou Psychique: Éducation de la Pensée, développement de la Volonté, pour être Heureux, Fort, Bien Portant et réussir en tout.Évaluation : 5 sur 5 étoiles5/5 (1)
- Force Mentale et Maîtrise de la Discipline: Renforcez votre Confiance en vous pour Débloquer votre Courage et votre Résilience ! (Comprend un Manuel Pratique en 10 Étapes et 15 Puissants Exercices)D'EverandForce Mentale et Maîtrise de la Discipline: Renforcez votre Confiance en vous pour Débloquer votre Courage et votre Résilience ! (Comprend un Manuel Pratique en 10 Étapes et 15 Puissants Exercices)Évaluation : 4.5 sur 5 étoiles4.5/5 (28)
- La Pensée Positive en 30 Jours: Manuel Pratique pour Penser Positivement, Former votre Critique Intérieur, Arrêter la Réflexion Excessive et Changer votre État d'Esprit: Devenir une Personne Consciente et PositiveD'EverandLa Pensée Positive en 30 Jours: Manuel Pratique pour Penser Positivement, Former votre Critique Intérieur, Arrêter la Réflexion Excessive et Changer votre État d'Esprit: Devenir une Personne Consciente et PositiveÉvaluation : 4.5 sur 5 étoiles4.5/5 (12)
- Le B.A.-Ba de la communication: Comment convaincre, informer, séduire ?D'EverandLe B.A.-Ba de la communication: Comment convaincre, informer, séduire ?Évaluation : 3 sur 5 étoiles3/5 (1)
- Réfléchissez et devenez riche: Le grand livre de l’esprit maîtreD'EverandRéfléchissez et devenez riche: Le grand livre de l’esprit maîtreÉvaluation : 4 sur 5 étoiles4/5 (509)
- Le TDA/H chez l'adulte: Apprendre à vivre sereinement avec son trouble de l'attentionD'EverandLe TDA/H chez l'adulte: Apprendre à vivre sereinement avec son trouble de l'attentionPas encore d'évaluation
- L'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)D'EverandL'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)Évaluation : 4 sur 5 étoiles4/5 (3032)
- Histoire de la psychologie scientifique: De la naissance de la psychologie à la neuropsychologie et aux champs d'application les plus actuelsD'EverandHistoire de la psychologie scientifique: De la naissance de la psychologie à la neuropsychologie et aux champs d'application les plus actuelsPas encore d'évaluation
- Harmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020D'EverandHarmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020Évaluation : 2.5 sur 5 étoiles2.5/5 (3)
- L'Interprétation des rêves de Sigmund Freud: Les Fiches de lecture d'UniversalisD'EverandL'Interprétation des rêves de Sigmund Freud: Les Fiches de lecture d'UniversalisPas encore d'évaluation
- 20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsD'Everand20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Jus de Fruits et de Légumes Crus: 57 recettes faciles et un Guide Pratique Complet pour améliorer votre alimentation .: Santé, Vitalité et Minceur, avec ... ET DURABLEMENTD'EverandJus de Fruits et de Légumes Crus: 57 recettes faciles et un Guide Pratique Complet pour améliorer votre alimentation .: Santé, Vitalité et Minceur, avec ... ET DURABLEMENTPas encore d'évaluation