Académique Documents
Professionnel Documents
Culture Documents
Devoir 4
Transféré par
RAZKAOUI AhmedTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Devoir 4
Transféré par
RAZKAOUI AhmedDroits d'auteur :
Formats disponibles
Niveau : 2BAC science Année scolaire …….
/……
Physique et chimie Durée :2 Heures
La présentation, le soin et la rédaction seront pris en compte pour un point dans la notation.
Justifier en expliquant votre démarche si cela est nécessaire.
Tout calcul doit être précédé de la formule utilisée.
La valeur numérique prise par une grandeur physique est toujours suivie d’une unité.
Respecter la notation des grandeurs utilisées dans l’énoncé.
EXERCICE 1 (7pts)
1- Évolution d'un système chimique.
Soit la réaction chimique suivante : HCOOH (aq) + C6H5COO – (aq) HCOO –(aq) + C6H5COOH(aq)
1-1- Exprimer la constante d'équilibre de cette réaction puis calculer sa valeur.
On donne : pKa1(HCOOH/ HCOO –)=3,8 et pKa2(C6H5COOH / C6H5COO –)=4,2
1-2- On dispose de solutions aqueuses d'acide méthanoïque et de benzoate de sodium de même concentration
molaire en soluté apporté c et de solutions aqueuses d'acide benzoïque et de méthanoate de sodium de même
concentration molaire en soluté apporté c '. On admettra que, dans leurs solutions aqueuses respectives :
[HCOOH (aq)] = c ; [C6H5COO – (aq)] = c ; [C6H5COOH (aq)] = c' ; [HCOO – (aq) ] = c'.
On mélange des volumes V = 10,0 mL égaux des quatre solutions ci-dessus.
Les concentrations molaires en soluté apporté c et c' ont les valeurs suivantes :c=10–2mol/Let c'=5.10–3mol/L.
Calculer le quotient de réaction dans l'état initial dans ce cas précis. Dans quel sens va évoluer le système
chimique ?
2- pile à combustible
Une pile à combustible comporte deux compartiments
séparés par une membrane électrolytique qui permet le
passage des protons H+. Le schéma ci-dessous modélise le
fonctionnement de la pile
Données : masses molaires :
M(H)=1,0 g.mol-1, M(O)=16,0 g.mol-1 , M(C)=12,0 g.mol-1
constante de faraday F=96500C/mol
masse volumique du méthanol liquide : = 0,79 g.mL-1
La pile débite un courant à travers un dipôle ohmique de résistance R selon le schéma ci-dessous :
L’équation associée à la réaction lorsque la pile débite est : 2CH3OH(aq) + 3O2(g) 2CO2(g) + 4H2O(l)
2-1- Les couples oxydant/réducteur mis en jeu sont CO2(g)/CH3OH(aq) et O2(g)/H2O(l).
Écrire les demi-équations électroniques rendant compte des transformations se produisant à chaque électrode.
Préciser à quelle électrode a lieu chaque réaction et indiquer s’il s’agit d’une oxydation ou d’une réduction.
2-2- Indiquer la polarité des électrodes sur le schéma de la pile à combustible et représenter le sens de
circulation des électrons dans le circuit extérieur, lorsque la pile fonctionne.
2-3- La pile débite un courant de 50mA pendant 2,0 h.
Exprimer puis calculer le nombre de moles d’électrons ne transférés spontanément pendant cette durée.
2-4- Exprimer la masse de méthanol consommé en fonction du nombre de moles d’électrons ne puis la calculer.
2-5- Exprimer puis calculer le volume de méthanol consommé.
EXERCICE 2 (6pts)
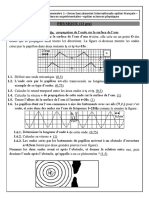
Pour envoyer un signal S(t) de fréquence fS , un groupe d’élèves précèdent a réalisé dans une deuxième étape le
montage représenté sur la figure 1 . Ils ont appliqué la tension p(t) = Pmcos(2πFpt) à l’entrée E1 et la tension
S(t) + Uo = Smcos(2πfSt) + Uo à l’entrée E2 ( U0 est la composante continue de la tension ) ; et on
visualisé sur l’écran d’un oscilloscope les tensions p(t) et S(t) + U0 puis la tension uS(t) à la sortie du circuit
intégré et ont obtenu les graphes représentés sur les figures 1 et 2 .
Figure 1 Figure 2 Figure 3
1- Quelle est la condition que doivent satisfaire les deux fréquences fS et FS pour avoir une bonne modulation ?
2- Relier les graphes des figures 2 et 3 aux tensions correspondantes .
3- Déterminer le taux de modulation m , sachant que la sensibilité verticale de l’oscilloscope est 1V/div .
Que peut-on conclure ?
4- La démodulation
d’amplitude est réalisée à
l’aide du montage de la
figure 4.
La partie 1 du montage
comprend la bobine (b’)
et un condensateur de
capacité C0 réglable entre figure 4
-12 -12
les deux valeurs 6.10 F et 12.10 F.
Le conducteur ohmique utilisé dans la partie 2 du montage a une résistance R1=30k .
4-1- Montrer que l’utilisation de la bobine (b’) dans le montage permet à la partie1 du montage de
sélectionner le signal uS(t) de fréquence F=105Hz.
4-2- On veut obtenir une bonne détection d’enveloppe en utilisant l’un des condensateurs de capacités :
10 nF ; 5 nF ; 0,5 nF ; 0,1 nF. Sachant que la fréquence de l'onde porteuse Fp=105Hz et la fréquence de la
tension modulante fs=5.103Hz, déterminer la capacité du condensateur qui convient.
4-3- Quel est le rôle de la partie 3 dans la démodulation ?
EXERCICE 3 (6pts)
Un skieur veut s’exercer sur une piste modélisée par la figure ci-dessous.
Avant de faire un premier essai, le skieur étudie les
forces qui s’exercent sur lui lors du glissage sur la
piste ABC.
Données
- Intensité de pesanteur g=9,8m/s².
- AB est un plan incliné d’un angle 20° par
rapport au plan horizontal passant par le point B.
On modélise le skieur et ses accessoires par un solide
(S) de masse m=80kg et de centre d’inertie G.
On considère sur la partie AB que les frottements ne
sont pas négligeables et on les modélise par une force constante.
1- Etude des forces appliquées sur le skieur entre A et B
Le skieur part du point A d’abscisse xA=0 dans le repère sans vitesse initiale à un instant que l’on considère
comme origine des temps t=0s.
Le skieur glisse sur le plan incliné AB suivant la ligne de la plus grande pente avec une accélération constante
a et passe par le point B avec une vitesse VB20 m /s.
1-1- En appliquant la deuxième loi de Newton, trouver en fonction de , a et g l’expression du coefficient de
frottement tan . Avec l’angle de frottement, défini par la normale à la trajectoire et la direction de la force
appliquée par le plan incliné sur le skieur.
1-2- A l’instant tB10s le skieur passe par le point B; Calculer la valeur de l’accélération a. En déduire
la valeur du coefficient de frottement tan.
1-3- Montrer que l’intensité de la force R exercée par le plan AB sur le skieur s’écrit sous la forme:
R=m.g.cos.√ . Calculer R
2- Étude du mouvement sur le plan horizontal :
Le skieur (S) continue son mouvement sur le plan horizontal BC pour s’arrêter à la position C . Le contact entre
le plan horizontal et le skieur (S) se fait avec frottements. La force de frottements est constante d’intensité f '.
Le mouvement de G est étudié dans le repère horizontal (B, ⃗ lié à un référentiel terrestre considéré galiléen.
Le centre d’inertie G passe par le point B avec une vitesse de VB20 m /s à un instant considéré comme
nouvelle origine des dates.
2-1- En appliquant la deuxième loi de Newton, trouver l’intensité f' sachant que la composante horizontale du
vecteur accélération du mouvement de G est ax= -3m.s-2.
2-2- Déterminer tC, l’instant d’arrêt du skieur .
2-3- Déduire la distance BC parcourue par G.
www.hammoumouna.jimdo.com Bonne chance
Vous aimerez peut-être aussi
- Devoir de Controle 1 Bac Math 21-22 (Copie Finale)Document5 pagesDevoir de Controle 1 Bac Math 21-22 (Copie Finale)Lotfi Bouchareb100% (1)
- 1-Projet Thématique SMEDDocument21 pages1-Projet Thématique SMEDAbdel-ali Sah100% (2)
- Tacs201 - Analyse Et Conception de Systemes - Kombate YendoubeDocument3 pagesTacs201 - Analyse Et Conception de Systemes - Kombate YendoubearmandPas encore d'évaluation
- DC2 Q M Copie FINALEDocument4 pagesDC2 Q M Copie FINALEomar sellemi0% (2)
- Dev Controle1 4scDocument4 pagesDev Controle1 4scSahbi Mabrouki YamenPas encore d'évaluation
- Série de Révision N°1Document5 pagesSérie de Révision N°1BaccariPas encore d'évaluation
- Sujet 622 CHIMIEDocument7 pagesSujet 622 CHIMIEakramadd2006Pas encore d'évaluation
- Devoir Bac MathDocument5 pagesDevoir Bac MathLotfi KhemiliPas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences Physiques - Bac Mathématiques (2016-2017) MR Jalel CHAKROUNDocument5 pagesDevoir de Contrôle N°2 - Sciences Physiques - Bac Mathématiques (2016-2017) MR Jalel CHAKROUNwalidPas encore d'évaluation
- dc1 4eme Sadiki 10-11Document4 pagesdc1 4eme Sadiki 10-11ben zayed aliPas encore d'évaluation
- Devoir de Controle N°2: Epreuve: Sciences PhysiquesDocument5 pagesDevoir de Controle N°2: Epreuve: Sciences PhysiquesNour NessahPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - Bac Math (2010-2011) MR Attaoui HechmiDocument5 pagesDevoir de Contrôle N°1 - Physique - Bac Math (2010-2011) MR Attaoui HechmiHanine HmidaPas encore d'évaluation
- Bac Blanc 2021bisDocument7 pagesBac Blanc 2021bisSahbi Mabrouki YamenPas encore d'évaluation
- Devoir de Contrôle N°3 - Sciences Physiques - Bac Technique (2015-2016) MR Abdmouleh NabilDocument5 pagesDevoir de Contrôle N°3 - Sciences Physiques - Bac Technique (2015-2016) MR Abdmouleh NabilMohamed El OuahdaniPas encore d'évaluation
- Devoir Corrigé de Synthèse N°1 - Sciences Physiques - Bac Math (2016-2017) MR Moncef AmaraDocument13 pagesDevoir Corrigé de Synthèse N°1 - Sciences Physiques - Bac Math (2016-2017) MR Moncef AmaraHanine HmidaPas encore d'évaluation
- Correction - Revision1 2021 4 TecDocument5 pagesCorrection - Revision1 2021 4 TecFM HELSENKIPas encore d'évaluation
- Devoir de Contrôle N°1 Avec Correction - Sciences Physiques - Bac Sciences Exp (2016-2017) MR TRAYIA NABIL PDFDocument8 pagesDevoir de Contrôle N°1 Avec Correction - Sciences Physiques - Bac Sciences Exp (2016-2017) MR TRAYIA NABIL PDFNour Al Islam0% (1)
- DC2 BacDocument4 pagesDC2 BacRidha HabibiPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - Bac Technique (2015-2016) MR Inoubli SlaheddineDocument5 pagesDevoir de Contrôle N°1 - Sciences Physiques - Bac Technique (2015-2016) MR Inoubli Slaheddineaziz bensaid2Pas encore d'évaluation
- Devoir de Synthèse N°1 - Sciences Physiques - Bac Sciences Exp (2017-2018) MR Handoura Naceur PDFDocument4 pagesDevoir de Synthèse N°1 - Sciences Physiques - Bac Sciences Exp (2017-2018) MR Handoura Naceur PDFMohamed SaidiPas encore d'évaluation
- Bacc TC Com Physique ChimieDocument59 pagesBacc TC Com Physique ChimieAfrit Komt100% (2)
- Control 2 Officiel 3Document5 pagesControl 2 Officiel 3salma benmiledPas encore d'évaluation
- Devoir de Contrôle N°2 - Sciences PhysiquesDocument3 pagesDevoir de Contrôle N°2 - Sciences Physiqueskougfst ldhd100% (1)
- Série+d'Exercices+ +Physique+Dipole+RC+ +Bac+Mathématiques+ (2012 2013) +Mr+AfdalDocument7 pagesSérie+d'Exercices+ +Physique+Dipole+RC+ +Bac+Mathématiques+ (2012 2013) +Mr+AfdalWiem BenchahbounPas encore d'évaluation
- Dev Synthese N°14scDocument6 pagesDev Synthese N°14scSahbi Mabrouki Yamen0% (1)
- Série Circuits RLC Libres 2016 2017 (Raddaoui Mourad) (Lycée Ibn Rochd Maknassy)Document2 pagesSérie Circuits RLC Libres 2016 2017 (Raddaoui Mourad) (Lycée Ibn Rochd Maknassy)Eya M'śPas encore d'évaluation
- BlancI PC BiofDocument7 pagesBlancI PC BiofwfwgPas encore d'évaluation
- Série 1 - Dipole RC - Soutien À Distance - Prof OTHMANEDocument13 pagesSérie 1 - Dipole RC - Soutien À Distance - Prof OTHMANEanass50% (2)
- Fiches Bac PhysiqueDocument70 pagesFiches Bac PhysiqueFlorent Akaffou0% (1)
- Po SP - Tle D..HervéDocument3 pagesPo SP - Tle D..HervémarioagbozoPas encore d'évaluation
- Devoir de Contrôle N°1 (Lycée Pilote Monastir) - Physique - 4ème Math (2009-2010) MR Mohsen Ben LamineDocument4 pagesDevoir de Contrôle N°1 (Lycée Pilote Monastir) - Physique - 4ème Math (2009-2010) MR Mohsen Ben LamineCrasy Akram Crasy Boy100% (3)
- Série N°1 2010 2011 (Antebli Makhlouf)Document6 pagesSérie N°1 2010 2011 (Antebli Makhlouf)Hiba JendoubiPas encore d'évaluation
- 612781dfded35sujet de Physique Chimie Bac D 1996Document5 pages612781dfded35sujet de Physique Chimie Bac D 1996isaacnewtonsm72Pas encore d'évaluation
- Devoir de Controle 2 2024 Bac MathDocument4 pagesDevoir de Controle 2 2024 Bac MathHamdi MinyarPas encore d'évaluation
- ) S Point 3 Ysique (1 PH : Tout Résultat Donné Sans Unité Sera Compté FauxDocument2 pages) S Point 3 Ysique (1 PH : Tout Résultat Donné Sans Unité Sera Compté FauxIsmailPas encore d'évaluation
- Devoir de Physique - Chimie TC 1Document3 pagesDevoir de Physique - Chimie TC 1Christophe NemlinPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - Bac Math (2010-2011) MR RaoufDocument5 pagesDevoir de Contrôle N°1 - Physique - Bac Math (2010-2011) MR Raoufahmed tounsiPas encore d'évaluation
- Devoir de Contrôle N°1 2010 2011 (Ben Dahmene) (Midoun)Document5 pagesDevoir de Contrôle N°1 2010 2011 (Ben Dahmene) (Midoun)ddddPas encore d'évaluation
- Devoir de Controle N°2 (18-19) PDFDocument4 pagesDevoir de Controle N°2 (18-19) PDFSmaali Faouzi Smaali0% (1)
- Devoir c1 4scDocument6 pagesDevoir c1 4scHammadi RekikPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - Bac Informatique (2012-2013) MR Daghsni Sahbi - 2Document3 pagesDevoir de Contrôle N°1 - Sciences Physiques - Bac Informatique (2012-2013) MR Daghsni Sahbi - 2Sahbi DaghsniPas encore d'évaluation
- DS3-4M - 2021 (Pilote Nabel)Document6 pagesDS3-4M - 2021 (Pilote Nabel)Jihed HorchaniPas encore d'évaluation
- DC1 (15 11 08)Document7 pagesDC1 (15 11 08)Seif Souid100% (1)
- Serie 1 Le Dipole RCDocument13 pagesSerie 1 Le Dipole RCBoussetta Zouhaier100% (1)
- Devoir de Contrôle N°2 - Sciences Physiques - Bac Sciences Exp (2013-2014) MR JELLALI ZAHREDDINEDocument4 pagesDevoir de Contrôle N°2 - Sciences Physiques - Bac Sciences Exp (2013-2014) MR JELLALI ZAHREDDINEMohamedBenKacemPas encore d'évaluation
- Devoir Synthese1 4info2016-20170 PDFDocument3 pagesDevoir Synthese1 4info2016-20170 PDFDaghsni SaidPas encore d'évaluation
- Devoir de Synthèse N°1 Lycée Pilote - Physique - Bac Math (2008-2009) Elève MarwaDocument5 pagesDevoir de Synthèse N°1 Lycée Pilote - Physique - Bac Math (2008-2009) Elève Marwachaari abdelouahad67% (3)
- Série D'exercices N°1 - Sciences Physiques DIPOLE RC - Bac Sciences Exp (2011-2012) MR ALIBI ANOUARDocument8 pagesSérie D'exercices N°1 - Sciences Physiques DIPOLE RC - Bac Sciences Exp (2011-2012) MR ALIBI ANOUARKais GuesmiPas encore d'évaluation
- I.A - Étude de La Résonance: G Gu GDocument14 pagesI.A - Étude de La Résonance: G Gu GAuréane DIACREPas encore d'évaluation
- Série D'exercices - Physique Oscillations Libres Amorties Et Non Amorties - Bac Sciences Exp (2010-2011) MR Baccari. Anis PDFDocument8 pagesSérie D'exercices - Physique Oscillations Libres Amorties Et Non Amorties - Bac Sciences Exp (2010-2011) MR Baccari. Anis PDFAzizElheni100% (2)
- RC Bac 2024Document6 pagesRC Bac 2024maram tvPas encore d'évaluation
- Devoir de Synthèse N°1 Lycée Pilote - Sciences Physiques - Bac Math (2012-2013) MR Boussaid Ali PDFDocument7 pagesDevoir de Synthèse N°1 Lycée Pilote - Sciences Physiques - Bac Math (2012-2013) MR Boussaid Ali PDFBarhoumi Mourad100% (4)
- Controle 1 21 22Document4 pagesControle 1 21 22Benmohamed ibtihelPas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2014-2015) MR Ramzi RebaiDocument4 pagesDevoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2014-2015) MR Ramzi RebaiImen AbbessiPas encore d'évaluation
- Chimie or Plase ProjDocument3 pagesChimie or Plase ProjSydahmed YoussefPas encore d'évaluation
- 4Dc213 PDFDocument4 pages4Dc213 PDFamath ndiayePas encore d'évaluation
- Devoir Physique 3 BacetplusDocument7 pagesDevoir Physique 3 BacetplusMed BriniPas encore d'évaluation
- Sujet 5Document6 pagesSujet 5Jihed HorchaniPas encore d'évaluation
- Devoir Bac TechDocument4 pagesDevoir Bac TechLotfi KhemiliPas encore d'évaluation
- Exercices d'optique et d'électromagnétismeD'EverandExercices d'optique et d'électromagnétismeÉvaluation : 5 sur 5 étoiles5/5 (1)
- Formulaire Exponentielle Et LogarithmeDocument1 pageFormulaire Exponentielle Et LogarithmeRAZKAOUI AhmedPas encore d'évaluation
- Devoir 4Document3 pagesDevoir 4Féz EyPas encore d'évaluation
- Exercices Ondes MécDocument4 pagesExercices Ondes MécRAZKAOUI AhmedPas encore d'évaluation
- Devoir 3-1bac FDocument2 pagesDevoir 3-1bac FRAZKAOUI AhmedPas encore d'évaluation
- Ondes 2Document1 pageOndes 2RAZKAOUI AhmedPas encore d'évaluation
- Ondes 1Document2 pagesOndes 1RAZKAOUI AhmedPas encore d'évaluation
- Exercices OndesDocument3 pagesExercices OndesRAZKAOUI AhmedPas encore d'évaluation
- 1er DS - 2bsmbiof-2018-2019Document3 pages1er DS - 2bsmbiof-2018-2019RAZKAOUI AhmedPas encore d'évaluation
- JJL CQ 580 301 PDFDocument40 pagesJJL CQ 580 301 PDFGuendouz GuendouzPas encore d'évaluation
- Rmacot 93Document53 pagesRmacot 93Hanane AzurePas encore d'évaluation
- SKILLS M12F Pannes Laminées À ChaudDocument104 pagesSKILLS M12F Pannes Laminées À ChaudYassine KandoussiPas encore d'évaluation
- Corrige 1Document5 pagesCorrige 1yves1ndri50% (2)
- Les Lois Hap 5.3Document16 pagesLes Lois Hap 5.3MERIEM AFFAPas encore d'évaluation
- Pourquoi Les Vaches Ne Peuvent Pas Descendre Les EscaliersDocument194 pagesPourquoi Les Vaches Ne Peuvent Pas Descendre Les EscaliersRadu Iliescu100% (1)
- FR Referentiel ActiviteDocument6 pagesFR Referentiel ActiviteJulienPas encore d'évaluation
- Séquence Boule À NeigeDocument1 pageSéquence Boule À NeigeEMERYPas encore d'évaluation
- MémoireDocument18 pagesMémoireMarina OugierPas encore d'évaluation
- Les Reptiliens ANNUNAKISDocument30 pagesLes Reptiliens ANNUNAKISSylvain LorgnierPas encore d'évaluation
- Materiel de SoudageDocument8 pagesMateriel de SoudageAzizPas encore d'évaluation
- Examen Partiel 190303Document7 pagesExamen Partiel 190303BOURAS Ihabe - بوراس إيهابPas encore d'évaluation
- Sae Courir 3Document21 pagesSae Courir 3api-673357128Pas encore d'évaluation
- TP Conception Des Antennes Sous CST STUDIO SUITE 2017-2022Document24 pagesTP Conception Des Antennes Sous CST STUDIO SUITE 2017-2022yousfi ferielPas encore d'évaluation
- Introduction Supply DemandDocument10 pagesIntroduction Supply DemandNoureddine Ben Bouzid100% (2)
- Comment Lire Le Nouveau Format de L'emploi Du Temps (EDT) ?Document11 pagesComment Lire Le Nouveau Format de L'emploi Du Temps (EDT) ?AïssaPas encore d'évaluation
- Miniprojet AtollDocument14 pagesMiniprojet AtollAbdou SadikPas encore d'évaluation
- Formation Sécurité IncendieDocument34 pagesFormation Sécurité IncendieZeyneb BelashPas encore d'évaluation
- Une Autre Histoire de La Renaissance by Didier Le FurDocument253 pagesUne Autre Histoire de La Renaissance by Didier Le Furrosamystica111100% (1)
- Flexion Simple (Bras Manipulateur)Document2 pagesFlexion Simple (Bras Manipulateur)SERGIOPas encore d'évaluation
- Activite 1 Choix Procede Materiau CesDocument5 pagesActivite 1 Choix Procede Materiau CesOubella MohamedPas encore d'évaluation
- Travail À FaireDocument1 pageTravail À FaireTud ErtPas encore d'évaluation
- Dossag SpectrophotométriqueDocument3 pagesDossag SpectrophotométriqueManel OtsPas encore d'évaluation
- Syllabus FAGR2001Document54 pagesSyllabus FAGR2001Barthélemy HoubenPas encore d'évaluation
- Corrigé TP2 CMNDocument10 pagesCorrigé TP2 CMNsnihhnouPas encore d'évaluation
- Conditions Generales Integrale HospiDocument26 pagesConditions Generales Integrale HospiRodrigo AhoutyPas encore d'évaluation
- L'Impact de La Gestion Prévisionnelle Des Emplois Et Des Compétences Sur La Motivation Des SalariésDocument102 pagesL'Impact de La Gestion Prévisionnelle Des Emplois Et Des Compétences Sur La Motivation Des SalariésAlidor Josue DrhPas encore d'évaluation
- CommunicationDocument28 pagesCommunicationBouziani Idrissi Mohammed100% (1)