Académique Documents
Professionnel Documents
Culture Documents
Allantoine Correction
Transféré par
zemmourmarwenTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Allantoine Correction
Transféré par
zemmourmarwenDroits d'auteur :
Formats disponibles
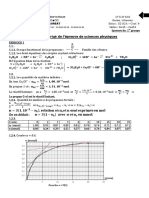
ÉVALUATION COMMUNE 2020
CORRECTION Yohan Atlan © https://www.vecteurbac.fr/
CLASSE : Première E3C : ☐ E3C1 ☒ E3C2 ☐ E3C3
VOIE : ☒ Générale ENSEIGNEMENT : physique-chimie
DURÉE DE L’ÉPREUVE : 1 h CALCULATRICE AUTORISÉE : ☒Oui ☐ Non
Allantoïne
1.
1.1.
Groupe Carbonyle
Groupe Carboxyle
1.2.
1.3.
Chacun des atomes de carbone fait une liaison double et deux liaisons simples : géométrie triangulaire
plane
2.
2.1.
1
1 : 1s
H
2 2 3
7N : 1s 2s 2p
Pour respecter la règle de l’octet (8 électrons sur sa dernière couche), l’atome d’azote fait 3 liaisons et
possède un doublet non liant.
Ainsi la géométrie de la molécule d’ammoniac sera pyramidale
2.2.
χN> χH Les liaisons NH sont polarisés.
Le barycentre (centre géométrique) des charges positives G+ est différent du barycentre des charges
négatives G- du fait de la géométrie de la molécule.
La molécule est donc polaire
CORRECTION Yohan Atlan © www.vecteurbac.fr
2.3.
2.3.1.
La grandeur qui figure en abscisse est le nombre d’onde σ
2.3.2.
La bande la plus à gauche du spectre est comprise entre 3200 et 3500 cm-1, il s’agit d’une bande double
forte.
D’après le tableau des données de spectroscopie infrarouge, la bande confirme une liaison
C–NH2
2.3.3.
D’après le tableau des données de spectroscopie infrarouge, pour une liaison C = O avec N voisin σ est
compris entre 1660 – 1685 cm-1 avec une bande forte et fine.
D’après le tableau des données de spectroscopie infrarouge, plusieurs liaisons peuvent être envisagées
pour ce nombre d’onde.
Nombre d’onde
Liaison Intensité
(cm-1)
Liaison C = O avec N voisin 1660 - 1685 Bande forte et fine
Liaison C = O aldéhyde et cétone 1650-1730 Bande forte et fine
Liaison C = O acide carboxylique 1680-1710 Bande forte et fine
Liaison C = C 1640-1680 Bande moyenne
Il peut s’agir d’une autre liaison.
Ainsi cette bande du spectre ne peut être attribuée sans ambiguïté à la liaison C=O de l’urée.
CORRECTION Yohan Atlan © www.vecteurbac.fr
3.
3.1.
a : transformation
b : transformation
c : séparation
d : purification
e : analyse
3.2.
Il s’agit de la synthèse de l’allantoïne. D’après les données, l’allantoïne est soluble dans l’eau
bouillante (150 g/L). Ainsi l’allantoïne est présente dans le milieu réactionnel sous forme dissoute
jusqu'à ce que sa concentration atteigne 150g/L. c’est pourquoi le précipité blanchâtre n’apparaît que
progressivement et au bout d’un certain temps.
3.3.
D’après les données, la solubilité de l’allantoïne dans l’eau : 150 g/L si eau bouillante et 5 g/L si eau très
froide. Ainsi sa solubilité dans l’eau diminue lorsque la température diminue.
L’utilisation de la glace permet de rendre solide l’allantoïne et permet sa séparation et récupération.
3.4.
Lors de la synthèse, l’allantoïne est formée. Cependant, il reste des réactifs dans le milieu réactionnel et
l’acide sulfurique (catalyseur). Il faut donc purifier le produit en le lavant avec de l’eau glacée.
L’eau est glacée afin de minimiser la dissolution de l’allantoïne.
3.5.
Déterminons les quantités de matière initiales des réactifs :
m!"é$ 13,6
n%!"é$ = = = 2,27. 10&' mol
M!"é$ 60,0
m()%*$ ,-./0.-%1!$
n%()%*$ ,-./0.-%1!$ =
M()%*$ ,-./0.-%1!$
Pourcentage massique de l’acide glyoxylique
m()%*$ ,-./0.-%1!$
P=
m2/-!3%/4
d’ou :
m()%*$ ,-./0.-%1!$ = P × m2/-!3%/4
Ainsi
P × m2/-!3%/4
n%()%*$ ,-./0.-%1!$ =
M()%*$ ,-./0.-%1!$
CORRECTION Yohan Atlan © www.vecteurbac.fr
La masse volumique est définie par :
m2/-!3%/4
ρ2/-!3%/4 =
V2/-!3%/4
d’ou :
m2/-!3%/4 = ρ2/-!3%/4 × V2/-!3%/4
Ainsi
P × ρ2/-!3%/4 × V2/-!3%/4
n%()%*$ ,-./0.-%1!$ =
M()%*$ ,-./0.-%1!$
50
× 1,3 × 10,0
n%()%*$ ,-./0.-%1!$ = 100 = 8,8. 10&5 mol
74,0
Équation 2 CH4 N2 O(s) + C2 H2 O3(aq) → C4 H6 N4 O3(s) + 2 H2 O(l)
État initial x=0mol 2,27. 10!" 8,8. 10!# 0 Solvant
État
x 2,27. 10!" − 2x 8,8. 10!# − x x Solvant
intermédiaire
État final x=xf 2,27. 10!" − 2x$ 8,8. 10!# − x$ xf Solvant
Calculons xmax :
2,27. 10&' − 2x6(0' = 0
2,27. 10&'
x6(0' = = 1,14. 10&' mol
2
8,8. 10&5 − x6(05 = 0
x6(05 = 8,8. 10&5 mol
x6(05 < x6(0'
x6(0 = x6(05 = 8,8. 10&5 mol
Calculons la masse théorique d’allantoïne
m78 = n78 × M = x6(0 × M = 8,8. 10&5 × 158,1 = 13,9 g
Calculons le rendement :
m$09
η=
m78
8,60
η= = 0,619 = 61,9%
13,9
CORRECTION Yohan Atlan © www.vecteurbac.fr
Vous aimerez peut-être aussi
- Etalonnage D'un Solution D'ions PermanganateDocument2 pagesEtalonnage D'un Solution D'ions Permanganateneval chenchouniPas encore d'évaluation
- TP Opu Seray - TeguarDocument6 pagesTP Opu Seray - TeguarBouchra BenabdallahPas encore d'évaluation
- PC Gene 059 Correction Exo1 Chi AllantoineDocument3 pagesPC Gene 059 Correction Exo1 Chi AllantoineEmmanuela KonanPas encore d'évaluation
- Série D'exercices N°1Document15 pagesSérie D'exercices N°1Abdelhak MakhloufPas encore d'évaluation
- Lycée Pilote Sfax DC 3 2009 CorrigéDocument2 pagesLycée Pilote Sfax DC 3 2009 CorrigéMaram BouaskerPas encore d'évaluation
- Devoir de Niveau N°6 de Sciences Physiques: EXERCICE 1 (5 Points)Document3 pagesDevoir de Niveau N°6 de Sciences Physiques: EXERCICE 1 (5 Points)Japhet BAOUNDOULAPas encore d'évaluation
- 61295cc080954devoir 1 Physique Chimie Niveau Terminale D LyceeDocument3 pages61295cc080954devoir 1 Physique Chimie Niveau Terminale D LyceeJaphet BAOUNDOULAPas encore d'évaluation
- Physique C PDFDocument4 pagesPhysique C PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Spécialité Physique-Chimie - Sujet Zéro - Corrigé EXERCICE 1 - Dépolluer Une Eau Avec Des Carapaces de Crevettes (10 Points)Document7 pagesSpécialité Physique-Chimie - Sujet Zéro - Corrigé EXERCICE 1 - Dépolluer Une Eau Avec Des Carapaces de Crevettes (10 Points)Mamadou Lamine NianePas encore d'évaluation
- 2021-09-Metro - Exo1-Correction-SyntheseEster-10ptsDocument3 pages2021-09-Metro - Exo1-Correction-SyntheseEster-10ptsMartin SALEHPas encore d'évaluation
- Série Corrigée de Révision - Sciences Physiques Correction de La Série de Révision Bac 2011 - Bac Mathématiques (2010-2011) MR Benaich PDFDocument15 pagesSérie Corrigée de Révision - Sciences Physiques Correction de La Série de Révision Bac 2011 - Bac Mathématiques (2010-2011) MR Benaich PDFSaifeddine MakniPas encore d'évaluation
- 2007 Antilles Exo1 Correction BenzoateMethyle 5.5ptsDocument3 pages2007 Antilles Exo1 Correction BenzoateMethyle 5.5ptsHafid Tlemcen Rossignol PoètePas encore d'évaluation
- Corrigé Sujet S2 1er Groupe PC Session Normale 2019 1Document7 pagesCorrigé Sujet S2 1er Groupe PC Session Normale 2019 1Mamadou NdiayePas encore d'évaluation
- Correction de DSN2 Bac 2020..Document3 pagesCorrection de DSN2 Bac 2020..dahnenanisPas encore d'évaluation
- Compo 1ère S Sem 2Document3 pagesCompo 1ère S Sem 2Boubacar BaldePas encore d'évaluation
- TP1 Electochimie 3émé AnnéeDocument10 pagesTP1 Electochimie 3émé AnnéeLïnâ ExØtîc DõlĽPas encore d'évaluation
- Corrige Td1 Uv Visible TsaDocument5 pagesCorrige Td1 Uv Visible TsaELAssaliAziz100% (4)
- TD1 Description Et Évolution-1 À 10 CorrDocument10 pagesTD1 Description Et Évolution-1 À 10 CorrmpofPas encore d'évaluation
- Devoir 3 Modele 1 Corrige 1Document4 pagesDevoir 3 Modele 1 Corrige 1hessasPas encore d'évaluation
- TD 4 CorrigéDocument7 pagesTD 4 CorrigéecosysPas encore d'évaluation
- C3Chim - Transformations - Limitees - Exercices - Sabatier PDFDocument5 pagesC3Chim - Transformations - Limitees - Exercices - Sabatier PDFAzizElheni0% (1)
- PC C2017 CorDocument10 pagesPC C2017 Corrktm.avotraPas encore d'évaluation
- C 02 Ab 1 eDocument5 pagesC 02 Ab 1 eMihnea GamanPas encore d'évaluation
- UE5 MMS M1 Examen 211207 CorrDocument10 pagesUE5 MMS M1 Examen 211207 CorrEslem Islam100% (1)
- 6 - S4 Corrigé S1Document4 pages6 - S4 Corrigé S1Oussam Ouadidi100% (2)
- 2010 Polynesie Spe Exo3 Correction AnanasDocument2 pages2010 Polynesie Spe Exo3 Correction Ananasla physique selon le programme FrançaisPas encore d'évaluation
- 2011 Antilles Exo1 Correction Luminol 6 5pointsDocument3 pages2011 Antilles Exo1 Correction Luminol 6 5pointsmohamedPas encore d'évaluation
- FTSCdevoirCinetique5 CorrigeDocument2 pagesFTSCdevoirCinetique5 CorrigeTay SsirPas encore d'évaluation
- D4 TS1 2023 LVN - WahabdiopDocument4 pagesD4 TS1 2023 LVN - Wahabdiopsokhnamaimounadiop662004Pas encore d'évaluation
- Examen National Physique Chimie SPC 2016 Normale Corrige 1Document9 pagesExamen National Physique Chimie SPC 2016 Normale Corrige 1othmane GbPas encore d'évaluation
- BacPC PDFDocument177 pagesBacPC PDFDéyana BAKELE100% (1)
- Chimie D Chap14 Correction ExosDocument4 pagesChimie D Chap14 Correction ExosSOULA CHAHINAZPas encore d'évaluation
- U C A D D: Exercice 1Document5 pagesU C A D D: Exercice 1Lindeltaylor DioufPas encore d'évaluation
- Corrigé Bacc SPC Série D Session 2022Document7 pagesCorrigé Bacc SPC Série D Session 2022andoPas encore d'évaluation
- مواضيع البكالوريا ل موريطانيا من 2002إلى 2012 PDFDocument177 pagesمواضيع البكالوريا ل موريطانيا من 2002إلى 2012 PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Correction de La Fiche 1Document5 pagesCorrection de La Fiche 1LARIBIPas encore d'évaluation
- 2014 CtresEtrangers Exo1 Correction Paracetamol 9pts PDFDocument3 pages2014 CtresEtrangers Exo1 Correction Paracetamol 9pts PDFLM MarouanePas encore d'évaluation
- Corrigé - Type - TleD. Essai Blan2024Document10 pagesCorrigé - Type - TleD. Essai Blan2024issaradjab13Pas encore d'évaluation
- Devoir de Synthèse N°2 - Sciences Physiques - Bac Math (2013-2014) MR Barhoumi EzzedineDocument5 pagesDevoir de Synthèse N°2 - Sciences Physiques - Bac Math (2013-2014) MR Barhoumi EzzedineWajih M'likiPas encore d'évaluation
- Exercices Corrigé .AdsorptionDocument8 pagesExercices Corrigé .Adsorptionkolta100% (2)
- Fiche de TD CHIMIE N°5 GA - 045754Document4 pagesFiche de TD CHIMIE N°5 GA - 045754Juste Landry OngoloPas encore d'évaluation
- TD Electrochimie Et Applications, L3 Chimie Et M1 SC Phys 2018-2019Document4 pagesTD Electrochimie Et Applications, L3 Chimie Et M1 SC Phys 2018-2019fernandPas encore d'évaluation
- Architecture Moléculaire Et StéréochimieDocument5 pagesArchitecture Moléculaire Et StéréochimielucatelliPas encore d'évaluation
- G1SPHCH02685 Sujet1Document9 pagesG1SPHCH02685 Sujet1kangadaniel0887Pas encore d'évaluation
- Concour Medecin FES (Electicité +acido-Base)Document4 pagesConcour Medecin FES (Electicité +acido-Base)Maskar HoussinePas encore d'évaluation
- DS N3 CorrectionDocument4 pagesDS N3 Correctionالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Corrigé Serie D 2021Document7 pagesCorrigé Serie D 2021ChristellePas encore d'évaluation
- BAC Blanc M.cisseDocument3 pagesBAC Blanc M.cisseMoussa CISSEPas encore d'évaluation
- Correction DS ExempleDocument4 pagesCorrection DS ExempleAngélique GUAZPas encore d'évaluation
- Série 1 (2020-2021)Document5 pagesSérie 1 (2020-2021)SBA Nabil ZakariaPas encore d'évaluation
- M28 - Cinétique - TD2 - CorrectionDocument7 pagesM28 - Cinétique - TD2 - CorrectionHassan DriouachPas encore d'évaluation
- Cinétique ChimiqueDocument1 pageCinétique ChimiqueCarla GastaldelloPas encore d'évaluation
- Corrigé de L'épreuve de Sciences Physiques: Universite C A D DDocument5 pagesCorrigé de L'épreuve de Sciences Physiques: Universite C A D DLindeltaylor DioufPas encore d'évaluation
- TS - BAC Blanc N°1 Corrigé - ObligatoireDocument4 pagesTS - BAC Blanc N°1 Corrigé - ObligatoirephytanjaPas encore d'évaluation
- Technique de Suivi Temporel D'une TransformationDocument8 pagesTechnique de Suivi Temporel D'une TransformationJosé Ahanda NguiniPas encore d'évaluation
- CO2 TS2 2016 LSLL Interrompu WahabdiopDocument4 pagesCO2 TS2 2016 LSLL Interrompu WahabdiopMed BriniPas encore d'évaluation
- 6-1 - Démarche de SélectionDocument3 pages6-1 - Démarche de Sélectionmouhsine kouchtabiPas encore d'évaluation
- Cours Reseaux ElectriquesDocument122 pagesCours Reseaux Electriquesmolodme380Pas encore d'évaluation
- Installations SanitairesDocument24 pagesInstallations SanitairesABDELKADER HOGGASPas encore d'évaluation
- Distributeur Hydraulique 4WE6 NG6 Cetop 3 Bosch RexrothDocument20 pagesDistributeur Hydraulique 4WE6 NG6 Cetop 3 Bosch RexrothMaintenanceBourgesPas encore d'évaluation
- LANO - Laboratoire Agronomique NOrmand - Matière OrganiqueDocument1 pageLANO - Laboratoire Agronomique NOrmand - Matière Organiquelaboratoire rabatPas encore d'évaluation
- 2022 NelleCaledo J1 Sujet OriginalDocument19 pages2022 NelleCaledo J1 Sujet Originalredatwitch2006Pas encore d'évaluation
- Systeme Photovoltaique Alimentant Un FilDocument86 pagesSysteme Photovoltaique Alimentant Un Filsouad laribiPas encore d'évaluation
- Série Ec - Dynamique de Rotation (3T) .2023 Idéal PDFDocument2 pagesSérie Ec - Dynamique de Rotation (3T) .2023 Idéal PDFBakari AnisPas encore d'évaluation
- Définitions Des Termes - Bilan ÉnergétiqueDocument8 pagesDéfinitions Des Termes - Bilan ÉnergétiqueMoctar CoulibalyPas encore d'évaluation
- Preuve de Physique-Chimie, BEPC, Année 2017, TogoDocument1 pagePreuve de Physique-Chimie, BEPC, Année 2017, TogozoroboscoPas encore d'évaluation
- Epreuve Phy2006 3annDocument2 pagesEpreuve Phy2006 3annMOUHSSINE CHADILIPas encore d'évaluation
- Cours M2 Catalyse PDFDocument78 pagesCours M2 Catalyse PDFamal agadirPas encore d'évaluation
- AcetyleneDocument7 pagesAcetyleneAbdoullah AbdoullahPas encore d'évaluation
- 5 ChromatoDocument7 pages5 ChromatopdfPas encore d'évaluation
- CORRECTION B COURS ALCENE - Microsoft Word-1Document1 pageCORRECTION B COURS ALCENE - Microsoft Word-1MohamedPas encore d'évaluation
- Présentation Cours Métallurgie - Chapitre IVDocument96 pagesPrésentation Cours Métallurgie - Chapitre IVdala3a0Pas encore d'évaluation
- Chapitre 03 Statiques Des FluidesDocument79 pagesChapitre 03 Statiques Des FluidesMilanoPas encore d'évaluation
- Labos Recherche Université de TunisDocument87 pagesLabos Recherche Université de Tunismaherskhiri.iscaePas encore d'évaluation
- Cours Materiaux MetalliquesDocument76 pagesCours Materiaux MetalliquesOuissamBenjdiyaPas encore d'évaluation
- 4 - La Mise en Condition Neuro-musculo-ArticulaireDocument44 pages4 - La Mise en Condition Neuro-musculo-ArticulaireMaroua KhoualdiaPas encore d'évaluation
- Variation de La Resistance Execrices EleveDocument3 pagesVariation de La Resistance Execrices EleveErnest AdouPas encore d'évaluation
- Rappel Semi-Conducteur Et Jonction PNDocument6 pagesRappel Semi-Conducteur Et Jonction PNAicha ZEBIRI100% (1)
- Méthode Et Appareils de Mesure de La RadioactivitéDocument8 pagesMéthode Et Appareils de Mesure de La RadioactivitéNasraddine HassanePas encore d'évaluation
- 10 Série 1Document2 pages10 Série 1Snaptube 2022Pas encore d'évaluation
- Correction LAgrivoltaïsme Enseignement Scientifique TerminaleDocument2 pagesCorrection LAgrivoltaïsme Enseignement Scientifique Terminalejosiastite22Pas encore d'évaluation
- UntitledDocument54 pagesUntitledSébastien MiclotPas encore d'évaluation
- ABIDI GhezielDocument105 pagesABIDI Ghezielilyes bensemmanePas encore d'évaluation
- Rev Ac Bas ConvertiDocument10 pagesRev Ac Bas ConvertiجعدبندرهمPas encore d'évaluation
- Dimensionnement Des Potelets Projet de CMDocument4 pagesDimensionnement Des Potelets Projet de CMLouis LissouckPas encore d'évaluation
- TDDocument10 pagesTDam47Pas encore d'évaluation