Académique Documents
Professionnel Documents
Culture Documents
Cinétique Chimique
Transféré par
Carla GastaldelloTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Cinétique Chimique
Transféré par
Carla GastaldelloDroits d'auteur :
Formats disponibles
aurélie 12 / 2003
Cinétique chimique : ordre de réaction
ordres de réaction 0, 1 ou 2 : temps de demi-réaction
méthode différentielle
par spectrophotométrie
En poursuivant votre navigation sur ce site, vous acceptez l’utilisation de
Cookies vous proposant des publicités adaptées à vos centres d’intérêts.
.
Zapping ... Agir pour la planète : un enjeu immédiat -…
.
ordres de réaction 0, 1 ou 2 : temps de demi-réaction
Soit une réaction dont le bilan est : A-->B ; la vitesse de réaction s'écrit : v=k[A]a.
a est l'ordre de la réaction, 0, 1 ou 2 ; k est la constante de vitesse. On note [A]0 la concentration
initiale du réactif A.
Pour chaque valeur de a :
1. Comment déterminer graphiquement la constante de vitesse k. Quelle est son unité ?
2. Quelle est la représentation de [R] en fonction du temps ?
3. Déterminer le temps de demi-réaction .
corrigé
la vitesse de réaction s'écrit : v= -d[A] /dt
la concentration [A] est solution de l'équation différentielle : -d[A] /dt =k[A]a.
réaction d'ordre 0 : -d[A] /dt =k0.
d'où [A]= -k0t + [A]0 droite de pente opposée à la constante de vitesse k0.
k0 s'exprime en mol L-1 s-1.
temps de demi-réaction t½ : durée au bout de laquelle la moitié du réactif limitant a été
consommée.
à t½ [A]=½[A]0 d'où ½[A]0 = -k0t ½ + [A]0 soit t ½ =[A]0 /(2k0).
réaction d'ordre 1 : -d[A] /dt = k1[A] ; k1 s'exprime en s-1.
d'où d[A] /[A]= -k1dt soit : ln[A] = -k1t +ln[A0]
Tracer la courbe d'équation ln [A]= f(t) , droite de pente -k1.
temps de demi-réaction t½ : ln(½[A0] )= -k1t ½ +ln[A0] ; t ½ =ln2 /k1.
réaction d'ordre 2 : -d[A] /dt = k2[A]2 ; k1 s'exprime en L mol-1 s-1.
d'où d[A] /[A]2= -k2dt soit : 1/[A] = k2t +1/[A0]
Tracer la courbe d'équation 1/[A] = f(t) , droite de pente k2.
temps de demi-réaction t½ : 1/(½[A0] )= k2t ½ +1/[A0] ; t ½ =1 /(k2[A0] ).
méthode différentielle
Considérons la réaction A-->B+C. La vitesse de réaction peut se mettre sous la forme v= k[A]a où
a est un réel. L'évolution de la concentration du composé A et de la vitesse -d[A]/dt sont donnés
dans le tableau ci-desous :
t (min) 1 10 15 20 25 35 50
[A] mol/L 0,44 0,23 0,18 0,14 0,11 0,07 0,04
-d[A]/dt *104
6,3 2,6 1,6 1,1 0,8 0,5 0,25
(molL-1min-1)
1. Déterminer les grandeurs k et a.
corrigé
la concentration [A] est solution de l'équation différentielle : -d[A] /dt =k[A]a.
soit ln (-d[A] /dt)=ln k + a ln[A], droite de coefficient directeur a et d'ordonnée à l'origine ln k.
si a=0, réaction d'ordre zéro : -d[A] /dt doit être une constante, ce qui est contraire aux données du
tableau.
t (min) 1 10 15 20 25 35 50
[A] mol/L 0,44 0,23 0,18 0,14 0,11 0,07 0,04
-d[A]/dt
6,3 10-4 2,6 10-4 1,6 10-4 1,1 10-4 0,8 10-4 0,5 10-4 0,25 10-4
(molL-1min-1)
ln[A] -0,776 -1,386 -1,66 -1,9 -2,12 -2,53 -2,995
ln (-d[A] /dt) -7,38 -8,31 -8,73 -9,1 -9,42 -9,99 -10,68
l'ordonnée à l'origine est égale à -6,4 : ln k=-6,4 d'où k = 1,7 10-3 (mol L-1)1,4 -1 min-1.
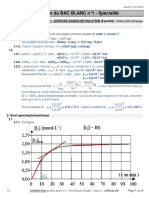
par spectrophotométrie
Oxydation des ions iodures I- par les ions peroxodisulfates S2O82- en solution aqueuse. 2I-+S2O82-
=I2 + 2SO42-.
La réaction admet l'ordre partiel p par rapport aux ions iodures et un ordre partiel n par rapport à
S2O82- . A la date t=0 on mélange 25 mL d'une solution d'iodure de potassium à 0,25 mol/L et 15
mL d'une solution de peroxodisulfate d'ammonium à 6,25 10-3 mol/L.
1. Ces conditions initiales permettent de déterminer l'ordre n de la réaction.Justifier. Donner
l'expression de la constante de vitesse apparente.
2. On mesure l'absorbance du mélange au cours du temps. Seul le diiode formé est coloré donc
responsable de l'absorbance. On rappelle la loi de Beer Lambert donnant l'absorbance A d'une
solution de concentration c placée dans une cuve de longueur L : A=eALc avec eA le
coefficient d'extinction molaire de la substance absorbante à la longueur d'onde l= 454 nm. A =
1250 L mol-1 cm-1.
- Expliquer comment la mesure de l'absorbance permet de déterminer la concentration des ions
peroxodisulfate au cours du temps.
- On obtient les résultats suivants :
t (min) 0 4 8 12 16
A 0 0,35 0,67 0,94 1,18
Montrer que ces résultats sont en accord avec une cinétique d'ordre n=1.
Calculer la constante de vitesse apparente.
corrigé
à l'instant initial, on a introduit : 25 10-3*0,25 = 6,25 10-3 mol d'ion I- et 15 10-3*6,25 10-3 = 9,37
10-5 mol d'ion peroxodisulfate. Les ions iodures sont en grand excès et la concentration des ions
iodures peut être considérée comme constante.
La vitesse de la réaction s'écrit : v = k [I- ]p[S2O82-]n avec k la constante de vitesse.
v = k' [S2O82-]n avec k' = k [I- ]p, constante de vitesse apparente.
La réaction admet l'ordre partiel n par rapport aux ions peroxodisulfate.
D'après la loi de Beer, la concentration en diiode [I2] est proportionnelle à l'absorbance A : [I2] =
A/(eAL) = A/1250.
2I- +S2O82- =I2 + 2SO42-
initial 6,25 10-3 mol 9,37 10-5 mol 0 0
en cours 6,25 10-3 -2x 9,37 10-5 -x x x
fin 6,25 10-3 -2*9,37 10-5 0 9,37 10-5 9,37 10-5
qté de matière : nS2O82- = 9,37 10-5 -x = 9,37 10-5 -nI2;
volume du mélange 0,04 L d'où : [S2O82- ]=9,37 10-5 /0,04 - [I2]= 2,34 10-3 -A/1250.
si la cinétique est d'ordre 1, on trace ln[S2O82- ] en fonction du temps :on doit alors obtenir une
droite dont la pente donne l'opposé de la constante de vitesse apparente k'.
t (min) 0 4 8 12 16
A 0 0,349 0,67 0,94 1,178
ln[S2O82- ] -0,605 -6,185 -6,44 -6,56
k' = 3,2 10-2 min-1.
retour - menu
Vous aimerez peut-être aussi
- Cinétique Chimique PDFDocument4 pagesCinétique Chimique PDFmostafa90raoufPas encore d'évaluation
- Td9chim2019 2020Document4 pagesTd9chim2019 2020Med Stu DentPas encore d'évaluation
- M28 - Cinétique - TD1 - CorrectionDocument7 pagesM28 - Cinétique - TD1 - CorrectionHassan DriouachPas encore d'évaluation
- Exercice Corrigé CinétiqueDocument13 pagesExercice Corrigé Cinétiquejakobslimani02Pas encore d'évaluation
- TSP2SP2Ch9T4-exos Resolus p245n11 246n15 250n25Document5 pagesTSP2SP2Ch9T4-exos Resolus p245n11 246n15 250n25mohPas encore d'évaluation
- C Ex02 Cin CaDocument3 pagesC Ex02 Cin CaZedexterPas encore d'évaluation
- 1cm3usujd 504803Document4 pages1cm3usujd 504803sowpapagora444Pas encore d'évaluation
- Série 1 Cinétique 2020 2021Document4 pagesSérie 1 Cinétique 2020 2021Li Na0% (1)
- M28 - Cinétique - TD2 - CorrectionDocument7 pagesM28 - Cinétique - TD2 - CorrectionHassan DriouachPas encore d'évaluation
- TD2 Correction PDFDocument8 pagesTD2 Correction PDFKhadija LakhdiriPas encore d'évaluation
- TD Cin & Cat SMC S5 .Document32 pagesTD Cin & Cat SMC S5 .Chai Mae100% (3)
- Chimie TD 3 Cinétique ChimiqueDocument4 pagesChimie TD 3 Cinétique ChimiqueFranck Momo100% (1)
- Srie Dexos Cintique L3-GPDocument6 pagesSrie Dexos Cintique L3-GPFatima YahiaPas encore d'évaluation
- Série Cinétique Chimique 2bac: P T P T RDocument9 pagesSérie Cinétique Chimique 2bac: P T P T Rrkibi.khadija2006Pas encore d'évaluation
- TD de CinétiqueDocument14 pagesTD de CinétiqueDieu-donné Akin100% (2)
- Kinetics - CinetiqueDocument8 pagesKinetics - CinetiqueRalphNkdPas encore d'évaluation
- Cinétique TDDocument5 pagesCinétique TDBadr MouslimPas encore d'évaluation
- Exos CH 04Document3 pagesExos CH 04lol testPas encore d'évaluation
- Ob s1 Cinetique ChimiqueDocument2 pagesOb s1 Cinetique Chimiquemedabdellahisamba34Pas encore d'évaluation
- S Rie D Exercices Corrig S Cin TiqueDocument6 pagesS Rie D Exercices Corrig S Cin Tiqueanie KheliliPas encore d'évaluation
- C2Chim Suivi Cinetique ExercicesDocument8 pagesC2Chim Suivi Cinetique ExercicesMohamed El OuahdaniPas encore d'évaluation
- TP N° 02 ThermodynamiqueDocument6 pagesTP N° 02 ThermodynamiquemutracePas encore d'évaluation
- SerieDocument7 pagesSeriemehdi benmassoudPas encore d'évaluation
- Fichier Produit 2658Document4 pagesFichier Produit 2658FlorinaPas encore d'évaluation
- Chapitre 3Document8 pagesChapitre 3Section E GPPas encore d'évaluation
- Correction Td3Document7 pagesCorrection Td3Harakat ElhoucinePas encore d'évaluation
- TD-cinetique ChimiqueDocument2 pagesTD-cinetique ChimiqueHaytem bossPas encore d'évaluation
- Correction Du TP - Suivi Temporel D'une Transformation Chimique Par ...Document3 pagesCorrection Du TP - Suivi Temporel D'une Transformation Chimique Par ...WaliD MerabeT0% (1)
- Série Corrigé CinétiqueDocument8 pagesSérie Corrigé Cinétiquejakobslimani02Pas encore d'évaluation
- Etude de La Réaction de Saponification de LDocument11 pagesEtude de La Réaction de Saponification de Lselmi nourelhouda100% (1)
- KineticsDocument30 pagesKineticsMoustapha BelmoudenPas encore d'évaluation
- Cours 4-ConvertiDocument4 pagesCours 4-ConvertiÑar Ďjes100% (1)
- BAC S1S3 1G SN 2022 SujetDocument4 pagesBAC S1S3 1G SN 2022 SujetMohamed Aly SawadogoPas encore d'évaluation
- Cinétique Chimique TD Corrigé 05Document8 pagesCinétique Chimique TD Corrigé 05elie mij kisalePas encore d'évaluation
- Exem PCDocument6 pagesExem PCwfwgPas encore d'évaluation
- Local Media6834814526131562016Document296 pagesLocal Media6834814526131562016Raouf Elwazr100% (1)
- TD Cinétique Chimique Série N°1 CorrectionDocument6 pagesTD Cinétique Chimique Série N°1 CorrectionadnanPas encore d'évaluation
- 2 - Suivi Temporel D'une Transformation - Vitesse de RéactionDocument31 pages2 - Suivi Temporel D'une Transformation - Vitesse de Réactionlahcen essPas encore d'évaluation
- 1cm5q85hc 441159Document5 pages1cm5q85hc 441159Med yahyaPas encore d'évaluation
- Bac PCDocument5 pagesBac PCOumar KakoroPas encore d'évaluation
- M28 Cinétique TD1Document2 pagesM28 Cinétique TD1Hassan DriouachPas encore d'évaluation
- 2007 09 National Exo1 Correction Iode 6 5ptsDocument4 pages2007 09 National Exo1 Correction Iode 6 5ptsYoussef Ismaili alaouiPas encore d'évaluation
- Cinetique Chimique ExosDocument3 pagesCinetique Chimique ExosAbel MalléPas encore d'évaluation
- Correction Synth1 4MDocument2 pagesCorrection Synth1 4MAmine AlaoUii AlaouiPas encore d'évaluation
- Avancement 2Document2 pagesAvancement 2Foudil LaouiciPas encore d'évaluation
- Cours 3 Cinétique Khenifi-ConvertiDocument6 pagesCours 3 Cinétique Khenifi-ConvertiÑar ĎjesPas encore d'évaluation
- CC Exos - 2009 2010 PDFDocument8 pagesCC Exos - 2009 2010 PDFSimplice AssemienPas encore d'évaluation
- Chimie TD 3 Cinétique Chimique PDFDocument4 pagesChimie TD 3 Cinétique Chimique PDFOussama El BouadiPas encore d'évaluation
- PC C2017 CorDocument10 pagesPC C2017 Corrktm.avotraPas encore d'évaluation
- TDCH5 CinetiqueDocument3 pagesTDCH5 CinetiqueahmadPas encore d'évaluation
- 2008 Bac PC Ter s2Document4 pages2008 Bac PC Ter s2Lindoucha DadouchaPas encore d'évaluation
- Simili 2020-Converti PDFDocument7 pagesSimili 2020-Converti PDFyasmine mahmoud100% (1)
- Examen Et Corrigé - Chimie I - 2017Document4 pagesExamen Et Corrigé - Chimie I - 2017kim namjoonPas encore d'évaluation
- TS - BAC Blanc N°1 Corrigé - Spécialité PDFDocument4 pagesTS - BAC Blanc N°1 Corrigé - Spécialité PDFphytanjaPas encore d'évaluation
- TP7 Cinétique Chimique Du Premier Ordre.Document14 pagesTP7 Cinétique Chimique Du Premier Ordre.Sellam Anis100% (1)
- Examen National Physique Chimie SPC 2019 Rattrapage SujetDocument7 pagesExamen National Physique Chimie SPC 2019 Rattrapage Sujethicham lahdissou100% (1)
- Support de Cours Cinétique Termochimie ENSA 1Document17 pagesSupport de Cours Cinétique Termochimie ENSA 1Håmzā El MrãbêtPas encore d'évaluation
- TP Modelisation MoleculesDocument2 pagesTP Modelisation MoleculesbelbaliabdelhekPas encore d'évaluation
- Sujet 1Document4 pagesSujet 1Yesmin RhimiPas encore d'évaluation
- Bepc Blanc PC 2024. Aeemb.Document2 pagesBepc Blanc PC 2024. Aeemb.Jean Oscar Bado100% (1)
- 02 Lewis-CorrectionDocument4 pages02 Lewis-CorrectionEL BOUJI SOUFIANEPas encore d'évaluation
- Chapitre 12Document27 pagesChapitre 12nadyPas encore d'évaluation
- Bac Blanc - Acides Bases Avec Correction MR SABOURDocument7 pagesBac Blanc - Acides Bases Avec Correction MR SABOURHassanEssoufiPas encore d'évaluation
- TD N°2 Diagramme Fer-CarboneDocument4 pagesTD N°2 Diagramme Fer-CarboneOuail BeddalPas encore d'évaluation
- Agglomèration Des Minerais de FerDocument22 pagesAgglomèration Des Minerais de Feradelbouabida5Pas encore d'évaluation
- Nanomatériaux Et Ses ApplicationsDocument50 pagesNanomatériaux Et Ses Applicationsan hamPas encore d'évaluation
- Devoir 3 Modele 2 Physique Chimie 1ac Semestre 1 CorrigeDocument1 pageDevoir 3 Modele 2 Physique Chimie 1ac Semestre 1 CorrigeAbdellah EL MAMOUNPas encore d'évaluation
- Cours TD'E 1et2Document2 pagesCours TD'E 1et2brahimza61Pas encore d'évaluation
- Chimie Organique - Notions Fondamentales - Richard HuotDocument593 pagesChimie Organique - Notions Fondamentales - Richard HuotRyanPas encore d'évaluation
- Cours - Interactions InterfacialesDocument17 pagesCours - Interactions Interfacialesbrahimza61Pas encore d'évaluation
- TP Chlmie (1) - 1 2Document18 pagesTP Chlmie (1) - 1 2amineoifikPas encore d'évaluation
- Tourmaline - WikipédiaDocument12 pagesTourmaline - WikipédiaDieu Le Veut MiahouamaPas encore d'évaluation
- Bepc Blanc Regional Ce 2023 PCTDocument1 pageBepc Blanc Regional Ce 2023 PCTmagaretmoagangPas encore d'évaluation
- Série PROPRIETES CHIMIQUES DES METAUX USUELSDocument2 pagesSérie PROPRIETES CHIMIQUES DES METAUX USUELSFallou NdiayePas encore d'évaluation
- TP 3 Extraction Diiode Par Le CyclohexaneDocument2 pagesTP 3 Extraction Diiode Par Le CyclohexaneBouhadPas encore d'évaluation
- Travaux Dirigés Chimie OrganiqueDocument3 pagesTravaux Dirigés Chimie Organiquezoungranasebastien102Pas encore d'évaluation
- Chemistry Paper 3 TZ2 HL MarkschemeDocument31 pagesChemistry Paper 3 TZ2 HL MarkschemekasomaisaackPas encore d'évaluation
- 100r00FRintraFG FeSiDocument4 pages100r00FRintraFG FeSiAshikPas encore d'évaluation
- Chimie Org CHP 1 SMPC S2 2024Document59 pagesChimie Org CHP 1 SMPC S2 2024abb32214Pas encore d'évaluation
- Rapport de Stage CMTDocument16 pagesRapport de Stage CMTANWAR EL ASSALIPas encore d'évaluation
- Catalogue BAC D PhysiqueDocument43 pagesCatalogue BAC D PhysiqueOussoumadina DialloPas encore d'évaluation
- 4e CHIMIE La StœchiométrieDocument4 pages4e CHIMIE La Stœchiométrie2mgrx9km8fPas encore d'évaluation
- 02 - Exerices Sur Concentration MassiqueDocument2 pages02 - Exerices Sur Concentration MassiqueEric DescampsPas encore d'évaluation
- Méthodes Thermiques - D'analyseDocument112 pagesMéthodes Thermiques - D'analyseBRAHIMPas encore d'évaluation
- Exercices Divers Sur Le Thème OxydoréductionDocument12 pagesExercices Divers Sur Le Thème Oxydoréductionissaradjab13Pas encore d'évaluation
- HySchools Methodes de Production D'hydrogene Powerpoint Pour Les ElevesDocument13 pagesHySchools Methodes de Production D'hydrogene Powerpoint Pour Les Eleveskaoutaramr8Pas encore d'évaluation
- Notice Groupe Électrogène mc6000Document32 pagesNotice Groupe Électrogène mc6000julien goudardPas encore d'évaluation