Académique Documents
Professionnel Documents
Culture Documents
tp1 Vinaigre
Transféré par
lamichi boudjemaaTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
tp1 Vinaigre
Transféré par
lamichi boudjemaaDroits d'auteur :
Formats disponibles
TS Tp1 : 3 dosages du vinaigre
BUT : comment contrôler la qualité d’un produit par dosage.
Produits testés : différents types de vinaigre du commerce.
Caractéristique à vérifier : le degré d’acidité d’un vinaigre dont le principal acide est l’ACIDE ACETIQUE
(éthanoïque) CH3COOH
Sur chaque bouteille est indiqué le degré d’acidité du vinaigre testé. Le degré d’acidité d’un vinaigre est égal à la
masse d’acide acétique équivalente à l’acidité totale de 100 g de vinaigre. Par exemple, un vinaigre de 8° a la même
acidité qu’une solution contenant 8 g d’acide acétique pour 100 g de vinaigre.
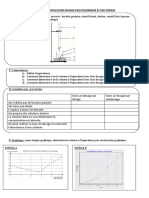
Principe du dosage
On utilise une réaction totale et rapide pour déterminer la concentration en acide éthanoïque de l’échantillon étudié
Ici action de la soude (Na+ + OH-) sur CH3COOH : CH3 –COOH + OH- CH3 –COO- + H2O
L’équivalence est atteinte quand les
2 réactifs sont entièrement
consommés
Vbeq = volume de soude versée
à l’équivalence
xm = cava= cb.vbeq
Cb.Vbeq
Donc ca =
Va
Comment repérer l’équivalence suivant les méthodes utilisées
Cas du titrage pH-métrique
Calcul de la courbe dérivée dans Excel
Expériences et mesures
Type de vinaigre testé :
Réaliser un dosage conductimétrique, un dosage pH-métrique et un dosage colorimétrique du vinaigre testé après
l’avoir dilué 10 fois, par de la soude à 0.1 mol/L
Compte rendu
1- Dilution : Expliquer comment la dilution 10x a été réalisée.
2- mesures
a. Dosage pH métrique
dpH
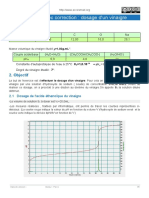
Tracer la courbe pH = f(Vb), Rajouter une colonne pour calculer la courbe dérivée : et faire tracer sur
dV
le même graphe. Par la méthode des tangentes et celle de la courbe dérivée, déterminer graphiquement
le volume équivalent Vbeq. Noter également le pH à l’équivalence.
b. Dosage conductimétrique
Tracer σ = f(Vb). Déterminer graphiquement le volume équivalent Vbeq
c. Dosage colorimétrique
Relever le volume équivalent Vbeq et indiquer le changement de teinte de l’indicateur utilisé.
3- Résultats
Pour chacune des 3 méthodes, trouver la concentration en acide éthanoïque de l’échantillon de vinaigre dilué
En déduire la concentration du vinaigre non dilué puis son degré d’acidité. Comparer les résultats des 3
expériences avec l’indication de l’étiquette de la bouteille de vinaigre. ( données : M(CH3COOH) = 60 g/mol ;
ρ(CH3COOH) =1g/mL )
4- Questions annexes
a) Justifier l’utilisation de la phénolphtaléine comme indicateur coloré plutôt que le rouge de méthyle.
(données zone de virage : phénolphtaléine : 8-10 ; rouge de méthyle : 4-6)
b) Justifier l’allure de la courbe σ = f(Vb) (aucun calcul nécessaire)
Donnée : expression générale de la conductivité :
σ = Σ λi x [Xi] = λ Na+ [Na+] + λ CH3COO- [CH3COO-] + λ OH- [OH-]
conductivités molaires ioniques :
Vous aimerez peut-être aussi
- Mes Recettes MédiévalesDocument6 pagesMes Recettes MédiévalesRadinPas encore d'évaluation
- Bac 2023 Physique-Chimie STL - Sujet - Jour 2Document14 pagesBac 2023 Physique-Chimie STL - Sujet - Jour 2LETUDIANT100% (1)
- Série Dosage PDFDocument8 pagesSérie Dosage PDFAya ArPas encore d'évaluation
- SectionB Groupe58Document26 pagesSectionB Groupe58misbah mohamedPas encore d'évaluation
- Fiches Exercices Titrages-2010Document3 pagesFiches Exercices Titrages-2010Daniel Parnor100% (1)
- TP N2 PH MetrieDocument15 pagesTP N2 PH MetrieSellam Anis100% (2)
- TP Dosage de L Acidite D Un VinaigreDocument3 pagesTP Dosage de L Acidite D Un VinaigreDjahid Jo75% (4)
- Série 1 - Dosage Acido-BasiqueDocument2 pagesSérie 1 - Dosage Acido-BasiqueBoussetta ZouhaierPas encore d'évaluation
- Chimie-Dosages Par TitragesDocument33 pagesChimie-Dosages Par TitragesSleh Ben SoltanPas encore d'évaluation
- Epreuves CP - 3ème Trim 2021Document9 pagesEpreuves CP - 3ème Trim 2021groupescolaireibnataimranPas encore d'évaluation
- 07 - Titrage PH VinaigreDocument3 pages07 - Titrage PH VinaigreChartier Julien50% (2)
- Titrage Du Vinaigre CorrectionDocument4 pagesTitrage Du Vinaigre CorrectionOstensible50% (2)
- 07 Titrage PH VinaigreDocument3 pages07 Titrage PH Vinaigrenabil douadiPas encore d'évaluation
- TP N 03Document6 pagesTP N 03AhmedPas encore d'évaluation
- TPDosage Vinaigre CorDocument3 pagesTPDosage Vinaigre CorCamille LegavePas encore d'évaluation
- Chimie B Chap8 Titrage AcidobasiqueDocument6 pagesChimie B Chap8 Titrage AcidobasiqueSamantha Farah100% (1)
- Dosages Acide ConvertiDocument6 pagesDosages Acide ConvertiAbir SoujaaPas encore d'évaluation
- Titrage VinaigreDocument2 pagesTitrage VinaigreDjahid Jo100% (2)
- Dosage Acido-Basique FRDocument3 pagesDosage Acido-Basique FRAicha DaouPas encore d'évaluation
- tp8 Dosage Phmetrique PDFDocument2 pagestp8 Dosage Phmetrique PDFMokhtarBensaidPas encore d'évaluation
- TP2 PDFDocument3 pagesTP2 PDFAz-eddine KaibaPas encore d'évaluation
- TP 1 CphysiDocument3 pagesTP 1 Cphysiazou korbaPas encore d'évaluation
- Null 231221 095942Document2 pagesNull 231221 095942zeinabhatemtarchichiPas encore d'évaluation
- TP C7 Vinaigre FrelatDocument3 pagesTP C7 Vinaigre FrelatAmelie PinchonPas encore d'évaluation
- Tp.3 Titrage PH Metrique Et ColorimétriqueDocument5 pagesTp.3 Titrage PH Metrique Et ColorimétriqueMalak El jadiriPas encore d'évaluation
- Rapport Degre D'aciditeDocument5 pagesRapport Degre D'aciditezeinabhatemtarchichiPas encore d'évaluation
- TP 1 Titrage PhmetriqueDocument3 pagesTP 1 Titrage Phmetriqueelhidhab2014Pas encore d'évaluation
- GRIESP Tle Titrage Destop 1207602Document9 pagesGRIESP Tle Titrage Destop 1207602Amelie PinchonPas encore d'évaluation
- TS - Chim 8 - TP Ch6Document2 pagesTS - Chim 8 - TP Ch6Omar KhalfiPas encore d'évaluation
- AE04-Titrage Destop-REGRESSI-2022-eleves - 2Document4 pagesAE04-Titrage Destop-REGRESSI-2022-eleves - 2Yazine ZeidPas encore d'évaluation
- Chimie-Dosages Par TitragesDocument35 pagesChimie-Dosages Par TitragesgrajzgrPas encore d'évaluation
- Série 1 - Dosage Acido-BasiqueDocument2 pagesSérie 1 - Dosage Acido-BasiqueAzdine MC100% (1)
- TP Dosage PhmetriqueDocument1 pageTP Dosage PhmetriqueNesrine BouzidPas encore d'évaluation
- TP Dosage D'un Vinaigre (ExAO)Document2 pagesTP Dosage D'un Vinaigre (ExAO)wassi laPas encore d'évaluation
- Série DosageDocument8 pagesSérie DosageAicha Daou100% (1)
- Serie Acide Fort Base Forte DosageDocument6 pagesSerie Acide Fort Base Forte DosageAmadou Oury DialloPas encore d'évaluation
- Exercices Application Dosage Par Etalonnage Et Par TitrageDocument3 pagesExercices Application Dosage Par Etalonnage Et Par TitrageMohamed Ali MahjoubPas encore d'évaluation
- Lycee Chimie Exercice DosageEtalonnageTitrage 1266274Document3 pagesLycee Chimie Exercice DosageEtalonnageTitrage 1266274Marius MissiPas encore d'évaluation
- Acice Fort Base Forte Exercice 1Document8 pagesAcice Fort Base Forte Exercice 1Hamidou Diatta100% (1)
- SeÌ Rie 1 - Dosage Acido-BasiqueDocument2 pagesSeÌ Rie 1 - Dosage Acido-Basiqueb01554837Pas encore d'évaluation
- Chap.6 TP12 Titrage PH Metrique D Un Vinaigre Correction PDFDocument2 pagesChap.6 TP12 Titrage PH Metrique D Un Vinaigre Correction PDFYouSsef EchafaiPas encore d'évaluation
- Chimie B Chap8 Titrage - Acidobasique PDFDocument6 pagesChimie B Chap8 Titrage - Acidobasique PDFMouloud IssaadPas encore d'évaluation
- Chimie-TP5 Suivi Phmetrique de L'acide Ethanoique Par La SoudeDocument2 pagesChimie-TP5 Suivi Phmetrique de L'acide Ethanoique Par La SoudeChartier Julien100% (1)
- Ach13 Corrige ExercicesDocument3 pagesAch13 Corrige ExercicesmohamedPas encore d'évaluation
- Titrages Acido-Basiques PDFDocument4 pagesTitrages Acido-Basiques PDFtarikPas encore d'évaluation
- Dosage 2Document3 pagesDosage 2Riadh Marouani100% (1)
- GPS Mesures Incertitudes 2014 S Determination Pka Acide EthDocument6 pagesGPS Mesures Incertitudes 2014 S Determination Pka Acide EthCassandra LamarchePas encore d'évaluation
- Exercice Corrigé Sur DosageDocument5 pagesExercice Corrigé Sur DosageIkram MgPas encore d'évaluation
- RFDS TP TS Titrage SimulationDocument17 pagesRFDS TP TS Titrage SimulationMoi De speedPas encore d'évaluation
- TP-PH-métrie ElectrochimieDocument14 pagesTP-PH-métrie ElectrochimieAya DgmPas encore d'évaluation
- 03 Titrages Acido BasiquesDocument7 pages03 Titrages Acido BasiquesMoha BaihiPas encore d'évaluation
- Analyse de Courbes de Titrage PH MetriquesDocument3 pagesAnalyse de Courbes de Titrage PH MetriquesDaniela DinicaPas encore d'évaluation
- Serie D'exercices Sur C5 Et C6: IA Kédougou - Cellule Mixte Des Sciences Physiques - Terminale S 2019-2020Document4 pagesSerie D'exercices Sur C5 Et C6: IA Kédougou - Cellule Mixte Des Sciences Physiques - Terminale S 2019-2020kathyPas encore d'évaluation
- 53 Bba 01 Ceda 68Document4 pages53 Bba 01 Ceda 68Bøũdįāf KhäwlåPas encore d'évaluation
- Ammoniaque CorrectionDocument6 pagesAmmoniaque CorrectionJean FoncePas encore d'évaluation
- Ch04 Dosage Par TitrageDocument2 pagesCh04 Dosage Par Titragesylvain zuchiattiPas encore d'évaluation
- Bac-Blanc 2022-2023 - MaisonDocument9 pagesBac-Blanc 2022-2023 - MaisonnjnPas encore d'évaluation
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- Ail 10Document6 pagesAil 10hoffer2Pas encore d'évaluation
- Cumulez Encore Plus Vite Vos Vignettes Avec Nos Marques PartenairesDocument7 pagesCumulez Encore Plus Vite Vos Vignettes Avec Nos Marques PartenairesEmma JouanPas encore d'évaluation
- 15 RAFkkDocument11 pages15 RAFkkzakaryae belaidiPas encore d'évaluation
- N 5 JESwid ONoxp A43 U5 Jif Eq 1 PN 4Document4 pagesN 5 JESwid ONoxp A43 U5 Jif Eq 1 PN 4zohraPas encore d'évaluation
- Ob - 290cc3 - Ue 2 2 s1 Equilibre Alimentaire LucieDocument50 pagesOb - 290cc3 - Ue 2 2 s1 Equilibre Alimentaire LucieSoosoo SouPas encore d'évaluation
- Communiquez Cluchi TranscriptionsDocument37 pagesCommuniquez Cluchi Transcriptionsyixinznzn325Pas encore d'évaluation
- Ou Prendre Sa Retraite A - ALGHERO en SardaigneDocument15 pagesOu Prendre Sa Retraite A - ALGHERO en SardaigneMarcel PirardPas encore d'évaluation
- Jeu Des Tickets de Caisse Niveau 1Document4 pagesJeu Des Tickets de Caisse Niveau 1claire.sacconePas encore d'évaluation
- Time 1Document8 pagesTime 1Noschika BrunoPas encore d'évaluation
- Catalogue Jayda 2021 - 2V PDFDocument30 pagesCatalogue Jayda 2021 - 2V PDFNasri MarwanePas encore d'évaluation
- Correction - LES EXERCICES, Partitifs, Definis, Adjectif PossessifsDocument3 pagesCorrection - LES EXERCICES, Partitifs, Definis, Adjectif Possessifsivygreen5596Pas encore d'évaluation
- Rapport de Sta5555555555555Document10 pagesRapport de Sta5555555555555Naima ElPas encore d'évaluation
- Feuille de Service J8Document5 pagesFeuille de Service J8nicanor512Pas encore d'évaluation
- Hygiene Generale de Vie D'Un Nourrisson: DR Z.Ait LhajDocument14 pagesHygiene Generale de Vie D'Un Nourrisson: DR Z.Ait LhajelissaminoPas encore d'évaluation
- RC 20 NeutreDocument1 pageRC 20 Neutreabbes fettahPas encore d'évaluation
- CE - Réponses - de - 101 - Textes - Résumé Abou IsraeDocument19 pagesCE - Réponses - de - 101 - Textes - Résumé Abou IsraeWaneeza AslamPas encore d'évaluation
- La Belle Au Bois DormantDocument5 pagesLa Belle Au Bois Dormantsoumaya ramyPas encore d'évaluation
- 02.pipistrelle Au SaharaDocument15 pages02.pipistrelle Au SaharaLyudmila SilenokPas encore d'évaluation
- AvertissementDocument129 pagesAvertissementmatcscribdPas encore d'évaluation
- Cours N°1Document4 pagesCours N°1aureadupontPas encore d'évaluation
- APS Fiches EntrainementDocument122 pagesAPS Fiches EntrainementCathy CARBONIPas encore d'évaluation
- Fiche Enseignant Raconter Des SaladesDocument5 pagesFiche Enseignant Raconter Des SaladesSofiene ChaiebPas encore d'évaluation
- 6eme Francais Module 6 Mouna ChahedDocument14 pages6eme Francais Module 6 Mouna ChahedInsaf Miled75% (4)
- Wolf Skin Omega 55582 Wolfcreek HighschoolDocument18 pagesWolf Skin Omega 55582 Wolfcreek HighschoolChristopher CollinetPas encore d'évaluation
- UserManualDocument64 pagesUserManualBleidd-ddynPas encore d'évaluation
- Mesure de Contenances CM1Document4 pagesMesure de Contenances CM1housseinmouna410Pas encore d'évaluation
- K Pour Katrine-N13 2023Document100 pagesK Pour Katrine-N13 2023karen.jPas encore d'évaluation