Académique Documents
Professionnel Documents
Culture Documents
Série 1 - Dosage Acido-Basique
Transféré par
Boussetta Zouhaier0 évaluation0% ont trouvé ce document utile (0 vote)
396 vues2 pagesd
Titre original
Série 1 . Dosage Acido-basique
Copyright
© © All Rights Reserved
Formats disponibles
DOCX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentd
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
396 vues2 pagesSérie 1 - Dosage Acido-Basique
Transféré par
Boussetta Zouhaierd
Droits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOCX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 2
Dosage acido-basique
Exercice n°1 : Acide benzoïque
1. On dose une solution (S) d’acide benzoïque
C6H5COOH de volume V=15,2mLet de
concentration C par une solution d’hydroxyde
de sodium de concentration Cb= 2,0.10-1 moL.L-1.
1.1- Écrire l’équation de la réaction du dosage.
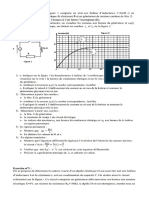
1.2- On obtient au cours de ce dosage
l’évolution du pH de la solution en fonction
du volume Vb de la solution d’hydroxyde de
sodium ajouté, fig 1.
a-Déterminer la concentration de la solution
de l’acide benzoïque.
b- Déterminer le pH du mélange à l’équivalence
en déduire la nature de la solution à ce point.
1.3- On dispose de deux Indicateurs colorés
suivant et leurs zones de virage:
Hélianthine : 3,2-4,4
Phénol phtaléine : 8,2-10,0 ; Choisir l’indicateur coloré quiconvient à ce dosage .Justifier votre choix.
1.4-Pour un volume versé Vb=6mL d’hydroxyde de sodium , calculer le taux d’avancement de cette réaction
de dosage, conclure .
2.A l’aide des mesures du pH des solutions aqueuses d’acide
benzoïque de concentrations différentes, on détermine le taux
d’avancement final de chaque solution. La courbe de la
2
figure2 représente la fonction 1 =f(1/C). Trouver
l’expression de la constante d’acidité pKA du couple acide
benzoïque / ion benzoate en fonction de et C. Faire l’A.N
3. Au cours du dosage précédent, montrer que pour un
V
( bE 1)
volume VbVbE on a :pH =pKA - log Vb . Pour quel volume Vb on aura pH=pKA ?
4. Pour Vb=10mL calculer le rapport A /AH dans le mélange (AH désigne l’acide benzoïque) .quelle est
-
l’espèce prédominante à ce point ?
5. Calculer la constante d’équilibre pour la réaction du dosage et vérifier le résultat de la question 1.4
Exercice n° 2 : Acide chlorhydrique et sa réaction avec l’ammoniac
L’objectif de cet exercice est l’étude de quelques propriétés de l’ammoniac et de l’hydroxylamine NH2OH
dissouts dans l’eau et de déterminer la concentration de l’ammoniac dans un produit commercial à l’aide
d’une solution d’acide chlorhydrique de concentration connue.
Données : toutes les mesures sont effectuées à 25°C.
- La masse volumique de l’eau : ρ =1g.cm-3
- La masse molaire du chlorure d’hydrogène : M = 36,5g/moL
- Le produit ionique de l’eau : pKe =14
- La constante d’acidité du couple NH4+/NH3 est KA1
- La constante d’acidité du couple NH3OH+/NH2OH est KA2
1-Préparation de la solution d’acide chlorhydrique :
On prépare une solution SA d’acide chlorhydrique de concentration CA=0,015mol/L en diluant une solution
commerciale de concentration C0 en cet acide et dont la densité par rapport à l’eau est
d =1,15. Le pourcentage massique de l’acide dans cette solution commerciale est P = 37%.
1.1. Trouver l’expression de la quantité de matière d’acide n(HCl) contenue dans un volume V de la solution
commerciale en fonction de P,d,V,ρ et M . vérifier que C0=11,6moL/L .
1.2. Calculer le volume qu’il faut prélever de la solution commerciale pour préparer 1L de la solution SA .
2- Etude de quelques propriétés d’une base dissoute dans l’eau
2.1. On considère une solution aqueuse d’une base B de concentration C. On note KA la constante d’acidité
du couple BH+/ B etle taux d’avancement final de sa réaction avec l’eau.
K e (1 )
KA
Montrer que : C. 2 .
2.2. On mesure lepH1d’une solution S1 d’ammoniac NH3 de concentration C=1.10-2moL/L et le pH2 d’une
solution S2 d’hydroxylamine NH2OH ayant la même concentration C ; On trouve alors
pH1=10,6 et pH2=9. Calculer les taux d’avancement finaux respectifs des réactions de NH3 et de NH2OH
avec l’eau.
2.3. Calculer la valeur de chacune des constantespKA1 et pKA2 .
3- Dosage acide-base d’une solution diluée d’ammoniac.
Pour déterminer la concentration CB d’une
solution commerciale concentrée
d’ammoniac, on procède par dosage
acido – basique .On prépare par dilution
une solution S de concentration C’=CB/1000 .
On réalise le dosage pH- métrique d’un
volume V =20 mL de la solution S à l’aide
d’une solution SA d’acide chlorhydrique de
concentration CA= 0,015moL/L.
On mesure le pH du mélange après chaque
addition d’un volume d’acide ; Les résultats
obtenus permettent de tracer la courbe de
dosage pH= f (VA ) .fig
3-1 Ecrire l’équation de la réaction du
dosage.
3-2 En utilisant la valeur du pH
correspondante à l’addition de 5mLd’acide
chlorhydrique ,calculer le taux
d’avancement final de la réaction du dosage.
Conclure .Vérifier ce résultat en calculant
la constante d’équilibre de cette réaction.
3-3 Déterminer le volume VAE en déduire C’
et CB .
3-4 Parmi les indicateurs colorés indiqués ci-dessous , choisir celui qui conviendra le mieux à ce dosage .
L’indicateur coloré Zone de virage 3-5 Pour un volume VAVAE , montrer que
V
( AE 1)
Phénolphtaléine 8 ,2 – 10 pH =pK + log VA
A1 .
Rouge de chlorophénol 5 ,2 - 6 ,8 3-6 Quel volume VA à ajouter pour que : 10NH3=15NH4+
Hélianthine 3 ,1 - 4 ,4 dans le mélange.
3-7 Quel est le nom de la solution obtenue à l’équivalence ?
Vous aimerez peut-être aussi
- Bac Math Pysh Acide Base Serie 4Document1 pageBac Math Pysh Acide Base Serie 4Nourhene Jlassi33% (3)
- Transformations Liees A Des Reactions Acide Base Exercices Non Corriges 1 1Document6 pagesTransformations Liees A Des Reactions Acide Base Exercices Non Corriges 1 1boufdili100% (2)
- Devoir de Synthèse N°1 2022 2023Document4 pagesDevoir de Synthèse N°1 2022 2023Mohamed Hamdene100% (2)
- B Blan 2021 (SP)Document7 pagesB Blan 2021 (SP)HAMADA1972Pas encore d'évaluation
- Examen Blanc N°2 Du Baccalauréat Année: 2020Document8 pagesExamen Blanc N°2 Du Baccalauréat Année: 2020Mehdi AgPas encore d'évaluation
- Série D'exercices - Physique Oscillations Électriques Libres Non Amorties - Bac Sciences Exp (2013-2014) MR Rouabhia PDFDocument4 pagesSérie D'exercices - Physique Oscillations Électriques Libres Non Amorties - Bac Sciences Exp (2013-2014) MR Rouabhia PDFAzizElheni100% (1)
- DC N - 1 SC - Exp PDFDocument6 pagesDC N - 1 SC - Exp PDFMohamed SaidiPas encore d'évaluation
- Exercices Ondes Mecaniques Progressives PeriodiquesDocument5 pagesExercices Ondes Mecaniques Progressives PeriodiquesMoulayMoulyPas encore d'évaluation
- Blanc Taiba FBDocument8 pagesBlanc Taiba FBsine abdellah0% (1)
- Examen Blanc PC ResiDocument10 pagesExamen Blanc PC ResiMouad ChakerPas encore d'évaluation
- Dev de Controle 1 Bac SC - ExpDocument5 pagesDev de Controle 1 Bac SC - ExpImed OmranePas encore d'évaluation
- Bac Blanc 2 SM (21-22)Document9 pagesBac Blanc 2 SM (21-22)Salma Bendaoud100% (1)
- Simili - 6h de Physique Chimie Pour Les SM MR SABOUR 2023Document10 pagesSimili - 6h de Physique Chimie Pour Les SM MR SABOUR 2023SABOUR MOHAMMEDPas encore d'évaluation
- Devoir 2 SP - 2022 - TaibaDocument4 pagesDevoir 2 SP - 2022 - TaibaMustapha Zaki100% (1)
- Simili 2022 PC FRDocument7 pagesSimili 2022 PC FRAmmar LokihiPas encore d'évaluation
- Bac Blanc 2021bisDocument7 pagesBac Blanc 2021bisSahbi Mabrouki YamenPas encore d'évaluation
- Dev Synthese N°14scDocument6 pagesDev Synthese N°14scSahbi Mabrouki Yamen0% (1)
- Serie Suivi 2 Bac Biof SM PC FrancaisDocument5 pagesSerie Suivi 2 Bac Biof SM PC FrancaisMoussa Traoré100% (1)
- Controle2 Partie 2 2022ههDocument4 pagesControle2 Partie 2 2022ههMouhibi Abdellah100% (1)
- SC-PHYS (Elèves) 1ères F1, F4, Ti1Document76 pagesSC-PHYS (Elèves) 1ères F1, F4, Ti1galen adjaklouPas encore d'évaluation
- Dipole RL 2023 Serie 2 A FaireDocument5 pagesDipole RL 2023 Serie 2 A Faireourabitayssir756100% (1)
- Devoir de Synthèse N°1 - Sciences Physiques - Bac Mathématiques (2020-2021) MR Sfaxi SalahDocument5 pagesDevoir de Synthèse N°1 - Sciences Physiques - Bac Mathématiques (2020-2021) MR Sfaxi SalahWajih M'likiPas encore d'évaluation
- Serie 1 Le Dipole RCDocument13 pagesSerie 1 Le Dipole RCBoussetta Zouhaier100% (1)
- Annales Du Bac - 1995-2005Document30 pagesAnnales Du Bac - 1995-2005Japhet BAOUNDOULAPas encore d'évaluation
- 3e DS1 2010 2011Document3 pages3e DS1 2010 2011fethi1100% (1)
- Blanc N°1 2023Document7 pagesBlanc N°1 2023Alaoui AminePas encore d'évaluation
- Epreuves Ems 1Document5 pagesEpreuves Ems 1Bÿbÿbätöü MbayePas encore d'évaluation
- Resume Des Projectiles 2 Bac SMDocument14 pagesResume Des Projectiles 2 Bac SMTunisie La terrePas encore d'évaluation
- Devoir de Synthese: FerchiouDocument4 pagesDevoir de Synthese: Ferchioufethi10% (1)
- Devoir 5 SM Biof Arsalan PDFDocument3 pagesDevoir 5 SM Biof Arsalan PDFMed BriniPas encore d'évaluation
- Série D'exercices - Physique - Dipole RLC Libre - Bac Mathématiques (2016-2017) MR Afdal AliDocument9 pagesSérie D'exercices - Physique - Dipole RLC Libre - Bac Mathématiques (2016-2017) MR Afdal AliChili 1111100% (1)
- Examen Blanc SM Inter2222 PDFDocument8 pagesExamen Blanc SM Inter2222 PDFMouad Chaker100% (1)
- إلامتحانات التجريبية 2023Document40 pagesإلامتحانات التجريبية 2023AYEX EDIT0% (1)
- Simili 2020-Converti PDFDocument7 pagesSimili 2020-Converti PDFyasmine mahmoud100% (1)
- Examen Blanc 2BIOFDocument8 pagesExamen Blanc 2BIOFAhmed El AtriPas encore d'évaluation
- Les Exams Nationaux PC 2008-2019Document164 pagesLes Exams Nationaux PC 2008-2019바드 에딘Pas encore d'évaluation
- Phy 5 PDFDocument8 pagesPhy 5 PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Series RL 20 Pages AdrarDocument20 pagesSeries RL 20 Pages AdrarFethi JerbiPas encore d'évaluation
- Chute Libre Verticale D Un Solide Exercices Non Corriges 2 1Document4 pagesChute Libre Verticale D Un Solide Exercices Non Corriges 2 1Ahid ImadPas encore d'évaluation
- Série Ec - RFD PlateformeDocument2 pagesSérie Ec - RFD PlateformeBakari AnisPas encore d'évaluation
- Série Dexercices Corrigés 2Document15 pagesSérie Dexercices Corrigés 2loic100% (1)
- Devoir PC 2bac SP International FR s1 4Document2 pagesDevoir PC 2bac SP International FR s1 4Rim KdPas encore d'évaluation
- Problème Corrigé - Lancement D'un ProjectileDocument6 pagesProblème Corrigé - Lancement D'un Projectilegzqg9cp7mt0% (1)
- Biof Exercices de Rotation 11-04-2020Document6 pagesBiof Exercices de Rotation 11-04-2020opoyui097Pas encore d'évaluation
- Devoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2016-2017) MR Abdmouleh NabilDocument6 pagesDevoir de Contrôle N°1 - Sciences Physiques - Bac Sciences Exp (2016-2017) MR Abdmouleh NabilAla AbidiPas encore d'évaluation
- Devoir Controle 1 - Physique - Lycée Pilote SfaxDocument3 pagesDevoir Controle 1 - Physique - Lycée Pilote SfaxMouhieddine Khaili100% (2)
- Dc3 Sadiki 2014 MathsDocument3 pagesDc3 Sadiki 2014 Mathslemia100% (1)
- Bac Blanc 2019Document6 pagesBac Blanc 2019khalid el yacoubi100% (1)
- Controle 3 2bac SMDocument2 pagesControle 3 2bac SMnouhayla100% (1)
- Durée Estimée: Date:: Univup Ma 2h00min 31 12 021Document7 pagesDurée Estimée: Date:: Univup Ma 2h00min 31 12 021Khaouda DrissPas encore d'évaluation
- Exam 3 SMDocument4 pagesExam 3 SMKhaouda Driss100% (1)
- DS1 (11 12 09)Document8 pagesDS1 (11 12 09)Seif Souid100% (5)
- Examen Blanc Spc2022 IcheDocument7 pagesExamen Blanc Spc2022 Ichesine abdellahPas encore d'évaluation
- Devoir de Synthèse N°1 Lycée Pilote - Physique - Bac Math (2008-2009) Elève MarwaDocument5 pagesDevoir de Synthèse N°1 Lycée Pilote - Physique - Bac Math (2008-2009) Elève Marwachaari abdelouahad67% (3)
- TD Dynamique Isf 2021Document5 pagesTD Dynamique Isf 2021mohamedPas encore d'évaluation
- Dev 03Document5 pagesDev 03Mohamed El OuahdaniPas encore d'évaluation
- Exercice 30 Suivi Temporel D'une Transformation ChimiqueDocument5 pagesExercice 30 Suivi Temporel D'une Transformation ChimiqueMoulayMoulyPas encore d'évaluation
- Devoir de Synthese: Un Système Chimique Est À L'équilibre Lorsque Les Grandeurs Qui Le DécriventDocument4 pagesDevoir de Synthese: Un Système Chimique Est À L'équilibre Lorsque Les Grandeurs Qui Le Décriventfethi1100% (3)
- SeÌ Rie 1 - Dosage Acido-BasiqueDocument2 pagesSeÌ Rie 1 - Dosage Acido-Basiqueb01554837Pas encore d'évaluation
- Série 1 - Dosage Acido-BasiqueDocument2 pagesSérie 1 - Dosage Acido-BasiqueAzdine MC100% (1)
- Revision Chimie Acide Base BoussettaDocument14 pagesRevision Chimie Acide Base BoussettaBoussetta Zouhaier100% (1)
- AvancementDocument2 pagesAvancementBoussetta Zouhaier0% (1)
- Série 1ère Année Les MélangesDocument1 pageSérie 1ère Année Les MélangesBoussetta Zouhaier100% (1)
- Serie 1 Le Dipole RCDocument13 pagesSerie 1 Le Dipole RCBoussetta Zouhaier100% (1)
- 1 RCDocument3 pages1 RCBoussetta ZouhaierPas encore d'évaluation
- Cours Dosage Acide BaseDocument9 pagesCours Dosage Acide BaseBoussetta Zouhaier100% (1)
- Dosage Acide Faible Base Forte IMPDocument2 pagesDosage Acide Faible Base Forte IMPBoussetta ZouhaierPas encore d'évaluation
- Détermination de L'inductance D'une BobineDocument2 pagesDétermination de L'inductance D'une BobineBoussetta Zouhaier100% (2)
- 1 RCDocument3 pages1 RCBoussetta Zouhaier100% (2)
- DSN2-1ere 2021.Document3 pagesDSN2-1ere 2021.Boussetta ZouhaierPas encore d'évaluation
- Preparation D Une Solution TitréeDocument2 pagesPreparation D Une Solution TitréeBoussetta Zouhaier50% (2)
- BOUSTAKAT Avec ExercicesDocument9 pagesBOUSTAKAT Avec ExercicesBoussetta ZouhaierPas encore d'évaluation
- Cours Dosage Acide Base 3Document8 pagesCours Dosage Acide Base 3Boussetta ZouhaierPas encore d'évaluation
- Série Principe D'inertieDocument1 pageSérie Principe D'inertieBoussetta ZouhaierPas encore d'évaluation
- DCN2-1ere 2021f-ConvertiDocument2 pagesDCN2-1ere 2021f-ConvertiBoussetta ZouhaierPas encore d'évaluation
- DCN2-1ere 2021fDocument3 pagesDCN2-1ere 2021fBoussetta ZouhaierPas encore d'évaluation
- Série Les Actions MécaniquesDocument3 pagesSérie Les Actions MécaniquesBoussetta ZouhaierPas encore d'évaluation
- Volume Des CorpsDocument3 pagesVolume Des CorpsBoussetta ZouhaierPas encore d'évaluation
- Devoir 1 Modele 3 Physique Chimie 1ac Semestre 1Document2 pagesDevoir 1 Modele 3 Physique Chimie 1ac Semestre 1Boussetta Zouhaier100% (2)
- Grille Vaporisation Par ÉbullitionDocument2 pagesGrille Vaporisation Par ÉbullitionBoussetta ZouhaierPas encore d'évaluation
- Reaction Acide Base Bac SDocument3 pagesReaction Acide Base Bac SBoussetta ZouhaierPas encore d'évaluation
- DCN2 1ereDocument3 pagesDCN2 1ereBoussetta ZouhaierPas encore d'évaluation
- Loi Coulomb PDFDocument3 pagesLoi Coulomb PDFBoussetta ZouhaierPas encore d'évaluation
- 2 RCDocument2 pages2 RCBoussetta ZouhaierPas encore d'évaluation
- Interaction ÉlectriqueDocument4 pagesInteraction ÉlectriqueBoussetta ZouhaierPas encore d'évaluation
- Ta Tac TPDocument4 pagesTa Tac TPAya ZeggariPas encore d'évaluation
- Procede PliageDocument13 pagesProcede PliagemounirPas encore d'évaluation
- Métaux en OrthopédieDocument4 pagesMétaux en OrthopédieAbdelghani ZenataPas encore d'évaluation
- 1 10-Photosynthese PDFDocument66 pages1 10-Photosynthese PDFFitahianaPas encore d'évaluation
- A1755 PDFDocument17 pagesA1755 PDFbertrand_0123456789Pas encore d'évaluation
- Cours l3 Tiaacqa Alteration Des Aliments Partie 1Document41 pagesCours l3 Tiaacqa Alteration Des Aliments Partie 1benzineb younesPas encore d'évaluation
- 04-Potentiel de Repos NDocument29 pages04-Potentiel de Repos NBook HunterPas encore d'évaluation
- Poly QCM SupplementairesDocument266 pagesPoly QCM SupplementairesMedoumar Alagude100% (2)
- Fiche TD 1 GPL3Document5 pagesFiche TD 1 GPL3serinebousehababenkPas encore d'évaluation
- Equilibres Chimiques, Énoncés Des ExercicesDocument36 pagesEquilibres Chimiques, Énoncés Des ExercicesAbdou WahidPas encore d'évaluation
- PFE Master Bakhat & BenelhadjDocument48 pagesPFE Master Bakhat & Benelhadjاحمد سالمPas encore d'évaluation
- 4 5922519954246075353 PDFDocument9 pages4 5922519954246075353 PDFIkeoPas encore d'évaluation
- Tout Le Cours - Thermodynamique PCSI MPSI PTSIDocument157 pagesTout Le Cours - Thermodynamique PCSI MPSI PTSISamt89% (9)
- Annexe 27 Effets DominoDocument9 pagesAnnexe 27 Effets DominoFiras BEN HMIDAPas encore d'évaluation
- TP. AlkylationDocument2 pagesTP. Alkylationabdo my100% (1)
- Présentation Soudage Par Faisceau D'électronsDocument21 pagesPrésentation Soudage Par Faisceau D'électronsMadani MecheriPas encore d'évaluation
- Presentation Projet Fin D'etudeDocument35 pagesPresentation Projet Fin D'etudefoufoua100% (2)
- Cours 2 Capteurs - Solaires ThermiquesDocument76 pagesCours 2 Capteurs - Solaires ThermiquesAbabacar ThiamPas encore d'évaluation
- COURS POLLUTION L3 SECTION E 2019-2020 Mme BALAMANEDocument8 pagesCOURS POLLUTION L3 SECTION E 2019-2020 Mme BALAMANEHalima ZaghbibPas encore d'évaluation
- H+ Et Salicyles2: Solutions Sur MesureDocument1 pageH+ Et Salicyles2: Solutions Sur Mesuresidi ahmedPas encore d'évaluation
- DO504832C CL Spec d703Document11 pagesDO504832C CL Spec d703Javier MoisésPas encore d'évaluation
- Deuxième Memoire Sur Une Nouvelle Action de La LumièreDocument1 pageDeuxième Memoire Sur Une Nouvelle Action de La LumièreSebouPas encore d'évaluation
- 17 SpectreDocument8 pages17 SpectrelemiaPas encore d'évaluation
- Chimie 24Document4 pagesChimie 24loic ngounouPas encore d'évaluation
- Yokogawa Présente Le Capteur Numérique À Distance EJXC40ADocument3 pagesYokogawa Présente Le Capteur Numérique À Distance EJXC40AArmand Muteb AmkPas encore d'évaluation
- Cours SDM Chap IIIDocument9 pagesCours SDM Chap IIIbourabahPas encore d'évaluation
- LaitierDocument7 pagesLaitierGhaithPas encore d'évaluation
- Les Matériaux Biosourcés - P - Fortin - Extrait SLDocument41 pagesLes Matériaux Biosourcés - P - Fortin - Extrait SLDavid OuadfelPas encore d'évaluation
- Fiches de Traitement D'essaisDocument2 pagesFiches de Traitement D'essaisbayo adefemiPas encore d'évaluation
- 06 Flexion Des Poutres DroitesDocument34 pages06 Flexion Des Poutres DroitesMed Amine Amri100% (1)