Académique Documents
Professionnel Documents
Culture Documents
Ester Bac Serie 1 202324 1 - 231116 - 153830
Transféré par
deissemmhidhi3Titre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Ester Bac Serie 1 202324 1 - 231116 - 153830
Transféré par
deissemmhidhi3Droits d'auteur :
Formats disponibles
Prof : Harzalli.
M
Niveau : 4ème math,sc.exp Equilibre chimique : estérification hydrolyse
Année scolaire :2023/2024
Exercice 1:
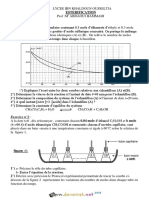
A la date t0 = 0s, on introduit n1 = 0,38mol d’acide propanoïque, n2 = 0,3mol d’éthanol et quelques gouttes
d’acide sulfurique. On homogénéise le mélange que l’on maintient durant toute l’expérience à une température
constante T = 80°C.
1) a) Ecrire, en formules semi – développées, l’équation de la réaction.
b) Donner le nom de l’ester formé.
2) Déterminer le volume d’éthanol pur utilisé pour préparer le mélange initial sachant que
ρéthanol = 0,79g.cm-3 et Méthanol = 46g.mol-1.
3) a) Dresser le tableau d’avancement de la réaction.
b) Calculer l’avancement maximal xmax.
4) A partir de l’instant t = 80min, le système chimique atteint un état remarquable, tel que la composition du
mélange reste constante.
a) Qu’appelle – t – on cet état ?
b) Sachant qu’à cet état le nombre de mole d’acide est double de celui de l’alcool, calculer l’avancement
final xf de la réaction.
c) En déduire le taux d’avancement final. Conclure.
d) Déterminer la composition du système lorsqu’il atteint cet état.
Exercice 2:
Au laboratoire et dans un erlenmeyer, on introduit, n0 moℓ d'éthanol (C2H5OH) et un volume, VA = 14,3 mL,
d'acide éthanoïque (CH3CO2H), afin d'obtenir un mélange équimolaire d'acide et d'alcool.
On ajoute avec précaution 1 mL d'acide sulfurique concentré. On adapte un tube réfrigèrent sur l'erlenmeyer et on
chauffe à la température de θ1 = 60°C.La réaction étudiée a pour équation chimique:
CH3CO2H + C2H5OH ⇄ CH3CO2C2H5 + H2O
➊ - a - Préciser deux caractères principales de cette réaction.
- b - Pourquoi chauffe-t-on le mélange acide éthanoïque éthanol ?
- c - Quel est l'intérêt du tube réfrigèrent ?
➋ - a - Exprimer la constante d'équilibre, K, associée à cette synthèse en fonction du taux d'avancement final τF
(rendement) de la réaction.
- b - Sachant que K = 4, montrer que τF = 2 .
3
➌ A l'équilibre chimique, on ajoute au contenu de l'erlenmeyer de l'eau glacée, puis on dose la quantité d'acide
restante par une solution aqueuse de soude de concentration molaire C = 2,5 moℓ.L‒1. Le volume de la solution de
soude nécessaire à l'équivalence est VE = 33,3 mL.
- a - Calculer la quantité de matière initiale, n0, de l'acide éthanoïque.
- b - Déduire la valeur de la masse volumique, ρAc, de l'acide éthanoïque.
➍ Dans les mêmes conditions, on mélange n0(Ac) = 0,25 moℓ du même acide et n0(Aℓ) = 0,5 moℓ d'éthanol puis
on chauffe à la température de θ2 = 80°C.
- a - Dire en le justifiant si, K augmente, diminue ou reste égale à 4.
- b - Calculer le taux d'avancement final, τ’F, de la réaction précédente et le comparer à τF.
Exercice 3:
Pour réaliser la réaction d’hydrolyse de l’éthanoate de méthyle CH3COOCH3, on mélange initialement 1,5mol de
cet ester avec 1mol d’eau.
1) Ecrire l’équation de la réaction d’hydrolyse de cet ester.
2) Dresser le tableau descriptif d’évolution de la réaction et calculer la valeur de l’avancement maximale x m.
𝑽𝒎é𝒍𝒂𝒏𝒈𝒆
3) Lorsque l’équilibre est atteint, on prélève V p = 𝟐𝟎
et on dose l’acide formé par une solution de soude
de concentration Cb=2mol.L .Le volume de soude ajouté à l’équivalence est Vb=10,1 ml.
-1
a-Calculer le taux d’avancement final τFde la réaction d’hydrolyse.
b-Exprimer la constante d’équilibre K en fonction de τF.Calculer sa valeur.
4) On mélange maintenant, à t= 0s, 1mol de cet ester, 1mol d’eau, 1mol d’acide et1mol d’alcool.
a-Préciser le sens d’évolution spontanée du système chimique.
b-Trouver la nouvelle valeur de l’avancement final x f.
Exercice 4:
On réalise l’hydrolyse du l’éthanoate de méthyle. L’équation de la réaction chimique qui modélise cette
Estérification Hydrolyse 2023/2024 H.M Page 1 sur 4
transformation chimique est : CH3COOCH3 + H2O ⇄ CH3COOH + CH3OH
5) Préciser les caractères de cette transformation chimique.
6) On mélange, à une température 1 maintenue constante, 0,2 mol d’éthanoate de méthyle avec 0,5 mol
d’eau. Lorsque l’état final est atteint, il se forme 0,1 mol d’acide éthanoïque.
a- Dresser le tableau descriptif de l’évolution de la transformation chimique au cours du temps.
b- Justifier que la réaction étudiée est limitée.
c- A l’état final, pourquoi dit-on que le système chimique est en équilibre dynamique ?
d- - Etablir l’expression de la constante d’équilibre K de la réaction en fonction de l’avancement final xf . En
déduire que K = 0,25.
7) On élève la température du mélange réactionnel à une valeur 2>1.
a- La composition du mélange à l’équilibre varie-t-elle ? Justifier la réponse.
b- Pour le même mélange initial, comparer les durées t1 et t2 nécessaires pour atteindre l’état final
respectivement aux températures 1 et 2 ? Justifier la réponse.
8) A la date t = 0 s, on mélange 2,5.10–1 mol d’éthanoate de méthyle, 10–1 mol d’eau, 10–1 mol d’acide
éthanoïque et 1,5. 10–1 mol de méthanol. A une date t, on dose l’acide restant dans le mélange par une
solution de soude dont la concentration molaire est Cb=2 mol.L–1. On trouve que le nombre de mole
d’acide restant est égal à 8.10 –2 mol.
a- Montrer qu’à t = 0, le système chimique n’est pas en équilibre et que c’est la réaction d’estérification
qui a lieu spontanément.
b- Calculer le volume Vb de soude nécessaire pour le dosage de l’acide restant à la date t .
c- A la date t, le système chimique est-il en équilibre ? Sinon, quelle serait le volume V d’eau pure qu’on
devrait ajouter ou retirer brusquement à cette date pour atteindre l’équilibre.
On donne : 𝜌eau = 1 g.cm-3 et Meau = 18g.mol-1.
Exercice 5:
On réalise une réaction d’estérification en mélangeant initialement n0= 0,06 mol d'acide éthanoïque CH3-COOH
et n0 = 0,06 mol d’éthanol CH3-CH2-OH (le mélange réactionnel est dans les proportions stœchiométriques). Le
mélange réactionnel est acidifié et maintenu chauffé à température constante.
La courbe 1 du graphe ci-contre donne l’évolution de la quantité de matière de
l’acide éthanoïque restant dans le mélange réactionnel au cours du temps.
1) a - Ecrire l’équation de la réaction chimique qui modélise
la transformation étudiée.
b - Préciser les propriétés de la transformation chimique
mis en évidence d’après la courbe 1.
2) a - En exploitant la courbe 1, déduire l’avancement final xf de la réaction.
Vérifier alors que le taux d’avancement final de la réaction est f 2/3 .
b - Montrer que la constante d’équilibre relative à la réaction étudiée
𝟐
𝝉𝒇
s’exprime par : 𝒌 = (𝟏−𝝉 ) , calculer k.
𝒇
3) On refait l’expérience, dans les mêmes conditions opératoires, mais en mélangeant initialement n0 = 0,06 mol
d'acide éthanoïque et n’0 mol d’éthanol avec n’0> n0. On obtient alors la courbe 2 du graphe ci-dessus.
a - Quelle est la nouvelle valeur x’f de l’avancement final de la réaction. En déduire alors la nouvelle
valeur ’f du taux d’avancement final de la réaction.
b - Etablir l’expression de la constante d’équilibre K en fonction de x’f ,n0 et n’0 .
c - Calculer alors la valeur de n’0 .
4) Quelle conclusion peut-on tirer à partir de ces deux expériences ?
Exercice 6:
On donne les masses molaires atomiques en g.mol-1 : H=1 , C=12 et O=16 .
On réalise un mélange initial qui renferme mac = 9,2g d’acide méthanoïque HCOOH et mal=12g de
propan-2-ol C3H7OH avec quelques gouttes d’acide sulfurique.
1) a- Ecrire , en formules semi-développées , l’équation de la réaction qui se produit .
b- Montrer que le mélange initial est équimolaire.
2) On répartit ce mélange dans des tubes à essais muni chacun d’un tube capillaire. Chaque tube contient un
volume V du mélange renfermant initialement n0 mol d’acide méthanoïque et n0 mol de propan-2-ol . Ces
tubes sont placés à la date t0=0 dans un bain-marie maintenu à 80°C .
A différentes dates , on dose la quantité d’acide restant dans chaque tube par une solution de soude NaOH de
concentration molaire Cb= 0,5 mol.L-1 .
A l’équivalence acide-base , le volume de la solution de soude ajouté est noté Vb .
a- Quel est le rôle du tube capillaire utilisé ?
Estérification Hydrolyse 2023/2024 H.M Page 2 sur 4
b- Dire comment peut-on détecter l’état d’équivalence acide-base.
c- Dresser le tableau descriptif d’évolution du système chimique dans chaque tube.
d- Exprimer l’avancement x de la réaction, dans chaque tube, en fonction de Cb , Vb et n0 (On négligera la
présence de l’acide sulfurique ) .
𝐱
3) La courbe ci-contre représente la variation du taux d'avancement 𝛕 = 𝐱
𝐦𝐚𝐱
de la réaction en fonction du volume Vb de la solution de soude ajouté pour doser
la quantité d’acide restant dans chaque tube .
Le volume nécessaire au dosage , à l’équilibre
dynamique , est Vb,éq = 16mL .
a- Montrer que le taux d’avancement de la réaction
𝐂 𝐕
à une date t s’écrit : 𝛕 = 1 - 𝐧𝐛 𝐛 .
𝟎
b- Déduire de la courbe que n0 = 0,02mol .
c- Quel caractère de la réaction nous indique la courbe ? Justifier.
4) a- Enoncer la loi d’action de masse.
b- Déterminer la composition du mélange lorsque l’état d’équilibre dynamique est atteint.
c- Calculer la constante d’équilibre K de la réaction .
5) L’équilibre dynamique est atteint au bout de ∆𝐭 = 50 min .
a- Déduire un deuxième caractère de cette réaction.
b- Calculer, en mol.s-1 , la vitesse moyenne de la réaction entre t0 = 0 et la date de l’équilibre .
6) A l’équilibre, on ajoute dans l’un des tubes non dosé par la soude : 10-2 mol de propan-2-ol et 3,5.10-2 mol
d’ester ayant la même formule semi-développée que l’ester formé.
a- Préciser, en le justifiant, comment varie le volume Vb,éq ajouté si on réalise le dosage par la même solution
de soude lorsque le nouvel état d’équilibre est atteint .
b- Lorsque l’équilibre chimique est atteint de nouveau , montrer que l’avancement final xf de la réaction
étudiée depuis la date t0=0 , vérifie l’équation suivante :1,25xf2 – 14,75.10-2 xf + 13,5.10-4 = 0
Calculer xf et déduire le volume Vb,éq ajouté à l’équivalence , dans ce nouvel état d’équilibre .
Exercice 7:
A l’instant t=0 min et à une température constante T 1, on mélange n1 mole d’acide carboxylique (A) de formule
CnH2nO2 et de masse molaire 74 g.mol-1 , n2 mole d’un alcool (B) de formule CmH2m+2O et de masse molaire
32 g.mol-1 et quelques gouttes d’acide sulfurique. On donne MC=12 g.mol-1 , MH= 1 g.mol-1 et MO=16 g.mol-1
1) Déterminer puis écrire le nom et la formule semi-développée de l’acide et de l’alcool.
2) Pourquoi a-t-on ajouté quelques gouttes d’acide sulfurique ?
3) Ecrire l’équation de la réaction d’estérification en utilisant les formules semi-développées.
Donner le nom d’ester (E) formé.
4) Dresser le tableau descriptif d’évolution du système.
5) Une étude expérimentale permet de tracer la courbe d’évolution de la quantité de matière de (A)
au cours du temps et celle de variation de la quantité de matière de l’ester (E) au cours du temps.
a- Indiquer brièvement la méthode expérimentale utilisée pour déterminer le nombre de mole de
(A) présent dans le mélange à un instant de date t quelconque.
b- Sachant que n1=2n2 , déterminer :
n1 et n2 et la composition finale du système chimique.
c- Enoncer la loi d’action de masse. Calculer la valeur de
la constante d’équilibre K.
d- Représenter, en le justifiant, sur le même graphe
e- l’allure des courbes de n(A) et de n(E) en fonction du temps
f- si la réaction est reproduite à une température T 2>T1.
6) On considère maintenant le système chimique formé par par
7) n’1 mol d’acide propanoïque et n’2 mol de méthanol tel que n’2=4n’1.
a- Dresser le tableau descriptif d’évolution du système.
b- Etablir l’expression de la constante d’équilibre K en fonction de n’1 ; n’2 et xf puis en fonction du
taux d’avancement final de la réaction f.Calculer f.
c-Pour déterminer la quantité de matière d’acide restant à l’équilibre dynamique, on dose le mélange
par une solution de soude de concentration molaire Cb=0,1 mol.L-1, le volume de base versé à
l’équivalence est VBE=7,1 mL. Déterminer la composition initiale et la composition finale du
système chimique.
Estérification Hydrolyse 2023/2024 H.M Page 3 sur 4
Exercice 8:bac Math 2019 session principale :
Estérification Hydrolyse 2023/2024 H.M Page 4 sur 4
Vous aimerez peut-être aussi
- Serie4 (Ben Amor)Document1 pageSerie4 (Ben Amor)Malek BerrguebPas encore d'évaluation
- 7 EsterificationDocument2 pages7 EsterificationsendibedPas encore d'évaluation
- Série D'exercices - Chimie Série Loi de Modération Et Loi D'action de Masse - Bac Math (2013-2014) MR Afdal AliDocument6 pagesSérie D'exercices - Chimie Série Loi de Modération Et Loi D'action de Masse - Bac Math (2013-2014) MR Afdal AliOussémaM'solli0% (1)
- Série N°4 Chimie Esterification 2013 2014 (Barhoumi Ezzedine)Document4 pagesSérie N°4 Chimie Esterification 2013 2014 (Barhoumi Ezzedine)Rams SoloPas encore d'évaluation
- EstérificationDocument2 pagesEstérificationIlyes Ben Jemaa0% (1)
- Exercices PC 2bac Science International FR 22 4Document4 pagesExercices PC 2bac Science International FR 22 4Sara MountaPas encore d'évaluation
- 16 REVISION CHIMIE (1er TRIMESTRE)Document4 pages16 REVISION CHIMIE (1er TRIMESTRE)Ilyes Ben Jemaa0% (1)
- Révision Equilibre ChimiqueDocument6 pagesRévision Equilibre ChimiquechadaPas encore d'évaluation
- 10-11 Ester +evolutionDocument11 pages10-11 Ester +evolutionEnidroun OutPas encore d'évaluation
- Série de Chimie - 4ème Année Sc. Exp - Technique & MathématiquesDocument3 pagesSérie de Chimie - 4ème Année Sc. Exp - Technique & MathématiquesأشرفالمبروكPas encore d'évaluation
- Magazine 17 Esterification PDFDocument5 pagesMagazine 17 Esterification PDFamal mansour0% (1)
- Exercices 3 Estérification Et Hydrolyse Des EstersDocument1 pageExercices 3 Estérification Et Hydrolyse Des EstersRedouane ElalamiPas encore d'évaluation
- Série Est-Hyd-Loi D'action de MasseDocument3 pagesSérie Est-Hyd-Loi D'action de Masseأسماء النخليPas encore d'évaluation
- 2003 Pondichery Sujet Exo1 Esterification 6ptsDocument3 pages2003 Pondichery Sujet Exo1 Esterification 6ptsDaniela DinicaPas encore d'évaluation
- Exercices PC 2bac Science International FR 22 2Document5 pagesExercices PC 2bac Science International FR 22 2HAMADA1972Pas encore d'évaluation
- Série D'exercices - Sciences Physiques Préparation Bac 2011 - Bac Mathématiques (2010-2011) MR BenaichDocument21 pagesSérie D'exercices - Sciences Physiques Préparation Bac 2011 - Bac Mathématiques (2010-2011) MR BenaichTawfiq Weld EL ArbiPas encore d'évaluation
- Série 4 Esrérification 2021Document6 pagesSérie 4 Esrérification 2021safouen mejbriPas encore d'évaluation
- Exercices 1 Estérification Et Hydrolyse Des EstersDocument1 pageExercices 1 Estérification Et Hydrolyse Des EstersRedouane ElalamiPas encore d'évaluation
- TD Equilibre Chimique 2016Document4 pagesTD Equilibre Chimique 2016Oumar TraoréPas encore d'évaluation
- Série 1 - équilibre Chimique (WWW - Pc1.ma)Document6 pagesSérie 1 - équilibre Chimique (WWW - Pc1.ma)b01554837Pas encore d'évaluation
- Série D'exercices N°2 - Chimie - Esterification - Hydrolyse - Bac Sciences Exp (2015-2016) MR Daghsni SahbiDocument4 pagesSérie D'exercices N°2 - Chimie - Esterification - Hydrolyse - Bac Sciences Exp (2015-2016) MR Daghsni SahbiAmine AlaoUii AlaouiPas encore d'évaluation
- EquilibreQoutionReactionExercices 16-17 PDFDocument4 pagesEquilibreQoutionReactionExercices 16-17 PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- TR ACIDOBASIQUES PCDocument11 pagesTR ACIDOBASIQUES PCalaeddinePas encore d'évaluation
- Série D'exercices - Sciences Physiques - Equilibre Chimique - Bac Technique (2017-2018) MR Gammoudi SoufienDocument2 pagesSérie D'exercices - Sciences Physiques - Equilibre Chimique - Bac Technique (2017-2018) MR Gammoudi SoufienInass LayachPas encore d'évaluation
- Serie 2 Les Transformations S'effectuants en Deux Sens Etat D'equilibre (2) - 1Document4 pagesSerie 2 Les Transformations S'effectuants en Deux Sens Etat D'equilibre (2) - 1yunuabou3Pas encore d'évaluation
- Chimie PDFDocument6 pagesChimie PDFleilaPas encore d'évaluation
- Bestcours NS 28FDocument8 pagesBestcours NS 28Frobi jungkookPas encore d'évaluation
- Série 1 - Équilibre ChimiqueDocument6 pagesSérie 1 - Équilibre ChimiqueMed RT100% (1)
- Envoi Mail Exercice Ts Estrification-HydrolyseDocument5 pagesEnvoi Mail Exercice Ts Estrification-HydrolyseSteve CohenPas encore d'évaluation
- Bac Math Pysh Acide Base Serie 4Document1 pageBac Math Pysh Acide Base Serie 4Nourhene Jlassi33% (3)
- Exercices 1 Estérification Et Hydrolyse Des EstersDocument1 pageExercices 1 Estérification Et Hydrolyse Des EstersRedouane ElalamiPas encore d'évaluation
- Cours - Chimie ESTERIFICATION - Bac Sciences Exp (2011-2012) MR TLILI TOUHAMIDocument2 pagesCours - Chimie ESTERIFICATION - Bac Sciences Exp (2011-2012) MR TLILI TOUHAMIMohamed HamdenePas encore d'évaluation
- Série D'exercices N°7 - Chimie Série Physique Dipole RLC SCIENCE & MATH - Bac Sciences Exp (2011-2012) MR TLILI TOUHAMI PDFDocument2 pagesSérie D'exercices N°7 - Chimie Série Physique Dipole RLC SCIENCE & MATH - Bac Sciences Exp (2011-2012) MR TLILI TOUHAMI PDFAzizElheni100% (1)
- Serie Ester 2023Document6 pagesSerie Ester 2023dhouabenrhoumaPas encore d'évaluation
- Les transf chimiq s’effectuant ds les deux sens - Série 2 - Soutien à distance - Prof OTHMANEDocument11 pagesLes transf chimiq s’effectuant ds les deux sens - Série 2 - Soutien à distance - Prof OTHMANEAyoub LatifPas encore d'évaluation
- Tdtsen 15 (Physique-Chimie) : Academie D'Enseignement de San Lycee Public de SanDocument5 pagesTdtsen 15 (Physique-Chimie) : Academie D'Enseignement de San Lycee Public de SanAlassane TraorePas encore d'évaluation
- Acides Et Bases PcDocument15 pagesAcides Et Bases Pcrkibi.khadija2006Pas encore d'évaluation
- Série Loi Daction de MasseDocument2 pagesSérie Loi Daction de MasseimedPas encore d'évaluation
- Série Loi Daction de MasseDocument2 pagesSérie Loi Daction de Masseimed100% (1)
- Exercices 2Transformations Liées à Des Réactions Acido – Basiques Dans Une Solution AqueuseDocument1 pageExercices 2Transformations Liées à Des Réactions Acido – Basiques Dans Une Solution Aqueuselabiadsihame73Pas encore d'évaluation
- 2008 AmNord Exo1 Sujet ReactionsTotalesDocument2 pages2008 AmNord Exo1 Sujet ReactionsTotalesla physique selon le programme Français100% (1)
- Série N°2 Chimie Equilibre Chimique Technique 2011 2012 (Alibi Anouar)Document4 pagesSérie N°2 Chimie Equilibre Chimique Technique 2011 2012 (Alibi Anouar)Hiba JendoubiPas encore d'évaluation
- Série N°8Document2 pagesSérie N°8Jihad ELPas encore d'évaluation
- Série D'exercices 4, État D'équilibre D'un Système Chimique, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHID - Unlocked PDFDocument6 pagesSérie D'exercices 4, État D'équilibre D'un Système Chimique, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHID - Unlocked PDFkhaled nawiPas encore d'évaluation
- Examens de Chimie-1Document17 pagesExamens de Chimie-1Anas HajimPas encore d'évaluation
- Exercice 4 Réactions Destérification Et Dhydrolyse LAHLALI PDFDocument5 pagesExercice 4 Réactions Destérification Et Dhydrolyse LAHLALI PDFBouba KhedherPas encore d'évaluation
- 2008 AmNord Exo1 Sujet ReactionsTotalesDocument2 pages2008 AmNord Exo1 Sujet ReactionsTotalesbaptlaser.fortnitePas encore d'évaluation
- Exerice Équilibre ChimiqueDocument2 pagesExerice Équilibre ChimiqueMouad HmiPas encore d'évaluation
- Équilbres ChimiquesDocument3 pagesÉquilbres Chimiquesbmm2Pas encore d'évaluation
- Devoir Synthèse-1 - 4 ScExp-2022Document6 pagesDevoir Synthèse-1 - 4 ScExp-2022Riadh BesbesPas encore d'évaluation
- Série 5 Transformations Associées À Des Réactions Acido-Basiques en Solution AqueuseDocument6 pagesSérie 5 Transformations Associées À Des Réactions Acido-Basiques en Solution AqueuseFATIMA fatiii100% (1)
- Exercice IDocument15 pagesExercice IInes De Paul Feudjeu100% (1)
- Acide BaseDocument19 pagesAcide Basehamzi0% (1)
- Equilibre ChimiqueDocument2 pagesEquilibre ChimiqueBoussetta ZouhaierPas encore d'évaluation
- Serie3 Reaction LimitéDocument1 pageSerie3 Reaction Limitéhurrem unsalezPas encore d'évaluation
- Série D'exercices 5, Transformations Associées À Des Réactions Acido-Basiques en Solution - Dosage, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHIDDocument12 pagesSérie D'exercices 5, Transformations Associées À Des Réactions Acido-Basiques en Solution - Dosage, 2BAC BIOF, SM, PC Et SVT, PR JENKAL RACHIDboudhar mohamed0% (1)
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- Équilibres en solution: Les Grands Articles d'UniversalisD'EverandÉquilibres en solution: Les Grands Articles d'UniversalisPas encore d'évaluation
- 5 TQPLASTIdentification Des Matiares PlastiquesDocument18 pages5 TQPLASTIdentification Des Matiares Plastiquesbrahim chalhoubPas encore d'évaluation
- Bfem PC de 2002 À 2020Document19 pagesBfem PC de 2002 À 2020Saphira Kouamé100% (2)
- مواضيع البكالوريا ل موريطانيا من 2002إلى 2012 PDFDocument177 pagesمواضيع البكالوريا ل موريطانيا من 2002إلى 2012 PDFالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Série 1: Exercice 1Document2 pagesSérie 1: Exercice 1roffaaPas encore d'évaluation
- Traité de Chimie, Appliquée Aux Arts (IA b29331717 0006)Document768 pagesTraité de Chimie, Appliquée Aux Arts (IA b29331717 0006)Orianne CourmesPas encore d'évaluation
- DS 1Document2 pagesDS 1valdx100% (1)
- 22 Guide Technique Risque Pour Les ReservoirsDocument17 pages22 Guide Technique Risque Pour Les Reservoirsvb_pol@yahooPas encore d'évaluation
- Chimie SolutionsDocument13 pagesChimie Solutionsfalilou loPas encore d'évaluation
- KSB Etachrom BCDocument22 pagesKSB Etachrom BCDrese ChahaizePas encore d'évaluation
- Hydrochimie Et Qualité Des Eaux TP Partie IDocument42 pagesHydrochimie Et Qualité Des Eaux TP Partie Ichenikherhadil3Pas encore d'évaluation
- Les Procédés Humides À La Soude Ou Au Carbonate de SoudeDocument4 pagesLes Procédés Humides À La Soude Ou Au Carbonate de SoudeChaimae BadourPas encore d'évaluation
- Nickelage Électrolytique. CaractéristiquesDocument9 pagesNickelage Électrolytique. CaractéristiquesBacem FarhatPas encore d'évaluation
- Polycopié de TP 1ére Année 2022Document16 pagesPolycopié de TP 1ére Année 2022fellahbillel60Pas encore d'évaluation
- Colmatage Par Matiere OrganiqueDocument2 pagesColmatage Par Matiere OrganiqueMeziane BouktitPas encore d'évaluation
- Gans NourritureDocument3 pagesGans NourritureNiki MorelliPas encore d'évaluation
- Cours 4 - Les Solutions Acides Et Les Solutions BasiquesDocument9 pagesCours 4 - Les Solutions Acides Et Les Solutions BasiquesrayangraphePas encore d'évaluation
- 07 - Titrage Colorimetrique DeboucheurDocument2 pages07 - Titrage Colorimetrique DeboucheurChartier JulienPas encore d'évaluation
- Chimie TleC, DDocument52 pagesChimie TleC, DDeffo100% (1)
- 2 Série Acide BaseDocument3 pages2 Série Acide BaseHayet Scphy100% (1)
- Cours - Chimie Solution Aqueuse de Base - 2ème Sciences (2014-2015) MR Mekni NejibDocument2 pagesCours - Chimie Solution Aqueuse de Base - 2ème Sciences (2014-2015) MR Mekni NejibMouhamed Ali SahbaniPas encore d'évaluation
- Composition PC Semestre 1 3eme 2019 2020Document1 pageComposition PC Semestre 1 3eme 2019 2020Elhadji GueyePas encore d'évaluation
- TP ViscosimetrieDocument10 pagesTP Viscosimetrieقصص حقيقية واقعيةPas encore d'évaluation
- Manuel Cultivez Votre Spiruline REVISION 2013Document226 pagesManuel Cultivez Votre Spiruline REVISION 2013Geoffrey VogelPas encore d'évaluation
- Dosage de La Vitamine CDocument10 pagesDosage de La Vitamine CalexisbradPas encore d'évaluation
- Série DosageDocument8 pagesSérie DosageAicha Daou100% (1)
- Serie D'exercices Les Grandeurs Physique Liées Ala Quantités de MatiereDocument2 pagesSerie D'exercices Les Grandeurs Physique Liées Ala Quantités de MatiereSaidi MohamedPas encore d'évaluation
- Devoir 3Document3 pagesDevoir 3Mofid PCPas encore d'évaluation
- FR PolyasimDocument5 pagesFR PolyasimtvbinterPas encore d'évaluation
- NFP98100Document12 pagesNFP98100Aurélia Le CalvezPas encore d'évaluation
- TP2 PDFDocument3 pagesTP2 PDFAz-eddine KaibaPas encore d'évaluation