Académique Documents
Professionnel Documents
Culture Documents
Cinetique Chimique Cours
Transféré par
Abdelhakim BailalCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Cinetique Chimique Cours
Transféré par
Abdelhakim BailalDroits d'auteur :
Formats disponibles
1
(PRE REQUIS DE PREMIERE)
Dfinition dune raction chimique
Une raction chimique est le rsultat de chocs efficaces et alatoires de molcules entre elles.
Lavancement dune raction est gal au nombre de moles de molcules nouvelles.
Le but est souvent de trouver les facteurs cintiques qui amliorent lavancement, en tenant
compte de la nature de la raction
Ractions doxydorduction
Une raction doxydorduction met en jeu un transfert dlectrons entre un oxydant et un rducteur.
Un oxydant est une entit chimique capable de gagner un ou plusieurs lectrons.
Un rducteur est une entit chimique capable de perdre un ou plusieurs lectrons
Une oxydation est une perte dlectrons
Une rduction est un gain dlectrons.
Au cours dune raction doxydorduction, un oxydant est rduit et un rducteur est oxyd.
Dans un QCM retenir une seule dfinition et en dduire les autres
2
La difficult est de savoir si un compos se comporte comme un oxydant ou comme un rducteur.
Suivant la raction doxydorduction envisage, un mme lment chimique peut jouer diffrents rles.
La rponse au niveau de terminale se situe obligatoirement dans lnonc du problme, ou dans la connaissance
des tables de potentiel redox (trs utile mais hors programme, voir la fin de ce cours)
Une raction d'oxydorduction implique un transfert d'lectrons. Une oxydation est une perte d'lectrons alors
qu'une rduction est un gain d'lectrons.
Un agent rducteur perd des lectrons, il sera donc oxyd. Un agent oxydant gagne des lectrons, il sera donc
rduit.
Dans la raction suivante :
6Fe
2+
+ Cr
2
O
7
2-
6Fe
3+
+ 2Cr
3+
Fe
2+
est oxyd en Fe
3+
car le fer perd un lectron. C'est l'inverse pour le chrome. Le nombre d'lectrons
changs est de 6 aprs avoir quilibr la raction.
On peut sparer cette raction en deux demi ractions, chacune d'elles impliquant un couple redox :
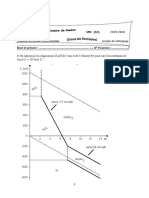
Pour savoir dans quel sens une raction redox a lieu spontanment, on peut utiliser la rgle du gamma
(cf. schma ci-dessus). Les valeurs permettant de faire ce schma proviennent du tableau en fin de cours.
On sait galement que spontanment, l'oxydant le plus fort oxyde le rducteur le plus fort, le couple de
rfrence tant H
+
/H
2
avec un potentiel standard Eo = 0V.
(Pour linstant il sagit dun moyen mnmotechnique)
Exemple de raction doxydorduction
) aq ( Fe (s) Cu ) s ( Fe ) aq ( Cu
2 2
On observe un changement de couleur et la perte en masse du mtal fer
Dans lexprience prcdente, un atome de fer perd deux lectrons : il est oxyd
e 2 ) aq ( Fe ) s ( Fe
2
Un ion cuivre II gagne deux lectrons : il est rduit
) (s Cu e 2 ) aq ( Cu
2
3
Le signe = traduit la possibilit de passer d'une forme l'autre selon les conditions.
Le nombre dlectrons perdus doit tre gal au nombre dlectrons gagns.
Vrifier toujours lgalit des charges entre produits et ractifs
Mthode pour crire lquation dune raction doxydorduction
Exemple de la raction entre lion permanganate et lion ferreux
Ecrire les couples en prsence et souligner les espces ractives
2
2 3
2
4
/
/
Mn M
F Fe
nO
e
Isoler une premire demi quation lectronique
(aq) Mn (aq) MnO
2
4
Assurer la conservation de l'lment oxygne avec des molcules d'eau
(l) O H 4 (aq) Mn (aq) MnO
2
2
4
Assurer la conservation de l'lment hydrogne avec des protons solvats en milieu acide
(l) O H 4 ) aq ( Mn (aq) H 8 (aq) MnO
2
2
4
Assurer la conservation de la charge avec des lectrons
(l) O H 4 ) aq ( Mn e 5 ) aq ( H 8 (aq) MnO
2
2
4
Refaire les tapes ci-dessus pour l'autre demi quation lectronique
e ) aq ( Fe ) aq ( Fe
3 2
Runir les deux demi quations lectroniques prcdentes avec le mme nombre dlectron donn et reus
En dduire l'quation bilan
2 3
( )x5 Fe Fe e
(l) O H 4 ) aq ( Mn e 5 ) aq ( H 8 ) aq ( MnO
2
2
4
(l) O H 4 ) aq ( Mn ) aq ( Fe 5 ) aq ( H 8 ) aq ( MnO ) aq ( Fe 5
2
2 3
4
2
4
CINETIQUE EN TERMINALE
Classification qualitative
Trois catgories de transformations chimiques :
Les transformations quasi instantanes
On dit que la raction est rapide. Sa dure est infrieure la seconde. On ne peut pas observer lvolution de la
raction lil. Cest le cas de certaines ractions de prcipitation. La formation du prcipit se fait
instantanment.
Les transformations lentes.
Une raction est lente si sa dure est de l'ordre de quelques secondes plusieurs minutes. On peut observer
l'volution de la raction.
Les transformations extrmement lentes ou infiniment lentes
Une raction est infiniment lente si sa dure est de l'ordre de plusieurs jours plusieurs semaines. On ne peut
pas observer lvolution de la raction lil.
Attention les considrations thermochimiques ne sont pas au programme de terminale mais il est
intressant de les avoir prsentes lesprit.
Ne pas confondre raction instantane et spontane
(Coup de grisou) O H CO O CH
2 2 2 4
Une raction spontane nest pas forcment instantane
Dans une quation chimique, on ne met une flche que lorsque la raction est totale (donc jamais en
terminale)
Raction instantane
5
Transformation rapide ou quasi instantane
Ractions de prcipitation souvent employes comme test didentification
L'quation de la formation de l'hydroxyde de Fer II est :
Fe
2+
+ 2OH
-
Fe(OH)
2
.
- L'quation de la formation de l'hydroxyde de Fer III est :
Fe
3+
+ 3OH
-
Fe(OH)
3
.
La couleur des deux solutions est la mme, bleue. Elle est due la prsence des ions Cu
2+
.
On ajoute chaque tube quelques gouttes dune solution concentre dhydroxyde de potassium. On constate la
formation dans chacun de deux tubes du mme prcipit qui est l'hydroxyde de Cuivre II de couleur bleue.
Les ions qui participent la formation de ce prcipit bleu sont les ions Cu
2+
et les ions OH
-
.
L'quation de formation de l'hydroxyde de Cuivre II est :
Cu
2+
+ 2OH
-
Cu(OH)
2
.
6
2
Transformation lente
Exemple de loxydation des ions iodure par leau oxygne
crire lquation de la raction chimique.
On mlange
2 2
O H et
I (
I K , )
O H I I O H H BILAN
e I I oxydation I I
O H e H O H rduction O H O H
2 2 2 2
2 2
2 2 2 2 2 2
2 2 2
2 2 /
2 2 2 /
Les
H sont apports par lacide
sulfurique
4 2
SO H
Lempois damidon sert de test
didentification de
2
I (bleu)
Equation bilan
(l) O 2H 2e ) aq ( 2H ) aq ( O H
2 2 2
2e ) aq ( I ) aq ( 2I
2
(l) O 2H ) aq ( I ) aq ( 2H ) aq ( 2I ) aq ( O H
2 2 2 2
On mesure la concentration en diiode dans le milieu ractionnel en fonction du temps :
Influence de la concentration sur lallure de la courbe
Les vitesses de la formation dun produit et de la disparition dun ractif diminuent quand la
concentration des ractifs diminue.
Rle de la temprature sur les coefficients de pente
0,00
1,00
2,00
3,00
4,00
0,00 5,00 10,00 15,00
t (min)
[ I
2
] en mol .L
-1
t
[ I
2
]
[I
2
]
2
[I
2
]
1
t
[ I
2
]
t
[ H
2
O
2
]
t
[ H
2
O
2
]
[H
2
O
2
]
1
[H
2
O
2
]
2
2 1
7
A concentration gale, les vitesses de la formation dun produit ou de la disparition dun ractif augmentent
avec la temprature.
Exemple de la dismutation du thiosulfate de soufre
crire lquation de la raction de dismutation
Raction du thiosulfate
O H SO S H O S BILAN
e H SO O H O S oxydation O S SO
O H S e H O S rduction S O S
2 2
2
3 2
2 2
2
3 2
2
3 2 2
2
2
3 2
2
3 2
2
4 2 2 /
3 2 4 6 /
Le thiosulfate est la fois rduit en souffre et
oxyd en dioxyde de souffre, on dit quil est
dismut
Comment acqurir les donnes numriques
1) Mthode chimique
Mthode destructive, peu commode pour les raisons suivantes:
a) Il faut titrer soit l'un des ractifs, soit l'un des produits pour dterminer x = f(t) avec le tableau d'volution.
b)L'tude est effectue en discontinu. Pour tre valable, tous les autres paramtres exprimentaux doivent
rester constants, ce qui est difficilement ralisable.
On effectue souvent une trempe sur le produit doser :
Lchantillon doser est dilu dans de leau glace pour stopper la raction. La trempe met en jeu
simultanment les facteurs cintiques concentration et temprature.
c) Il faut effectuer des prlvements dans le milieu ractionnel ou disposer de plusieurs chantillons.
Dans tous les cas, il faut travailler sur des quantits relativement importantes.
2) Mthodes physiques
1) Conductimtrie : Pour les milieux ractionnels contenant des ions subissant une transformation, la
mesure de la conductivit permet d'accder la concentration de ces ions.
.
2) PH-mtrie : Pour les milieux ractionnels contenant des ions oxonium H
3
O
+
subissant une
transformation, la mesure du pH donne accs la concentration de ces ions.
3) Mesure de volume ou de pression : lorsqu'un gaz est mis en jeu.
4) Spectrophotomtrie : Utilise lorsque l'une des espces mises en jeu est colore.
Ces mthodes physiques sont de plus en plus utilises pour les raisons suivantes :
Les mesures se font en continu, elles sont rapides, elles ncessitent de faibles quantits de matire.
Toutes ces mthodes sont mises en uvre dans des problmes de bac, dont la rsolution doit tre
assimile.
8
Cintique et avancement
Vous devez matriser la mise en forme des donnes sous la forme dun tableau davancement
Lavancement x est la quantit de matire de lun des produits.
Vitesse volumique de raction
1 dx
v
V dt
(V est le volume total de la solution exprim en litre)
Soit la raction
2 3 4 A B C D
T = 0 N
a
N
b
0 0
En cours N
a
-x N
b
2x 3x 4x
final N
a
-x
f
N
b
2x
f
3x
f
4x
f
n chantillo
q
2
3 2
2
V . 2
V ]. O S [
] I [
X
max
correspond au ractif limitant ( ne pas confondre avec X
f
qui correspond la
quantit de produit rellement obtenu)
Relation entre les vitesses des diffrents lments :
( ) ( 2 ) ( 3 ) ( 4 )
1 1 1
2 3 4
dx d A x d B x d C x d D x
v
dt dt dt dt dt
dy dA dB dC dD
v
dt dt dt dt dt
Attention
Le signe signifie quil sagit de la vitesse de disparition dun ractif
La valeur numrique doit toujours tre positive et suivie de lunit correcte
Elle est gale loppose du coefficient de pente de la tangente.
9
Lacide oxalique H
2
C
2
O
4
et l'ion permanganate MnO
4
-
Suivi par spectrophotomtrie.
Rglage du spectrophotomtre:
Afin d'effectuer les mesures de l'absorbance du milieu ractionnel, on doit rgler la longueur d'onde dela
lumire dans la gamme delongueursd'onde quela solution va absorber principalement (la complmentaire de
la coloration observe).
Dans la raction tudie seule l'ion permanganate est color. Pour choisir cette longueur d'onde on effectue le
spectred'absorption d'une solution dilue de permanganate de potassium.
10
Dans quelle gamme de longueur d'onde doit-on choisir la lumire produite par le spectrophotomtre ?
La solution de permanganate de potassium absorbe le vert( bande noire) . La gamme de longueur d'onde
absorbe est 500 - 560 nm.
Le spectrophotomtre doit tre rgl sur la longueur d'onde donnant le maximum d'absorption.
Quelle est la couleur de l'ion permanganate en solution aqueuse ?
La couleur perue est la couleur complmentaire de la couleur absorbe, donc la solution de
permanganate de potassium est violette.
Exprience :
Dans un bcher de 50 mL on mlange V
1
= 10 mL d'une solution de permanganate de potassium acidifie de
concentration C
1
= 0,001 mol/L.
On ajoute une spatule de nitrate de manganse II, Mn(NO
3
)
2
; les ions Mn
2+
catalysent la raction. On
suppose que le volume de la solution ne varie pas lors de la dissolution de ce solide.
A l'instant t=0, on ajoute V
2
=10mL d'une solution d'acide oxalique de concentration C
2
= 0,01 mol/L. On
homognise le mlange et on verse immdiatement une partie du mlange dans une cellule du
spectrophotomtre. Toutes les minutes on note les valeurs de l'absorbance de la solution.
temps (min) 1 2 3 4 5 6 7 8
absorbance A 0,65 0,42 0,275 0,175 0,115 0,075 0,045 0,03
On rappelle que l'absorbance de la solution est proportionnelle la concentration molaire des ions
permanganate. Dans les conditions de l'exprience A= 2000 [MnO
4
-
]
La raction est une raction d'oxydorduction faisant intervenir les couples oxydant / rducteur suivants :
MnO
4
-
/Mn
2+
; CO
2
/ H
2
C
2
O
4
La raction est totale.
1. Ecrire l'quation de la raction.
a) Ecrivez de manire claire les donnes
Solution MnO
4
-
C
1
= 10
-3
mol.L
-1
V
1
= 10 mL
Solution H
2
C
2
O
4
C
2
= 10
-2
mol.L
-1
V
2
= 10mL
b) Ecrire les couples en prsence
c) Ecrire les demi quations
Rduction de l'ion permanganate :
2 x { MnO
4
-
+ 8H
+
+ 5e
-
= Mn
2+
+ 4 H
2
O} (rduction = gain dlectrons)
11
Oxydation de l'acide oxalique :
5 x{ H
2
C
2
O
4
=2 CO
2
+ 2H
+
+ 2e
-
} (oxydation = perte dlectrons)
2MnO
4
-
+ 6H
+
+ 5 H
2
C
2
O
4
=10 CO
2
+ 2Mn
2+
+ 8 H
2
O
Montrer que le protocole est tel que l'acide oxalique est en excs
Quantit de matire initiale
n
MnO4-
= 10
-3
*0,01 = 10
-5
mol = 0,01 mmol
n
H2C2O4
: = 0,01*0,01 = 10
-4
mol = 0,1 mmol
On construit le tableau davancement
2MnO
4
-
5 H
2
C
2
O
4
+ 6H
+
= 10 CO
2
+ 2Mn
2+
+ 8 H
2
O
initial 10
-5
mol 10
-4
mol excs 0 0 solvant
en cours 10
-5
-2x 10
-4
-5x 10x 2x solvant
final
10
-5
-2x
max
=0
x
max
= 5 10
-6
mol
10
-4
-5x
max
=7,5 10
-5
mol
10x
max
= 5 10
-5
mol 2x
max
= 10
-5
mol solvant
2. Reprsenter sur un graphique les valeurs de l'absorbance en fonction du temps.
Daprs la loi de Beer Lamber labsorbance est toujours proportionnelle la concentration
Dfinir la vitesse volumique de la raction en fonction de l'avancement x de la raction, puis en fonction de
l'absorbance.
Vrification
A=2000C
12
Soit A= 2000 (10
-5
-2x)/V et en drivant par rapport au temps :
dA/dt = 2000*(-2)/Vdx /dt ou v= 1/V dx/dt = -1/4000 dA/dt
a) A l'aide du graphe dterminer la valeur de cette vitesse la date t = 4 min.
v(t=4 min) = 0,083/4000= 2 10
-5
mol L
-1
min
-1
.
b) A l'aide des donnes du protocole dterminer l'absorbance de la solution la date t=0, valeur
inaccessible la mesure.
[MnO
4
-
]
t=0
dans le mlange avant que la raction ne dbute : 10
-5
/ ((10+10) 10
-3
)= 5 10
-4
mol.
A
t=0
= 2000 [MnO
4
-
]
t=0
= 2000*5 10
-4
= 1 .
c) Dterminer par le calcul la concentration de l'ion permanganate lorsque l'avancement est gal la
moiti de l'avancement final de la raction. En dduire le temps de demi raction.
Le temps de demi raction est la dure au bout de laquelle l'avancement x est gal la moiti de la valeur
de l'avancement final. La raction tant totale, l'avancement final est gal l'avancement maximal soit
x
max
= 5 10
-6
mol
x
= 2,5 10
-6
mol
[MnO
4
-
] = (10
-5
-2x)/V avec V = 0,02 L
[MnO
4
-
] = (10
-5
-2*2,5 10
-6
) / 0,02 = 2,5 10
-4
mol/L
A = 2000 [MnO
4
-
] = 2000* 2,5 10
-4
= 0,5
on reporte sur la courbe , on en dduit t
1/2
= 1,7 min
tude cintique en suivant la pression
L'exprience suivante a pour but de dterminer le temps de demi-raction t de la raction entre l'acide
chlorhydrique et le magnsium dont l'quation de la raction est :
Mg + 2H
3
O
+
= H
2
+ Mg
2+
+ 2H
2
O.
La transformation est suppose totale.
Protocole :
Dans un ballon on introduit un volume L=10 mL d'une solution concentre d'acide chlorhydrique (H
3
O
+
; Cl
-
)
de concentration C= 8 mol/L. A l'instant initial on plonge un ruban de magnsium de longueur L= 5,1 cm. Trs
rapidement on ferme le ballon avec un bouchon perc qui permet de relier, par un tuyau, le contenu du ballon
avec un manomtre. On note rgulirement la valeur de la pression indique sur le manomtre.
Donnes : masse linique du ruban de magnsium : = 1g/m ;masse molaire du magnsium : 24,3 g/mol;
Volumedu ballon vide : V
0
=100 mL ; P
atm
=1,1 10
5
Pa ; T=293 K ; R=8,31 S.I
13
tude thorique de la raction :
1. Dterminer les quantits de matire de chacun des deux ractifs l'tat initial.
Quantit de matire initiale
Mg : masse (g) / masse molaire (g/mol)
Masse = 1*0,051 = 0,051 g donc 0,051/24,3 = 2,1 10
-3
mol = 2,1 mmol.
Ion oxonium : concentration (mol/L) fois volume (litre) = 8*0,01 = 0,08 mol = 80 mmol
2. Dterminer la valeur x
max
de l'avancement maximal.
3. A l'instant initial, la pression dans le ballon est gale la pression atmosphrique. Au fur et mesure
de la production de gaz, la pression va augmenter. Son expression gnrale est P= P
atm
+ P(H
2
) o
P(H
2
) est la pression du dihydrogne occupant tout le volume disponible dans le ballon.
- Donner l'expression de la quantit de matire de dihydrogne produit en fonction de l'avancement
x.
- En dduire l'expression de l'avancement x en fonction de la pression totale P des volumes V
0
et V,
de la temprature T et de P
atm
. On considre que H
2
se comporte comme un gaz parfait.
Suivi de la pression
Les rsultats obtenus sont rassembls dans le tableau suivant :
t(s) 0 10 20 30 40 50 60 70 80
P ( 10
5
Pa) 1,1 1,13 1,24 1,34 1,41 1,48 1,54 1,6 1,65
1. Calculer les valeurs de l'avancement x de la raction aux dates tudies.
Mg + 2H
3
O
+
= H
2
+ Mg
2+
+ 2H
2
O.
initial 2,1 mmol 80 mmol 0 0
en cours 2,1-x 80-2x x x
final
2,1-x
max
=0
x
max
= 2,1 mmol
80-2x
max
=75,8 mmol
x
max
= 2,1 mmol x
max
= 2,1 mmol
2. Reprsenter graphiquement l'volution de l'avancement en fonction du temps
x=n
H2
=P
H2
(V
0
-V) / (RT)
P
H2
=P -P
atm
x =(P -P
atm
)(V
0
-V) / (RT). (volumeen m
3
)
x =10
5
(P-1,1)(0,1-0,01) 10
-3
/ (8,31 *293)
x =3,7 10
-3
(P-1,1).exprim en mol
t(s) 0 10 20 30 40 50 60 70 80
P ( 10
5
Pa) 1,1 1,13 1,24 1,34 1,41 1,48 1,54 1,6 1,65
x =3,7 10
-3
(P-1,1) 0 1,11 10
-4
5,2 10
-4
8,9 10
-4
1,15 10
-3
1,41 10
-3
1,63 10
-3
1,85 10
-3
2,04 10
-3
14
Dfinir le temps de demi raction t et dterminer graphiquement sa valeur.
Le temps de demi raction est la dure au bout de laquelle l'avancement x est gal la moiti de la valeur
de l'avancement final : le graphe indique environ t= 34 s.
3. Dterminer les valeurs des pressions P
max
et P
(respectivement pression maximale et pression au
temps de demi-raction).
x = 3,7 10
-3
(P-1,1) donne P=1,1 +x /3,7 10
-3
(pression en bar)
P
max
= 1,1 + 2,1/3,7 = 1,67 bar
P = 1,1 + 1,05 /3,7 = 1,38 bar
4. Au bout de 80 s, peut-on dire que la raction est termine ? Justifier.
Au bout de t=80s, l'avancement est trs proche de la valeur x
max
(soit 2,1 mmol) : on peut considrer la
raction pratiquement termine.
Influence de certains paramtres
1. Si on avait utilis la mme masse de magnsium que prcdemment mais sous forme de limaille
(poudre fine), la valeur du temps de demi raction aurait-elle t plus grande ou plus petite que dans
l'exprience prcdente ? Justifier.
La raction s'effectue la surface du magnsium solide : en augmentant la surface du solide (en utilisant
une poudre), on augmente la surface de contact entre les ractifs ; en consquence la vitesse de la
raction va augmenter. Alors t diminue et sera infrieur la valeur prcdente.
2. Mme question si on avait plac le ballon dans un cristallisoir d'eau chaude.
La vitesse de la raction augmente avec la temprature : alors t sera infrieur 34 s si on travaille
une temprature plus leve.
15
Suivi de raction par spectrophotomtrie
L'ion dichromate Cr
2
O
7
2-
est l'oxydant du couple Cr
2
O
7
2-
/ Cr
3+
. L'acide oxalique est le rducteur C
2
H
2
O
4
du
couple C
2
H
2
O
4
/ CO
2
.
1. Ecrire l'quation de la raction d'oxydo rduction qui se produit entre l'ion dichromate et l'acide
oxalique en milieu acide.
Pour R-Cl : masse molaire = 92,6 g/mol ; densit d= 0,85.
Rduction de l'oxydant : Cr
2
O
7
2-
+ 14 H
+
+ 6e
-
--> 2Cr
3+
+ 7H
2
O
Oxydation du rducteur : 3 fois { C
2
H
2
O
4
--> 2 CO
2
+ 2H
+
+ 2e
-
}
Oxydo rduction: Cr
2
O
7
2-
+ 14 H
+
+ 3 C
2
H
2
O
4
--> 2Cr
3+
+ 6 CO
2
+ 6H
+
+ 7H
2
O
Cr
2
O
7
2-
+ 8 H
+
+ 3 C
2
H
2
O
4
--> 2Cr
3+
+ 6 CO
2
+ 7H
2
O
2. On suit l'volution de la raction par spectrophotomtrie.
- A quelle longueur d'onde faut-il se placer (figure 1) pour dterminer le plus prcisment possible
la concentration des ions dichromate ? Justifier.
- Justifier la couleur orange de la solution.
On choisit la longueur d'onde correspondant au maximum d'absorption soit 450 nm.
La solution absorbe dans le bleu ; la couleur complmentaire du bleu est le jaune, couleur de la solution
contenant les ions dichromates.
3. Justifier l'utilit du graphe n2.
- Dterminer l'quation A = f([Cr
2
O
7
2-
]
A partir de solutions talons de concentrations connues, on trace la courbe d'talonnage pour = 450 nm :
partir de la mesure de l'absorbance de la solution titrer. On peut alors en dduire la concentration.
L'absorbance est proportionnelle la concentration en ion dichromate ( figure 2) ; dterminer le
coefficient directeur de la droite : ce coefficient vaut : 1,4 / 0,012 = 116,7 L mol
-1
.
A= 116,7 [Cr
2
O
7
2-
] ou [Cr
2
O
7
2-
] = 8,7 10
-3
A
4. A t=0 on ralise le mlange suivant :
- v
1
=10 mL acide oxalique C
1
= 0,4 mol/L ;
- v
2
= 10 mL solution acidifie dichromate de potassium C
2
= 0,02 mol/L
16
On agite et on place une partie du mlange dans une cuve dans un spectrophotomtre. On relve
l'absorbance ( figure 3).
Dduire de la courbe A=f(t) la reprsentation graphique de [Cr
2
O
7
2-
] = f(t)
Le graphe [Cr
2
O
7
2-
] = f(t) a mme allure que le graphe A= f(t) car A et [Cr
2
O
7
2-
] sont proportionnelles.
5. Dresser le tableau d'volution du systme.
Quantit initiale des ractifs (mol) = concentration (mol/L) fois volume (L)
Dichromate : 0,02*0,01 = 2 10
-4
mol = 0,2 mmol
Acide oxalique : 0,4 * 0,01 = 4 10
-3
mol = 4 mmol
Cr
2
O
7
2-
+3 C
2
H
2
O
4
+8 H
+
--> 2 Cr
3+
+ 6 CO
2
+ 7 H
2
O
initial 0,2 mmol 4 excs 0 0 solvant
en cours 0,2-x 4-3x 2x 6x
final 0,2-x
max
= 0
4-3x
max
= 4-3*0,2
=3,4 mmol
2x
max
6x
max
0,2-x
max
=0 donne x
max
= 0,2 mmol ;
Le ractif limitant est l'ion dichromate.
6. Montrer que l'avancement x est reli l'absorbance A par la formule : x = (0,2-A/6) 10
-3
.
- Calculer x pour diffrentes valeurs et tracer la courbe x= f(t).
- Trouver le ractif limitant et dterminer le temps de demi raction en supposant la raction
totale.
Quantit de matire d'ion dichromate restant en solution une date t : ( 0,2- x ) mmol
Volume de la solution : 20 mL
[Cr
2
O
7
2-
] (0,2-x) / 20 = 8,7 10
-3
A (rsultat trouv ci dessus)
0,2-x = 20*8,7 10
-3
A = 0,174 A
x = 0,2-0,174 A = 0,2 -A/6 mmol ou bien (0,2 -A/6) 10
-3
mol
temps (min) 0 10 20 30 40
A(lecture graphe
3)
1,2 0,8 0,5 0,3 0,2
x(mmol) 0 0,0667 0,117 0,15 0,167
Le temps de demi raction t est la dure au bout de laquelle l'avancement est gal la moiti de
l'avancement final.
Lavancement final est gal l'avancement maximal pour une raction totale.
17
T voisin de 18 min.
Etude cintique par conductimtrie
On s'intresse la raction d'oxydorduction entre les ions peroxodisulfate S
2
O
8
2-
et les ions iodures I
-
en
solution aqueuse.
Couples oxydant / rducteur : S
2
O
8
2-
/ SO
4
2-
et I
2
/ I
-
.
Dans un bcher on introduit un volume V
1
= 40 mL d'une solution aqueuse de peroxodisulfate de potassium
(2K
+
; S
2
O
8
2-
) de concentration C
1
= 0,1 mol/L . l'instant t=0, on ajoute V
2
= 60 mL d'une solution d'iodure
de potassium (K
+
: I
-
) de concentration C
2
= 0,15 mol/L. On obtient la courbe suivante :
1. Ecrire les demi quations lectroniques pour chacun des deux couples qui interviennent dans cette
raction.
Rduction de l'ion peroxodisulfate : S
2
O
8
2-
+ 2e
-
-->2SO
4
2-
Oxydation de l'ion iodure : 2I
-
-->2e
-
+ I
2
.
2. En dduire l'quation de la raction entre les ions peroxodisulfates et les ions iodures.
S
2
O
8
2-
+2I
-
-->2SO
4
2-
+ I
2
.
3. En notant x l'avancement de la raction l'instant t, donner les expressions des concentrations
des diverses espces prsentes dans le mlange en fonction de x et du volume V de la solution. On
ngligera les ions oxonium et hydroxyde minoritaires devant les autres ions.
18
S
2
O
8
2-
+2I
-
-->2SO
4
2-
+ I
2
initial 40*0,1 = 4 mmol 60*0,15 = 9 mmol 0 0
en cours 4-x 9-2x 2x x
fin
4-x
max
=0
x
max
=4 mmol
9-2x
max
=1 mmol 2x
max
=8 mmol x
max
=4 mmol
la date t, concentration des espces prsentes :
[S
2
O
8
2-
] = (4-x)/V
[I
-
] = (9-2x)/V
[SO
4
2-
] = 2x/V
[I
2
] = x/V
4. On rappelle que la conductance G d'une telle solution a pour expression:
G= k(
1
[S
2
O
8
2-
]+
2
[I
-
]+
3
[SO
4
2-
]+
4
[K
+
]) o les
i
reprsentent les conductivits molaires
ioniques ( qui ne dpendent que de la nature de l'ion et de la temprature) et k la constante de cellule.
Montrer que la relation entre la conductance G et l'avancement x de la raction est de la forme :
G=1/V(A+Bx) o V est le volume constant de la solution, et A et B des constantesA =1,9 mS L et B=42
mS L mol
-1
.
[K
+
]=(40*0,1*2+60*0,15) / 100 = 0,17 mol/L
G= k/V(
1
(4-x)+
2
(9-2x)+
3
2x+
4
0,017)
G= k/V(4
1
+9
2
+0,017
4
+ (2
3
-
1
-2
2
)x).
5. Dfinir la vitesse volumique de la raction en fonction de l'avancement x. En dduire son
expression en fonction de G.
Vitesse volumique de la raction : v = 1/ V dx/dt
G= 1/V (A+Bx);
Driver par rapport au temps cette expression
dG/dt = B/V dx/dt soit v = 1/B dG/dt.
6. A l'aide du graphique, dterminer la valeur de la vitesse volumique la date t = 1 min.
v (t=1 min) = 1/42*0,0108 = 2,57 10
-4
mol L
-1
s
-1
..
19
7. En utilisant le rsultat prcdent, dterminer graphiquement l'instant partir duquel on peut que
considrer la raction est termine.
Si dG/dt = 0 (tangente horizontale) la vitesse de la raction est nulle ; la raction est alors termine.
Lecture graphe : partir de t = 2 min la raction peut tre considre comme termine.
Raction suivie par conductimtrie
Le chlorure de tertiobutyle (CH
3
)
3
C-Cl peut ragir avec l'eau :
(CH
3
)
3
C-Cl +H
2
O--> H
+
(aq) + Cl
-
(aq)+(CH
3
)
3
C-OH
Par la suite (CH
3
)
3
C-Cl sera not R-Cl et (CH
3
)
3
C-OH sera not R-OH.
Dans deux bchers diffrents on introduit 30 g d'eau et 20 g d'actone. L'un des bchers est maintenu 40C,
l'autre 30C. Quand l'quilibre thermique est atteint on plonge la sonde du conductimtre dans l'un des
bchers et on met en route l'agitation. On ajoute alors 1 mL de tertiobutyle et on suit l'volution de la
conductivit en fonction du temps. On fait de mme avec l'autre bcher.
1. Calculer la quantit initiale n
0
de tertiobutyl R-Cl
Quantit de matire initiale de R-Cl : n
0
(mol)= masse( g) / masse molaire (g/mol)
Masse (g) = densit * volume(mL) = 0,85*1 = 0,85 g
n
0
= 0,85 / 92,6 = 9,18 10
-3
= 9,18 mmol.
2. Dresser le tableau d'volution du systme. A t
infini
, la raction suppose totale est termine.
R-Cl eau -->H
+
+ Cl
-
+ R-OH
initial 9,18 mmol excs 0 0 0
en cours 9,18-x x x x
final 9,18-x
max
= 0 x
max
= 9,18 mmol x
max
= 9,18 mmol x
max
= 9,18 mmol
9,18-x
max
=0 donne x
max
= 9,18 mmol
3. Quelles sont les espces chimiques responsables de l'volution de la conductivit ?
- Exprimer
infini
conductivit au bout d'un temps trs long en fonction de n
0
et V ( volume total)
- Exprimer
t
conductivit au bout d'un temps t en fonction de n
0
et V .
- Montrer que x = n
0
t
/
infini
(x: avancement de la raction)
20
Les ions chlorures Cl
-
et les ions H
+
sont responsables de l'volution de la conductivit
= (
H+
+
Cl-
) c
H+
et
Cl-
conductivit molaire ionique ( S m/mol)
[ H
+
]en mol/m
3
.
4. Calculer x diffrentes dates pour les temprature 30 et 40C. Regrouper les rsultats sous
forme d'un tableau. On donne
infini
=8,4 mS cm
-1
40C et
infini
=7,6 mS cm
-1
30C.
- Tracer les graphes x= f(t) pour les deux tempratures.
- Justifier les positions relatives des deux courbes
- Admettent-elles la mme limite ?
- Calculer dans chaque cas le temps de demi raction.
Pour R-Cl : masse molaire =92,6 g/mol ; densit d=0,85.
Au bout d'un temps trs long, la raction est termine : celle ci tant totale l'avancement final est gal
l'avancement maximal et c = x
max
/ V = n
0
/ V
infini
= (
H+
+
Cl-
) n
0
/ V
de mme :
t
= (
H+
+
Cl-
) x / V
t
/
nfini
= x /n
0
d'o x = n
0
t
/
infini
.
30C :
date t (min) 0 2 5 10 14 25
t
(lecture graphe) 0 1,5 3 5 5,5 7
t
/
infini
0 0,2 0,4 0,66 0,72 0,92
x = n
0
t
/
infini
(mmol) 0 1,8 3,6 6 6,6 8,4
40C :
date t (min) 0 2 5 10 14 25
t
(lecture graphe) 0 3 5 7 8 8
t
/
infini
0 0,36 0,6 0,83 0,95 0,95
x = n
0
t
/
infini
(mmol) 0 3,3 5,4 7,6 8,7 8,7
La temprature est un facteur cintique : plus la temprature est
leve plus la dure de la transformation est courte.
Do la position de la courbe bleue.
Ces deux courbes, issues de mesures exprimentales, admettent
peu prs la mme limite savoir x
max
voisin de n
0
=9,18 mmol.
Le temps de demi raction est le temps au bout duquel x = x
final
.
30C : t = 6 min
A 40C : t = 4 min.
Vous aimerez peut-être aussi
- Corr Serie 3 Prob SMC s4 - CompressedDocument4 pagesCorr Serie 3 Prob SMC s4 - CompressedAbdelhakim BailalPas encore d'évaluation
- CHP 1 2023Document14 pagesCHP 1 2023Abdelhakim BailalPas encore d'évaluation
- SMC s3 Ratt 2017Document8 pagesSMC s3 Ratt 2017Abdelhakim BailalPas encore d'évaluation
- Correction Epreuve de Chimie Des Electrolytes 2013 2014Document5 pagesCorrection Epreuve de Chimie Des Electrolytes 2013 2014Abdelhakim BailalPas encore d'évaluation
- SMC S3 Chim Exp Norm 2021Document2 pagesSMC S3 Chim Exp Norm 2021Abdelhakim BailalPas encore d'évaluation
- Correction Epreuve de Chimie Des Electrolytes 2014 20152Document5 pagesCorrection Epreuve de Chimie Des Electrolytes 2014 20152Abdelhakim BailalPas encore d'évaluation
- SMPC S2 CHP 1 Chimie Des Solutions 21Document15 pagesSMPC S2 CHP 1 Chimie Des Solutions 21Abdelhakim BailalPas encore d'évaluation
- Chapitre IIDocument48 pagesChapitre IIAbdelhakim Bailal100% (1)
- SMPC S1 Série 2 2021Document11 pagesSMPC S1 Série 2 2021Abdelhakim BailalPas encore d'évaluation
- Dm5optionPSI CorrigeDocument6 pagesDm5optionPSI CorrigeAbdelhakim BailalPas encore d'évaluation
- SMPC s1chp IV 2020Document40 pagesSMPC s1chp IV 2020Abdelhakim Bailal100% (1)
- ChmTheo S5 Chapitre 7Document32 pagesChmTheo S5 Chapitre 7Abdelhakim BailalPas encore d'évaluation
- Série 1 s5 20Document9 pagesSérie 1 s5 20Abdelhakim BailalPas encore d'évaluation
- DM 5 Option PCDocument8 pagesDM 5 Option PCAbdelhakim BailalPas encore d'évaluation
- ChmTheo S5 Chap3 PDFDocument24 pagesChmTheo S5 Chap3 PDFAbdelhakim BailalPas encore d'évaluation
- SMC S3 Ratt 2021Document7 pagesSMC S3 Ratt 2021Abdelhakim BailalPas encore d'évaluation
- Nouvelle Doc 9 Avr. 2021 20.23Document4 pagesNouvelle Doc 9 Avr. 2021 20.23Abdelhakim Bailal100% (1)
- SMPC 2020 RattDocument3 pagesSMPC 2020 RattAbdelhakim BailalPas encore d'évaluation
- SMC S3 Électrolytes Norm 2021Document4 pagesSMC S3 Électrolytes Norm 2021Abdelhakim BailalPas encore d'évaluation
- Master CHP 4 Corrosion 2021Document31 pagesMaster CHP 4 Corrosion 2021Abdelhakim BailalPas encore d'évaluation
- ChmTheo S5 Chap3 PDFDocument24 pagesChmTheo S5 Chap3 PDFAbdelhakim BailalPas encore d'évaluation
- ChmTheo S5 Chap2Document16 pagesChmTheo S5 Chap2Abdelhakim BailalPas encore d'évaluation
- ChmTheo S5 Chap1Document12 pagesChmTheo S5 Chap1Abdelhakim Bailal100% (2)
- SMPC s2 CHP 2Document31 pagesSMPC s2 CHP 2Abdelhakim BailalPas encore d'évaluation
- SMC5Document75 pagesSMC5Mohamed Amine ZaouiPas encore d'évaluation
- Chimie1an06 Cours - Exercices Kouachi PDFDocument214 pagesChimie1an06 Cours - Exercices Kouachi PDFMokhtarBensaid100% (3)
- SMC S3 Chim Exp Ratt 2020 PDFDocument2 pagesSMC S3 Chim Exp Ratt 2020 PDFAbdelhakim BailalPas encore d'évaluation
- Chapitre 14 Diagramme e PHDocument9 pagesChapitre 14 Diagramme e PHAbdelhakim BailalPas encore d'évaluation
- Energie Réticulaire PDFDocument1 pageEnergie Réticulaire PDFAbdelhakim BailalPas encore d'évaluation
- Energie RéticulaireDocument1 pageEnergie RéticulaireAbdelhakim Bailal0% (1)
- ELECTROPHORESEDocument36 pagesELECTROPHORESE[AE]86% (7)
- TP Opu 2Document12 pagesTP Opu 2Amani mimoPas encore d'évaluation
- Chapitre III AbsorptionDocument9 pagesChapitre III AbsorptionAymene TibaPas encore d'évaluation
- Derakane Chemical Resistance GuideDocument70 pagesDerakane Chemical Resistance GuideJohan ConradiePas encore d'évaluation
- Chapitre II Nomenclature PFDocument18 pagesChapitre II Nomenclature PFyahya haziniPas encore d'évaluation
- Chap 3 Solidification Des Métaux 2020 - TexteDocument68 pagesChap 3 Solidification Des Métaux 2020 - TexteYessine Omrane100% (3)
- Rapport de StageDocument11 pagesRapport de StageAbdelkader BenazizaPas encore d'évaluation
- Chemistry Paper 1 TZ1 HLDocument16 pagesChemistry Paper 1 TZ1 HLDilaksPas encore d'évaluation
- Titane In2p3 3 DefinitifDocument85 pagesTitane In2p3 3 DefinitifSemlali ZakariaPas encore d'évaluation
- Les Huiles VegetalesDocument3 pagesLes Huiles VegetalesIngrid KoutioPas encore d'évaluation
- Guide Additiftous Les Noms, Famille, VégétarienDocument12 pagesGuide Additiftous Les Noms, Famille, Végétariengaggg100% (1)
- Astra LineDocument2 pagesAstra LineissamosPas encore d'évaluation
- Analyses Des Eaux de Réseau de La Ville de Béjaia Et Évaluation de Leur Pouvoir Entartant PDFDocument102 pagesAnalyses Des Eaux de Réseau de La Ville de Béjaia Et Évaluation de Leur Pouvoir Entartant PDFزيد بخليفة100% (1)
- 4 BentemamDocument4 pages4 Bentemamfplm.infoPas encore d'évaluation
- Elements Bloc P Halogenes 1Document25 pagesElements Bloc P Halogenes 1Yc YacinePas encore d'évaluation
- Cours Elastomère M1 2020-2021Document37 pagesCours Elastomère M1 2020-2021Hakim BT100% (1)
- Biophysique2an SolutionsDocument71 pagesBiophysique2an SolutionsMina RhmPas encore d'évaluation
- Applications NitrurationDocument1 pageApplications NitrurationDarkedgePas encore d'évaluation
- 7SP06TEWO1820Document15 pages7SP06TEWO1820Nathan YikouPas encore d'évaluation
- Biofuel Et PlastiqueDocument34 pagesBiofuel Et PlastiqueOuerghi AyaPas encore d'évaluation
- Fiche de Revision Physique Chimie 2021 Premiere Constitution D Un Systeme ExercicesDocument3 pagesFiche de Revision Physique Chimie 2021 Premiere Constitution D Un Systeme ExercicesAccétude BéziersPas encore d'évaluation
- Chapitre II - COAGULATION - FLOCULATIONDocument41 pagesChapitre II - COAGULATION - FLOCULATIONSara Qrm50% (2)
- TD Matériaux Composites 7522Document4 pagesTD Matériaux Composites 7522Hassen Tarchoune100% (4)
- MémoireDocument87 pagesMémoireseiftaleb96Pas encore d'évaluation
- Acido BasiqueDocument7 pagesAcido BasiquesimokatyPas encore d'évaluation
- Phy 4 ASDocument84 pagesPhy 4 ASYoutube WorldPas encore d'évaluation
- Sertesseuse PDFDocument117 pagesSertesseuse PDFzanati abdelhakPas encore d'évaluation
- Exercice Eau Oxygenee + Corrige PDFDocument3 pagesExercice Eau Oxygenee + Corrige PDFCamusPas encore d'évaluation
- Chimie (9 Points) : Exercice N° 1: (5,5 PTS)Document3 pagesChimie (9 Points) : Exercice N° 1: (5,5 PTS)Ghada DaddouPas encore d'évaluation
- 4cchap2 PDFDocument4 pages4cchap2 PDFndiouma diouf100% (1)