Académique Documents
Professionnel Documents
Culture Documents
Acidimetrie Acides Doacidfo
Transféré par
MOUNA MESFARTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Acidimetrie Acides Doacidfo
Transféré par
MOUNA MESFARDroits d'auteur :
Formats disponibles
Université du Maine - Faculté des Sciences Acide fort - base forte
Dosage acide fort – base forte
Acide fort HA :
titré, concentration (à déterminer) ca, volume va : HA + H2 O → H3 O + + A − .
Base forte NaOH
titrant, concentration cb, volume vb (à verser à la burette) : NaOH → Na + + OH− .
L’équation bilan de la réaction de dosage s’écrit : H3O + + OH− → 2 H2O .
L’équivalence est atteinte lorsque : n0 (H3O + ) = n(OH− )versé c’est à dire lorsque c a .v a = c b .v b,éq .
vb c v c v
Pour étudier la variation du pH en fonction de vb, on utilise : x= = b b = b b .
v b,éq c b v b,éq c a v a
• x=0 ; vb=0 ; pH = − log c a .
H3O + + OH− → 2 H2O
• 0 〈 x 〈 1 ; 0 < v b < v b, éq ; quantités int roduites c av a cbvb
quantités à l' équilibre c av a − cbvb ε
[H O ] = c vv
3
+ a a − c b vb
+ vb
c v
= a a (1 − x) et
v a + vb
pH = − log
cava
v a + vb
− log(1 − x )
a
§ x = 1 ; v b = v b,éq ;
l’électroneutralité s’écrit : [H O ]+ [Na ] = [OH ]+ [A ] ;
3
+ + − −
la conservation de la matière nous donne [Na ] = [Cl ] = vc +vv .
+ − a a
a b
On obtient donc : [H O ] = [OH ] = (K
3
+ −
e)
1
2 et pH=7.
§ x 〉1 ; v b 〉 v b,éq ; nOH− ,res tan t = nOH− ,versé − nOH− ,ayant réagi = c b ( v b − v b,éq )
[OH ] = c
− b (v b
va + vb
− v b,éq )
[H O ] = K
3
+
e
v a + vb
c b (v b − v b,éq ) 14
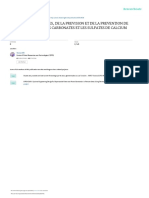
acide fort / base forte (Ca = Cb; Va = 10 mL)
cava 12
pH = 14 + log + log( x − 1) .
v a + vb
10
8
Etant donné la valeur du pH à l’équivalence, la zone pH = pHéquiv = 7
Ca = 10-1M
pH
de virage de l’indicateur coloré devra contenir la valeur de 6
Ca = 10-2M
Ca = 10-3M
pH=7. Ca = 10-4M
4
La précision du dosage est d’autant plus grande que
les solutions sont plus concentrées puisque le saut de pH à 2
Vb = Vb équiv
l’équivalence est plus important (figure ci-contre). 0
0 5 10 15 20
Vb (mL)
Vous aimerez peut-être aussi
- CalculacidDocument2 pagesCalculacidtv tvPas encore d'évaluation
- Acidimetrie Acides CalculacidDocument2 pagesAcidimetrie Acides CalculacidMar WaPas encore d'évaluation
- DoacidfaDocument3 pagesDoacidfaMOUNA MESFARPas encore d'évaluation
- Correction National 2020 - SM - NDocument12 pagesCorrection National 2020 - SM - NProf YOUSSEF MOUJAHID أستاذ يوسف مجاهدPas encore d'évaluation
- Diapositives Supplémentaires DosagesDocument4 pagesDiapositives Supplémentaires Dosagesdyhp2pswsrPas encore d'évaluation
- Fonctions Usuelles - Fonctions HyperboliquesDocument2 pagesFonctions Usuelles - Fonctions Hyperboliqueschaddad abdllahPas encore d'évaluation
- Cours Dosage Acide Base 3Document8 pagesCours Dosage Acide Base 3Boussetta ZouhaierPas encore d'évaluation
- Cours Dosage Acide BaseDocument9 pagesCours Dosage Acide BaseBoussetta ZouhaierPas encore d'évaluation
- Examen National Physique Chimie Sciences Maths 2017 Normale CorrigeDocument9 pagesExamen National Physique Chimie Sciences Maths 2017 Normale Corrigeel ghazi benrrabhiPas encore d'évaluation
- Examen PC-SN-2020 PC-BIOF CorrectionDocument9 pagesExamen PC-SN-2020 PC-BIOF CorrectionmedPas encore d'évaluation
- Bac 2Document124 pagesBac 2Ahmed EL YousfyPas encore d'évaluation
- Résumé CHP 8Document3 pagesRésumé CHP 8James MerhejPas encore d'évaluation
- Calculs de PH Des Solutions Aqueuses Diluees: HO C HODocument7 pagesCalculs de PH Des Solutions Aqueuses Diluees: HO C HOabalotouadjeiPas encore d'évaluation
- Chapitre IV 1Document37 pagesChapitre IV 1sidiPas encore d'évaluation
- Baccor 17 SM 1Document9 pagesBaccor 17 SM 1Souhail El AsferPas encore d'évaluation
- 2008 AmNord Exo1 Correction ReactionsTotales 7ptsDocument3 pages2008 AmNord Exo1 Correction ReactionsTotales 7ptsla physique selon le programme Français100% (2)
- CH 5 (Neutralisation)Document12 pagesCH 5 (Neutralisation)Seif Souid88% (8)
- Dosage Acido Basique Cours LatexDocument3 pagesDosage Acido Basique Cours LatexSaif Yassine Touil100% (1)
- Chimie B Chap8 Titrage - Acidobasique PDFDocument6 pagesChimie B Chap8 Titrage - Acidobasique PDFMouloud IssaadPas encore d'évaluation
- Transformations Chimiques S Effectuant Dans Les 2 Sens Cours LatexDocument3 pagesTransformations Chimiques S Effectuant Dans Les 2 Sens Cours LatexBadr ElPas encore d'évaluation
- CH 2Document6 pagesCH 2Kamelia EtoillefillantePas encore d'évaluation
- N-2017 SM (F), CorrectionDocument9 pagesN-2017 SM (F), CorrectionHassan ElbahraouiPas encore d'évaluation
- Examen National Physique Chimie Sciences Maths 2020 Normale CorrigeDocument13 pagesExamen National Physique Chimie Sciences Maths 2020 Normale Corrigeasmae khalilPas encore d'évaluation
- Corr Examen PC BAC18N-SM FR Prof - JamilDocument8 pagesCorr Examen PC BAC18N-SM FR Prof - JamilSouhail El AsferPas encore d'évaluation
- Methode GranDocument29 pagesMethode GranASMAA KherrazPas encore d'évaluation
- Chapitre 1-6Document19 pagesChapitre 1-6Wiame NaimPas encore d'évaluation
- Etat D Equilibre D Un Systeme Chimique Cours LatexDocument3 pagesEtat D Equilibre D Un Systeme Chimique Cours LatexNa JouaPas encore d'évaluation
- Fascicule 2007-2008-2eme Partie Chi PhysikDocument96 pagesFascicule 2007-2008-2eme Partie Chi PhysikHenri Elias HabibPas encore d'évaluation
- Constante D Acidite TP Enonce + CorrigeDocument3 pagesConstante D Acidite TP Enonce + CorrigeAliFriend100% (1)
- Examen National Physique Chimie Sciences Maths 2017 Normale CorrigeDocument9 pagesExamen National Physique Chimie Sciences Maths 2017 Normale CorrigeMohamed MohaPas encore d'évaluation
- 1 - Transformation Liée À Des Réactions Acides Et BasesDocument15 pages1 - Transformation Liée À Des Réactions Acides Et BasesTaha BoulmanePas encore d'évaluation
- TamponDocument4 pagesTamponChouaib MeraoumiaPas encore d'évaluation
- Equilibre Acido-BasiqueDocument2 pagesEquilibre Acido-Basiquetiennou.lololPas encore d'évaluation
- Corige SCPH S1Document9 pagesCorige SCPH S1Anafan DiemePas encore d'évaluation
- Cours Chap 8 Force Des Acides Et Des Bases PMDocument8 pagesCours Chap 8 Force Des Acides Et Des Bases PMLellia SEMMARPas encore d'évaluation
- Rapport de TP ElectrochimieDocument15 pagesRapport de TP ElectrochimieSimo Boumahrachi100% (2)
- Corrige Bac Normale Physique Chimie PC FrancaisDocument4 pagesCorrige Bac Normale Physique Chimie PC FrancaiselmehdiPas encore d'évaluation
- TleD CH L9 Couple Acide-BaseDocument12 pagesTleD CH L9 Couple Acide-BaseMarcPas encore d'évaluation
- Reactions Acide-BaseDocument8 pagesReactions Acide-BaseMahmoud GazzahPas encore d'évaluation
- Baccor16svt2-Fr (WWW - Pc1.ma)Document6 pagesBaccor16svt2-Fr (WWW - Pc1.ma)ELHassanTamraoui0% (1)
- Correction Examen PC Juillet 2017 2bac SM FRDocument10 pagesCorrection Examen PC Juillet 2017 2bac SM FRNoussaiba El rhaliPas encore d'évaluation
- CompteRenduTP N 3Document12 pagesCompteRenduTP N 3youssef ibn seddikPas encore d'évaluation
- Chapitre 5B Complété Force Des Acides Et Des BasesDocument5 pagesChapitre 5B Complété Force Des Acides Et Des Basesairfann67Pas encore d'évaluation
- Corrige - Examen de Chimie Des Solutions (SMPC - s2) Session Normale-1Document7 pagesCorrige - Examen de Chimie Des Solutions (SMPC - s2) Session Normale-1charki zakariaPas encore d'évaluation
- Devoir Corrigé de Baccalauréat - Sciences Physiques - Principale 2017 - Bac Sciences Exp (2016-2017) MR Guitouni AnisDocument5 pagesDevoir Corrigé de Baccalauréat - Sciences Physiques - Principale 2017 - Bac Sciences Exp (2016-2017) MR Guitouni Anisolfa essefiPas encore d'évaluation
- Cours Chimie 02Document3 pagesCours Chimie 02imen dimessiPas encore d'évaluation
- Chapitre IIDocument12 pagesChapitre IIPascal GadedjissoPas encore d'évaluation
- 2004 03 NelleCaledo Exo1 Correction KaAcidebenzoique 4ptsDocument2 pages2004 03 NelleCaledo Exo1 Correction KaAcidebenzoique 4ptsAlain StantéPas encore d'évaluation
- Acide BaseDocument6 pagesAcide BaseCalixte TakamPas encore d'évaluation
- 2008 09 Antilles Exo3 Correction Titrage DemiEq Pka 4ptsDocument2 pages2008 09 Antilles Exo3 Correction Titrage DemiEq Pka 4ptsla physique selon le programme FrançaisPas encore d'évaluation
- Chapitre II - Chimie II - Equilibres ChimiquesDocument19 pagesChapitre II - Chimie II - Equilibres Chimiqueskim namjoonPas encore d'évaluation
- PH Des Solutions AqueusesDocument5 pagesPH Des Solutions AqueusesMoulham KhalidPas encore d'évaluation
- Acide BaseDocument14 pagesAcide Baseالغزيزال الحسن EL GHZIZAL HassanePas encore d'évaluation
- Transformation Et Réaction Acido-BasiqueDocument15 pagesTransformation Et Réaction Acido-BasiqueaffanefatimaezzahraaPas encore d'évaluation
- Dosage Acidobasique - DM CorrigéDocument3 pagesDosage Acidobasique - DM CorrigéHanae MansouriPas encore d'évaluation
- PH2SCH06Document3 pagesPH2SCH06chadaPas encore d'évaluation
- HypequiDocument2 pagesHypequiYoussef jebabdiPas encore d'évaluation
- PB3 3Document4 pagesPB3 3one piece to drawPas encore d'évaluation
- Bac Blanc N2 Corr Ex3Document1 pageBac Blanc N2 Corr Ex3la physique selon le programme FrançaisPas encore d'évaluation
- Manipulation 1Document5 pagesManipulation 1MOUNA MESFARPas encore d'évaluation
- Corrigé TD-partie1-MECMIDocument12 pagesCorrigé TD-partie1-MECMIMOUNA MESFARPas encore d'évaluation
- TP - DSC CuSO4.5h2ODocument5 pagesTP - DSC CuSO4.5h2OMOUNA MESFARPas encore d'évaluation
- SyntheseDocument30 pagesSyntheseMOUNA MESFARPas encore d'évaluation
- SM-AICHOUNI SARA-Chimie Fondamentale-TPs - Chimie Analytique I - L2-S4Document6 pagesSM-AICHOUNI SARA-Chimie Fondamentale-TPs - Chimie Analytique I - L2-S4MOUNA MESFARPas encore d'évaluation
- Chapitre 10Document39 pagesChapitre 10MOUNA MESFARPas encore d'évaluation
- 0809 CorrectiondosageDocument3 pages0809 CorrectiondosageMOUNA MESFARPas encore d'évaluation
- L. Chimie Parcours RechercheDocument65 pagesL. Chimie Parcours RechercheMOUNA MESFARPas encore d'évaluation
- Transformation Liée À Des Réactions Acides Et Bases (WWW - Pc1.ma)Document21 pagesTransformation Liée À Des Réactions Acides Et Bases (WWW - Pc1.ma)Abderrazzak ElhaimerPas encore d'évaluation
- Les Acides Et Les Bases - 3 ACDocument3 pagesLes Acides Et Les Bases - 3 ACaznag hicham0% (1)
- Extraction Isolement LiquideDocument6 pagesExtraction Isolement Liquideelhidhab2014Pas encore d'évaluation
- Série 4 PHDocument2 pagesSérie 4 PHYahya LahmarPas encore d'évaluation
- BENOTHMANE - AICHA NIHED - Chimie. - Chimie PhysiqueDocument101 pagesBENOTHMANE - AICHA NIHED - Chimie. - Chimie PhysiqueFatima-ezzahra BoubagraPas encore d'évaluation
- 01-SA1 Réactions Acido-BasiquesDocument12 pages01-SA1 Réactions Acido-BasiquesberthouPas encore d'évaluation
- L'Essentiel en Chimie-3 (N.hebbar-EP D'oran) Chap-2,3,4Document47 pagesL'Essentiel en Chimie-3 (N.hebbar-EP D'oran) Chap-2,3,4SERGIOPas encore d'évaluation
- C PB11 Saq CaDocument8 pagesC PB11 Saq CaZineb ZahimPas encore d'évaluation
- DM - 8 Magnetisme +chimie Solu +thermo Chimie PDFDocument4 pagesDM - 8 Magnetisme +chimie Solu +thermo Chimie PDFBrandy OdonnellPas encore d'évaluation
- Osmotech 2202osmotech 2202Document2 pagesOsmotech 2202osmotech 2202Akram DerhemPas encore d'évaluation
- TD Chimie 3em 1Document8 pagesTD Chimie 3em 1LAWSON NICOLASPas encore d'évaluation
- Exo PHDocument2 pagesExo PHNaimboulah BjrPas encore d'évaluation
- Equilibres de ComplexationDocument10 pagesEquilibres de ComplexationLawrence Mundene-timotheePas encore d'évaluation
- Polycopier de Resumé Du Cours Avec Exercices Et Corridés de Chim-SolDocument101 pagesPolycopier de Resumé Du Cours Avec Exercices Et Corridés de Chim-Solbenyamina imanePas encore d'évaluation
- HDR 2005 PDFDocument110 pagesHDR 2005 PDFJean-Jacques RahobisoaPas encore d'évaluation
- Corrige - Examen de Chimie Des Solutions (SMPC - s2) Session Normale-1Document7 pagesCorrige - Examen de Chimie Des Solutions (SMPC - s2) Session Normale-1charki zakariaPas encore d'évaluation
- 6-Activité Enzymatique (Biochimistes)Document14 pages6-Activité Enzymatique (Biochimistes)Sioud BesmaPas encore d'évaluation
- Fromage de Chèvre Spécificités Technologiques Et Économiques PDFDocument81 pagesFromage de Chèvre Spécificités Technologiques Et Économiques PDFtolmousPas encore d'évaluation
- Maroc Prog2013 Chimie PcsiDocument14 pagesMaroc Prog2013 Chimie PcsiBrandy OdonnellPas encore d'évaluation
- Fiche de Révisions N°3Document3 pagesFiche de Révisions N°3Mohamed Ayoub BouchikhiPas encore d'évaluation
- Epreuve de Physique ChimieDocument5 pagesEpreuve de Physique ChimieBile DjetouanPas encore d'évaluation
- TP Procèdèes Oxidations AvoncèsDocument43 pagesTP Procèdèes Oxidations Avoncèsgoufifaromaissa139Pas encore d'évaluation
- Série 4 - Oxydation Des MétauxDocument2 pagesSérie 4 - Oxydation Des MétauxRimPas encore d'évaluation
- Cycles BiogeochimDocument198 pagesCycles BiogeochimWillPas encore d'évaluation
- 3-1 Produits DangereuxDocument19 pages3-1 Produits DangereuxMohamed EttahiriPas encore d'évaluation
- TD2 CSDocument2 pagesTD2 CSSimo Maro100% (1)
- TD Solutions Aqueuses - Acide Fort Base Forte PH 2016Document6 pagesTD Solutions Aqueuses - Acide Fort Base Forte PH 2016Oumar Traoré100% (2)
- Devoir 2 Modele 8 Physique Chimie 3ac Semestre 1Document2 pagesDevoir 2 Modele 8 Physique Chimie 3ac Semestre 1bouthaina taziPas encore d'évaluation
- Chapitre Solubilité 2018Document22 pagesChapitre Solubilité 2018Younes AsfalouPas encore d'évaluation
- 2023 Asie J1 Exo3 Sujet Salicylate BeerLambert K 4 5ptsDocument4 pages2023 Asie J1 Exo3 Sujet Salicylate BeerLambert K 4 5ptsstephankorgo42Pas encore d'évaluation