Académique Documents
Professionnel Documents
Culture Documents
22indicateur Coloré
Transféré par
Hanine Hmida0 évaluation0% ont trouvé ce document utile (0 vote)
3 vues1 pageTitre original
22indicateur coloré
Copyright
© © All Rights Reserved
Formats disponibles
DOC, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOC, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
3 vues1 page22indicateur Coloré
Transféré par
Hanine HmidaDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme DOC, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 1
indicateur coloré
dosage acide faible base forte
Le jus de chou rouge a une couleur qui dépend du pH.
pH 0-3 4-6 7-8 9 -12 13 -14
couleur rouge violet bleu vert jaune
On se propose de l’utiliser comme indicateur coloré acido-basique naturel. Trois solutions de concentrations molaires
volumiques voisines de 0,1 mol.L - 1 sont testées par cet indicateur coloré. On obtient les résultats suivants :
solution A B C
couleur rouge violet vert
1. a- Donner le caractère acido-basique de chaque solution.
b- On verse un certain volume d’eau sur la solution C; dire si sa couleur vire au bleu ou au jaune; Expliquer .
2. Une détermination plus précise du pH des solutions A et B donne les résultats suivants :pHA = 2,9 et pHB = 1
a- L’une de ces solutions est une solution d’acide éthanoïque, acide faible. Laquelle ? Justifier la réponse.
b- Écrire l’équation de l’action de cet acide sur l’eau. Donner l’expression de la constante d’acidité Ka du
couple acide-base mis en jeu.
3. Vous disposez du matériel suivant : pipettes jaugées : 1 mL ; 5 mL ; 10 mL ; 20 mL ; poire à pipeter ; fioles
jaugées : 50 mL ; 100 mL ; 200 mL ; pH-mètre avec sonde étalonnée ; éprouvettes graduées : 10 mL ; 50
mL ; 100 mL ; agitateur magnétique ; burette de 25 mL ; barreau aimanté et d’eau distillée ; béchers.
Comment, à partir de la solution identifiée à la question ci dessus, préparer un volume v =100 mL de solution
d’acide éthanoïque diluée dix fois ?
a- Décrire brièvement le protocole expérimental ;
b- Trouver la nouvelle valeur de son pH .
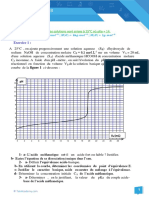
4. Sur la figure ci dessous, on trouve la courbe expérimentale du dosage d’un volume VA = 20 mL de la solution
d’acide éthanoïque diluée par une solution d’hydroxyde de sodium (la soude) de concentration molaire
volumique 0,01 mol.L – 1 .
La courbe tracée (1) donne la variation du pH en fonction du volume VB de base versée.
a. Écrire l’équation de la réaction de dosage.
b. Qu’appelle-t-on équivalence ? Déterminer l’abscisse du point d’équivalence
sur la courbe expérimentale.
c. En déduire la concentration molaire volumique de la solution d’acide
éthanoïque.
d. En l’absence de pH-mètre, l’indicateur coloré chou rouge permet-il de
visualiser l’équivalence ? Justifier la réponse.
e. Déterminer, par le calcul, la valeur du pHE à l’équivalence .
Vous aimerez peut-être aussi
- DosageDocument2 pagesDosagePhysique ChimiePas encore d'évaluation
- Serie D'exercices Sur C5 Et C6: IA Kédougou - Cellule Mixte Des Sciences Physiques - Terminale S 2019-2020Document4 pagesSerie D'exercices Sur C5 Et C6: IA Kédougou - Cellule Mixte Des Sciences Physiques - Terminale S 2019-2020kathyPas encore d'évaluation
- Fiches Exercices Titrages-2010Document3 pagesFiches Exercices Titrages-2010Daniel Parnor100% (1)
- Serie Acide Fort - Base Forte TS2Document3 pagesSerie Acide Fort - Base Forte TS2Amadou Oury DialloPas encore d'évaluation
- Série D'exercices N°10 - Sciences Physiques Dosage Acido Basique - Bac Sciences Exp (2011-2012) MR ALIBI ANOUAR 3Document8 pagesSérie D'exercices N°10 - Sciences Physiques Dosage Acido Basique - Bac Sciences Exp (2011-2012) MR ALIBI ANOUAR 3Tawfiq Weld EL Arbi75% (4)
- Reactions Acido BasiquesDocument3 pagesReactions Acido Basiquesh3r3t1kPas encore d'évaluation
- Serie Acide Fort Base Forte DosageDocument6 pagesSerie Acide Fort Base Forte DosageAmadou Oury DialloPas encore d'évaluation
- Série Autoprolyse de L'eau Produit Ionique PH D'une Solution - Acide Fort - Base Forte - 113943Document2 pagesSérie Autoprolyse de L'eau Produit Ionique PH D'une Solution - Acide Fort - Base Forte - 113943dememamebousso09Pas encore d'évaluation
- Transformation Liée À Des Réactions Acides Et Bases (WWW - Pc1.ma)Document21 pagesTransformation Liée À Des Réactions Acides Et Bases (WWW - Pc1.ma)Abderrazzak ElhaimerPas encore d'évaluation
- Acice Fort Base Forte Exercice 1Document8 pagesAcice Fort Base Forte Exercice 1Hamidou Diatta100% (1)
- Acidite D Un VinaigreDocument6 pagesAcidite D Un Vinaigreboudriat ahmedPas encore d'évaluation
- Cours - Chimie Dosage - Bac Technique (2010-2011) Elève RadhouaneDocument5 pagesCours - Chimie Dosage - Bac Technique (2010-2011) Elève RadhouaneTawfiq Weld EL ArbiPas encore d'évaluation
- Exo 54 - Dosage Acide Benzoique EDocument2 pagesExo 54 - Dosage Acide Benzoique EislameilhamiPas encore d'évaluation
- TleD - CH - L11 - Dosage Acido-BasiqueDocument10 pagesTleD - CH - L11 - Dosage Acido-BasiqueHamadi DialloPas encore d'évaluation
- Dosage 2Document3 pagesDosage 2Riadh Marouani100% (1)
- DOSAGE COLORIMETRIQUE Et Phmétrique Aspirine CorrigéDocument3 pagesDOSAGE COLORIMETRIQUE Et Phmétrique Aspirine Corrigétdi44617Pas encore d'évaluation
- Série 1 - Dosage Acido-BasiqueDocument2 pagesSérie 1 - Dosage Acido-BasiqueBoussetta ZouhaierPas encore d'évaluation
- Variation Du PH Au Cours Des Dosages Acide PDFDocument13 pagesVariation Du PH Au Cours Des Dosages Acide PDFAzizElheniPas encore d'évaluation
- SeÌ Rie 1 - Dosage Acido-BasiqueDocument2 pagesSeÌ Rie 1 - Dosage Acido-Basiqueb01554837Pas encore d'évaluation
- 26 Dosage 3Document3 pages26 Dosage 3Ilyes Ben Jemaa0% (1)
- Dosages Acide ConvertiDocument6 pagesDosages Acide ConvertiAbir SoujaaPas encore d'évaluation
- TPDosage Vinaigre CorDocument3 pagesTPDosage Vinaigre CorCamille LegavePas encore d'évaluation
- C7 Af BF WahabDiopDocument5 pagesC7 Af BF WahabDiopGaye BachirPas encore d'évaluation
- 2005 National Sujet Exo3 Chouxrouge 6 5ptsDocument4 pages2005 National Sujet Exo3 Chouxrouge 6 5ptsadnanPas encore d'évaluation
- Dosage Acide Base IndicDocument3 pagesDosage Acide Base IndicAs Ma50% (2)
- Serie 9 CHIMIE DES SOLUTIONS AQUEUSES 2Document2 pagesSerie 9 CHIMIE DES SOLUTIONS AQUEUSES 2deyinPas encore d'évaluation
- Serie 7 8 Acides Faibles Bases Faibles Solutions TamponsDocument10 pagesSerie 7 8 Acides Faibles Bases Faibles Solutions TamponsBrahim DahaiPas encore d'évaluation
- Série 1 - Dosage Acido-BasiqueDocument2 pagesSérie 1 - Dosage Acido-BasiqueAzdine MC100% (1)
- Dosage Acide BaseDocument4 pagesDosage Acide BaseSaifeddine Makni0% (1)
- Acides Faibles Et Bases Faibles Couples Acide-Base & Constante D'AciditeDocument5 pagesAcides Faibles Et Bases Faibles Couples Acide-Base & Constante D'AciditeNjuga Sene100% (1)
- TD #3 Chimie Analytique - 2 Année Pharmacie Batna2 - Dr. MaghchicheDocument4 pagesTD #3 Chimie Analytique - 2 Année Pharmacie Batna2 - Dr. Maghchicheromaissa benchadiPas encore d'évaluation
- Serie CoronaDocument15 pagesSerie CoronaJoséphine NancassePas encore d'évaluation
- Série Dosage PDFDocument8 pagesSérie Dosage PDFAya ArPas encore d'évaluation
- TP1 CorigeDocument2 pagesTP1 CorigeSamir MirPas encore d'évaluation
- 5 - Chap5-Dosages Et Calcul D'incertitude - Mode de Compatibilité PDFDocument63 pages5 - Chap5-Dosages Et Calcul D'incertitude - Mode de Compatibilité PDFoulaiPas encore d'évaluation
- TD-Acide Base - PH - WahabdiopDocument3 pagesTD-Acide Base - PH - WahabdiopNDEYE FATOU CISSE NIASSEPas encore d'évaluation
- Série DosageDocument8 pagesSérie DosageAicha Daou100% (1)
- Https0781948u.index Education - netpronoteFichiersExternes8fDocument5 pagesHttps0781948u.index Education - netpronoteFichiersExternes8fmka araPas encore d'évaluation
- 1cm3f8bgn 485037Document5 pages1cm3f8bgn 485037modou BADIANEPas encore d'évaluation
- HTTP://WWW - France Examen - Com/annales Bac Terminale Generale Scientifiq...Document3 pagesHTTP://WWW - France Examen - Com/annales Bac Terminale Generale Scientifiq...la physique selon le programme FrançaisPas encore d'évaluation
- Exercices C7 TSDocument2 pagesExercices C7 TSkondemamadousaidouPas encore d'évaluation
- TitrageDocument3 pagesTitrageelhijaziyoussefPas encore d'évaluation
- C8-Sol Tampon PDFDocument7 pagesC8-Sol Tampon PDFsKiroxPas encore d'évaluation
- Indicateurs ColorésDocument3 pagesIndicateurs ColorésAicha DiabyPas encore d'évaluation
- Série Réaction Acide BaseDocument5 pagesSérie Réaction Acide BaseScriblouPas encore d'évaluation
- TD Tampon 2024 LSLLDocument2 pagesTD Tampon 2024 LSLLAmadou Oury DialloPas encore d'évaluation
- Exercices 1transformations Liées À Des Réactions Acido - Basiques Dans Une Solution AqueuseDocument1 pageExercices 1transformations Liées À Des Réactions Acido - Basiques Dans Une Solution AqueuseAyoub ShaitPas encore d'évaluation
- Reactions Acide BaseDocument5 pagesReactions Acide BaseRitaj-Rayane KarimPas encore d'évaluation
- Titrage Du Vinaigre CorrectionDocument4 pagesTitrage Du Vinaigre CorrectionOstensible50% (2)
- NEW EVAL CHIMIE TC, D CrucialDocument3 pagesNEW EVAL CHIMIE TC, D Crucialb60032595Pas encore d'évaluation
- 2011 Liban Exo3 Sujet AciditeVin 4ptsDocument3 pages2011 Liban Exo3 Sujet AciditeVin 4ptsgrajzgrPas encore d'évaluation
- Dosages Acido Basique SM 3 TP2Document5 pagesDosages Acido Basique SM 3 TP2azertyiashmy1234Pas encore d'évaluation
- Série D'exercices - Sciences Physiques Dosage - Bac Math + SC Exp (2014-2015)Document4 pagesSérie D'exercices - Sciences Physiques Dosage - Bac Math + SC Exp (2014-2015)Serigne Abdou NiassePas encore d'évaluation
- TD PH COUPLE-ACIDE-BASE 2016Document13 pagesTD PH COUPLE-ACIDE-BASE 2016Oumar TraoréPas encore d'évaluation
- 5 Reactions Acido BasiquesDocument3 pages5 Reactions Acido BasiquesYouness SinePas encore d'évaluation
- TP Dosage PhmetriqueDocument1 pageTP Dosage PhmetriqueNesrine BouzidPas encore d'évaluation
- Ex 1Document6 pagesEx 1teghre chekhne El koryPas encore d'évaluation
- TP 1 Titrage PhmetriqueDocument3 pagesTP 1 Titrage Phmetriqueelhidhab2014Pas encore d'évaluation
- TP3 4 013Document4 pagesTP3 4 013Hanine HmidaPas encore d'évaluation
- 01 Chi TSDocument2 pages01 Chi TSHanine HmidaPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - Bac Math (2010-2011) MR Benjeddou RachidDocument5 pagesDevoir de Contrôle N°1 - Physique - Bac Math (2010-2011) MR Benjeddou RachidKarim RouagPas encore d'évaluation
- Lycee Rue Taieb Elmhiri Menzel Temime Cours-7: Forces Et Equilibre Sciences Physiques: Classes: 2 Sciences BaccariDocument6 pagesLycee Rue Taieb Elmhiri Menzel Temime Cours-7: Forces Et Equilibre Sciences Physiques: Classes: 2 Sciences BaccariHanine HmidaPas encore d'évaluation
- 11RL Bobine RéelleDocument1 page11RL Bobine RéelleHanine HmidaPas encore d'évaluation
- LumiereDocument2 pagesLumiereHanine HmidaPas encore d'évaluation
- 2010 Metropole Exo3 Sujet Genepac 4ptsDocument3 pages2010 Metropole Exo3 Sujet Genepac 4ptsla physique selon le programme FrançaisPas encore d'évaluation
- Livre Vers Le Bacc T2Document27 pagesLivre Vers Le Bacc T2Hanine Hmida50% (2)
- Devoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR Boussada 2Document5 pagesDevoir de Contrôle N°1 - Physique - 1ère AS (2010-2011) MR Boussada 2Hanine HmidaPas encore d'évaluation
- Devoir de Controle N°2: A - CHIMIE:8 PointsDocument3 pagesDevoir de Controle N°2: A - CHIMIE:8 PointsHanine HmidaPas encore d'évaluation
- 1cm4262ir 903092Document2 pages1cm4262ir 903092Ibrahima DioufPas encore d'évaluation
- Laplace TPDocument4 pagesLaplace TPHanine HmidaPas encore d'évaluation
- Les acides α aminés 00000000000000000000Document7 pagesLes acides α aminés 00000000000000000000Hanine HmidaPas encore d'évaluation
- dc2... 1ere ..... 2016Document3 pagesdc2... 1ere ..... 2016Hanine HmidaPas encore d'évaluation
- Mouvement Sinusoidal 2023Document2 pagesMouvement Sinusoidal 2023Hanine HmidaPas encore d'évaluation
- La Relation Fondamentale de Rotation - Estérification Essentiel À Retenir: 1-Cas D'un Point MatérielDocument2 pagesLa Relation Fondamentale de Rotation - Estérification Essentiel À Retenir: 1-Cas D'un Point MatérielboustakatbPas encore d'évaluation
- DS5 1bac 2Document6 pagesDS5 1bac 2Hanine HmidaPas encore d'évaluation
- Chapitre 7. Électromagnétisme. 7.1 Magnétisme. 7.1.1 AimantsDocument30 pagesChapitre 7. Électromagnétisme. 7.1 Magnétisme. 7.1.1 AimantsHanine HmidaPas encore d'évaluation
- Cours 6Document33 pagesCours 6Hanine HmidaPas encore d'évaluation
- Exercices Sur Le Magnetisme 1 Superposition de Champs - CompressDocument11 pagesExercices Sur Le Magnetisme 1 Superposition de Champs - CompressHanine HmidaPas encore d'évaluation
- Devoir de Synthèse N°1 - Sciences Physiques - 3ème Sciences Exp (2016-2017) MR Handoura NaceurDocument3 pagesDevoir de Synthèse N°1 - Sciences Physiques - 3ème Sciences Exp (2016-2017) MR Handoura NaceurHanine HmidaPas encore d'évaluation
- 2maes-C1-2019 2 INFDocument3 pages2maes-C1-2019 2 INFHanine HmidaPas encore d'évaluation
- Serie - Champ MagnetiqueDocument2 pagesSerie - Champ MagnetiqueHanine HmidaPas encore d'évaluation
- Cours Lycée Pilote - Chimie Les Amides Aliphatiques - Bac Sciences Exp (2011-2012) MR SfaxiDocument6 pagesCours Lycée Pilote - Chimie Les Amides Aliphatiques - Bac Sciences Exp (2011-2012) MR Sfaxiakre303650% (6)
- Composition Cem 1er Semestre 3eme 2013Document2 pagesComposition Cem 1er Semestre 3eme 2013falilou loPas encore d'évaluation
- 1cm420omd 81578Document1 page1cm420omd 81578el hadji malick DioumPas encore d'évaluation
- TeveninDocument8 pagesTeveninHanine HmidaPas encore d'évaluation
- Champmagnetique 6cDocument3 pagesChampmagnetique 6cHanine HmidaPas encore d'évaluation
- 3 EmeDocument2 pages3 EmeHanine HmidaPas encore d'évaluation
- CH 3 Me Info - 15Document1 pageCH 3 Me Info - 15Hanine HmidaPas encore d'évaluation
- HerbicideDocument74 pagesHerbicidengolo konePas encore d'évaluation
- Catalogue HoliMaker-F3DF 2023Document16 pagesCatalogue HoliMaker-F3DF 2023Théo ThaiPas encore d'évaluation
- Guide Terre ExcaveesDocument12 pagesGuide Terre ExcaveesAlae IdPas encore d'évaluation
- Licence 2 (Parcours Physique-Chimie) Année 2016-2017 TD2: Alcanes, Alcènes Et Alcynes Exercice 1Document3 pagesLicence 2 (Parcours Physique-Chimie) Année 2016-2017 TD2: Alcanes, Alcènes Et Alcynes Exercice 1Najimou Alade TidjaniPas encore d'évaluation
- Polymérisation en Émulsion GMP 18Document17 pagesPolymérisation en Émulsion GMP 18mennanesalaheddinePas encore d'évaluation
- Chim434 Synthese Asymetrique CoursDocument251 pagesChim434 Synthese Asymetrique Coursdidier kpadonouPas encore d'évaluation
- Cours Cosmetics Derniere VersionDocument211 pagesCours Cosmetics Derniere VersionSelma GhozaliPas encore d'évaluation
- TD GravimétrieDocument1 pageTD GravimétrieAbderrahmane AmzidPas encore d'évaluation
- Exposé de Français DrogueDocument6 pagesExposé de Français Drogueadama balloPas encore d'évaluation
- Prep Ech ICPDocument3 pagesPrep Ech ICPMamane ImranaPas encore d'évaluation
- Ressuage 2000Document3 pagesRessuage 2000Fa TehPas encore d'évaluation
- AminesDocument3 pagesAminesOumar TraoréPas encore d'évaluation
- Pfe Sameh Maizi .EAEEDocument157 pagesPfe Sameh Maizi .EAEEManong Sheguey100% (1)
- CTM 2 Dosage ÉtalonnageDocument3 pagesCTM 2 Dosage ÉtalonnageNatiPas encore d'évaluation
- Les Risques ProfessionnelsDocument63 pagesLes Risques Professionnelsbellahcene100% (3)
- st160065 PDFDocument84 pagesst160065 PDFYoucefPas encore d'évaluation
- Acide UriqueDocument1 pageAcide UriqueKadri BrahimPas encore d'évaluation
- Exercices Oxydo-RéductionDocument2 pagesExercices Oxydo-RéductionAlexis Baron100% (3)
- Gest Et Trait Des Décht Sol (C1+TD1) - M1GPEDocument19 pagesGest Et Trait Des Décht Sol (C1+TD1) - M1GPEIshak Zakaria MadaniPas encore d'évaluation
- Chapitre II - Chimie II - Equilibres ChimiquesDocument19 pagesChapitre II - Chimie II - Equilibres Chimiqueskim namjoonPas encore d'évaluation
- 4 Les Gisements HydrothermauxDocument5 pages4 Les Gisements HydrothermauxIbrahim Bichara AbdelkerimPas encore d'évaluation
- French Polishing MethodeDocument35 pagesFrench Polishing MethodeJobePas encore d'évaluation
- Chapitre 10 CeramiqueDocument3 pagesChapitre 10 Ceramiqueomar sahamoudiPas encore d'évaluation
- Instrukcja SpeedexDocument2 pagesInstrukcja SpeedexGabi RodriguezPas encore d'évaluation
- Monoxyde de DihydrogèneDocument5 pagesMonoxyde de DihydrogèneTestPas encore d'évaluation
- 2007 Controlab Equipement-GeneralDocument20 pages2007 Controlab Equipement-GeneralAli HamdanePas encore d'évaluation
- Chapitre I Matériaux PolymèresDocument9 pagesChapitre I Matériaux Polymèresimene.benyahiaPas encore d'évaluation
- Cours 1Document13 pagesCours 1Ikram GrPas encore d'évaluation
- E4.1 Étanchéité Toiture Terrasse Et Toiture InclinéeDocument90 pagesE4.1 Étanchéité Toiture Terrasse Et Toiture Inclinéesam hadPas encore d'évaluation
- Traitements de SurfaceDocument4 pagesTraitements de SurfaceOualidPas encore d'évaluation