Académique Documents
Professionnel Documents
Culture Documents
Chapitre 1 Un Niveau D'organisation Les Éléments Chimiques 2
Transféré par
Aymane JiraouiTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Chapitre 1 Un Niveau D'organisation Les Éléments Chimiques 2
Transféré par
Aymane JiraouiDroits d'auteur :
Formats disponibles
Chapitre 1 : Un niveau d’organisation : les éléments chimiques
- Produire et analyser différentes représentations graphiques de l’abondance des éléments chimiques (proportions)
dans l’Univers, la Terre, les êtres vivants.
- Reconnaître si l’équation d’une réaction nucléaire relève d’une fusion ou d’une fission
- Calculer le nombre de noyaux restants au bout de n demi-vies
- Estimer la durée nécessaire pour obtenir une certaine proportion de noyaux restants
- Utiliser une représentation graphique pour déterminer une demi-vie
- Utiliser une décroissance radioactive pour une datation (ex carbone 14)
LES ÉLÉMENTS CHIMIQUES DANS L’UNIVERS
1) La composition chimique de l’Univers
L’Univers est formé de 118 éléments chimiques différents.
L’hydrogène !!𝐻 est l’élément chimique le plus abondant : il représente à
lui seul près de 75 % des atomes présents dans l’Univers.
Sur Terre, on a observé 94 éléments chimiques à l’état
naturel, 24 autres ont été créés artificiellement.
2) La répartition des éléments chimiques
Les éléments sont répartis de manière inégale dans l’Univers : on trouve majoritairement de l’hydrogène et
de l’hélium dans les étoiles, tandis que la Terre est formée principalement d’oxygène et de silicium.
LES RÉACTIONS NUCLÉAIRES
1) La fusion, à l’origine de la synthèse des noyaux
Selon les théories les plus récentes, les premiers atomes ont été formés quelques
minutes après le « Big Bang ». L’Univers était alors extrêmement chaud (109 K) et
dense, les particules élémentaires se sont agglomérées pour former des noyaux
d’hydrogène, de deutérium ( "!𝐻 ou 𝐷) et d’hélium et de lithium. Cette réaction
nucléaire est appelée fusion nucléaire. Au cours d’une réaction de fusion, des noyaux
légers forment un noyau plus lourd en éjectant une particule et en libérant de
l’énergie.
L’élément le plus stable est le fer (Z = 26). Toutes les fusions nucléaires jusqu’au fer vont
donc libérer de l’énergie et, réciproquement, il faudra fournir de l’énergie pour créer les
éléments de numéro atomique supérieur à 26.
Pour cette raison, le fer est le dernier élément créé par le processus de fusion
« classique ». Tous les autres éléments sont créés lors de l’explosion des étoiles à leur fin
de vie.
D’après le cours du livre scolaire
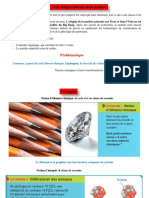
2) Les réactions nucléaires au cœur des étoiles
Les autres éléments sont formés au sein des étoiles, formées par accrétion des atomes créés lors du Big Bang.
Les noyaux légers fusionnent et produisent des noyaux plus lourds. On y trouve ainsi plusieurs éléments
comme l’oxygène (Z = 8), le carbone (Z = 6), mais aussi des noyaux plus lourds comme le fer (Z = 26).
Sous l’impact de neutrons ou d’autres particules légères,
certains noyaux se cassent : c’est la fission. Au cours d’une telle
réaction, des noyaux lourds se cassent en deux noyaux plus
légers sous l’impact d’un neutron ou d'un proton. La réaction
s’accompagne de l’éjection d’une particule et libère de l’énergie.
Ces éléments chimiques sont dispersés à la fin de la vie de l’étoile.
DÉSINTÉGRATION DES NOYAUX RADIOACTIFS
1) La radioactivité
Certains noyaux sont instables : on dit qu’ils sont radioactifs.
La radioactivité est un phénomène naturel, qui résulte de
la transmutation d’un noyau en un autre. Ainsi, les désintégrations
successives ont contribué à la formation des 94 éléments
chimiques que l’on trouve sur Terre.
La radioactivité est aléatoire, inéluctable, irréversible, spontanée et indépendante de la substance dans
laquelle le noyau radioactif se trouve.
2) Évolution du nombre de noyaux et demi-vie
La population de noyaux d’un échantillon décroît au cours du temps, elle est divisée par deux au bout d’une
durée appelée « demi-vie ».
La courbe ci-contre représente l’évolution du nombre N de noyaux radioactifs en fonction du temps t. La
désintégration suit une loi mathématique de décroissance.
N0 représente le nombre de noyaux radioactifs à l’instant t0 (origine des dates) ; t1/2 représente la demi-vie.
D’après le cours du livre scolaire
Vous aimerez peut-être aussi
- Fermions: Les Grands Articles d'UniversalisD'EverandFermions: Les Grands Articles d'UniversalisPas encore d'évaluation
- Chapitre 1Document3 pagesChapitre 1ykwt7nhrhhPas encore d'évaluation
- Suite Chap1 - 27sept23 2Document2 pagesSuite Chap1 - 27sept23 2orlaneleguellec0809Pas encore d'évaluation
- L'Origine Des Éléments ChimiquesDocument1 pageL'Origine Des Éléments ChimiquesJustine CelantePas encore d'évaluation
- Chapitre 1 Un Niveau D Organisation Les Elements ChimiquesDocument56 pagesChapitre 1 Un Niveau D Organisation Les Elements ChimiquespokinalaPas encore d'évaluation
- Origine ActiviteDocument3 pagesOrigine ActiviteNagwa ElimamPas encore d'évaluation
- Origine ActiviteDocument3 pagesOrigine ActiviteNagwa ElimamPas encore d'évaluation
- Chapitre 1Document8 pagesChapitre 1fortrieceliaPas encore d'évaluation
- Un Niveau D'organisation: Les Éléments Chimiques: AristoteDocument10 pagesUn Niveau D'organisation: Les Éléments Chimiques: AristoteWadih MansourPas encore d'évaluation
- 1es Chap 1 103Document5 pages1es Chap 1 103zbp8ntntqwPas encore d'évaluation
- La NucléosynthèseDocument2 pagesLa NucléosynthèseSalif KouyatePas encore d'évaluation
- FrancioniDocument8 pagesFrancionikenzatazi2007Pas encore d'évaluation
- Chapitre 01 Éléments Chimiques Classe de Première Enseignement ScientifiqueDocument8 pagesChapitre 01 Éléments Chimiques Classe de Première Enseignement ScientifiqueAlix FaucretPas encore d'évaluation
- Expose de Technique Et Stockage de L'energie Groupe 3Document17 pagesExpose de Technique Et Stockage de L'energie Groupe 3Enoch KazimotoPas encore d'évaluation
- conferences_2007_MOURSLIDocument12 pagesconferences_2007_MOURSLIsaidalihachim0000Pas encore d'évaluation
- Chapitre 3 Les Éléments ChimiqueDocument3 pagesChapitre 3 Les Éléments ChimiqueAymen Ben BrahimPas encore d'évaluation
- 1 PT1 NucléosynthèseDocument4 pages1 PT1 NucléosynthèseEyhoxPas encore d'évaluation
- GéologieDocument105 pagesGéologieKoogPas encore d'évaluation
- 1ES Acvivité 1 Eléments ChimqiuesDocument3 pages1ES Acvivité 1 Eléments ChimqiuesSidhoum SidPas encore d'évaluation
- Chapitre N°1 CoursDocument8 pagesChapitre N°1 Coursmimi abouryPas encore d'évaluation
- Symphonie ChimiqueDocument43 pagesSymphonie ChimiqueArthur MaréchalPas encore d'évaluation
- Chapitre 1 Les Éléments ChimiquesDocument7 pagesChapitre 1 Les Éléments Chimiquesoliviacali188Pas encore d'évaluation
- Poussieres Detoiles CompressDocument7 pagesPoussieres Detoiles CompressAïcha BenhadiPas encore d'évaluation
- Activité Réaction NucléaireDocument4 pagesActivité Réaction NucléairesdfghjPas encore d'évaluation
- 1 Elements ChimiquesDocument4 pages1 Elements ChimiquesNaji AnasPas encore d'évaluation
- Fission Et FusionDocument3 pagesFission Et FusionGianni cabelloPas encore d'évaluation
- Cours Thème 1 Une Longue Histoire de La MatièreDocument9 pagesCours Thème 1 Une Longue Histoire de La MatièreAudrey100% (1)
- La Radioactivité (Modifié)Document19 pagesLa Radioactivité (Modifié)IssamLfPas encore d'évaluation
- Développement TPEDocument48 pagesDéveloppement TPEbatchouPas encore d'évaluation
- Support de Cours PH244 Radioactivité 2021 2022Document16 pagesSupport de Cours PH244 Radioactivité 2021 2022Ghislain Desire EtapePas encore d'évaluation
- Progression-Enseig ScientDocument5 pagesProgression-Enseig Scient1ere21 CHERKAOUI FarisPas encore d'évaluation
- Act Info Diversite Et Origine Des Elements Chimiques 1Document6 pagesAct Info Diversite Et Origine Des Elements Chimiques 1Jeune KirlingerPas encore d'évaluation
- Thème 1 - Activité 01 (1) 2Document3 pagesThème 1 - Activité 01 (1) 2qh6xhd65fyPas encore d'évaluation
- cours complet phy des reacteurs-27-58Document32 pagescours complet phy des reacteurs-27-58Malak SoulaPas encore d'évaluation
- Seconde Univers Chap3 Chapitre 3Document5 pagesSeconde Univers Chap3 Chapitre 3Oumayma MansourPas encore d'évaluation
- 01 Un Niveau d' Organisation Les Éléments Chimiques P3Document2 pages01 Un Niveau d' Organisation Les Éléments Chimiques P3alexandra sPas encore d'évaluation
- Les Neutrinos Des Particules SurprenantesDocument16 pagesLes Neutrinos Des Particules SurprenantesSALIOU FALLPas encore d'évaluation
- Enseignement Scientifique CoursDocument7 pagesEnseignement Scientifique Courstaboulet.au.fromagePas encore d'évaluation
- ES Activité 2Document1 pageES Activité 2Nora LagouPas encore d'évaluation
- Poly AtomistiqueDocument21 pagesPoly AtomistiqueOussam OuadidiPas encore d'évaluation
- 01 - 1ère-Activité1 - 2-Juste Les Questions-Correction'Document2 pages01 - 1ère-Activité1 - 2-Juste Les Questions-Correction'Youldes GhoumaPas encore d'évaluation
- I.1 Un Niveau D'organisationDocument15 pagesI.1 Un Niveau D'organisationSabine BenichouPas encore d'évaluation
- 1ES - Correction Exos Mdu ManuelDocument2 pages1ES - Correction Exos Mdu ManuelmeryemPas encore d'évaluation
- Energie Fossile Et Energie NucleaireDocument10 pagesEnergie Fossile Et Energie NucleaireSicke LunkomoPas encore d'évaluation
- Réaction Nucléaire Provoquée PDF - Décembre2023Document3 pagesRéaction Nucléaire Provoquée PDF - Décembre2023m3861650Pas encore d'évaluation
- Cours de GeochimieDocument33 pagesCours de GeochimieHamed BathilyPas encore d'évaluation
- WWW - Futura Sciences - Com L Energie Nucleaire de A A Z 16-09-2002Document11 pagesWWW - Futura Sciences - Com L Energie Nucleaire de A A Z 16-09-2002giada19Pas encore d'évaluation
- Énérgie Nucléaire ExposéDocument2 pagesÉnérgie Nucléaire Exposéouhabi fatihaPas encore d'évaluation
- Étoiles 1Document2 pagesÉtoiles 1odahdal52Pas encore d'évaluation
- Cours 1 - Décroissance Radioactive PDFDocument7 pagesCours 1 - Décroissance Radioactive PDFMoufida ZouaghiPas encore d'évaluation
- Séquence 1 Éléments Chimiques Élèves 3Document9 pagesSéquence 1 Éléments Chimiques Élèves 3Hugo Cortot100% (1)
- TD Nucleaire 201112 SpanoDocument5 pagesTD Nucleaire 201112 SpanoSAid LeHoufi100% (1)
- ChimieDocument45 pagesChimieapi-446600404Pas encore d'évaluation
- Les Matieres Radioactives Et L Energie Nucleaire Cours 2Document5 pagesLes Matieres Radioactives Et L Energie Nucleaire Cours 2Achraf NatikPas encore d'évaluation
- Polycopie PDFDocument91 pagesPolycopie PDFMaroua SekkoutPas encore d'évaluation
- Rayonnemnt RadioactifDocument8 pagesRayonnemnt RadioactifBig juniorPas encore d'évaluation
- 8 - Les Réactions NucléairesDocument20 pages8 - Les Réactions Nucléairesngz.h.phucPas encore d'évaluation
- Radioactivité CoursDocument6 pagesRadioactivité CoursNOUSSAPas encore d'évaluation
- Le SoleilDocument5 pagesLe SoleilAbdellah haddadiPas encore d'évaluation
- Activ 1-2 - Interaction Lumière Matière - ADocument3 pagesActiv 1-2 - Interaction Lumière Matière - AguillaumeboblozePas encore d'évaluation
- Images Et Couleurs - Fiche de Révision AfterclasseDocument7 pagesImages Et Couleurs - Fiche de Révision AfterclasseAymane JiraouiPas encore d'évaluation
- Generalites Sur Les Fonctions Exercices Corriges 1 2 PDF PDF Fonction Monotone Fonction (Mathématiques) 2Document1 pageGeneralites Sur Les Fonctions Exercices Corriges 1 2 PDF PDF Fonction Monotone Fonction (Mathématiques) 2Aymane JiraouiPas encore d'évaluation
- Correction Cellule Structure Complexe' ' 'Document6 pagesCorrection Cellule Structure Complexe' ' 'Aymane JiraouiPas encore d'évaluation
- La Vision Et L'image - 1S - Cours Physique-Chimie - KartableDocument20 pagesLa Vision Et L'image - 1S - Cours Physique-Chimie - KartableAymane JiraouiPas encore d'évaluation
- Correction Tp4 MeioseDocument2 pagesCorrection Tp4 MeioseAymane JiraouiPas encore d'évaluation
- Lecture Linéaire N 4 Le M. de F. Acte III, 10 2Document3 pagesLecture Linéaire N 4 Le M. de F. Acte III, 10 2Aymane Jiraoui100% (1)
- Bilan Chapitre 2 La Replication de l' Adn Et Variabilite GenetiqueDocument3 pagesBilan Chapitre 2 La Replication de l' Adn Et Variabilite GenetiqueAymane JiraouiPas encore d'évaluation
- Fonction Traiter Conversions NumeriquesDocument5 pagesFonction Traiter Conversions NumeriquesAymane JiraouiPas encore d'évaluation
- Le Systeme Musculaire Resume de Cours MaDocument1 pageLe Systeme Musculaire Resume de Cours MaAymane JiraouiPas encore d'évaluation
- Lecture Linéaire N 4 Le M. de F. Acte III, 10 2Document3 pagesLecture Linéaire N 4 Le M. de F. Acte III, 10 2Aymane Jiraoui100% (1)
- LDP Ses 2depdfDocument54 pagesLDP Ses 2depdfAymane JiraouiPas encore d'évaluation
- R L ValleeDocument4 pagesR L ValleeLionel ElyansunPas encore d'évaluation
- GEOCHIMIEDocument32 pagesGEOCHIMIEGilchrist Willy Adopo100% (1)
- CH 8 Radioactivite Reactions NucleairesDocument4 pagesCH 8 Radioactivite Reactions Nucleaireslouis jasonPas encore d'évaluation
- Modèle de LatomeDocument3 pagesModèle de Latomeعبد الفتاح الشقراويPas encore d'évaluation
- Burkina 2016 Physique Serie C E 1er TourDocument4 pagesBurkina 2016 Physique Serie C E 1er TourSawadogo LassinaPas encore d'évaluation
- Radioactivite Cours Ls-1Document31 pagesRadioactivite Cours Ls-1Arfa BouchtaPas encore d'évaluation
- Capture D'écran . 2022-06-08 À 17.26.29Document21 pagesCapture D'écran . 2022-06-08 À 17.26.29FirstofalltimePas encore d'évaluation
- 6 Noyaux Et Énergie ConvertiDocument7 pages6 Noyaux Et Énergie ConvertiKawtar kawtarPas encore d'évaluation
- Annales D1RP1S1Document2 pagesAnnales D1RP1S1bouckanellyPas encore d'évaluation
- CentraleDocument2 pagesCentralePhobos Elfa100% (1)
- TD Proba-Stat Tronc Commun Polytech ClermontDocument2 pagesTD Proba-Stat Tronc Commun Polytech Clermonthamza dahbiPas encore d'évaluation
- Série D'exercices: Éléments, Atomes, Classification Périodique Des Éléments - 2nd - SunudaaraDocument1 pageSérie D'exercices: Éléments, Atomes, Classification Périodique Des Éléments - 2nd - SunudaarafodekambalouPas encore d'évaluation
- Cours 207 Serie 1 PDFDocument88 pagesCours 207 Serie 1 PDFYahya Hamdani100% (1)
- Le Dipôle RC: Fiches de RevisionDocument8 pagesLe Dipôle RC: Fiches de RevisionYoussef WerfelliPas encore d'évaluation
- Initiation À La Physique QuantiqueDocument42 pagesInitiation À La Physique Quantiquekaishark666Pas encore d'évaluation
- Papiers Millimetres 2Document4 pagesPapiers Millimetres 2KarimBenA100% (1)
- La TerreDocument2 pagesLa TerreHanine HmidaPas encore d'évaluation
- Chimie Organique 1Document54 pagesChimie Organique 1Hélène MariePas encore d'évaluation
- Centre Universitaire de Ghardaïa Institut Des Sciences de La Nature Et de La VieDocument1 pageCentre Universitaire de Ghardaïa Institut Des Sciences de La Nature Et de La Viesoufiane souf100% (1)
- Chimie TechinfoDocument175 pagesChimie TechinfoBen Salem NoureddinePas encore d'évaluation
- Astronomie SolaireDocument20 pagesAstronomie SolaireClayssaNelPas encore d'évaluation
- Devoir 2 Hikma 2020 2bac SM Prof - Kraidy (WWW - Pc1.ma)Document4 pagesDevoir 2 Hikma 2020 2bac SM Prof - Kraidy (WWW - Pc1.ma)Majed Gharib100% (1)
- Combustion: (1 Partie)Document32 pagesCombustion: (1 Partie)Mourad AmiourPas encore d'évaluation
- Sciences-Physique S1-S3-1er-gr 2007Document4 pagesSciences-Physique S1-S3-1er-gr 2007Doro CisséPas encore d'évaluation
- Cours de Physique Generale Tran Minh Tam UniversiteDocument409 pagesCours de Physique Generale Tran Minh Tam UniversiteStandardPas encore d'évaluation
- Physique Cours 2Document8 pagesPhysique Cours 2louise bertrandPas encore d'évaluation
- Rihab Exercices Corrigés RadioactivitéDocument18 pagesRihab Exercices Corrigés RadioactivitéKHALIFA EL HARFIPas encore d'évaluation
- Leçon Chapitre 1Document59 pagesLeçon Chapitre 1azerazerazerPas encore d'évaluation
- Diagraphies Et Interprétation KM 2020Document50 pagesDiagraphies Et Interprétation KM 2020Rachelter Hr100% (1)
- Cours IRMDocument60 pagesCours IRMjean dupontPas encore d'évaluation