Académique Documents
Professionnel Documents
Culture Documents
Grandeurs Physiques Liees A La Quantite de Matiere Resume de Cours 3
Transféré par
Jonathan MURETTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Grandeurs Physiques Liees A La Quantite de Matiere Resume de Cours 3
Transféré par
Jonathan MURETDroits d'auteur :
Formats disponibles
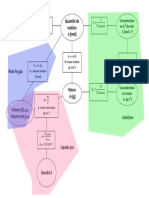
Fiche de revision n°1 Prof : AIT-ZAABOUN Aissam
1er BAC SM & SE F
A température constante, pour
Les relation pour calculer
une quantité de matière donnée
La quantité de matière
de gaz : P×V = constante T(K) = t (°C) + 273
NA : le nombre d'Avogadro
𝑵 NA= 6,02.1023 mol-1
Loi de Boyle Mariote Echelle Kelvin 𝒏=
𝑵𝑨 N : nombre d’entités
Les grandeurs
Cst du gaz parfait M : masse molaire en
Volume (m3) = 8.314 (SI)
𝒎
𝒏= (g/mol)
Tempé - physique liées à la 𝑴 m : la masse en (g)
PxV=nxRxT
quantité de matière
rature (K)
𝒎 𝝆 ∗ 𝑽 𝒅 ∗ 𝝆𝒆𝒂𝒖 ∗ 𝑽
Pression (Pa) Quantité de 𝒏 𝑿 = = =
matière (mol) 𝑴 𝑿 𝑴 𝑿 𝑴 𝑿
𝒎
𝝆= : La masse volumique (𝑘𝑔. 𝑚−3 )
la quantité de matière d’un gaz 𝑽
Relation des gaz parfaits
𝝆
𝒅= : La densité d'un corps
𝑽 VM : Le volume molaire 𝝆𝒆𝒂𝒖
𝒏 𝑿 = (L/mol )
𝑽𝑴
𝑴 𝑿 V : le volume du gaz (L)
𝒅=
𝟐𝟗
𝑪(𝑿) : La concentration molaire (mol/L)
Densité d'un gaz 𝑪𝒎 𝑿 . 𝑽
par rapport à l'air la quantité de matière
𝒏 𝑿 = 𝑪 𝑿 .𝑽 = 𝑪𝒎 : La concentration massique (g/L)
dans une solution 𝑴 𝑿 V : le volume de solution en (L)
Vous aimerez peut-être aussi
- Révision - Chimie - 2BACBiof, PR MOUJAHID YoussefDocument37 pagesRévision - Chimie - 2BACBiof, PR MOUJAHID YoussefBIKOLA FFPas encore d'évaluation
- Chapitre 3 Les Grandeurs Physiques Liées À La Quantité de MatièreDocument3 pagesChapitre 3 Les Grandeurs Physiques Liées À La Quantité de Matièreateich simohamedPas encore d'évaluation
- Carte Mentale Mole Complétée - Physique-ChimieDocument1 pageCarte Mentale Mole Complétée - Physique-ChimieDodiePas encore d'évaluation
- YahyaDocument2 pagesYahyapfePas encore d'évaluation
- Exercice Gravitation Systeme Solaire Poids MasseDocument3 pagesExercice Gravitation Systeme Solaire Poids MasseHamza Derar0% (1)
- Oscilloscope Tension Alternative CorrigeDocument2 pagesOscilloscope Tension Alternative CorrigeT MaursPas encore d'évaluation
- Modelisation Des Transformations Chimiques Bilan de La Matiere Exercices Non Corriges 1Document3 pagesModelisation Des Transformations Chimiques Bilan de La Matiere Exercices Non Corriges 1Jou mohammedPas encore d'évaluation
- Interactions Et Champs: Chapitre 8Document5 pagesInteractions Et Champs: Chapitre 8Aymen Ben BrahimPas encore d'évaluation
- TP ChimieDocument14 pagesTP ChimieZohair RamiPas encore d'évaluation
- Controle 1 S2 3APIC Mod1 (WWW - Pc1.ma)Document3 pagesControle 1 S2 3APIC Mod1 (WWW - Pc1.ma)Mohamed FLPas encore d'évaluation
- I.3.4 TP Structure de L'atomeDocument2 pagesI.3.4 TP Structure de L'atomevaldx100% (1)
- Polycopie Optique MokhtariDocument54 pagesPolycopie Optique MokhtarihubfriPas encore d'évaluation
- Titrage Avec Suivi ColorimetriqueDocument3 pagesTitrage Avec Suivi Colorimetriquemohammed younes100% (1)
- Contrôle 1 PR - ELANSARI SMDocument2 pagesContrôle 1 PR - ELANSARI SMHassan Dib100% (1)
- Livre Physique-Chimie 2ACDocument51 pagesLivre Physique-Chimie 2ACHASSANPas encore d'évaluation
- Synthese Des Especes Chimiques Exercices Non Corriges 1Document2 pagesSynthese Des Especes Chimiques Exercices Non Corriges 1Hema Eddine Alkhalil100% (1)
- Cour-1-La DissolutionDocument2 pagesCour-1-La DissolutionSmaali Faouzi SmaaliPas encore d'évaluation
- Lecon Phy 8Document4 pagesLecon Phy 8ahmed soussiPas encore d'évaluation
- Progression - Physique-Chimie 4emeDocument1 pageProgression - Physique-Chimie 4emeLassene BambaPas encore d'évaluation
- Examen National Physique Chimie Sciences Maths 2010 Normale SujetDocument8 pagesExamen National Physique Chimie Sciences Maths 2010 Normale SujetŤăhã ÊìîPas encore d'évaluation
- Grandeurs Physiques Liees A La Quantite de Matiere Cours 1 4Document3 pagesGrandeurs Physiques Liees A La Quantite de Matiere Cours 1 4Lucifer MorningstarPas encore d'évaluation
- Carte Mentale Cohésion de La MatièreDocument1 pageCarte Mentale Cohésion de La MatièreHellPas encore d'évaluation
- Les Diagramme D'equilibre (Solide-Liquide)Document10 pagesLes Diagramme D'equilibre (Solide-Liquide)Said BennayaPas encore d'évaluation
- 1-Verreries: F4: Matériels de ChimieDocument14 pages1-Verreries: F4: Matériels de ChimieFd MtPas encore d'évaluation
- TP N°18 MODELISER UNE SOURCE REELLE DE TENSION 2022Document8 pagesTP N°18 MODELISER UNE SOURCE REELLE DE TENSION 2022Cthulhu ClassePas encore d'évaluation
- Cours Pr. Hicham Mahajar Pr. Youssef TabitDocument7 pagesCours Pr. Hicham Mahajar Pr. Youssef TabitMohamed JaadiPas encore d'évaluation
- Chapitre I 1ère Partie Structure de La Matière-Chapitre 1Document5 pagesChapitre I 1ère Partie Structure de La Matière-Chapitre 1Assia IhaddadenePas encore d'évaluation
- Série Chim 3Document2 pagesSérie Chim 3Aissam brqPas encore d'évaluation
- Rappel ElectrostatiqueDocument14 pagesRappel ElectrostatiqueAbdelhamid ElmadaniPas encore d'évaluation
- c2 1bac Biof - Les Grandeurs Liées À La Quantité de Matière Prof - Sbiro (WWW - Pc1.ma) PDFDocument2 pagesc2 1bac Biof - Les Grandeurs Liées À La Quantité de Matière Prof - Sbiro (WWW - Pc1.ma) PDFHAMADA1972100% (2)
- CR 1 - LA DISSOLUTION DANS L'EAUDocument2 pagesCR 1 - LA DISSOLUTION DANS L'EAUanas saidiPas encore d'évaluation
- Résumé-FonCtions - 2BAC-SCDocument1 pageRésumé-FonCtions - 2BAC-SCAbde Aitoutbib100% (1)
- Equilibre Deux ForceDocument5 pagesEquilibre Deux Forcesimo lamePas encore d'évaluation
- C6Chim - Titrages - Exos - Ph&conduct&color PDFDocument9 pagesC6Chim - Titrages - Exos - Ph&conduct&color PDFAzizElheniPas encore d'évaluation
- Contrôle N°1 Semestre 1 Physique Tronc Commun Biof SCDocument2 pagesContrôle N°1 Semestre 1 Physique Tronc Commun Biof SCfayssalfayssal487100% (1)
- Cours de Physique Chimie Avec Les Exercices Et Les Solutions SemestreDocument132 pagesCours de Physique Chimie Avec Les Exercices Et Les Solutions SemestreMicasa- sama100% (1)
- Concentration Et Solutions Électrolytiques: Exercice 1Document9 pagesConcentration Et Solutions Électrolytiques: Exercice 1king of DarknessPas encore d'évaluation
- 1 Adaptation D'un Générateur À Un RécepteurDocument6 pages1 Adaptation D'un Générateur À Un RécepteurFEGARYPas encore d'évaluation
- CHP 1 Lois de NewtonDocument11 pagesCHP 1 Lois de NewtonSaad Filali Oujdi100% (1)
- IE2005meca3 3Document2 pagesIE2005meca3 3Mofid PCPas encore d'évaluation
- Devoir 3 Modele 2 Physique Chimie 2ac Semestre 2Document1 pageDevoir 3 Modele 2 Physique Chimie 2ac Semestre 2hamza manafPas encore d'évaluation
- 1ere S - Chimie - Chapitre 1 - La Mole - Partie 1Document21 pages1ere S - Chimie - Chapitre 1 - La Mole - Partie 1Fidel ْ100% (1)
- Mesure Du Volume Des Solides Et Des Liquides Activites 2Document3 pagesMesure Du Volume Des Solides Et Des Liquides Activites 2Sassi Lassaad0% (1)
- 4 5890728413047557017 PDFDocument35 pages4 5890728413047557017 PDFSamuel Loïc100% (1)
- Carte Mentale Atome DétailléeDocument1 pageCarte Mentale Atome DétailléeCharline Scharre100% (1)
- Activité 1 La Maille CristallineDocument2 pagesActivité 1 La Maille Cristallinedoums0% (1)
- Préparation de Solution de Laboratoire: C R M E F R S KDocument53 pagesPréparation de Solution de Laboratoire: C R M E F R S KOussama ZnPas encore d'évaluation
- Annales Physique Chimie CNC Concours National Commun Marocain PDFDocument7 pagesAnnales Physique Chimie CNC Concours National Commun Marocain PDFAz-eddine KaibaPas encore d'évaluation
- Cours Thermodynamique Physique - Chap0Document26 pagesCours Thermodynamique Physique - Chap0الدعم الجامعيPas encore d'évaluation
- Fiche Technique 7-ConductimetrieDocument2 pagesFiche Technique 7-ConductimetrieYassir RochdPas encore d'évaluation
- SMPC s2 CHP 2Document31 pagesSMPC s2 CHP 2Abdelhakim BailalPas encore d'évaluation
- CM4 Réaction ChimiqueDocument16 pagesCM4 Réaction ChimiqueSemaya SahsahPas encore d'évaluation
- Les Trois Etats - 1 AC PDFDocument3 pagesLes Trois Etats - 1 AC PDFaznag hicham100% (1)
- Equilibre D Un Corps Sous L Action de 2 Forces Cours 1Document3 pagesEquilibre D Un Corps Sous L Action de 2 Forces Cours 1zakariaePas encore d'évaluation
- Correction de La Série N°4 de MPM - 2020-2021-FacultatifDocument7 pagesCorrection de La Série N°4 de MPM - 2020-2021-FacultatifMounirPas encore d'évaluation
- Python Exemple 3Document2 pagesPython Exemple 3Lazhar BOUCHAOURPas encore d'évaluation
- Resume PC Option SVTDocument33 pagesResume PC Option SVTHiba Naji100% (1)
- Chimie Resumé Grandeur Liee A La Quantite de Matiere PDFDocument2 pagesChimie Resumé Grandeur Liee A La Quantite de Matiere PDFKarimBenA100% (14)
- Exercice Thermo Pcsi ProblèmeDocument2 pagesExercice Thermo Pcsi ProblèmeTipeX McPas encore d'évaluation
- TD1 TM 2022Document13 pagesTD1 TM 2022Section E GP100% (1)
- Benghalia Meryem AmalDocument178 pagesBenghalia Meryem AmalFATIMA EL KRIMAIPas encore d'évaluation
- Protocole CristalDocument7 pagesProtocole CristalLanja IvogneaPas encore d'évaluation
- Exam 1 ThermDocument2 pagesExam 1 ThermMahfoud OmarPas encore d'évaluation
- VolumetrieDocument9 pagesVolumetriebounegabPas encore d'évaluation
- TSGC TMGC Thermodynamique-De-BaseDocument81 pagesTSGC TMGC Thermodynamique-De-BaseAmine benjmiaPas encore d'évaluation
- BCH 211 Chromato-1Document6 pagesBCH 211 Chromato-1jacques KUEVI-AKOEPas encore d'évaluation
- Perméation GazeuseDocument19 pagesPerméation GazeuseKrim Issam Eddine100% (1)
- La Geometrie de Quelques Molecules Serie D Exercices 1Document4 pagesLa Geometrie de Quelques Molecules Serie D Exercices 1Hicham HichamPas encore d'évaluation
- Fabrication Du PlastiqueDocument3 pagesFabrication Du PlastiquealexandroPas encore d'évaluation
- Bac Blanc N2 Corr Ex3Document1 pageBac Blanc N2 Corr Ex3la physique selon le programme FrançaisPas encore d'évaluation
- ÜüüüDocument2 pagesÜüüüRamboAkkkoPas encore d'évaluation
- Cohésion Solide MoléculairesDocument2 pagesCohésion Solide MoléculairesSimonPas encore d'évaluation
- Synthèse2018 2019Document8 pagesSynthèse2018 2019Serine DebbihPas encore d'évaluation
- II - Amplificateurs OptiqueDocument6 pagesII - Amplificateurs OptiqueJoffin Soume100% (1)
- Correction TD 6 - 4P050Document14 pagesCorrection TD 6 - 4P050badid SusskindPas encore d'évaluation
- Chimie EvaluationDocument8 pagesChimie EvaluationMBOTAKE LawsonPas encore d'évaluation
- Fabrication Du Chlorure de BenzoyleDocument3 pagesFabrication Du Chlorure de BenzoyleAnis BouhousPas encore d'évaluation
- Thermodynamique 2Document7 pagesThermodynamique 2penbird97Pas encore d'évaluation
- CHimie Terminale S Tome 1Document49 pagesCHimie Terminale S Tome 1Anna Guéye88% (8)
- Module 2Document33 pagesModule 2oclgi.oouPas encore d'évaluation
- 8-2-Chapter II - Transfert Thermique en Régime Permanent-Unidimensionnel 18-12-2018Document15 pages8-2-Chapter II - Transfert Thermique en Régime Permanent-Unidimensionnel 18-12-2018Hkbv GjvcPas encore d'évaluation
- Corrigé Série N°1Document7 pagesCorrigé Série N°1simo GriPas encore d'évaluation
- TD1 ThermochimieDocument2 pagesTD1 ThermochimieHamza Hamizo100% (1)
- Correction - TD SM2 Liaison CovalenteDocument11 pagesCorrection - TD SM2 Liaison CovalenteLo MomathPas encore d'évaluation
- TD PCE DecourDocument122 pagesTD PCE DecourGildo TamenePas encore d'évaluation
- Cours Opu Ii - M 1 GCDocument45 pagesCours Opu Ii - M 1 GCGhada19 Tiah100% (1)
- Concentration Massique-MolaireDocument2 pagesConcentration Massique-MolaireAmin Marshmello100% (1)
- La vie des abeilles: Prix Nobel de littératureD'EverandLa vie des abeilles: Prix Nobel de littératureÉvaluation : 4 sur 5 étoiles4/5 (41)
- Améliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesD'EverandAméliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesÉvaluation : 5 sur 5 étoiles5/5 (2)
- L'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)D'EverandL'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)Évaluation : 4 sur 5 étoiles4/5 (3032)
- Secrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieD'EverandSecrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieÉvaluation : 5 sur 5 étoiles5/5 (2)
- Le profilage au service du football: Démarche scientifique pour un recrutement et entraînements optimisésD'EverandLe profilage au service du football: Démarche scientifique pour un recrutement et entraînements optimisésPas encore d'évaluation
- Électrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsD'EverandÉlectrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Semer avec succès pour rassembler avec abundance. Jardin organique et synergique: Calcul des meilleurs jours pour l'ensemencement de chaque légumeD'EverandSemer avec succès pour rassembler avec abundance. Jardin organique et synergique: Calcul des meilleurs jours pour l'ensemencement de chaque légumePas encore d'évaluation
- Harmonisation Energétique des Personnes: Manuel de Curothérapie 2020D'EverandHarmonisation Energétique des Personnes: Manuel de Curothérapie 2020Évaluation : 4 sur 5 étoiles4/5 (8)
- Un régime quantiqueD'EverandUn régime quantiqueÉvaluation : 5 sur 5 étoiles5/5 (1)
- 20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsD'Everand20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsÉvaluation : 5 sur 5 étoiles5/5 (1)
- 160 ressources pour se lancer dans la vidéo quand on n’y connait rienD'Everand160 ressources pour se lancer dans la vidéo quand on n’y connait rienPas encore d'évaluation
- Transformez votre vie: Utilisez le pouvoir créateur qui est en vous pour construire votre vie à l'image de ce que vous voulez qu'elle soitD'EverandTransformez votre vie: Utilisez le pouvoir créateur qui est en vous pour construire votre vie à l'image de ce que vous voulez qu'elle soitÉvaluation : 4 sur 5 étoiles4/5 (14)
- Manuel de fabrication du savon: Je fabrique mes savons facilementD'EverandManuel de fabrication du savon: Je fabrique mes savons facilementÉvaluation : 5 sur 5 étoiles5/5 (4)
- Technologie automobile: Les Grands Articles d'UniversalisD'EverandTechnologie automobile: Les Grands Articles d'UniversalisPas encore d'évaluation
- Jus de Fruits et de Légumes Crus: 57 recettes faciles et un Guide Pratique Complet pour améliorer votre alimentation .: Santé, Vitalité et Minceur, avec ... ET DURABLEMENTD'EverandJus de Fruits et de Légumes Crus: 57 recettes faciles et un Guide Pratique Complet pour améliorer votre alimentation .: Santé, Vitalité et Minceur, avec ... ET DURABLEMENTPas encore d'évaluation
- L'Ombre à l'Univers: La structure des particules élémentaires XIIfD'EverandL'Ombre à l'Univers: La structure des particules élémentaires XIIfPas encore d'évaluation
- Approvisionnement et traitement de l’eau: Les Grands Articles d'UniversalisD'EverandApprovisionnement et traitement de l’eau: Les Grands Articles d'UniversalisPas encore d'évaluation
- Harmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020D'EverandHarmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020Évaluation : 2.5 sur 5 étoiles2.5/5 (3)
- Géologie de l'Amérique: Les Grands Articles d'UniversalisD'EverandGéologie de l'Amérique: Les Grands Articles d'UniversalisPas encore d'évaluation
- 500 secrets pour avoir un potager merveilleuxD'Everand500 secrets pour avoir un potager merveilleuxÉvaluation : 2 sur 5 étoiles2/5 (1)
- Enseigner une Langue Etrangère Par l’Apprentissage HybrideD'EverandEnseigner une Langue Etrangère Par l’Apprentissage HybridePas encore d'évaluation
- Le B.A.-Ba de la communication: Comment convaincre, informer, séduire ?D'EverandLe B.A.-Ba de la communication: Comment convaincre, informer, séduire ?Évaluation : 3 sur 5 étoiles3/5 (1)
- Puissance naturelles - Que faire si votre "meilleure partie" est en grève?: Puissance naturelles-améliorer les recours pour augmenter la virilité de la capacité à obtenir une érection de fermetéD'EverandPuissance naturelles - Que faire si votre "meilleure partie" est en grève?: Puissance naturelles-améliorer les recours pour augmenter la virilité de la capacité à obtenir une érection de fermetéÉvaluation : 3.5 sur 5 étoiles3.5/5 (3)