Académique Documents
Professionnel Documents
Culture Documents
Correction Benzene 3-4-5
Transféré par
serignesidisowTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Correction Benzene 3-4-5
Transféré par
serignesidisowDroits d'auteur :
Formats disponibles
1
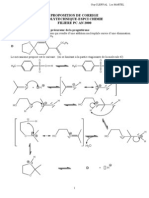
CORRECTION :
1. Trouvons la formule brute de B puis celle de A :
Soit B= CxHy → M(B)=12x+y=112 (1)
Or B contient en masse 6 fois plus de carbone que d’hydrogène : MB(C)=6MB(H)
→ 12x=6y→2x=y
112
Dans (1) : 12𝑥 + 2𝑥 = 112 → 14𝑥 = 112 → 𝑥 = = 8 𝑒𝑡 𝑦 = 2 × 8 = 16
14
FB(B)=C8H16
Par ailleurs, l’hydrogénation de A a donné B. Or l’hydrogénation c’est la fixation
d’atomes d’hydrogènes sur un composé insaturé à partir d’une réaction avec H :
M(B)-M(A)=112-106=6 ; comme M(H)=1g/mol donc il y a 6 atomes d’H qui se sont fixés
par hydrogénation
FB(A)=C8H10
2. Equation bilan de l’hydrogénation de A
C8H10+3H2 (Ni)→ C8H16
ELITE SCIENCE « LA SCIENCE AUTREMENT »
TEL : 77-106-98-79 / 76-312-52-24
2
3. FSD possibles de A
4. A donne par substitution un dérivé chloré contenant 25,2% de chlore.
a. Formule brute de C
Formule générale de C= C8H10-xClx ; M(C)=12x8+10-x+35,5x=106+34,5x
35,5𝑥 106+34,5𝑥
Rapport centésimal : = → 3550𝑥 = 2671,2 + 869,4𝑥
25,2 100
2671,2
→ 2680,6𝑥 = 2671,2 → 𝑥 = ≈1
2680,6
FB (C)=C8H9Cl
b. Equation de passage de A vers C
C8H10 + Cl2 (AlCl3) →C8H9Cl + HCl
5. FSD possibles de B et les nommer :
ELITE SCIENCE « LA SCIENCE AUTREMENT »
TEL : 77-106-98-79 / 76-312-52-24
3
6. A peut être obtenu par une réaction de Friedel et Craft par action du chlorure
d’éthyle (monochloroéthane) sur le benzène.
a. Conditions expérimentales : utilisation de catalyseur sous forme d’acide de
Lewis (AlX3 ou FeX3)
Equation-bilan : C6H6 + CH3CH2Cl (AlX3/FeX3)→ C8H10 + HX
b. Formule semi-développée de A C6H5-CH2-CH3 : éthylbenzène
c. FSD de B : C6H11-CH2-CH3 : éthylcyclohexane
Pour C, le Cl se fixe sur la position 1 (chlore commence par C) donc le groupe éthyl se
déplace : on aura donc 1, chloro 2, éthylbenzène ; 1, chloro 3, éthylbenzène ou
1, chloro 4, éthylbenzène
ELITE SCIENCE « LA SCIENCE AUTREMENT »
TEL : 77-106-98-79 / 76-312-52-24
4
CORRECTION :
1. Déduisons-en la nature du composé A : puisqu’il peut subir aussi bien une réaction
de substitution (bromation) et une réaction d’addition (hydrogénation) donc A est
un composé aromatique. Montrons qu’il s’agit d’une monobromation :
Formule générale du composé bromé : C8H10-xBrx
M=12x8+10-x+80x=106+79x
80𝑥 106+79𝑥
Rapport centésimal : = → 8000𝑥 = 4558 + 3397𝑥 → 4603𝑥 = 4558 →
43 100
4558
𝑥= ≈1
4603
Donc il s’agit d’une monobromation
2. Formules semi-développés de A
ELITE SCIENCE « LA SCIENCE AUTREMENT »
TEL : 77-106-98-79 / 76-312-52-24
5
3. B décolore l’eau de brome : B contient une double liaison caractéristique des
alcènes
4. Comme B est le styrène, donc A= éthylbenzène
5. Les dérivés monobromés sont au nombre de 3 car l’atome de brome a trois
possibilités de fixation par rapport au groupe éthyle (voir exercice précédent)
FSD : C6H5(Br)-CH2-CH3 : 1, bromo 2, éthylbenzène ; 1, bromo 3, éthylbenzène ou
1, bromo 4, éthylbenzène
ELITE SCIENCE « LA SCIENCE AUTREMENT »
TEL : 77-106-98-79 / 76-312-52-24
6
CORRECTION :
1. Formule brute du composé :
M=C6H6-xClx=12𝑥6 + 6 − 𝑥 + 35,5𝑥 = 78 + 34,5𝑥 = 147 → 34,5𝑥 = 69 → 𝑥 = 2
FB=C6H4Cl2
𝟑
Equation-bilan : C6H6+ Cl2 (AlCl3)→ C6H4Cl2+ HCl
𝟐
2. FSD et nom des isomères
3. Rendement de la réaction
7,8
Bilan molaire : n(C6H6)=n(C6H4Cl2) or n(C6H6)= = 0,1𝑚𝑜𝑙= n(C6H4Cl2)
78
Donc m(C6H4Cl2)=nxM=0,1x147=14,7g
𝑚𝑒 8,8
R= × 100 = × 100 = 𝟓𝟗, 𝟖𝟔%
𝑚𝑡 14,7
ELITE SCIENCE « LA SCIENCE AUTREMENT »
TEL : 77-106-98-79 / 76-312-52-24
Vous aimerez peut-être aussi
- Glucides: Les Grands Articles d'UniversalisD'EverandGlucides: Les Grands Articles d'UniversalisPas encore d'évaluation
- Semi ConducteurDocument38 pagesSemi ConducteurDriss AhdPas encore d'évaluation
- Acide Et Base - Dosage (Récupération Automatique)Document39 pagesAcide Et Base - Dosage (Récupération Automatique)Driss Droussi100% (3)
- TD N°8-2 PDFDocument4 pagesTD N°8-2 PDFWalid GLPas encore d'évaluation
- Car Bony Les Alpha-Beta InsaturesDocument7 pagesCar Bony Les Alpha-Beta InsaturesJean-François Abena100% (2)
- Chimie Organique TD Corr 01 1 - CompressedDocument3 pagesChimie Organique TD Corr 01 1 - CompressedMoustapha Mbow100% (1)
- PhosphatationDocument30 pagesPhosphatationOualidPas encore d'évaluation
- Chimie Organique TD1Document7 pagesChimie Organique TD1Mira MaroPas encore d'évaluation
- Correction Exercices Chap 10Document12 pagesCorrection Exercices Chap 10cqfd242100% (1)
- Corrigé PC 1DDocument2 pagesCorrigé PC 1DAdeline Kwadzo100% (2)
- Solution Des Exercices - Les Acides Carboxyliques - Ts - SunudaaraDocument7 pagesSolution Des Exercices - Les Acides Carboxyliques - Ts - SunudaaraJule BaPas encore d'évaluation
- SPE Term - Devoir Commun 2 - Sujet 2 - CORRECTIONDocument4 pagesSPE Term - Devoir Commun 2 - Sujet 2 - CORRECTIONMariam LahlouPas encore d'évaluation
- Devoir Maison RP: Exercice 1Document6 pagesDevoir Maison RP: Exercice 1Ayoub DjouabiPas encore d'évaluation
- TD Chimie OrganiqueDocument9 pagesTD Chimie Organiqueass mohPas encore d'évaluation
- TP D'éléctrochimieDocument7 pagesTP D'éléctrochimieHanou BouPas encore d'évaluation
- Serie C4-benzene-WahabDiopDocument2 pagesSerie C4-benzene-WahabDiophamd kabore100% (2)
- Corrigé - Type - TleD. Essai Blan2024Document10 pagesCorrigé - Type - TleD. Essai Blan2024issaradjab13Pas encore d'évaluation
- Exercices Avec Solution SV2-STU2Document18 pagesExercices Avec Solution SV2-STU2SaoudPas encore d'évaluation
- Fiche de TD N3, Ex. 2Document3 pagesFiche de TD N3, Ex. 2Elaziouti AbdelkaderPas encore d'évaluation
- Corrigés Leçon 4 - Le BenzèneDocument4 pagesCorrigés Leçon 4 - Le Benzèneholyeric50Pas encore d'évaluation
- C 00 XP 1 CDocument13 pagesC 00 XP 1 CMihnea GamanPas encore d'évaluation
- Chimie D Chap14 Correction ExosDocument4 pagesChimie D Chap14 Correction ExosSOULA CHAHINAZPas encore d'évaluation
- Corrigé PC TleDDocument2 pagesCorrigé PC TleDSamuel OLOJEDEPas encore d'évaluation
- Correction TD 3 - Thermochimie (Exos 7,8,9)Document4 pagesCorrection TD 3 - Thermochimie (Exos 7,8,9)Amir NadeauPas encore d'évaluation
- 6 AcideDocument4 pages6 AcideAzumi ChanPas encore d'évaluation
- TD L2 BiochimieDocument19 pagesTD L2 BiochimieGaetan Djoufo100% (1)
- CC 07 SujetDocument4 pagesCC 07 SujetAugustin WiniguePas encore d'évaluation
- SEQ 2 CHIMIE THEORIQUE Tle CDDocument3 pagesSEQ 2 CHIMIE THEORIQUE Tle CDUlriche Enama EbandaPas encore d'évaluation
- U C A D D: Exercice 1Document5 pagesU C A D D: Exercice 1Lindeltaylor DioufPas encore d'évaluation
- Controle de Cinétique 2019 2020 Avec CorrigéDocument7 pagesControle de Cinétique 2019 2020 Avec CorrigéMy ProofPas encore d'évaluation
- TD COD1 Alcane Et HC Insatur e 2024.PDF Filename UTF 8''TD COD1 Alcane Et HC Insaturée 2024Document3 pagesTD COD1 Alcane Et HC Insatur e 2024.PDF Filename UTF 8''TD COD1 Alcane Et HC Insaturée 2024jerytsiriniainaPas encore d'évaluation
- Fractionné 20240212 2129Document7 pagesFractionné 20240212 2129Mouhamed lamine SonkoPas encore d'évaluation
- TD 1Document4 pagesTD 1Abdou HajjajiPas encore d'évaluation
- Lycée Pilote Sfax DC 3 2009 CorrigéDocument2 pagesLycée Pilote Sfax DC 3 2009 CorrigéMaram BouaskerPas encore d'évaluation
- Alcools - 2 - Forum de Sciences Physiques - 286701Document6 pagesAlcools - 2 - Forum de Sciences Physiques - 286701JOEL EBENEZER SOUMAHINPas encore d'évaluation
- 1cm432qpm 757086Document4 pages1cm432qpm 757086Nana DiakitéPas encore d'évaluation
- Serie N°1: Acides Carboxyliques Et Ses Derivees - TS: Nommer Les Composés SuivantsDocument6 pagesSerie N°1: Acides Carboxyliques Et Ses Derivees - TS: Nommer Les Composés SuivantsRom DantePas encore d'évaluation
- QCM - Medecine ChimieMr SABOUR 2023Document9 pagesQCM - Medecine ChimieMr SABOUR 2023SABOUR MOHAMMEDPas encore d'évaluation
- Exercice Et Solution Fours ChauidierDocument46 pagesExercice Et Solution Fours ChauidierMourad MatmourPas encore d'évaluation
- Série D'exercices Sur Les Acides Carboxyliques Et Dérivés - Ts - SunudaaraDocument5 pagesSérie D'exercices Sur Les Acides Carboxyliques Et Dérivés - Ts - SunudaaraJule BaPas encore d'évaluation
- n-1 PDFDocument39 pagesn-1 PDFZineb DahmaniPas encore d'évaluation
- TD Amine AcidesCarboxyliques 2020 LSLL - Wahab DDocument4 pagesTD Amine AcidesCarboxyliques 2020 LSLL - Wahab DOumou Khaïry Diop100% (1)
- Série 1Document3 pagesSérie 1Hiba JendoubiPas encore d'évaluation
- Axlou Toth Pour L'innovation: Composés Aromatiques (Le Benzène)Document6 pagesAxlou Toth Pour L'innovation: Composés Aromatiques (Le Benzène)djibril fayePas encore d'évaluation
- SERIE C3 1ère S1 LES ALCENES ET LES ALCYNESDocument2 pagesSERIE C3 1ère S1 LES ALCENES ET LES ALCYNESdieyecheikh2014Pas encore d'évaluation
- Al CoolsDocument13 pagesAl Coolsbmm2Pas encore d'évaluation
- A E R M O S MédecineDocument4 pagesA E R M O S MédecineIssouf BerthePas encore d'évaluation
- Serie 4-Thermochimie PDFDocument4 pagesSerie 4-Thermochimie PDFajb4duPas encore d'évaluation
- Sem 1 S10405Document4 pagesSem 1 S10405jamjamalPas encore d'évaluation
- Examen FST MARJAOUI MohamedDocument6 pagesExamen FST MARJAOUI MohamedMed MohamedPas encore d'évaluation
- Alcénes - Alcynes 1S1-1S2 AT 22 Renf FinDocument6 pagesAlcénes - Alcynes 1S1-1S2 AT 22 Renf Finpapaaliouba3Pas encore d'évaluation
- Marolet MaDocument5 pagesMarolet MamedsalemeddahPas encore d'évaluation
- Série 2 + SolutionDocument9 pagesSérie 2 + Solutionمريم ياسمينPas encore d'évaluation
- Exercice Chimie 02Document3 pagesExercice Chimie 02matmatijamelPas encore d'évaluation
- TP PSC Final1Document12 pagesTP PSC Final1Malek SaidaouiPas encore d'évaluation
- Exercices Sur Les AlcoolsDocument9 pagesExercices Sur Les AlcoolsJacobPas encore d'évaluation
- Capture D'écran . 2023-05-11 À 02.16.46Document3 pagesCapture D'écran . 2023-05-11 À 02.16.46cmamadouidrissaPas encore d'évaluation
- Exercices HalogenoalcanesDocument10 pagesExercices HalogenoalcanesJean-François Abena100% (1)
- Combustion ExoDocument2 pagesCombustion ExoSimo El AzaarPas encore d'évaluation
- Correction AlcanesDocument2 pagesCorrection AlcanesMichael VoulnangPas encore d'évaluation
- 2022 NelleCaledo J1 ExoA Correction AcBenzoique 5ptsDocument2 pages2022 NelleCaledo J1 ExoA Correction AcBenzoique 5ptsredatwitch2006Pas encore d'évaluation
- Examen National Physique Chimie SPC 2020 Normale Corrige 3Document10 pagesExamen National Physique Chimie SPC 2020 Normale Corrige 3hicham lahdissouPas encore d'évaluation
- Série Corrigée de Révision - Sciences Physiques Correction de La Série de Révision Bac 2011 - Bac Mathématiques (2010-2011) MR Benaich PDFDocument15 pagesSérie Corrigée de Révision - Sciences Physiques Correction de La Série de Révision Bac 2011 - Bac Mathématiques (2010-2011) MR Benaich PDFSaifeddine MakniPas encore d'évaluation
- Serie3 GRD ClssDocument7 pagesSerie3 GRD ClssabdelouahedPas encore d'évaluation
- TP Soluté Du Dakin MIDocument3 pagesTP Soluté Du Dakin MIassi leuumPas encore d'évaluation
- Spe Physique Chimie 2021 Zero 1 Sujet OfficielDocument11 pagesSpe Physique Chimie 2021 Zero 1 Sujet OfficielChahid OUAAZIZIPas encore d'évaluation
- Oxydo-Reduction: ManganmétrieDocument8 pagesOxydo-Reduction: ManganmétrieBsissaSoltaniPas encore d'évaluation
- Version Fin 4Document74 pagesVersion Fin 4ALI100% (2)
- La Classification Des Roches SédimentairesDocument9 pagesLa Classification Des Roches SédimentairesAida GueyePas encore d'évaluation
- Solutions Aqueuses Nouveau 2023Document79 pagesSolutions Aqueuses Nouveau 2023Fannes DesignPas encore d'évaluation
- Cours Microbiologie s3Document37 pagesCours Microbiologie s3Fara MendrikaPas encore d'évaluation
- 05 Controle #3 Semestre 1Document2 pages05 Controle #3 Semestre 1hoissinekhadija59Pas encore d'évaluation
- TleD - CH - L3 - Les AminesDocument8 pagesTleD - CH - L3 - Les AminesBertrand FamaPas encore d'évaluation
- Douceur de Miel Nettoyant Visage Hbo13.13.07Document1 pageDouceur de Miel Nettoyant Visage Hbo13.13.07zineb hafidiPas encore d'évaluation
- Cours Béton Armé YANGOTIKALA Selon EC2 Via BAELDocument85 pagesCours Béton Armé YANGOTIKALA Selon EC2 Via BAELBenNdangiPas encore d'évaluation
- Cours Designation Des Materiaux PlastiqueDocument1 pageCours Designation Des Materiaux PlastiqueAnas Win'sPas encore d'évaluation
- MaBiologie - Theorie - v2Document274 pagesMaBiologie - Theorie - v2AyaPas encore d'évaluation
- Semaines 9 Et 10 Classes 4e SPC Chapitre 6Document7 pagesSemaines 9 Et 10 Classes 4e SPC Chapitre 6Stephane CreachPas encore d'évaluation
- MémoireDocument16 pagesMémoireLotfi AbderezzakPas encore d'évaluation
- PHCH 3e ch02 p031 Exercices Supp EleveDocument6 pagesPHCH 3e ch02 p031 Exercices Supp ElevejanaPas encore d'évaluation
- TD Electrochimie Et Applications, L3 Chimie Et M1 SC Phys 2018-2019Document4 pagesTD Electrochimie Et Applications, L3 Chimie Et M1 SC Phys 2018-2019fernandPas encore d'évaluation
- MetamorphismeDocument44 pagesMetamorphismeNour El imene DallouliPas encore d'évaluation
- 1Document28 pages1mohamed boubakeurPas encore d'évaluation
- Cours de Geologie Generale EnvironnementDocument76 pagesCours de Geologie Generale EnvironnementMohamPas encore d'évaluation
- Exercices Dérivés Carbonylés Partie 1: Exercice 1: Pour DébuterDocument13 pagesExercices Dérivés Carbonylés Partie 1: Exercice 1: Pour DébuterMoncef AbbesPas encore d'évaluation
- Rapport de Stage Probatoire Au Laboratoire de Suivi de La Qualité Des EauxDocument133 pagesRapport de Stage Probatoire Au Laboratoire de Suivi de La Qualité Des EauxBarthélemy Bawar Dit WarbiPas encore d'évaluation
- Série N°3 Microsoft WordDocument2 pagesSérie N°3 Microsoft WordMohamed ELPas encore d'évaluation
- Chimie-TleC D TI-Eval4Document6 pagesChimie-TleC D TI-Eval4hamidaPas encore d'évaluation
- Milieux de Culture BacDocument7 pagesMilieux de Culture Bacagag.salahPas encore d'évaluation