Académique Documents
Professionnel Documents
Culture Documents
Cours 15 - Les Combustions
Transféré par
adnanTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Cours 15 - Les Combustions
Transféré par
adnanDroits d'auteur :
Formats disponibles
Www.AdrarPhysic.
Fr
Leçon N° 4
Les combustions
I- Transformation physique et transformation chimique :
1- Transformation physique :
Une transformation physique est le passage d'un corps d'un état physique à une autre, sans modification de la
nature des molécules mises en jeu.
𝐇𝟐 𝐎(𝐬) 𝐇𝟐 𝐎(𝐋)
Les molécules restent identiques mais leur disposition change .
2- Transformation chimique :
On appelle transformation chimique toute transformation au cours de laquelle des substances disparaissent et
de nouvelles substances apparaissent.
𝐥𝐞𝐬 𝐫é𝐚𝐜𝐭𝐢𝐟𝐬 𝐋𝐞𝐬 𝐩𝐫𝐨𝐝𝐮𝐢𝐬
• Les espèces chimiques consommées sont les réactifs.
• Les nouvelles espèces chimiques formées sont les produits.
II- Notion de la combustion :
Une combustion est une transformation chimique qui nécessite toujours deux réactifs : un comburant, un
combustible et une source de chaleur, pour donner d’autres corps appelés Produits.
▪ Un combustible est un corps qui peut brûler.
▪ Le comburant est la substance qui est capable de faire brûler le combustible.
III- Combustion du carbone :
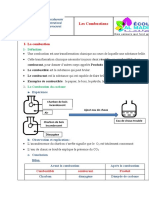
1- Expérience :
Dans l’air, enflammant jusqu’à incandescence un morceau de charbon de bois. Introduisant le charbon
incandescent dans un flacon rempli de dioxygène pur.
Quand la combustion du charbon de bois cesse, on retire le reste du morceau et on verse l’eau de chaux dans
le flacon, puis on le ferme et on agite.
Charbon de bois
incandescent
Ajoute eau de chaux
Dioxygène
Eau de chaux se trouble
2- Observation :
• La combustion du carbone est plus vive dans le dioxygène pur.
• L’eau de chaux se trouble explique la présence du dioxyde de carbone .
3- Conclusion :
• La combustion du carbone est une transformation chimique, au cours de laquelle des corps disparaissent
(carbone et dioxygène) qui s’appellent les réactifs .et un autre nouveau corps se forme (Le dioxyde de carbone)
qui s’appellent les produits.
• On peut exprimer le bilan de cette transformation de la manière suivante.
Carbone + Dioxygène → Dioxyde de carbone
Les réactifs Les produits
Avant la combustion Après la combustion
Combustible Comburant Produit
Charbon Dioxygène Dioxyde de carbone
Remarque :
Page 1 of 2
Www.AdrarPhysic.Fr
Www.AdrarPhysic.Fr
o La combustion s'arrête lorsque l’un ou les deux réactifs a disparu totalement.
o Toutes les combustions nécessitent le dioxygène comme comburant.
IV- Combustion du butane :
Le butane est un gaz de formule chimique C4H10
Ce gaz principalement utilisé comme combustible à usage domestique, en grande partie pour la cuisson…...
1- Combustion complète du butane :
a- Expérience : Au laboratoire, Pour faire la combustion du butane, on utilise le bec bunsen.
Dans ce cas, La virole du bec bunsen doit être ouverte au cours de la combustion.
b- Observation :
▪ La flamme est bleue.
▪ Il se forme de la buée (eau).
▪ Il se forme du dioxyde de carbone, car lorsque l’on met de l’eau de chaux dans le verre à pied, elle se
trouble.
c- Conclusion :
Lors de la combustion complète du butane : le combustible (butane) et le comburant (dioxygène) sont
consommés.
Il se forme des produits nouveaux : la vapeur d’eau (buée), le dioxyde de carbone.
Le bilan de cette combustion est :
Butane + dioxygène → Dioxyde de carbone + eau
2- Combustion incomplète :
a- Expérience : Dans ce cas, La virole du bec bunsen doit être fermé au cours de la combustion.
b- Observation :
• La flamme est jaune.
• Il se forme de la buée (eau) et un dépôt noir.
• Il se forme du dioxyde de carbone, car lorsque l’on met de l’eau de chaux dans le verre à pied, elle se
trouble.
• En plus de l’eau et dioxyde de carbone, Il se forme du carbone et aussi un gaz, incolore et inodore, le
monoxyde de carbone.
c- Conclusion :
Lorsque le dioxygène est en quantité insuffisante, la combustion est dite incomplète. Et Il se forme des
produits nouveaux : la vapeur d’eau, le dioxyde de carbone, aussi des particules de carbone et le
monoxyde de carbone.
Le bilan de cette combustion est :
Butane + dioxygène → Dioxyde de carbone + eau + carbone + monoxyde du carbone
Page 2 of 2
Www.AdrarPhysic.Fr
Vous aimerez peut-être aussi
- Histoire de La Littérature FrançaiseDocument308 pagesHistoire de La Littérature FrançaiseBreno Gomes89% (9)
- Les Combustions Cours 1Document4 pagesLes Combustions Cours 1Sadik LamhandazPas encore d'évaluation
- Cours Fours Et Chaudières - Labsi 2018 - EtudiantsDocument23 pagesCours Fours Et Chaudières - Labsi 2018 - EtudiantsElHadi S Zidane67% (6)
- Les Combustions Cours 3Document5 pagesLes Combustions Cours 3km.aouadiPas encore d'évaluation
- CombustionDocument3 pagesCombustionHamidou ElbihawiPas encore d'évaluation
- Chapitre5 PDFDocument9 pagesChapitre5 PDFelkendyPas encore d'évaluation
- CombustionsDocument23 pagesCombustionsmaria khadijaPas encore d'évaluation
- CombustionsDocument23 pagesCombustionsNajwa HaddadPas encore d'évaluation
- CR 4 Les CombustionsDocument22 pagesCR 4 Les Combustionskawtar bourkanPas encore d'évaluation
- LES CombustionDocument4 pagesLES Combustionwalid bakkouriPas encore d'évaluation
- La CombustionDocument3 pagesLa Combustionelmouden rachidPas encore d'évaluation
- 7 - Les CombustionsDocument25 pages7 - Les CombustionsadnanPas encore d'évaluation
- Les CombustionsDocument5 pagesLes Combustionsjad.bnfdlPas encore d'évaluation
- Les Combustions - Partie 2Document8 pagesLes Combustions - Partie 2Marc EvansPas encore d'évaluation
- Chapitre 5combustion Livret DocxDocument6 pagesChapitre 5combustion Livret Docxalseiny923Pas encore d'évaluation
- V 801 Giz 0 UqDocument3 pagesV 801 Giz 0 UqAbdo GamingPas encore d'évaluation
- Les Combustions Resume de Cours 1Document3 pagesLes Combustions Resume de Cours 1Sa MoPas encore d'évaluation
- Combustion 4emeDocument6 pagesCombustion 4emeAbđė Ěł ŁğđPas encore d'évaluation
- 4 1 Chapitre - 4 2Document5 pages4 1 Chapitre - 4 2Rachid BouhssainPas encore d'évaluation
- Les Combustions Cours PPT 2Document25 pagesLes Combustions Cours PPT 2hamza manaf100% (1)
- Les Combustions Cours PPT 1Document14 pagesLes Combustions Cours PPT 1mohamedimziln2005Pas encore d'évaluation
- C C04 Combustions - Cor 2008Document5 pagesC C04 Combustions - Cor 2008Houzal-dine SaidPas encore d'évaluation
- ILEPHYSIQUE Chimie 4 Combustions Transformations Chimiques CoursDocument3 pagesILEPHYSIQUE Chimie 4 Combustions Transformations Chimiques CoursMoussa BanaPas encore d'évaluation
- Combustion CoursDocument6 pagesCombustion CoursNessrine ZahiPas encore d'évaluation
- Les Combustions - Partie 1Document4 pagesLes Combustions - Partie 1Marc EvansPas encore d'évaluation
- Les Combustions - Partie 1Document4 pagesLes Combustions - Partie 1Marc EvansPas encore d'évaluation
- CHP 4 Les CombustionsDocument6 pagesCHP 4 Les Combustionsnaceur rbiiPas encore d'évaluation
- Les-Combustions 062405Document12 pagesLes-Combustions 062405Abdellah ElmahniPas encore d'évaluation
- Cours 14 - Les CombustionsDocument3 pagesCours 14 - Les CombustionsadnanPas encore d'évaluation
- Les CombustionsDocument12 pagesLes CombustionsDoudou DidouPas encore d'évaluation
- Chap 7 La Combustion Du CarboneDocument10 pagesChap 7 La Combustion Du Carbonechoulio95100Pas encore d'évaluation
- Chap 1 Les CombustionsDocument6 pagesChap 1 Les CombustionsmazhourPas encore d'évaluation
- LDP Cycle4 Chap08Document4 pagesLDP Cycle4 Chap08TOUFOULATI Mon enfancePas encore d'évaluation
- 4SP41TEWB6123C02 CorrigeCoursPhysiqueChimie-U02Document12 pages4SP41TEWB6123C02 CorrigeCoursPhysiqueChimie-U02d.g.zahra17Pas encore d'évaluation
- Cours PPT 1 - CombustionsDocument13 pagesCours PPT 1 - CombustionsadnanPas encore d'évaluation
- Combustion Du CarboneDocument56 pagesCombustion Du CarboneimanfekryahmedPas encore d'évaluation
- Série 2 - Les CombustionsDocument2 pagesSérie 2 - Les CombustionsYouSsra A'sPas encore d'évaluation
- Combustion du carbone et du butane ناـــتوــبــلا و نوـــبرــكــلا قارــتــحاDocument4 pagesCombustion du carbone et du butane ناـــتوــبــلا و نوـــبرــكــلا قارــتــحاlona lonaPas encore d'évaluation
- La Combustion ProjetDocument8 pagesLa Combustion ProjetFatma Ezzahra Rziga100% (1)
- Chimie 6eDocument2 pagesChimie 6eNemir MimirPas encore d'évaluation
- La Réaction Chimique - Les Combustions - Prof - TAHIRI (WWW - Pc1.ma)Document4 pagesLa Réaction Chimique - Les Combustions - Prof - TAHIRI (WWW - Pc1.ma)Nassima NassomaPas encore d'évaluation
- Exercices de Revisions Pour Le 2eme Brevet BlancDocument6 pagesExercices de Revisions Pour Le 2eme Brevet BlancLola TomasPas encore d'évaluation
- Combustions PDFDocument4 pagesCombustions PDFandoPas encore d'évaluation
- Les Combustions Exercices Non Corriges 7Document2 pagesLes Combustions Exercices Non Corriges 7Said100% (3)
- 4e Chap4 Cours CombustionDocument4 pages4e Chap4 Cours CombustionandoPas encore d'évaluation
- Réaction Chimique PROF - OUTOUJANE (WWW - Pc1.ma)Document2 pagesRéaction Chimique PROF - OUTOUJANE (WWW - Pc1.ma)bihi.102.haytamPas encore d'évaluation
- Cours Fours Et ChaudièresDocument23 pagesCours Fours Et ChaudièresKhalil LasferPas encore d'évaluation
- 4e Chap4Document5 pages4e Chap4zehwa aliPas encore d'évaluation
- PC 5ème - L9 - Combustion Du CarboneDocument6 pagesPC 5ème - L9 - Combustion Du CarbonewonderplancadiPas encore d'évaluation
- La Réaction Chimique - Les CombustionsDocument4 pagesLa Réaction Chimique - Les CombustionsPicasso BosePas encore d'évaluation
- Expérimente: AttentionDocument4 pagesExpérimente: AttentionmaouthonjiPas encore d'évaluation
- C7 Correction Exercices ImpressionDocument6 pagesC7 Correction Exercices ImpressionzoePas encore d'évaluation
- 4ème - Classe Inversée - Combustion Du CarboneDocument2 pages4ème - Classe Inversée - Combustion Du CarboneAurélie JclynPas encore d'évaluation
- Chapitre 6 - Transformation ChimiqueDocument4 pagesChapitre 6 - Transformation Chimiqueroxane.bouskela1Pas encore d'évaluation
- Exercices - Chimie 4.3 - CombustionsDocument4 pagesExercices - Chimie 4.3 - CombustionsAbđė Ěł Łğđ100% (1)
- 4e - 6 - Les Combustions - Support ÉlèveDocument6 pages4e - 6 - Les Combustions - Support ÉlèvePlateny AMOUSSOUPas encore d'évaluation
- 06 Notion de Reaction ChimiqueDocument3 pages06 Notion de Reaction Chimiquemedabdellahisamba34Pas encore d'évaluation
- Les Transformations Et Les Reactions ChimiquesDocument4 pagesLes Transformations Et Les Reactions ChimiquesinezPas encore d'évaluation
- 5 - (Khales) Réaction Chimique (FR)Document48 pages5 - (Khales) Réaction Chimique (FR)saminousalissouhPas encore d'évaluation
- 7 - Les CombustionsDocument25 pages7 - Les CombustionsadnanPas encore d'évaluation
- Cours PPT 1 - CombustionsDocument13 pagesCours PPT 1 - CombustionsadnanPas encore d'évaluation
- Cours 14 - Les CombustionsDocument3 pagesCours 14 - Les CombustionsadnanPas encore d'évaluation
- Cours 4 - Les Actions MécaniquesDocument3 pagesCours 4 - Les Actions MécaniquesadnanPas encore d'évaluation
- Cours 3 $ 1 Les Actions Mécaniques - Les ForcesDocument6 pagesCours 3 $ 1 Les Actions Mécaniques - Les ForcesadnanPas encore d'évaluation
- Cours 3 - Les Actions MécaniquesDocument3 pagesCours 3 - Les Actions MécaniquesadnanPas encore d'évaluation
- Cours 3 - Les Atomes Et Les IonsDocument4 pagesCours 3 - Les Atomes Et Les IonsadnanPas encore d'évaluation
- Cours 8 - Les Atomes Et Les IonsDocument3 pagesCours 8 - Les Atomes Et Les IonsadnanPas encore d'évaluation
- S.2 4 2.chimie Conc PH TP ExAO - PHDocument8 pagesS.2 4 2.chimie Conc PH TP ExAO - PHadnanPas encore d'évaluation
- TP Exao Conductimetrie Destop VMPADocument3 pagesTP Exao Conductimetrie Destop VMPAadnanPas encore d'évaluation
- Cours 6 - Les Atomes Et Les IonsDocument4 pagesCours 6 - Les Atomes Et Les IonsadnanPas encore d'évaluation
- DS1-Solutions Aqueuses - Premier PrincipeDocument13 pagesDS1-Solutions Aqueuses - Premier PrincipeadnanPas encore d'évaluation
- TP Dosage Acido-Basique Par Conductimétrie (ExAO)Document8 pagesTP Dosage Acido-Basique Par Conductimétrie (ExAO)adnanPas encore d'évaluation
- Corrige Examen Session 1 2010Document5 pagesCorrige Examen Session 1 2010adnanPas encore d'évaluation
- TP 04: Dosage Par Précipitation: Argentimètrie Dosage Des Chlorures Par La Méthode de MohrDocument3 pagesTP 04: Dosage Par Précipitation: Argentimètrie Dosage Des Chlorures Par La Méthode de MohradnanPas encore d'évaluation
- Cours 7 - Les Lois de La Réaction ChimiqueDocument2 pagesCours 7 - Les Lois de La Réaction ChimiqueadnanPas encore d'évaluation
- 2QCM Elect Ses1 SMPC 19-20Document2 pages2QCM Elect Ses1 SMPC 19-20adnanPas encore d'évaluation
- Chapitre 2 Partie 1Document4 pagesChapitre 2 Partie 1adnanPas encore d'évaluation
- Chapitre 1Document43 pagesChapitre 1adnanPas encore d'évaluation
- Plasturgie 2004Document8 pagesPlasturgie 2004adnanPas encore d'évaluation
- CF 3 F 78 F 237Document2 pagesCF 3 F 78 F 237adnanPas encore d'évaluation
- smc5 Session 1 2020Document7 pagessmc5 Session 1 2020adnanPas encore d'évaluation
- TD Cinétique Chimique Série N°1 CorrectionDocument6 pagesTD Cinétique Chimique Série N°1 CorrectionadnanPas encore d'évaluation
- Rapport de Stage TT - TSIRA618 Hamri JassemDocument22 pagesRapport de Stage TT - TSIRA618 Hamri JassemHamri Zayneb100% (1)
- Les Troubles de L'odorat (Ok)Document17 pagesLes Troubles de L'odorat (Ok)EbePas encore d'évaluation
- Le Feng Shui - Comment Aménager Sa Maison Façon - Feng ShuiDocument19 pagesLe Feng Shui - Comment Aménager Sa Maison Façon - Feng ShuikhassimPas encore d'évaluation
- Yves Denéchère - La Migration Singulière Des Adoptés Dans L'espace Euro-AméricainDocument9 pagesYves Denéchère - La Migration Singulière Des Adoptés Dans L'espace Euro-Américainhedoncdmx69Pas encore d'évaluation
- Dans Ce LabDocument3 pagesDans Ce LabDiana ZoboPas encore d'évaluation
- Sin - Ax - Sin - BX - 2Document3 pagesSin - Ax - Sin - BX - 2Anton BaëzaPas encore d'évaluation
- L'educationDocument8 pagesL'educationIBrahima IB LengAniPas encore d'évaluation
- Sup Livres 060309Document12 pagesSup Livres 060309tinderpaperPas encore d'évaluation
- Extraction Separation Et Identification Des Especes Chimiques Exercices Non Corriges 2 PDFDocument3 pagesExtraction Separation Et Identification Des Especes Chimiques Exercices Non Corriges 2 PDFmortadaPas encore d'évaluation
- Propos 20d 27introductionDocument2 pagesPropos 20d 27introductionJean Eddy OlibertPas encore d'évaluation
- LMPS AUSIM Livre Blanc Classification Des DonnéesDocument20 pagesLMPS AUSIM Livre Blanc Classification Des DonnéesSucitu EmanuelPas encore d'évaluation
- Samba Serveur Contrôleur de DomaineDocument16 pagesSamba Serveur Contrôleur de DomaineRANDRIANASOLO FrancoPas encore d'évaluation
- Correction+-+fonctions+mesurables +propriétés+des+mesures PDFDocument36 pagesCorrection+-+fonctions+mesurables +propriétés+des+mesures PDFŞȫɾAȳȁPas encore d'évaluation
- 210-U-10 Polymères Et Résines CompositesDocument26 pages210-U-10 Polymères Et Résines CompositesBESSAIH RymPas encore d'évaluation
- Disque Dur 2Document41 pagesDisque Dur 2fares cherniPas encore d'évaluation
- Daf Liste Editions Et Exemplaires Bif Version Site 2016Document6 pagesDaf Liste Editions Et Exemplaires Bif Version Site 2016Ernst LudwigPas encore d'évaluation
- Rapport Finale PDFDocument58 pagesRapport Finale PDFmohamedPas encore d'évaluation
- Gram. 34 Cours 1Document2 pagesGram. 34 Cours 1Kim MisoyaPas encore d'évaluation
- VSS791500T DataSheet FRFR E2365897355Document2 pagesVSS791500T DataSheet FRFR E2365897355Narcis PatrascuPas encore d'évaluation
- Cours de Requete SpatialeDocument15 pagesCours de Requete SpatialePaul JuniorPas encore d'évaluation
- Routage StatiqueDocument43 pagesRoutage Statiqueidjboha kokoPas encore d'évaluation
- AndréSimpson - Les Manoeuvres D'accostage - 202102210900Document43 pagesAndréSimpson - Les Manoeuvres D'accostage - 202102210900JDR49100% (1)
- FR - Accreditation - Certification Requirements and Training GuideDocument14 pagesFR - Accreditation - Certification Requirements and Training GuideYoussef FatihiPas encore d'évaluation
- CourrierDocument4 pagesCourrier795rxrgvk9Pas encore d'évaluation
- Renault Logan SymbolDocument2 pagesRenault Logan SymbolkokondroPas encore d'évaluation
- Labels AlimentairesDocument11 pagesLabels AlimentairesMaimouna Ba100% (1)
- Rituel_de_Table_au_rite_francais_et_signDocument18 pagesRituel_de_Table_au_rite_francais_et_signMakasitoPas encore d'évaluation
- Ressources 0002017189671 Ncfra 4-T01c01-039-File-Coup de Pouce EvalDocument4 pagesRessources 0002017189671 Ncfra 4-T01c01-039-File-Coup de Pouce EvalNoaPas encore d'évaluation
- Fuite Des Cerveaux, Le Mal Qui Ronge L'afriqueDocument2 pagesFuite Des Cerveaux, Le Mal Qui Ronge L'afriqueGilbertOumPas encore d'évaluation