Académique Documents
Professionnel Documents
Culture Documents
PHYSIOLOGE DE L'AXE HYPOTHALAMO HYPOPHYSAIRE Poly Pharmacie
PHYSIOLOGE DE L'AXE HYPOTHALAMO HYPOPHYSAIRE Poly Pharmacie
Transféré par
RAZAFINARSON JulianotTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
PHYSIOLOGE DE L'AXE HYPOTHALAMO HYPOPHYSAIRE Poly Pharmacie
PHYSIOLOGE DE L'AXE HYPOTHALAMO HYPOPHYSAIRE Poly Pharmacie
Transféré par
RAZAFINARSON JulianotDroits d'auteur :
Formats disponibles
Université Constantine 3 Constantine, le 16/03/2022
Faculté de Médecine
Service de Physiologie
Pr. Khelifi 1ière Année Pharmacie
PHYSIOLOGIE DE L’AXE HYPOTHALAMO HYPOPHYSAIRE
I- Anatomie fonctionnelle
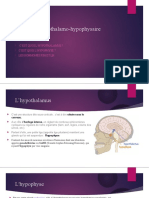
L’hypothalamus, situé à la base de l’encéphale dans le plancher du troisième ventricule, est un centre nerveux
intégrateur très important qui présente une fonction endocrine. Il est sous le contrôle des centres supérieurs du
cerveau. C’est le principal organe d’intégration pour la régulation des milieux intérieurs, du rythme veille-
sommeil, ainsi que de la croissance, du développement corporel et mental et de la reproduction de l’espèce.
L’hypophyse est une glande endocrine appelée également glande pituitaire, elle est présente dans le cerveau de
tous les vertébrés, elle peut être considérée comme l’une des glandes endocrines les plus importantes par le
nombre des hormones qu’elle sécrète et par la variété des activités biologiques qu’elle contrôle. Elle se loge dans
la selle turcique juste au dessous de l’hypothalamus auquel elle est reliée par une tige appelée infundibulum ou
tige pituitaire contenant des fibres nerveuses et des petits vaisseaux sanguins. Elle est composée de 2 parties
morphologiquement et embryologiquement distinctes: l’adéno-hypophyse ou antéhypophyse, et la neuro-
hypophyse ou posthypophyse.
La posthypophyse est le lieu de stockage et de sécrétion d’hormones synthétisées par l’hypothalamus
Les relations entre l’hypothalamus et l’hypophyse sont de 2 types :
- Relations d'ordre vasculaire avec l'antéhypophyse
- Relation de continuité d'ordre nerveux avec la posthypophyse
L’axe hypothalamo-hypophysaire désigne l'ensemble des relations qui s'établissent entre l'hypothalamus et
l'hypophyse.
L'hypothalamus contrôle l'ensemble des fonctions hypophysaires et subit un rétrocontrôle hypophysaire ou des
organes cibles de l'hypophyse.
II- Les hormones hypothalamiques
Les neurones hypothalamiques sécrètent des neuromédiateurs activateurs ou inhibiteurs de la sécrétion des
hormones hypophysaires appelés Releasing Factors ou Facteurs de libération hormonale qui sont acheminés
d'abord le long des axones puis déversés dans le réseau vasculaire hypophysaire, qui les conduit jusqu'aux
cellules antéhypophysaires
Les liaisons avec la posthypophyse étant nerveuses, les hormones hypothalamiques sont acheminées le long des
axones jusqu'au lobe postérieur de l'hypophyse où elles sont stockées
A- Les facteurs de libération hormonale
Ce sont des hormones de nature polypeptidique qui contrôlent l'ensemble des sécrétions hypophysaires :
TRH (thyrotropin releasing hormone). CRH (Corticotropin Releasing Hormone)
Gn-RH ou LH-RH (Luteotropin Releasing Hormone).
GH-RH (Growth Hormone Releasing Hormone).
GHIH ou SRIF (Somatotropin Release Inhibiting Factor) ou Somatostatine
PIF (Prolactin Inhibiting Factor). PRH (Prolactin Releasing Factor)
B- Les hormones posthypophysaires
Elles sont fabriquées par l’hypothalamus mais stockées puis libérées par la posthypophyse.
Deux hormones l’ADH et l’ocytocine qui présentent de grandes analogies structurales.
1- Vasopressine : hormone antidiurétique (ADH)
De nature peptidique, synthétisée dans le noyau supra-optique sous forme de préprohormone. Après clivage
l’ADH est stockée dans des granules neurosécrétoires qui sont transportés par les neurophysines II le long d’un
axone dans la posthypophyse, où elles sont stockées. L’ADH est libérée selon les besoins, en réponse à
l’hyperosomolalité ou à l’hypovolémie. Sa demie vie est très courte (quelques mn)
a- Stimulation de la sécrétion de l’ADH
- Stimulation osmotique : Les osmorécepteurs hypothalamiques sont très sensibles à de faibles variations (1-
2%) de l’osmolalité plasmatique. Une fois stimulés ils envoient des signaux aux cellules post hypophysaires qui
sécrètent alors rapidement de petite quantité d’ADH. On appelle set point le seuil d’osmolalité plasmatique à
partir duquel la sécrétion d’ADH commence. Ce set point varie d’un individu à l’autre entre 280 et 290
mOsmol/kg d’eau. En dessous de ce seuil, la concentration d’ADH circulante est indétectable. Au-dessus de ce
seuil, la relation entre la sécrétion d’ADH et l’osmolalité plasmatique est linéaire, une augmentation de 1
mOsmole/Kg d’eau augmente de 0,5 pg/mL la concentration d’ADH circulante. Un décalage des seuils de
sécrétion de la vasopressine et de la soif d’environ 10 mOsm.kg-1 permet en cas de restriction hydrique de
stimuler la réabsorption rénale d’eau avant de stimuler la prise de boisson par la soif.
- Stimulation volémique : La du volume sanguin ou la diminution de la pression artérielle stimule la sécrétion
d’ADH. Les récepteurs qui interviennent sont les barorécepteurs aortiques et carotidiens et les volorécepteurs de
l’oreillette droite. Ils sont sensibles à des variations de 15% de la volémie, l’hypophyse répond à cette stimulation
par la libération de grande quantité d’ADH.
b- Les récepteurs de l’ADH : trois types de récepteurs
Les récepteurs V1 : présents au niveau vasculaire et confèrent à l’ADH une action vasoconstrictive.
Les récepteurs V2 : situés à la membrane basolatérale des cellules du canal collecteur rénal et sont impliqués
dans la fonction de réabsorption d’eau par l’ADH
Les récepteurs V3 : situés au niveau des cellules corticotropes de l’antéhypophhyse.
c- Effets biologiques
Effets sur le rein : L’ADH a pour principal rôle
d’augmenter la perméabilité à l’eau du tube collecteur, en se
fixant au récepteur V2. Ce récepteur est couplé à une protéine G,
le second messager est l’AMPc.
La réponse cellulaire étant l’ouverture des aquaporine 2.
Effets sur les vaisseaux : A forte concentration l’ADH
agit sur les récepteurs V1 des muscles lisses des artérioles, par
la voie de la phospholipase C et les IPP qui augmentent la concentration du Ca++ intracellulaire (Second
messager). Il en résulte une vasoconstriction et élévation de la PA.
- Effet sur l’antéhypophyse : elle stimule la sécrétion de l’ACTH par action sur le récepteur V1b ou V3 via la
voie de la phospholipase C, IPP, IP, le second messager étant le Ca++.
d- Régulation de la sécrétion
La sécrétion d’ADH est favorisée par l’hyperosmolarité, l’hypovolémie , l’angiotensine II, l’aldostérone et le
SNC. Cependant elle est inhibée par le froid et l’alcool
2- Ocytocine
C’est une hormone peptidique synthétisée par les noyaux para ventriculaire de l'hypothalamus et sécrétée par
l'hypophyse postérieure, agit principalement sur les muscles lisses de l'utérus et des glandes mammaires.
a- Effets biologiques
- L’ocytocine est une hormone utérotonique, elle entraîne la contraction du muscle lisse utérin et joue un rôle
important, dans l’initiation et le déroulement du travail au terme de la gestation. Dans l'utérus, le nombre de
récepteurs à l'ocytocine augmente en fin de grossesse, rendant toute stimulation de plus en plus efficace.
- Au niveau des seins, elle stimule les contractions des cellules myoépithéliales des lobules mammaires
permettant ainsi l’éjection de lait.
L’ocytocine agit sur des récepteurs couplés à la protéine G présents sur la membrane des cellules musculaires
lisse de l’utérus et du sein, le mécanisme se fait pat la voie de la phospholipase C. Le second messager est le Ca++
b- Régulation de la sécrétion
La dilation du col utérin pendant le travail stimule l’hypothalamus libérant ainsi l’ocytocine en grande quantité.
Les mouvements fœtaux et la pression sur le col utérin provoquent un stimulus nerveux vers l'hypothalamus.
La succion du mamelon permet une sécrétion de l’ocytocine au bout de 30 – 60s par voie reflexe.
Il existe un mécanisme de rétroaction positive (réflexe de Fergusson) : les contractions utérines stimulent la
libération de l’ocytocine par la posthypophyse.
Le stress émotionnel et l’alcool inhibent la libération de l’hormone
IV- Hormones antéhypophysaires
On trouve dans la glande antéhypophysaire au moins 5 types de cellules. Ces cellules n’ont pas une activité
continue. Elles libèrent leurs produits de sécrétion par période ± longue.
On distingue :
Les cellules lactotropes : sécrétant la prolactine qui agit sur les glandes mammaires.
Les cellules somatotropes : sécrétant l’hormone de croissance qui agit sur l’os, le muscle, le tissu adipeux
et le foie.
Les cellules corticotropes : sécrètent l’ACTH qui agit sur le cortex surrénalien.
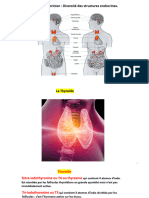
Les cellules thyréotropes : sécrétant la TSH qui agit sur la thyroïde.
Les cellules gonadotropes : sécrétant les gonadotrophines LH et FSH qui agissent sur les ovaires et les
testicules
A- La prolactine
Hormone polypeptidique, synthétisée et sécrétée par les cellules lactotropes de l’antéhypophyse. Sa sécrétion est
sensible au stress, sa demi-vie est de l'ordre de 30 min, son taux plasmatique de l'ordre de 20 ng/mL chez la
femme et inférieur de 15 ng/mL chez l'homme.
Pendant la grossesse : la prolactine s’élève progressivement durant toute la grossesse, à partir de la 8ème semaine
elle est sécrétée à une concentration de 100 ng/mL. Le taux à terme est autour de 200ng/ml
1- Effets biologiques
Effet mammotrope : permet en synergie avec la progestérone et les œstrogènes le développement des glandes
mammaires.
Effet lactogénique : - permet la monté laiteuse et l’entretient de la lactation après l’accouchement
- Élaboration du lait par les cellules acineuses puis leur sécrétion dans la lumière des acini.
Pendant la grossesse le taux de prolactine s’élève et participe au développement de la glande mammaire mais les
œstrogènes bloquent les effets de la prolactine sur la lactation. Après l’accouchement, la chute des estrogènes et
de la progestérone permet l’initiation de la lactation.
L'action de la prolactine est facilitée par diverses hormones notamment le cortisol, la thyroxine, l’insuline,
l’IGFI, l’œstrogène et la progestérone …
A concentration élevée, la prolactine bloque la synthèse de GnRH et inhibe l'ovulation chez la femme.
2- Régulation de la sécrétion de prolactine
La PRF (Prolactin Releasing Factor) stimule la libération de prolactine
La TRH (Thyreotropin Releasing Hormone) est un puissant stimulateur de la sécrétion de Prolactine.
La PIF (Prolactin Inhibiting Factor) inhibe la libération de la prolactine. Cette hormone a été identifiée plus tard
comme étant la dopamine.
Les œstrogènes augmentent le taux de prolactine en diminuant la sécrétion de dopamine et en agissant
directement sur l'hypophyse.
La succion entraîne une stimulation du complexe aréolo-mammaire, qui lui-même stimule le complexe
hypothalamo-hypophysaire. Le reflexe de succion envoie des signaux par la voie nerveuse afférente pour inhiber
la sécrétion de la dopamine par l’hypothalamus. La levée de l’inhibition, augmente la sécrétion de la prolactine à
chaque tétée et augmente la lactogenèse.
Après sevrage, la lactation diminue progressivement pour s’interrompre dans 2 semaines et la sécrétion de la
prolactine diminue. Il en résulte une atrophie mécanique des cellules épithéliales et destruction des cellules
alvéolaires, les débris sont nettoyés par les macrophages.
B- Hormone de croissance (GH)
Appelé également somatotropine (STH), est une hormone peptidique de 191 acides aminés, synthétisée et
sécrétée par les cellules somatotropes qui représentent 50 % des cellules antéhypophysaires. Elle présente une
grande spécificité zoologique, elle n’est donc active que chez l’espèce qui la synthétise.
1- Sécrétion
La libération de la GH s’effectue par exocytose, selon un mode pulsatile. Elle apparaît au cours de la vie fœtale
après 70 jours de gestation. Chez l’enfant, la sécrétion de GH est intermittente au cours du nycthémère. Des
pulses surviennent toutes les 3 à 4 heures et les pulses les plus importantes sont observées une à deux heures
après le début du sommeil profond. Sa sécrétion augmente de façon importante pendant la phase pré-pubertaire.
Sa demi-vie est très courte.
2- Effets biologiques
Les effets biologiques de la GH sont multiples. Elles s’exercent sur presque tous les tissus principalement osseux
et musculaire et tous les viscères à l’exception du cerveau. La GH n’agit pas toujours directement sur les cellules
cibles. Elle permet parfois la synthèse et l’action d’un ensemble de facteurs d’origine hépatique :
IGFs Les somatomédines ou insulin-like Growth-factor IGFs : Ce sont des intermédiaires de la majorité des
actions de la GH sur la croissance et la synthèse protéique. L’IGF-1 et l'IGF-2 sont des peptides de la famille de
l’insuline synthétisés dans la majorité des tissus mais principalement dans le foie. Le rôle de l'IGF-1 dans la
croissance est prédominant, alors que le rôle physiologique de l'IGF-2 n’est pas encore connu. La synthèse et la
sécrétion l'IGF-1, sont stimulées par la GH. Il sont transportés par les binding-protein (IGF-BP).
a. Effets métaboliques directs de la GH:
- Métabolisme glucidique: La GH augmente la glycogénolyse et diminue l'utilisation périphérique du glucose.
Elle est donc hyperglycémiante
- Métabolisme lipidique: La GH stimule la lipolyse par action sur la lipoprotéine lipase hormonosensible, ce qui
augmente les concentrations plasmatiques d'acides gras libres. Elle stimule l'utilisation cellulaire de ces acides
gras pour fournir de l'énergie cellulaire à la place du glucose.
- Métabolisme protéique: La GH stimule la synthèse protéique. Cette action est renforcée par l'IGF-1. La GH
augmente le transport transmembranaire des acides aminés et augmente leur incorporation dans les protéines.
L'administration de GH entraîne une augmentation de la masse maigre et surtout de la masse musculaire, ce qui
entraîne une augmentation des capacités d'adaptation à l'exercice et explique l'utilisation de la GH comme
produit de dopage.
- Métabolisme minéral: La GH augmente la rétention du sodium, du potassium et des phosphates, ce qui favorise
la croissance tissulaire. Elle stimule l'absorption intestinale du calcium et du magnésium, ce qui favorise la
formation osseuse.
b. Effets indirects de la GH exercés par l'intermédiaire de l'IGF-1
L'IGF-1 stimule la prolifération et la différenciation des cellules du cartilage de conjugaison (qui sépare les
épiphyses des diaphyses) qui permet la croissance en longueur des os longs, dont dépendra la taille définitive de
l’adulte. Cette action endocrine perdure jusqu'à l'ossification de la plaque cartilagineuse par les stéroïdes sexuels
à la fin de la puberté. L'IGF-1 stimule aussi la différenciation et la croissance de nombreux tissus les ovaires, les
testicules, les corticosurrénales, les muscles, les reins, les poumons. . .
IV- Régulation de la sécrétion
1- Le GHRH (Growth Releasing Hormon ou somatocrinine) hypothalamique se lie à des récepteurs spécifiques
sur les cellules somatotropes et stimule la synthèse de la GH.
2- La somatostatine GHIH secrétée par l’hypothalamus, le SN central et périphérique ainsi que d’autres organes
comme le pancréas et le tractus gastro-intestinal. Elle a un pouvoir inhibiteur sur la sécrétion de GH.
Le caractère pulsatile est lié à la libération alternée des deux facteurs hypothalamiques. Il semble que la GHRH
soit essentielle pour induire l'épisode sécrétoire, alors que la somatostatine est importante pour contrôler les
valeurs basses entre les pics.
La synthèse et la sécrétion de somatostatine sont stimulées par une élévation des taux sériques de somatomédine.
3- La ghrèline: synthétisée dans le noyau arqué et l’estomac stimule la libération de la GH
4- Les hormones périphériques exercent aussi un rôle sur la sécrétion de GH: le cortisol à des doses supra
physiologiques stimule la production hypothalamique de somatostatine qui bloque la synthèse de GH et diminue
ainsi la croissance. L’œstradiol diminue la production de somatostatine et donc augmente la production de GH.
5- Certains facteurs nutritionnels stimulent la libération de GH: la baisse de la glycémie, la diminution de la
concentration plasmatique des acides gras libres et l'augmentation de certains acides aminés comme l'arginine.
Vous aimerez peut-être aussi
- Comprendre Toute La FinanceDocument26 pagesComprendre Toute La Financeمرح و فرفشة50% (2)
- Les Chakras Et Le Corps Éthérique (Coquet Michel)Document217 pagesLes Chakras Et Le Corps Éthérique (Coquet Michel)Teddy Ravatsy100% (1)
- QE de Physiologie EndocrinoDocument12 pagesQE de Physiologie EndocrinoN.Pas encore d'évaluation
- Exploration de L'axe GonadotropeDocument113 pagesExploration de L'axe Gonadotropeyolene mumbaPas encore d'évaluation
- 1 As - Projet 1 Entier (5 Séquences)Document74 pages1 As - Projet 1 Entier (5 Séquences)HacerMellal83% (36)
- Le Système EndocrinienDocument23 pagesLe Système Endocrinienchadi ouechtatiPas encore d'évaluation
- Glande EndocrineDocument30 pagesGlande EndocrineMACON824Pas encore d'évaluation
- Cours 6Document27 pagesCours 6BouabidiPas encore d'évaluation
- Le Cycle Sexuel Chez La Femme TCDocument9 pagesLe Cycle Sexuel Chez La Femme TCSarah DiomandePas encore d'évaluation
- Physiologie Du Complexe Hypothalamo-HypophysaireDocument5 pagesPhysiologie Du Complexe Hypothalamo-HypophysaireZied Bouabene100% (1)
- L'axe Hypothalamo-HypophysaireDocument11 pagesL'axe Hypothalamo-Hypophysairegeorge.guergourPas encore d'évaluation
- UE8 TC Physio Cours 2 - Régulation Endocrinienne Tutorat 2013-2014Document10 pagesUE8 TC Physio Cours 2 - Régulation Endocrinienne Tutorat 2013-2014Ali EL Kihel100% (1)
- Exploration de L Axe GonadotropeDocument14 pagesExploration de L Axe GonadotropeDjouhaina BeggahPas encore d'évaluation
- Rapport de Stage Realisation D Un ERPDocument51 pagesRapport de Stage Realisation D Un ERPmohamed benaichPas encore d'évaluation
- Axe Hypothalamo-Hypophysaire (Resume)Document7 pagesAxe Hypothalamo-Hypophysaire (Resume)Maroua BenchoufiPas encore d'évaluation
- Grand Oral SesDocument2 pagesGrand Oral Sesapi-657069168Pas encore d'évaluation
- A.Saudreau Les Degrees de Vie Spirituel 1 PDFDocument596 pagesA.Saudreau Les Degrees de Vie Spirituel 1 PDFpbelo1Pas encore d'évaluation
- Correction Du Devoir IntroductionDocument5 pagesCorrection Du Devoir IntroductionMme et Mr LafonPas encore d'évaluation
- 02-PHYSIOLOGE DE L'AXE HYPOTHALAMO HYPOPHYSAIRE Poly-1Document3 pages02-PHYSIOLOGE DE L'AXE HYPOTHALAMO HYPOPHYSAIRE Poly-1alimkettouchePas encore d'évaluation
- PHYSIOLOGE DE L'AXE HYPOTHALAMO HYPOPHYSAIRE PolyDocument4 pagesPHYSIOLOGE DE L'AXE HYPOTHALAMO HYPOPHYSAIRE PolyFatima zahra NaciriPas encore d'évaluation
- Régulation Physiologique Du Complexe Hypothalamo - HypophysaireDocument15 pagesRégulation Physiologique Du Complexe Hypothalamo - HypophysaireRyanPas encore d'évaluation
- Le Systeme EndocrinienDocument13 pagesLe Systeme EndocrinienAlexiPas encore d'évaluation
- Axe Hypothalamo HypophysaireDocument4 pagesAxe Hypothalamo HypophysaireAbderahmene GhodbanePas encore d'évaluation
- 3-Cours Endocrinologie Et Régulation Des Systèmes Chapitre 2 M1 TOXICOLOGIE 2020-2021 BOUBEKRIDocument32 pages3-Cours Endocrinologie Et Régulation Des Systèmes Chapitre 2 M1 TOXICOLOGIE 2020-2021 BOUBEKRIBERDJOUH YoucefPas encore d'évaluation
- MNE CM3bis Physiologie Axe Hypothalamo HypophysaireDocument13 pagesMNE CM3bis Physiologie Axe Hypothalamo HypophysaireSoheib RahrahPas encore d'évaluation
- Cours - 3 Les Régulation Hormonale de La MétabolismeDocument9 pagesCours - 3 Les Régulation Hormonale de La Métabolismemiss anthropocenePas encore d'évaluation
- GYNECO Prof MBUYAMBA - 090159Document189 pagesGYNECO Prof MBUYAMBA - 090159reneddymutombo22Pas encore d'évaluation
- 2-Complexe Hypothalamo-Hypophysaire PDFDocument26 pages2-Complexe Hypothalamo-Hypophysaire PDFthierno amadou bahPas encore d'évaluation
- Physiologie de L'Hypophyse: MASTER 1 Médecine 2023Document61 pagesPhysiologie de L'Hypophyse: MASTER 1 Médecine 2023Lorlyna MandzeyiPas encore d'évaluation
- 62 Coursts 08Document4 pages62 Coursts 08Nicoleta ChivuPas encore d'évaluation
- Le Systeme Endocrinien WDocument9 pagesLe Systeme Endocrinien WsafemindPas encore d'évaluation
- Physio Endocrino23-01glandes EndocrinesDocument4 pagesPhysio Endocrino23-01glandes EndocrinesVictorin FANDREBOPas encore d'évaluation
- Ahh M2decineDocument22 pagesAhh M2decinemalakzerizer2005Pas encore d'évaluation
- Notions D'endocrinoDocument119 pagesNotions D'endocrinoyaya camaraPas encore d'évaluation
- La Reproduction Chez Les Mammiferes Resume Lecon2 Module 2Document6 pagesLa Reproduction Chez Les Mammiferes Resume Lecon2 Module 2Antoine S.Pas encore d'évaluation
- Axe HypothalmoDocument43 pagesAxe HypothalmoDoc BelhadjPas encore d'évaluation
- Hypophys e 4Document32 pagesHypophys e 4trx100% (1)
- TP 2 1 Biologie AnimaleDocument7 pagesTP 2 1 Biologie Animaleazertyiashmy1234Pas encore d'évaluation
- Cours Final SomatostatineDocument4 pagesCours Final Somatostatineemawatsn122Pas encore d'évaluation
- 2 Relations Hypothalamus Hypophyse BDocument27 pages2 Relations Hypothalamus Hypophyse BOXGAMINGXOPas encore d'évaluation
- Cours Endocrinologie de La ReproductionDocument49 pagesCours Endocrinologie de La ReproductionLukusa MauricePas encore d'évaluation
- Chapitre V MineDocument19 pagesChapitre V MineMer IemPas encore d'évaluation
- Principes Des Systemes de Controle HormonalDocument2 pagesPrincipes Des Systemes de Controle Hormonalfafoufa133Pas encore d'évaluation
- Hypothalamo HypophysaireDocument8 pagesHypothalamo HypophysaireMaktabatiLB PlannersPas encore d'évaluation
- Les Neurohormones Chez HommeDocument17 pagesLes Neurohormones Chez HommeNisrine 2112Pas encore d'évaluation
- Cours 3Document16 pagesCours 3azizhseck2Pas encore d'évaluation
- Le Système Hypothalamo-Hypophysaire: DR Souleymane THIAM Assistant Biochimie L2S3Document54 pagesLe Système Hypothalamo-Hypophysaire: DR Souleymane THIAM Assistant Biochimie L2S3s22g9ndkwjPas encore d'évaluation
- PDF Document 3Document3 pagesPDF Document 3Fatou Bintou RassoulPas encore d'évaluation
- Axe HPT-HPPDocument36 pagesAxe HPT-HPPRezagui ImadPas encore d'évaluation
- 5-La Corticosurrénale (CS)Document32 pages5-La Corticosurrénale (CS)DëLux OwOPas encore d'évaluation
- 2014 7 Le Systeme EndocrinienDocument15 pages2014 7 Le Systeme EndocrinienSamira MBasskarPas encore d'évaluation
- Endocrinologie IDocument88 pagesEndocrinologie Iritajbeily1611Pas encore d'évaluation
- Révisions 2.2Document16 pagesRévisions 2.2lenapaquiePas encore d'évaluation
- 2-Axehthp M1bse EtudiantsDocument50 pages2-Axehthp M1bse EtudiantsHq sishPas encore d'évaluation
- Document de L'hypothalamus, Fiche MedecineDocument1 pageDocument de L'hypothalamus, Fiche Medecine00mohamedjbeli00Pas encore d'évaluation
- T3A2 Sexualite Et ProcreationDocument34 pagesT3A2 Sexualite Et ProcreationBechirMoussiPas encore d'évaluation
- Relation Hypothalamo-HypophysaireDocument8 pagesRelation Hypothalamo-HypophysaireAsla AsmaPas encore d'évaluation
- Endocrinologie Fœto-PlacentaireDocument21 pagesEndocrinologie Fœto-PlacentaireNour ALPas encore d'évaluation
- Fichier Produit 2218Document5 pagesFichier Produit 2218Alycia SafaPas encore d'évaluation
- 5.0 Endocrinologie NaassilaDocument62 pages5.0 Endocrinologie NaassilaMohamed AraouchiPas encore d'évaluation
- T3A2 Acti2 FCTT OvairesDocument3 pagesT3A2 Acti2 FCTT Ovairesbianca fPas encore d'évaluation
- Retenir Seq 5 Part 3Document6 pagesRetenir Seq 5 Part 3Julia NicolettiPas encore d'évaluation
- Physiologie Endocrinienne m1023Document71 pagesPhysiologie Endocrinienne m1023liliahadjali57Pas encore d'évaluation
- 9.fonctions Gonadiques FémininesDocument51 pages9.fonctions Gonadiques FémininesAmmar ChaouiPas encore d'évaluation
- Axe Hypothalamo-HypophysaireDocument25 pagesAxe Hypothalamo-HypophysaireAnfelDiivaPas encore d'évaluation
- TD1 Regulation SABRINA.2019Document5 pagesTD1 Regulation SABRINA.2019axelPas encore d'évaluation
- Hormones HypothalamiquesDocument14 pagesHormones Hypothalamiquesdjamila benaissaPas encore d'évaluation
- Activité - Les Pièces de La MaisonDocument4 pagesActivité - Les Pièces de La MaisonlakhanicherishalPas encore d'évaluation
- Demande de StageDocument1 pageDemande de StageIbrahima SkPas encore d'évaluation
- Evaluation Diagnostique - 1 BACSDocument2 pagesEvaluation Diagnostique - 1 BACSmeryemPas encore d'évaluation
- Etat Et JusticeDocument12 pagesEtat Et Justicenoa.blain49Pas encore d'évaluation
- Bounty Maison LightDocument2 pagesBounty Maison LightArribardPas encore d'évaluation
- (Brico) Tridome - 19 Poser Une FenêtreDocument2 pages(Brico) Tridome - 19 Poser Une FenêtreMadidj_2014Pas encore d'évaluation
- BOMP 1525 Du Mardi 13 Août 2019Document84 pagesBOMP 1525 Du Mardi 13 Août 2019Moussa Karim AlioPas encore d'évaluation
- EcoChap2 Défaillances Etat Marché Découvrir Cours Hamza MustafaDocument3 pagesEcoChap2 Défaillances Etat Marché Découvrir Cours Hamza Mustafahamza attariPas encore d'évaluation
- FAQ OBD-Honda FRDocument3 pagesFAQ OBD-Honda FRCarlos SoaresPas encore d'évaluation
- L'ego-Histoire en PerspectiveDocument11 pagesL'ego-Histoire en PerspectiveNicoleta AldeaPas encore d'évaluation
- Art Du MontageDocument18 pagesArt Du MontageAndré FélixPas encore d'évaluation
- Offre de ServiceDocument6 pagesOffre de Services.elgasmiPas encore d'évaluation
- Bertrand, Alexandre Louis Joseph (1820-1902) - La Religion Des Gaulois Les Druides Et La Druidisme (E. Leroux, 1897)Document394 pagesBertrand, Alexandre Louis Joseph (1820-1902) - La Religion Des Gaulois Les Druides Et La Druidisme (E. Leroux, 1897)highrangePas encore d'évaluation
- Correction Projets PowerPointDocument16 pagesCorrection Projets PowerPointrakez bassemPas encore d'évaluation
- ArticleDocument18 pagesArticleAbderrahim ElPas encore d'évaluation
- Cps Type Des Marches de Travaux 2015Document29 pagesCps Type Des Marches de Travaux 2015azoughPas encore d'évaluation
- 9.douleur ThoraciqueDocument22 pages9.douleur ThoraciqueFerhani OuaPas encore d'évaluation
- Orca Share Media1663662719481 6977907198972110101Document43 pagesOrca Share Media1663662719481 6977907198972110101Bilel LoussifPas encore d'évaluation
- Fiches TD Micro IIIDocument4 pagesFiches TD Micro IIIABRAHAM NENE100% (1)
- QCM Séisme À ImprimerDocument18 pagesQCM Séisme À ImprimerDieudonné AdokoPas encore d'évaluation
- Daressy Statues I 1906Document427 pagesDaressy Statues I 1906Eugenia MuñozPas encore d'évaluation
- Les Imperfections de L Oeil 2Document5 pagesLes Imperfections de L Oeil 2s18db911Pas encore d'évaluation
- RCAD Acier Manuel FR 50Document284 pagesRCAD Acier Manuel FR 50Nanescu LilianaPas encore d'évaluation