Académique Documents
Professionnel Documents
Culture Documents
Exercices - Evolution Spontanée - Chapitre 7 - Correction
Transféré par
Marwan AzertyTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Exercices - Evolution Spontanée - Chapitre 7 - Correction
Transféré par
Marwan AzertyDroits d'auteur :
Formats disponibles
Physique-chimie - Classe de Terminale Spécialité
Correction - Exercices d’entrainement : Evolution spontanée d’un système chimique
Exercice 3 : Durée de fonctionnement d’une pile cuivre-aluminium
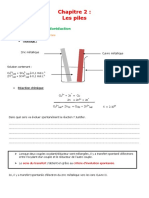
1. Réaliser le schéma rigoureusement légendé de la pile.
A ajouter sur le schéma :
Sens de circulation de I
Sens de circulation des e-
Ions présents dans le
pont salin (si donné dans
l’exercice)
Bornes de l’ampèremètre
(mA et COM)
Vocabulaire :
Cathode + et Anode -
2. L’ampèremètre indique que le courant circule de la plaque de cuivre vers la plaque d’aluminium à l’extérieur de la
pile. Préciser, en le justifiant, la polarité de la pile. Compléter votre schéma en indiquant cette polarité.
Le courant circule de la plaque de cuivre vers la plaque d'aluminium, les électrons circulent donc de la plaque
d'aluminium vers la plaque de cuivre. La plaque d'aluminium (borne –) libère des électrons qui sont
consommés à la plaque de cuivre (borne +).
3. L’équation d’oxydoréduction de fonctionnement de la pile est : 3 Cu2+ (aq) + 2Al (s) = 3 Cu (s) + 2 Al3+ (aq). Écrire
les équations des réactions se produisant à chaque électrode.
A la cathode (+), il se produit une réduction, soit consommation d'électrons telle que :
Cu2+ (aq) + 2e– = Cu (s)
A l'anode (–), il se produit une oxydation, soit une libération d'électrons telle que : Al (s) = Al3+ (aq) + 3e–
D’après le principe de Lavoisier, les deux demi-équations s’équilibre entre-elles ; l’échange électronique doit
être le même :
Cu2+ (aq) + 2e– = Cu (s) x3
Al (s) = Al3+ (aq) + 3 e– x2
Il vient l’équation d’oxydoréduction ayant lieu : 3 Cu2+ (aq) + 2Al (s) 3 Cu (s) + 2 Al3+ (aq)
4. La constante d’équilibre associée à l’équation d’oxydoréduction est K = 10200. Déterminer le quotient initial de
réaction du système ainsi constitué. Le sens d’évolution du système étudié est-il cohérent ?
A près avoir appliqué la définition du quotient de réaction [à faire], on obtient :
Avec : [Cu]i = [Al]i = 1 mol.L-1 par approximation
Qr,i = [calcul à poser] = 2,0 (2 c.s) < K = 10200 ; la transformation est donc effectuée dans le sens direct.
La transformation évolue dans le sens de la formation de cuivre solide Cu (s) et d'ions aluminium Al3+ (aq).
Ce qui est cohérent avec le sens du courant obtenu expérimentalement.
Étude de la pile en fonctionnement
1. Déterminer les quantités de matière initiales en moles des réactifs de l’équation chimique (1). Compléter le
tableau descriptif de l’évolution du système. En déduire la valeur de l’avancement maximal.
ni (Cu2+) = [Cu2+]i × Vsolution = 5,0.10–1 × 50.10–3 = 2,5.10–2 mol
ni (Al) = m(Al)/M(Al) = 1,0/27,0 = 3,7.10-2 mol
Physique-chimie - Classe de Terminale Spécialité
Équation 3 Cu2+(aq) + 2 Al(s) 3 Cu(s) + 2 Al3+(aq)
Avancement
État du système Quantités de matière (mol)
(mol)
ni (Cu2+) = ni (Al) = ni (Cu) = ni (Al3+) =
État initial 0
2,5.10–2 mol 3,7.10-2 mol 14.10–2 mol 2,5.10–2 mol
En cours de
x ni (Cu2+) - 3x ni (Al3+) – 2x ni (Cu) - 3x ni (Al3+) - 2x
transformation
Afin de retrouver le réactif limitant, on a autant d’hypothèses que de réactifs :
Si Cu2+ (aq) est le réactif limitant, alors : ni (Cu2+) - 3xmax = 0 mol.
Soit, xmax = ni (Cu2+)/3 = (2,5.10-2)/3 = 8,3.10-3 mol.
Si Al (s) est le réactif limitant, alors : ni (Al3+) – 2x’max = 0 mol.
Soit, x’max = ni (Al3+)/2 = (3,7.10-2)/2 = 1,9.10-9 mol.
Le réactif limitant est donc Cu2+ (aq) tel que : xmax = 8,3.10-3 mol < x’max = 1,9.10-9 mol.
2. Calculer la quantité maximale d’électricité que peut débiter cette pile.
D’après les deux demi-équations, six électrons sont transférés au circuit extérieur. Ainsi, jusqu’à l’usure de
la pile, il y a 6xmax e- transférés entre les deux électrodes par le circuit extérieur tel que :
Qmax = n(e-).F = 6xmax x F Soit, Qmax = 6 x 8,3.10-3 x 9,6.104 = 4,8.103 C
Vous aimerez peut-être aussi
- Experiences de Chimie - Aspects Pedagogiques Et Sequences D'enseignement - Capes - Capet - AgregationDocument544 pagesExperiences de Chimie - Aspects Pedagogiques Et Sequences D'enseignement - Capes - Capet - AgregationAmadou Soufi Diallo100% (1)
- 2012 Centrale MP Physique Chimie - CorrigéDocument8 pages2012 Centrale MP Physique Chimie - CorrigéLarbi BadrourPas encore d'évaluation
- Les Ormus La Poudre Miraculeuse - LA TERRE ET SES ENIGMESDocument10 pagesLes Ormus La Poudre Miraculeuse - LA TERRE ET SES ENIGMESAdli AdilPas encore d'évaluation
- 2021 09 Metro Sujet2 Correction ExoB Pile 5ptsDocument5 pages2021 09 Metro Sujet2 Correction ExoB Pile 5ptsDany ObeidPas encore d'évaluation
- 2010 09 Antilles Exo1 Sujet Zinc 6 5ptsDocument4 pages2010 09 Antilles Exo1 Sujet Zinc 6 5ptsPablo VidalPas encore d'évaluation
- Chimie C Chap11 ElectrolyseDocument5 pagesChimie C Chap11 Electrolysemghaete100% (1)
- PilesDocument17 pagesPilesOthmane HassounPas encore d'évaluation
- 2017-2018 Ie2Document4 pages2017-2018 Ie2Eugene FoucherPas encore d'évaluation
- Chapitre 7, Transformations Spontanées Dans Les Piles Et Récupération de L'énergie, Activités, Exercices D'application, 2BAC BIOF, PR JENKAL RACHIDDocument3 pagesChapitre 7, Transformations Spontanées Dans Les Piles Et Récupération de L'énergie, Activités, Exercices D'application, 2BAC BIOF, PR JENKAL RACHIDaristide mabialaPas encore d'évaluation
- Bacblanc PC Option PC Verfrancais 020Document5 pagesBacblanc PC Option PC Verfrancais 020JASSERPas encore d'évaluation
- Chimie Série 4 FBDocument10 pagesChimie Série 4 FBZayd Taibi0% (1)
- Seri PilesDocument3 pagesSeri Pilessaid khachouPas encore d'évaluation
- TD Électrochimie de Chimie Analytique 2eme Année Pharmacie DR DJAOUDocument5 pagesTD Électrochimie de Chimie Analytique 2eme Année Pharmacie DR DJAOUmoh moh100% (1)
- 2007 Afrique Spe Correction Piles 4ptsDocument2 pages2007 Afrique Spe Correction Piles 4ptsMartin SALEHPas encore d'évaluation
- 2003 09 Polynesie Sujet Exo1 Pile OxRed 6 5ptsDocument2 pages2003 09 Polynesie Sujet Exo1 Pile OxRed 6 5ptskjnokinikoPas encore d'évaluation
- 09 Les Piles CorrectionDocument6 pages09 Les Piles CorrectionChartier Julien100% (1)
- 5351 Entrainement TSDocument6 pages5351 Entrainement TSmohammed laadili100% (1)
- Transformations Spontanées Dans Les PilesDocument4 pagesTransformations Spontanées Dans Les PilesHassan OubassourPas encore d'évaluation
- 0809 CpilesDocument4 pages0809 CpilesHarilaza Ny aina RZFPas encore d'évaluation
- Cours 1 Les Piles Et Récupération D'énergieDocument6 pagesCours 1 Les Piles Et Récupération D'énergieBOURASSPas encore d'évaluation
- PilechimiqueDocument2 pagesPilechimiqueSaid OumansourPas encore d'évaluation
- C23 - Correction Exercice 9Document1 pageC23 - Correction Exercice 9mohamed abdoulkaderPas encore d'évaluation
- Devoir de Synthèse N°3 Avec Correction - Sciences Physiques - Bac Technique (2015-2016) MR Ridha SlimiDocument7 pagesDevoir de Synthèse N°3 Avec Correction - Sciences Physiques - Bac Technique (2015-2016) MR Ridha SlimiMeriam KooliPas encore d'évaluation
- Piles Corriges D ExercicesDocument3 pagesPiles Corriges D ExercicesAmine AlaoUii AlaouiPas encore d'évaluation
- Devoir 1 Modele 1 Physique Chimie 2 Bac SPC Semestre 2 Corrige 1Document2 pagesDevoir 1 Modele 1 Physique Chimie 2 Bac SPC Semestre 2 Corrige 1Moukil ÀYoùbPas encore d'évaluation
- 1 - Transformation Spontanées Dans Le Piles Et Production D'énergieDocument7 pages1 - Transformation Spontanées Dans Le Piles Et Production D'énergieTaha BoulmanePas encore d'évaluation
- PilesDocument6 pagesPilesmohamed laghribPas encore d'évaluation
- AE Fabrication D'une Pile Cuivre-ZincDocument4 pagesAE Fabrication D'une Pile Cuivre-ZincsocranedeoufPas encore d'évaluation
- TD Elec3Document13 pagesTD Elec3nnzokomeoliennePas encore d'évaluation
- Exercices 9 Les Piles Et Récupération D'énergieDocument1 pageExercices 9 Les Piles Et Récupération D'énergieMajed GharibPas encore d'évaluation
- Exercices Chimie Des MatériauxDocument14 pagesExercices Chimie Des Matériaux7box.bePas encore d'évaluation
- SeÌ Rie 1 - Transformation Spontaneì Es Dans Le Piles (WWW - AdrarPhysic.Fr) 3Document2 pagesSeÌ Rie 1 - Transformation Spontaneì Es Dans Le Piles (WWW - AdrarPhysic.Fr) 3b01554837Pas encore d'évaluation
- Série N°17Document4 pagesSérie N°17Jihad ELPas encore d'évaluation
- Fiche Exercies Les Piles-TsDocument10 pagesFiche Exercies Les Piles-Tsmalou230193100% (2)
- CH17 ExercicesDocument3 pagesCH17 ExercicesSamuel ZougbedePas encore d'évaluation
- Fiche Cours11 Les PilesDocument4 pagesFiche Cours11 Les PilesLesGens Bossent0% (1)
- Chapitre 2 2011-2012 Les Piles ElectrochimiqueDocument8 pagesChapitre 2 2011-2012 Les Piles ElectrochimiqueHAMADA19720% (1)
- TD - Electrochimie - IUT Bobo Mai 2022Document5 pagesTD - Electrochimie - IUT Bobo Mai 2022Abdoul Kader OUATTARAPas encore d'évaluation
- Les Piles 1Document4 pagesLes Piles 1lamia lamiaPas encore d'évaluation
- Devoir 1 Physique Et Chimie 2bac Sciences Physiques BIOF 2nd Semestre Modele 1Document5 pagesDevoir 1 Physique Et Chimie 2bac Sciences Physiques BIOF 2nd Semestre Modele 1Niaama SabsiboPas encore d'évaluation
- Simili 2020-Converti PDFDocument7 pagesSimili 2020-Converti PDFyasmine mahmoud100% (1)
- 2006 Reunion Exo1 Correction Pile Condo 8ptsDocument3 pages2006 Reunion Exo1 Correction Pile Condo 8ptsaa.aa1Pas encore d'évaluation
- 2017-2018 IE2 CorrigeDocument4 pages2017-2018 IE2 CorrigeEugene FoucherPas encore d'évaluation
- Chimie C Chap10 Les PilesDocument7 pagesChimie C Chap10 Les PilesImed LatrechPas encore d'évaluation
- ds3 4eme Sadiki 13 ScExpDocument4 pagesds3 4eme Sadiki 13 ScExpLotfi Bouchareb0% (1)
- EXO4Document6 pagesEXO4Arthur Franck Patrick BledouPas encore d'évaluation
- Transformations Spontanees Dans Les Piles Et Production D Energie Exercices Non Corriges 5Document5 pagesTransformations Spontanees Dans Les Piles Et Production D Energie Exercices Non Corriges 5qwerty aertyPas encore d'évaluation
- Alfiziaa Oalkimiaa Alom Fiziaiia 2014 Aldora Alistdrakia Almodhoa 2Document7 pagesAlfiziaa Oalkimiaa Alom Fiziaiia 2014 Aldora Alistdrakia Almodhoa 2linaichrak06Pas encore d'évaluation
- Devoir Blanc VDocument6 pagesDevoir Blanc Vzack slPas encore d'évaluation
- TD ElectrochimieDocument4 pagesTD ElectrochimieRaja RajouPas encore d'évaluation
- Chap Piles CouleurDocument4 pagesChap Piles CouleurIsmail ait talebPas encore d'évaluation
- Examen PC Juillet 2014 2bac FRDocument7 pagesExamen PC Juillet 2014 2bac FRmedPas encore d'évaluation
- 1ère D DEVOIR - CopierDocument17 pages1ère D DEVOIR - CopierSawadogoPas encore d'évaluation
- SiwarDocument2 pagesSiwarYoussef ChaouachiPas encore d'évaluation
- Examen National Physique Chimie SPC 2012 Normale SujetDocument6 pagesExamen National Physique Chimie SPC 2012 Normale Sujetlina khalloqPas encore d'évaluation
- Série Les PilesDocument4 pagesSérie Les Pilesookayokay15Pas encore d'évaluation
- Serie n15Document4 pagesSerie n15Yossri HmaiedPas encore d'évaluation
- Devoir 1 S2 2 Bac STE (WWW - Pc1.ma)Document4 pagesDevoir 1 S2 2 Bac STE (WWW - Pc1.ma)medPas encore d'évaluation
- TD Métallurgie SE1 Exercice 1: Université Moulay Ismail ENSAM, MeknèsDocument8 pagesTD Métallurgie SE1 Exercice 1: Université Moulay Ismail ENSAM, Meknèsmathématiques de zéro. physiques de zéro.100% (1)
- 2013 09 Antilles Exo2 Correction Ibuprofene 11ptsDocument2 pages2013 09 Antilles Exo2 Correction Ibuprofene 11ptsMarwan AzertyPas encore d'évaluation
- Exercices - Cinétique Chimique - Chapitre 6 - CorrectionDocument5 pagesExercices - Cinétique Chimique - Chapitre 6 - CorrectionMarwan AzertyPas encore d'évaluation
- 2013 09 Antilles Exo2 Correction Ibuprofene 11ptsDocument2 pages2013 09 Antilles Exo2 Correction Ibuprofene 11ptsMarwan AzertyPas encore d'évaluation
- Exercices - Cinétique Chimique - Chapitre 6 - CorrectionDocument5 pagesExercices - Cinétique Chimique - Chapitre 6 - CorrectionMarwan AzertyPas encore d'évaluation
- Ressources Complémentaires Activités de GroupeDocument2 pagesRessources Complémentaires Activités de GroupeMarwan AzertyPas encore d'évaluation
- Ressources Complémentaires Activités de GroupeDocument2 pagesRessources Complémentaires Activités de GroupeMarwan AzertyPas encore d'évaluation
- Exercices - Cinétique Chimique - Chapitre 6Document3 pagesExercices - Cinétique Chimique - Chapitre 6Marwan Azerty100% (2)
- 2013 09 Antilles Exo2 Correction Ibuprofene 11ptsDocument2 pages2013 09 Antilles Exo2 Correction Ibuprofene 11ptsMarwan AzertyPas encore d'évaluation
- Serie D'exercices Sur C5 Et C6: IA Kédougou - Cellule Mixte Des Sciences Physiques - Terminale S 2019-2020Document4 pagesSerie D'exercices Sur C5 Et C6: IA Kédougou - Cellule Mixte Des Sciences Physiques - Terminale S 2019-2020kathyPas encore d'évaluation
- Chapitre 1Document19 pagesChapitre 1douoPas encore d'évaluation
- Corrige Enzmeta Sv4 Srp16 AlifDocument2 pagesCorrige Enzmeta Sv4 Srp16 AlifAzizPas encore d'évaluation
- Comment Les Roches Endogenes S Alterent EllesDocument2 pagesComment Les Roches Endogenes S Alterent Ellesochou kokola jean ericPas encore d'évaluation
- Chimie Des Solutions - Exam-SN - 21-22Document1 pageChimie Des Solutions - Exam-SN - 21-22hichamakaya1Pas encore d'évaluation
- RamanDocument6 pagesRamanuyuyiuiuiPas encore d'évaluation
- 2014 Physique Chimie Juin 2014Document7 pages2014 Physique Chimie Juin 2014NamelessPas encore d'évaluation
- Brochure TP AsperineDocument7 pagesBrochure TP AsperineNina NinaPas encore d'évaluation
- Document 1: Synthèse de L'aspirineDocument4 pagesDocument 1: Synthèse de L'aspirineSa LimPas encore d'évaluation
- Tableau Mendeleiev DefisCEADocument1 pageTableau Mendeleiev DefisCEAعبدالرزاق اغزيلPas encore d'évaluation
- Decroissance RadioactiveDocument11 pagesDecroissance Radioactivedawd.bouzaherPas encore d'évaluation
- Corrige Exo 2 Titrages DirectsDocument2 pagesCorrige Exo 2 Titrages Directssouhailbusiness2005Pas encore d'évaluation
- VS-Series Operators ManualDocument113 pagesVS-Series Operators ManualA'nnaial AlmogadamPas encore d'évaluation
- CC2 SujetaDocument1 pageCC2 SujetaJULIENPas encore d'évaluation
- Expose EnvironnementDocument30 pagesExpose EnvironnementdarzzzPas encore d'évaluation
- Solutions 3Document19 pagesSolutions 3Cheikh Ismaïla BAPas encore d'évaluation
- Vie D'un Médicament de La Conception PDFDocument9 pagesVie D'un Médicament de La Conception PDFLawrence Mundene-timotheePas encore d'évaluation
- Métallurgie Du Chrome: Alain DefranceDocument15 pagesMétallurgie Du Chrome: Alain Defranceimen mehriPas encore d'évaluation
- Memoire Final 2022Document97 pagesMemoire Final 2022FATIH HALIMAPas encore d'évaluation
- Voiture A Biocarburant de 2eme Et 3eme Generation 0Document6 pagesVoiture A Biocarburant de 2eme Et 3eme Generation 0Vidal KabeyaPas encore d'évaluation
- Terminale S Devoir en Classe N°5 08/04/2006: CHIMIE: L'acide BenzoïqueDocument2 pagesTerminale S Devoir en Classe N°5 08/04/2006: CHIMIE: L'acide BenzoïqueNaouma ChahdPas encore d'évaluation
- Opti Lion Ops Guide FrenchDocument176 pagesOpti Lion Ops Guide FrenchKader SmailiPas encore d'évaluation
- Devoir Surveille N2 TS1 17-12-2022Document2 pagesDevoir Surveille N2 TS1 17-12-2022Serigne Abdou NiassePas encore d'évaluation
- ModélisationDocument22 pagesModélisationdinoPas encore d'évaluation
- CHIMIE Orga n3 Pharma Etudes 2022Document2 pagesCHIMIE Orga n3 Pharma Etudes 2022mariamtolo48Pas encore d'évaluation
- Hermida 2008Document212 pagesHermida 2008BelzébuthAbscissePas encore d'évaluation
- Osmose InverseDocument3 pagesOsmose InverseMohamed OudorPas encore d'évaluation
- Sujet 20de 20stage 20P2023 5fFuseMetal-FADocument2 pagesSujet 20de 20stage 20P2023 5fFuseMetal-FAJihen BoukadidaPas encore d'évaluation