Académique Documents
Professionnel Documents
Culture Documents
Cinétique Chimique Exercices - 06
Transféré par
neval chenchouniTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Cinétique Chimique Exercices - 06
Transféré par
neval chenchouniDroits d'auteur :
Formats disponibles
Université KASDI MERBAH –Ouargla-
Faculté des Sciences, de la Technologie et des Sciences de la matière
Département de Génie des Procédés
3ème année Licence LMD Génie des Procédés
TD : Cinétique chimique 2011-2012
Série II
Ex 1 :
La réaction de dissociation isotherme en phase gazeuse de NH3, en N2 et H2 est suivie par la mesure
du temps de demi-réaction (t1/2) pour des pressions initiales variables (P0). On obtient les résultats
suivants :
P0 (mm Hg) 280 140 70
T1/2 (min) 8.0 4.0 2.0
Déterminer l’ordre et la constante de vitesse apparente. (On supposera que les gaz ce comportent
comme des gaz parfaits).
Ex 2 :
Dans un réacteur fermé, la décomposition catalytique de l’hydrazine (N2H4) sur du tungstène à 1200
o
C donne les résultats suivants :
P0 (mm Hg) 310 150 65
T1/2 (min) 8.0 3.89 1.67
1- Montrer que la réaction est d’ordre zéro.
2-Calculer la constante de vitesse.
Ex 3 :
Dans un réacteur fermé, l’éthylamine se décompose selon la réaction :
C2H5NH2 (g) → C2H4 (g) + NH3 (g)
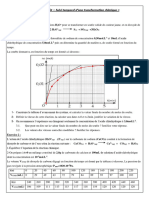
la réaction a lieu à 500 oC et la pression initiale de 55 mmHg. Les mesures de la variation de
pression totale en fonction du temps sont résumées dans le tableau suivant :
t(min) 1 2 4 8 10 20 30 40
ΔP(mmHg) 5 9 17 29 34 47 52 53.5
1- Montrer que la réaction est de premier ordre.
2-Calculer la constante de vitesse, puis le temps de demi-réaction.
Université KASDI MERBAH –Ouargla-
Faculté des Sciences, de la Technologie et des Sciences de la matière
Département de Génie des Procédés
3ème année Licence LMD Génie des Procédés
TD : Cinétique chimique 2011-2012
Série III
Ex 1 :
L’azoéthane se décompose dans réacteur fermé à 300 oC selon la réaction :
C2H5N= NC2H5 (g) → C4H10 (g) + N2 (g).
Cette décomposition suit une loi cinétique du premier ordre.
1- Déterminer la fraction η de l’azoéthane décomposé au bout de 2 minutes, sachant que
l’augmentation de pression est de 10%. La pression initiale est égale à 150 mmHg.
2- Calculer la constante de vitesse k de la réaction à 25 oC sachant que l’énergie d’activation est
égale à 200 kJ/mole.
3- Calculer le temps nécessaire pour obtenir un taux de décomposition de 10% à 25 oC.
Ex 2 :
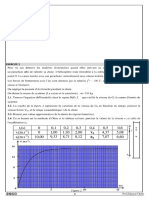
A 530 oC, le proanal se décompose en éthane et monoxyde de carbone selon la réaction :
C2H5COH (g) → C2H6 (g) + CO (g).
On mesure le temps de demi-réaction à différentes pressions initiales. On a ainsi les résultats :
P0 (mmHg) 60 121 184 290 420 479
t1/2(s) 1480 820 665 492 385 328
1- Déterminer l’ordre de la réaction.
2-Calculer la constante de vitesse.
Ex 3 :
On introduit 10-2 mole de soude NaOH et 10-2 mole d’un ester soluble dans 1 litre d’eau à 27 0C.
1- Sachant que la réaction est d’un ordre global égal à deux et qu’au bout de 2 heures, les 3/4 de
l’ester sont saponifiés. Calculer la constante de vitesse et le temps de demi-réaction.
2- La vitesse de la réaction est multipliée par quatre lorsque la température passe de 27 0C à 127 0C.
Calculer le temps de demi-réaction à 127 0C ainsi que l’énergie d’activation de la réaction.
Vous aimerez peut-être aussi
- Série Corrigé CinétiqueDocument8 pagesSérie Corrigé Cinétiquejakobslimani02Pas encore d'évaluation
- Exo Cinetique Corrige AmmadoucheDocument82 pagesExo Cinetique Corrige AmmadouchetalebPas encore d'évaluation
- Serie de TD N°123 L2 Raff 22 23Document5 pagesSerie de TD N°123 L2 Raff 22 23Clash of Clans Bilal DzPas encore d'évaluation
- TD Cin & Cat SMC S5 .Document32 pagesTD Cin & Cat SMC S5 .Chai Mae100% (3)
- FDS - TD Cinétique Chimique - 2013Document6 pagesFDS - TD Cinétique Chimique - 2013Lenz Daniel Jean Paul100% (1)
- Soutien Pcsi 3 Vitesse Et Loi de VitesseDocument5 pagesSoutien Pcsi 3 Vitesse Et Loi de VitesseHarakat ElhoucinePas encore d'évaluation
- S Rie D Exercices Corrig S Cin TiqueDocument6 pagesS Rie D Exercices Corrig S Cin Tiqueanie KheliliPas encore d'évaluation
- Exercices - Série 01avec Correction (Réacteurgp)Document2 pagesExercices - Série 01avec Correction (Réacteurgp)Cherif LaifaPas encore d'évaluation
- Srie Dexos Cintique L3-GPDocument6 pagesSrie Dexos Cintique L3-GPFatima YahiaPas encore d'évaluation
- TD Cin & Cat SMC s5 Série 1-5 Enoncés 2020-2021Document11 pagesTD Cin & Cat SMC s5 Série 1-5 Enoncés 2020-2021Chai MaePas encore d'évaluation
- TD HLCH420 Cinétique Chimique 16-17Document4 pagesTD HLCH420 Cinétique Chimique 16-17y_aitabdellahPas encore d'évaluation
- TD 2Document3 pagesTD 2Simo ELyamani100% (2)
- Exercice Corrigé CinétiqueDocument13 pagesExercice Corrigé Cinétiquejakobslimani02Pas encore d'évaluation
- TD 05 06 ChimieDocument4 pagesTD 05 06 ChimieWalid aghazafiPas encore d'évaluation
- Fiche TD N01Document2 pagesFiche TD N01amiira bouzouadaPas encore d'évaluation
- 6 TDPCSIcinetique 2015Document8 pages6 TDPCSIcinetique 2015Nguissaly SonkoPas encore d'évaluation
- Cinétique Chimique Exercices 01.TextMarkDocument4 pagesCinétique Chimique Exercices 01.TextMarkAbedPas encore d'évaluation
- Cinetique-chimique-Exercices 01 CompressedDocument4 pagesCinetique-chimique-Exercices 01 Compressedelmadani boutayebPas encore d'évaluation
- Série TD N°1. Chimie IIDocument2 pagesSérie TD N°1. Chimie IIchaima gasmi100% (1)
- TD Thermodynamique Des ÉquilibresDocument19 pagesTD Thermodynamique Des Équilibresbrahimza61Pas encore d'évaluation
- Serie1 Corrigé CinetiqueDocument7 pagesSerie1 Corrigé Cinetiquemohammed laadili100% (2)
- TD Procédés Dadsorption Et SéparationDocument3 pagesTD Procédés Dadsorption Et SéparationDZ TECH100% (3)
- Td1 - Thermodynamique - 1Document5 pagesTd1 - Thermodynamique - 1abderrahmane lalaouiPas encore d'évaluation
- 2024 - Devoir 2 - Cinétique ChimiqueDocument3 pages2024 - Devoir 2 - Cinétique Chimiqueredbubbllee.nPas encore d'évaluation
- TDcinét Chim.17-18Document3 pagesTDcinét Chim.17-18Joseph AmondPas encore d'évaluation
- Travaux DirigésDocument9 pagesTravaux Dirigéssad girlPas encore d'évaluation
- Exercices CINETIQUE L2-2016-2017Document4 pagesExercices CINETIQUE L2-2016-2017Fati Fleur100% (5)
- Série Cinétique ChimiqueDocument1 pageSérie Cinétique ChimiqueYoucef KrPas encore d'évaluation
- Serie 1 Cinétique Et Catalyse Homogã Ne.2023Document3 pagesSerie 1 Cinétique Et Catalyse Homogã Ne.2023st13.chelabi212131033628Pas encore d'évaluation
- Thermochimie SMPC - TDDocument26 pagesThermochimie SMPC - TDoulaidPas encore d'évaluation
- Exercices Cinétique (Loi de Vitesse) - EtingueDocument2 pagesExercices Cinétique (Loi de Vitesse) - EtingueLenz Daniel Jean PaulPas encore d'évaluation
- TD2 Chimie Generale +CORRIGE 2016-2017Document10 pagesTD2 Chimie Generale +CORRIGE 2016-2017Awatif BePas encore d'évaluation
- TD1 ThermochimieDocument2 pagesTD1 ThermochimieHamza Hamizo100% (1)
- C.P 22-23 CinetiqueDocument2 pagesC.P 22-23 CinetiquediarratogsibPas encore d'évaluation
- PDFDocument1 pagePDFabderrachid bouzinePas encore d'évaluation
- Série + Corrigè de La Série de TD N°1 FinaleDocument8 pagesSérie + Corrigè de La Série de TD N°1 Finaleemiliabelkacemi100% (1)
- TD 1 Thermochimie L2CDocument2 pagesTD 1 Thermochimie L2Cmeyemarion99Pas encore d'évaluation
- Série 1Document4 pagesSérie 1Lamia ALACHAHER100% (1)
- Cinétique Chimique Exercices 04.TextMarkDocument16 pagesCinétique Chimique Exercices 04.TextMarkAbedPas encore d'évaluation
- TD 4 La ThermochimieDocument6 pagesTD 4 La Thermochimiekouma100% (1)
- Série 1 - Thermochimie - 2APDocument2 pagesSérie 1 - Thermochimie - 2APAyoub AitboubkerPas encore d'évaluation
- Série D'exercices #2 (1 Principe de La Thermodynamique)Document3 pagesSérie D'exercices #2 (1 Principe de La Thermodynamique)RaoufyyPas encore d'évaluation
- TD Thermodynamique Et Chimie Des Solutions Salamani ADocument6 pagesTD Thermodynamique Et Chimie Des Solutions Salamani Asalma koudriPas encore d'évaluation
- Résolutions Des TDDocument41 pagesRésolutions Des TDghislain AlowakinnouPas encore d'évaluation
- TD1 GMP2 2022Document3 pagesTD1 GMP2 2022Hassan ChehouaniPas encore d'évaluation
- TD N°1) Chimie Phy 2023Document2 pagesTD N°1) Chimie Phy 2023riyan raisPas encore d'évaluation
- 2019-2020 TD Total.Document7 pages2019-2020 TD Total.asics tigerPas encore d'évaluation
- Cahier de TD (Thermodynamique)Document41 pagesCahier de TD (Thermodynamique)yousraghanem23Pas encore d'évaluation
- 11 Thermochimie1 Td-EnonceDocument3 pages11 Thermochimie1 Td-Enoncecours importantPas encore d'évaluation
- Ex 1Document2 pagesEx 1soulaimaneelaouni220Pas encore d'évaluation
- TD Cinetique ChimiqueDocument3 pagesTD Cinetique ChimiqueSimplice Assemien100% (3)
- Poly TD Dynamique 2018-19Document13 pagesPoly TD Dynamique 2018-19kasoolPas encore d'évaluation
- SuiviDocument3 pagesSuivihahaPas encore d'évaluation
- Travaux Diriges de Cinetique Chimique L1Document4 pagesTravaux Diriges de Cinetique Chimique L1Mama El karimiPas encore d'évaluation
- M28 Cinétique TD1Document2 pagesM28 Cinétique TD1Hassan DriouachPas encore d'évaluation
- Série de TD N°2 Final PDFDocument2 pagesSérie de TD N°2 Final PDFAbderrahmane100% (1)
- Electrochimie GP Ef 2017correctionDocument4 pagesElectrochimie GP Ef 2017correctionAbdelatif100% (2)
- Titrage Suivi Par PotentiométrieDocument6 pagesTitrage Suivi Par Potentiométrieneval chenchouniPas encore d'évaluation
- Médiamutation Du ManganèseDocument3 pagesMédiamutation Du Manganèseneval chenchouni100% (1)
- Le Mercure Et Ses Ions en Solution Aqueuse AcideDocument5 pagesLe Mercure Et Ses Ions en Solution Aqueuse Acideneval chenchouniPas encore d'évaluation
- Etalonnage D'un Solution D'ions PermanganateDocument2 pagesEtalonnage D'un Solution D'ions Permanganateneval chenchouniPas encore d'évaluation
- Étude D'une Pile À Combustible Au Méthanol02Document3 pagesÉtude D'une Pile À Combustible Au Méthanol02neval chenchouni100% (1)
- P3 TD 2S CTD 2023-2024Document5 pagesP3 TD 2S CTD 2023-2024seckseckaPas encore d'évaluation
- 5SBUAA5Document34 pages5SBUAA5Michel PretPas encore d'évaluation
- TP Livret PDFDocument68 pagesTP Livret PDFAliMchirguiPas encore d'évaluation
- tp1 tp2Document4 pagestp1 tp2Adrar HectorPas encore d'évaluation
- DS N°3 - Banc D'épreuve Hydraulique (Corrigé) PDFDocument8 pagesDS N°3 - Banc D'épreuve Hydraulique (Corrigé) PDFElmehdi ElmessaoudiPas encore d'évaluation
- Capture D'écran . 2022-06-08 À 17.26.29Document21 pagesCapture D'écran . 2022-06-08 À 17.26.29FirstofalltimePas encore d'évaluation
- Chap1 GENERALITES PDFDocument10 pagesChap1 GENERALITES PDFAdams SamassiPas encore d'évaluation
- 2023 Metro SI J1 ExoA Sujet Badminton 10pts 30minDocument3 pages2023 Metro SI J1 ExoA Sujet Badminton 10pts 30minWN MPas encore d'évaluation
- CC1 2018 - 2019 - Sujet PDFDocument2 pagesCC1 2018 - 2019 - Sujet PDFgilgamesh king of the worldPas encore d'évaluation
- Devoir de Niveau N°3 de Sciences PhysiquesDocument3 pagesDevoir de Niveau N°3 de Sciences PhysiquesJaphet BAOUNDOULAPas encore d'évaluation
- Vigilance Et Conduite Automobile CorrigeDocument2 pagesVigilance Et Conduite Automobile CorrigedayaPas encore d'évaluation
- CH 6 CorrectionexercicesDocument4 pagesCH 6 Correctionexercicesmaelle sirventPas encore d'évaluation
- Limite de BetzDocument3 pagesLimite de BetzOmar ErrajiPas encore d'évaluation
- Os Chimie Corrige Ch1Document16 pagesOs Chimie Corrige Ch1laura sofia brunelle cyr100% (2)
- ChariotDocument8 pagesChariotNoureddine HermetienPas encore d'évaluation
- MP1 TD 2023 24-ImpressionDocument38 pagesMP1 TD 2023 24-Impressionbassel.taha19Pas encore d'évaluation
- Prépa Médecine STAC - Physique 2Document53 pagesPrépa Médecine STAC - Physique 2Joan Brunel TAKAMTE KAMGAPas encore d'évaluation
- AD BertozziDocument3 pagesAD BertozziKahil LaibPas encore d'évaluation
- Mecanique Du Point Chapitre5Document15 pagesMecanique Du Point Chapitre5amedeeagbenyegahPas encore d'évaluation
- En Meca Travail Exe SynthDocument3 pagesEn Meca Travail Exe Synthjonathanzdd91Pas encore d'évaluation
- TDMeca Flu 1Document3 pagesTDMeca Flu 1Majda El-aouniPas encore d'évaluation
- 12Document2 pages12Levier PoidsPas encore d'évaluation
- SV النهائي) الاختبار الاول 2023-2024)Document3 pagesSV النهائي) الاختبار الاول 2023-2024)jourymestrah3182019Pas encore d'évaluation
- Controle 2 S1 TC FR (WWW - Pc1.ma)Document1 pageControle 2 S1 TC FR (WWW - Pc1.ma)Azaroual MOhammadPas encore d'évaluation
- Mécanique 1re Année MPSI-PCSI-PTSIDocument0 pageMécanique 1re Année MPSI-PCSI-PTSIOussam Ouadidi75% (4)
- Pendule Horizontal Et Vertical PDFDocument8 pagesPendule Horizontal Et Vertical PDFMOSTAFAPas encore d'évaluation
- BrevetDocument6 pagesBrevetdadimarwane59Pas encore d'évaluation
- Chute Libre Verticale D Un Solide Exercices Non Corriges 2 1Document4 pagesChute Libre Verticale D Un Solide Exercices Non Corriges 2 1Ahid ImadPas encore d'évaluation
- 03 Etincelle Manuels 3ac PC Biof Guide FinaleDocument114 pages03 Etincelle Manuels 3ac PC Biof Guide FinaleMAACHI HAMIDPas encore d'évaluation
- CO1 TS1 2024 IapgDocument4 pagesCO1 TS1 2024 Iapgpapa samba sarrPas encore d'évaluation
- Améliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesD'EverandAméliorer votre mémoire: Un Guide pour l'augmentation de la puissance du cerveau, utilisant des techniques et méthodesÉvaluation : 5 sur 5 étoiles5/5 (2)
- Géobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainD'EverandGéobiologie de l'habitat et Géobiologie sacrée: Pour un lieu sainÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- Technologie automobile: Les Grands Articles d'UniversalisD'EverandTechnologie automobile: Les Grands Articles d'UniversalisPas encore d'évaluation
- Électrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsD'EverandÉlectrotechnique | Pas à Pas: Bases, composants & circuits expliqués pour les débutantsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Revue des incompris revue d'histoire des oubliettes: Le Réveil de l'Horloge de Célestin Louis Maxime Dubuisson aliéniste et poèteD'EverandRevue des incompris revue d'histoire des oubliettes: Le Réveil de l'Horloge de Célestin Louis Maxime Dubuisson aliéniste et poèteÉvaluation : 3 sur 5 étoiles3/5 (3)
- Guide De Démarrage De L'Apiculture: Le Guide Complet Pour Élever Des AbeillesD'EverandGuide De Démarrage De L'Apiculture: Le Guide Complet Pour Élever Des AbeillesPas encore d'évaluation
- 20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsD'Everand20 Véritables remèdes de nos grands-mères pour maigrir vite et enfin perdre du poidsÉvaluation : 5 sur 5 étoiles5/5 (1)
- Anatomie & 100 étirements essentiels pour le running: Principes de base, Techniques, Tableaux de séries, Précautions à prendre, Conseils, Programmes d'étirementsD'EverandAnatomie & 100 étirements essentiels pour le running: Principes de base, Techniques, Tableaux de séries, Précautions à prendre, Conseils, Programmes d'étirementsPas encore d'évaluation
- Anatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursD'EverandAnatomie & 100 étirements essentiels: Techniques, Bénéfices attendus, Précautions à prendre, Conseils, Tableaux de séries, DouleursPas encore d'évaluation
- L'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)D'EverandL'Art de la guerre: Traité de stratégie en 13 chapitres (texte intégral)Évaluation : 4 sur 5 étoiles4/5 (3032)
- Production et propagation des sons: Les Grands Articles d'UniversalisD'EverandProduction et propagation des sons: Les Grands Articles d'UniversalisPas encore d'évaluation
- Affirmations positives : Perte de poids pour les femmesD'EverandAffirmations positives : Perte de poids pour les femmesPas encore d'évaluation
- L'Art de La Magie au Bougie Wicca: Le Guide du Débutant à la Pratique de la Magie au Bougie de WiccaD'EverandL'Art de La Magie au Bougie Wicca: Le Guide du Débutant à la Pratique de la Magie au Bougie de WiccaÉvaluation : 3 sur 5 étoiles3/5 (1)
- Secrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieD'EverandSecrets ancestraux d'un maître guérisseur: Un sceptique occidental, un maître oriental et les plus grands secrets de la vieÉvaluation : 5 sur 5 étoiles5/5 (2)
- Le B.A.-Ba de la communication: Comment convaincre, informer, séduire ?D'EverandLe B.A.-Ba de la communication: Comment convaincre, informer, séduire ?Évaluation : 3 sur 5 étoiles3/5 (1)
- Mes inventions (Traduit): Autobiographie de Nikola TeslaD'EverandMes inventions (Traduit): Autobiographie de Nikola TeslaÉvaluation : 4.5 sur 5 étoiles4.5/5 (2)
- La vie des abeilles: Prix Nobel de littératureD'EverandLa vie des abeilles: Prix Nobel de littératureÉvaluation : 4 sur 5 étoiles4/5 (41)
- Harmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020D'EverandHarmonisation Energétique des Lieux: Habitat et haut-lieux sacrés 2020Évaluation : 2.5 sur 5 étoiles2.5/5 (3)
- Physique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresD'EverandPhysique quantique pour les débutants: Découvrez les fondements de la mécanique quantique et la façon dont elle affecte le monde dans lequel nous vivons à travers ses théories les plus célèbresÉvaluation : 5 sur 5 étoiles5/5 (2)