Académique Documents
Professionnel Documents
Culture Documents
2004 09 Polynesie Spe Sujet TA TAC
Transféré par
Ahmed TafouktTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
2004 09 Polynesie Spe Sujet TA TAC
Transféré par
Ahmed TafouktDroits d'auteur :
Formats disponibles
Polynsie 09/2004 Calculatrice autorise(4 points) TITRE ALCALIMTRIQUE D UNE EAU MINRALE
Les eaux minrales contiennent de nombreuses espces chimiques dissoutes. Ces eux minrales sont particulirement riches en ions bicarbonate . Ce nom dsigne en fait les ions hydrognocarbonate HCO3(aq). Donnes : - Zone de virage de quelques indicateurs colors : Phnolphtaline: Incolore Vert de bromocrsol: Jaune 3,8 Vert 5,4 Bleu 8 Rose ple 10 Fuschia pH pH
- Valeurs de quelques pKa de couples acido-basiques : Pour le couple (H3O+ / H2O) : pKa1 = 0 Pour le couple (H2O / HO) : pKa2 = 14 Pour le couple (CO2, H2O / HCO3) : pKa3 = 6,3 Pour le couple (HCO3 / CO32) : pKa4 = 10,3 - Masses molaires atomiques : M(H) = 1 g.mol-1 ; M(O) = 16 g.mol-1 ; M(C) = 12 g.mol-1 .
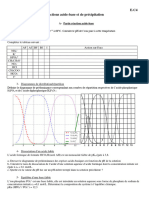
Pour effectuer le dosage alcalimtrique, on prlve V1 = 50,0 mL deau minrale que lon titre par une solution dacide chlorhydrique de concentration Ca= 2,010-2 mol.L-1. Un systme dacquisition permet de mesurer le pH au cours du dosage. On obtient ainsi la courbe donnant le pH en fonction de Va, volume dpH dacide vers, et celle de sa drive = f(Va). Ces courbes sont donnes en annexe ( rendre avec dVa la copie). 1. Le titre alcalimtrique TA La mesure du titre alcalimtrique TA permet de dterminer la concentration en ions carbonate CO32-(aq). On donne la dfinition du TA : c'est le volume, exprim en millilitres, de solution dacide chlorhydrique de concentration Ca = 2,010-2 mol.L-1 en ions H3O+(aq) ncessaires pour doser les ions carbonate CO32 - (aq) dans 100 mL deau minrale en prsence de phnolphtaline. 1.1 En vous servant du diagramme donn en annexe,donner le pH de leau minrale. 1.2 tablir le diagramme de prdominance des espces carbonates. En dduire la forme prdominante de ces espces dans cette eau minrale. 1.3 Quelle teinte prend la phnolphtaline dans cette eau ? 1.4 Par ajout dacide chlorhydrique, la phnolphtaline changera-t-elle de couleur ? Peut-on dterminer par lobservation un volume quivalent ? 1.5 Justifier la valeur nulle du TA de cette eau minrale.
2. Le titre alcalimtrique complet TAC Le titre alcalimtrique complet TAC est li la concentration totale en ions hydrognocarbonate HCO3-(aq) et carbonate CO32 - (aq). On donne la dfinition du TAC : cest le volume, exprim en millilitres, de solution dacide chlorhydrique de concentration Ca = 2,010-2 mol.L-1 ncessaires pour doser 100 mL deau minrale en prsence de vert de bromocrsol. 2.1. Ecrire lquation de la raction utilise pour le titrage. 2.2. Calculer na la quantit d'ions H3O+(aq) introduite lorsque Va = 14,0 mL. Evaluer n'a la quantit dions H3O+(aq) restant dans le volume total du mlange ractionnel. Justifier lutilisation de cette raction pour raliser un dosage. 2.3. Dterminer les coordonnes du point dquivalence. 2.4..Justifier le choix du vert de bromocrsol comme indicateur color.
2.5. Dterminer la concentration molaire C des ions hydrognocarbonate dans cette eau minrale.
2.6. Dterminer la concentration massique T des ions hydrognocarbonate dans cette eau minrale. 2.7. Dterminer le TAC de cette eau minrale.
ANNEXE
pH
Titrage des ions hydrognocarbonate contenus dans 50 mL d'eau minrale par l'acide chlorhydrique 0 -0,2 -0,4 -0,6 -0,8 -1 drive
8 7 6 5 4 3 2 1 0
- 1,2 0 5 10
volume d'acide ajout (Va) en mL
15
20
25
30
Vous aimerez peut-être aussi
- TP - 1 - Traitement EauxDocument4 pagesTP - 1 - Traitement Eauxnasa nasaPas encore d'évaluation
- AlcalinitéDocument2 pagesAlcalinitéAlkatel Al HanounePas encore d'évaluation
- E.C4 - Réaction Acide Base Et de PrécipitationDocument4 pagesE.C4 - Réaction Acide Base Et de Précipitationnoamassin78Pas encore d'évaluation
- TP Dosage Ions HydrogenocarbonateDocument3 pagesTP Dosage Ions Hydrogenocarbonatefszkd2mgg9Pas encore d'évaluation
- Exos21 Acides BasesDocument4 pagesExos21 Acides BasesSohaib LaminePas encore d'évaluation
- CHP 2 TD - Chimie - SolutionDocument8 pagesCHP 2 TD - Chimie - SolutionSimplice Assemien100% (2)
- TP AnalytiqueDocument7 pagesTP AnalytiqueRoubio Hiba100% (1)
- Ta TacDocument4 pagesTa TacSalah-Eddine Saidi100% (1)
- TP AlcaliniteDocument3 pagesTP Alcaliniteجعدبندرهم100% (2)
- TD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - MonobaseDocument5 pagesTD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - MonobaseLOUkmen Bel100% (1)
- TAC - Titre Alcalimétrique CompletDocument8 pagesTAC - Titre Alcalimétrique Completabderrahimn67% (3)
- Corrigé Série 2Document7 pagesCorrigé Série 2Doudou SamiPas encore d'évaluation
- Feuille de TD N°1-1 PageDocument8 pagesFeuille de TD N°1-1 Pagesalma BahoPas encore d'évaluation
- F Spect P 10 CorrigeDocument2 pagesF Spect P 10 CorrigeMohamed EL AminePas encore d'évaluation
- Examen Blanc N°2 Du Baccalauréat Année: 2020Document8 pagesExamen Blanc N°2 Du Baccalauréat Année: 2020Mehdi AgPas encore d'évaluation
- 2004 09 Polynesie Spe Correction TA TACDocument2 pages2004 09 Polynesie Spe Correction TA TACRekkab MohamedPas encore d'évaluation
- Ex 1Document6 pagesEx 1teghre chekhne El koryPas encore d'évaluation
- TD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - MonobaseDocument5 pagesTD: Réactions Acido-Basiques: Exercice N°1: Diagramme de Distribution Pour Un Couple Monoacide - Monobaseel hazbi fadilaPas encore d'évaluation
- Série D'éxercices Des Transformations Associées Aux Réactions Acido-Basiques2024Document3 pagesSérie D'éxercices Des Transformations Associées Aux Réactions Acido-Basiques2024sassin2006Pas encore d'évaluation
- MPSI2 TD1 R Acido BasiqueDocument4 pagesMPSI2 TD1 R Acido Basiquehidamohamed326Pas encore d'évaluation
- Epreuve Chimie 1 Preparation Au CNC 2021Document7 pagesEpreuve Chimie 1 Preparation Au CNC 2021Meriem El AbzazePas encore d'évaluation
- 15 Corrigé Série 2Document7 pages15 Corrigé Série 2Snaptube 2022Pas encore d'évaluation
- TD CG - 01 Acides BasesDocument5 pagesTD CG - 01 Acides BasesMed BriniPas encore d'évaluation
- TP - Titre AlcalimtrieauDocument2 pagesTP - Titre Alcalimtrieausbe3centrlePas encore d'évaluation
- DM Nâ°1Document8 pagesDM Nâ°1grégoire beraudPas encore d'évaluation
- AlcalinitéDocument4 pagesAlcalinitéHoc InePas encore d'évaluation
- Solutions Aqueuses IpDocument13 pagesSolutions Aqueuses IpEmmanuel PolvenskyPas encore d'évaluation
- TPV L'Alcalimétrique Des EauxDocument3 pagesTPV L'Alcalimétrique Des Eauxridatbk025Pas encore d'évaluation
- TD Exercices-Corrigés PDFDocument21 pagesTD Exercices-Corrigés PDFabdelouahed.rhaouiPas encore d'évaluation
- Chaima Rabab 2Document6 pagesChaima Rabab 2gaoudachaima123Pas encore d'évaluation
- Transformations Chimiques S Effectuant Dans Les 2 Sens Exercices Non Corriges 1 1Document4 pagesTransformations Chimiques S Effectuant Dans Les 2 Sens Exercices Non Corriges 1 1boufdili0% (2)
- Acides Bases PDFDocument8 pagesAcides Bases PDFHafidi AhmedPas encore d'évaluation
- C.P 22-23 Solution AqueusesDocument2 pagesC.P 22-23 Solution AqueusesdiarratogsibPas encore d'évaluation
- TA-TAC Pour Les ÉtudiantsDocument3 pagesTA-TAC Pour Les ÉtudiantsAmine KPas encore d'évaluation
- LACH1 Serie 2 2013Document2 pagesLACH1 Serie 2 2013Hassine WajihPas encore d'évaluation
- Traveaux Dirigés 2Document6 pagesTraveaux Dirigés 2Aymen BaccouchePas encore d'évaluation
- Solutionaqueusechap 2TDDocument2 pagesSolutionaqueusechap 2TDHamzaPas encore d'évaluation
- Nothing To DoDocument9 pagesNothing To DomugiPas encore d'évaluation
- Acides Faibles Et Bases Faibles Couples Acide-Base & Constante D'AciditeDocument5 pagesAcides Faibles Et Bases Faibles Couples Acide-Base & Constante D'AciditeNjuga Sene100% (1)
- Le TP Se Déroule en 4 Étapes. Documents FournisDocument9 pagesLe TP Se Déroule en 4 Étapes. Documents FournisAnacleto AlfredoPas encore d'évaluation
- Couple Acide - Base: ExercicesDocument16 pagesCouple Acide - Base: ExercicesAhamadi ElhouyounPas encore d'évaluation
- Cours de VirologieDocument5 pagesCours de VirologieFrancisca AgboviPas encore d'évaluation
- TD Acide Faible Base Faible Constante Dacidite TS2 2023 2024Document12 pagesTD Acide Faible Base Faible Constante Dacidite TS2 2023 2024fallccheikhPas encore d'évaluation
- Corrigé Série 1Document5 pagesCorrigé Série 1Mohamed ECHAMAI100% (2)
- Série TD 3 Chimie 2Document2 pagesSérie TD 3 Chimie 2salma koudriPas encore d'évaluation
- 2006 09 National Exo1 Sujet pHPoisson 6 5ptsDocument5 pages2006 09 National Exo1 Sujet pHPoisson 6 5ptsla physique selon le programme FrançaisPas encore d'évaluation
- TD 5Document2 pagesTD 5Serena SouaibyPas encore d'évaluation
- Chapitre IV-Equilibre Calcocarbonique-CDocument8 pagesChapitre IV-Equilibre Calcocarbonique-CSafa HAISSOUNAPas encore d'évaluation
- TD Risa Uman 2017 Final 2Document9 pagesTD Risa Uman 2017 Final 2Sa Majesté David50% (2)
- Corrigé Série 2Document8 pagesCorrigé Série 2Chk YahyaPas encore d'évaluation
- 2010 AmNord Exo1 Sujet Eau 6 5ptsDocument3 pages2010 AmNord Exo1 Sujet Eau 6 5ptsHarakat ElhoucinePas encore d'évaluation
- TD Eq - CHMQ L1-S2 (CPGE)Document5 pagesTD Eq - CHMQ L1-S2 (CPGE)Btn Princii IsraëlPas encore d'évaluation
- 2010 AmNord Exo1 Sujet Eau 6 5ptsDocument3 pages2010 AmNord Exo1 Sujet Eau 6 5ptsla physique selon le programme FrançaisPas encore d'évaluation
- 201701271158125 (3)Document9 pages201701271158125 (3)Ali RammalPas encore d'évaluation
- Chimie Eau - (19-20)Document24 pagesChimie Eau - (19-20)zohirPas encore d'évaluation
- TP 3: Détermination Du TA, TAC Et TH D'une Eau.Document11 pagesTP 3: Détermination Du TA, TAC Et TH D'une Eau.Romayssa Zitouni100% (2)
- Équilibres en solution: Les Grands Articles d'UniversalisD'EverandÉquilibres en solution: Les Grands Articles d'UniversalisPas encore d'évaluation
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- Glucides: Les Grands Articles d'UniversalisD'EverandGlucides: Les Grands Articles d'UniversalisPas encore d'évaluation
- Série 4 PHDocument2 pagesSérie 4 PHYahya LahmarPas encore d'évaluation
- Hydrochimie Qualité de EauxDocument29 pagesHydrochimie Qualité de EauxabderrahimnPas encore d'évaluation
- Chapitre IIDocument28 pagesChapitre IIchaima sagiPas encore d'évaluation
- DM - 8 Magnetisme +chimie Solu +thermo Chimie PDFDocument4 pagesDM - 8 Magnetisme +chimie Solu +thermo Chimie PDFBrandy OdonnellPas encore d'évaluation
- Epreuve de Physique ChimieDocument5 pagesEpreuve de Physique ChimieBile DjetouanPas encore d'évaluation
- Metrologie-Ph LNEDocument9 pagesMetrologie-Ph LNEmetrologue laboratoirePas encore d'évaluation
- Troubles de L'équilibre Acido-Basique PDFDocument24 pagesTroubles de L'équilibre Acido-Basique PDFsarah hPas encore d'évaluation
- TD2 CSDocument2 pagesTD2 CSSimo Maro100% (1)
- Oefa. Sem - 8Document17 pagesOefa. Sem - 8martingarciamPas encore d'évaluation
- Correction TD Réactivité Chimiqie BCG S2 2020Document29 pagesCorrection TD Réactivité Chimiqie BCG S2 2020Aya ElksabiPas encore d'évaluation
- 3-1 Produits DangereuxDocument19 pages3-1 Produits DangereuxMohamed EttahiriPas encore d'évaluation
- Devoir 2 Modele 8 Physique Chimie 3ac Semestre 1Document2 pagesDevoir 2 Modele 8 Physique Chimie 3ac Semestre 1bouthaina taziPas encore d'évaluation
- Equilibres de ComplexationDocument10 pagesEquilibres de ComplexationLawrence Mundene-timotheePas encore d'évaluation
- 2023 Asie J1 Exo3 Sujet Salicylate BeerLambert K 4 5ptsDocument4 pages2023 Asie J1 Exo3 Sujet Salicylate BeerLambert K 4 5ptsstephankorgo42Pas encore d'évaluation
- Cours Chimie GénéraleDocument62 pagesCours Chimie GénéraleFouad BenallalPas encore d'évaluation
- BENOTHMANE - AICHA NIHED - Chimie. - Chimie PhysiqueDocument101 pagesBENOTHMANE - AICHA NIHED - Chimie. - Chimie PhysiqueFatima-ezzahra BoubagraPas encore d'évaluation
- Mécanique TerrestreDocument6 pagesMécanique TerrestreMouad DohmiPas encore d'évaluation
- Burkina Bac 2020 Sciences Physiques Serie C Normale 2etourDocument4 pagesBurkina Bac 2020 Sciences Physiques Serie C Normale 2etourMohamed Aly SawadogoPas encore d'évaluation
- Les Acides Et Les Bases - 3 ACDocument3 pagesLes Acides Et Les Bases - 3 ACaznag hicham0% (1)
- Chapitre Solubilité 2018Document22 pagesChapitre Solubilité 2018Younes AsfalouPas encore d'évaluation
- 15 Corrigé Série 2Document7 pages15 Corrigé Série 2Snaptube 2022Pas encore d'évaluation
- Extraction Isolement LiquideDocument6 pagesExtraction Isolement Liquideelhidhab2014Pas encore d'évaluation
- Exercices 5 Etat D'équilibre D'un Système Chimique (PR Hammou Mouna)Document1 pageExercices 5 Etat D'équilibre D'un Système Chimique (PR Hammou Mouna)Ahmed AhmedPas encore d'évaluation
- HDR 2005 PDFDocument110 pagesHDR 2005 PDFJean-Jacques RahobisoaPas encore d'évaluation
- Maroc Prog2013 Chimie PcsiDocument14 pagesMaroc Prog2013 Chimie PcsiBrandy OdonnellPas encore d'évaluation
- GlycineDocument7 pagesGlycineMatthieu EmondPas encore d'évaluation
- Exo PHDocument2 pagesExo PHNaimboulah BjrPas encore d'évaluation
- Transformation Liée À Des Réactions Acides Et Bases (WWW - Pc1.ma)Document21 pagesTransformation Liée À Des Réactions Acides Et Bases (WWW - Pc1.ma)Abderrazzak ElhaimerPas encore d'évaluation
- BDocument3 pagesBdotse kodzo hetsuPas encore d'évaluation
- Characterizing The Impact of Pyrite Addition On THDocument14 pagesCharacterizing The Impact of Pyrite Addition On THAlexPas encore d'évaluation