Académique Documents
Professionnel Documents
Culture Documents
ANSM 20201223 - Surv - Vaccins - Covid - 2020 - VF
Transféré par
liviteTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
ANSM 20201223 - Surv - Vaccins - Covid - 2020 - VF
Transféré par
liviteDroits d'auteur :
Formats disponibles
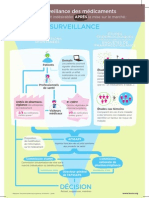
LA SURVEILLANCE DES VACCINS COVID-19
L’ANSM a mis en place un double dispositif renforcé afin d'assurer le suivi
et la gestion des effets indésirables liés aux vaccins contre la Covid-19.
PHARMACOVIGILANCE PHARMACO-ÉPIDÉMIOLOGIE
Les professionnels de santé doivent déclarer tout effet Analyse des données du système national
indésirable suspecté d'être en lien avec la vaccination, des données de santé (SNDS) par EPI-PHARE
en particulier les effets graves et/ou inattendus.
Les personnes vaccinées et leur entourage peuvent déclarer
elles-mêmes les effets indésirables.
Objectif : quantification des risques de survenue
d'évènements indésirables graves à l'échelle de la
population ciblée par la vaccination
Échanges et partage
Déclarations sur d'informations,
signalement-sante.gouv.fr y compris avec l'Europe Vaccination
ou directement auprès d'un centre (date, dose, lieu…)
régional de pharmacovigilance (CRPV) Patients vaccinés
(âge, sexe,
pathologies…)
Analyse médicale des déclarations
par les experts des CRPV :
• évaluation de la gravité et du lien
éventuel avec la vaccination
• détection des signaux de sécurité
Assurance Maladie
(consommation de
soins, base DCIR2)
Consolidation des données de
pharmacovigilance pour chaque vaccin Évènements
indésirables
au travers d'un rapport
(hospitalisations,
Hospitalisations décès…)
(base PMSI3)
Comité de suivi hebdomadaire ANSM/CRPV :
analyse collégiale des signaux de sécurité
Si le signal de sécurité est confirmé par l'un ou l'autre
de ces dispositifs, l’ANSM met en place des mesures adaptées
(contre-indication pour certaines populations, information, retrait de l’autorisation…)
1. GIS : Groupement d’intérêt scientifique
2.²DCIR : Datamart de consommation interrégime
Suivez-nous sur @ansm ansm.sante.fr
3. PMSI : Programme de médicalisation des systèmes d'information
Vous aimerez peut-être aussi
- Dossiers vaccination et politiques vaccinales: Les dossiers MorphéusD'EverandDossiers vaccination et politiques vaccinales: Les dossiers MorphéusPas encore d'évaluation
- Leem Médicaments APRESDocument1 pageLeem Médicaments APRESJean-Philippe RivièrePas encore d'évaluation
- La Surveillance Du Médicament Après AMMDocument1 pageLa Surveillance Du Médicament Après AMMLeemPas encore d'évaluation
- La PharmacovigilanceDocument34 pagesLa Pharmacovigilanceyoucef benaissaPas encore d'évaluation
- Covid 19 Aefi ReportDocument35 pagesCovid 19 Aefi Reportchristox01Pas encore d'évaluation
- Covid 19 Vaccins - Rapport Hebdomadaire 4 - ModernaDocument18 pagesCovid 19 Vaccins - Rapport Hebdomadaire 4 - ModernaMatilde AlmeidaPas encore d'évaluation
- Covid, Vaccins Et Science Aux Origines D'une Défiance, Par Ariane Denoyel (Le Monde Diplomatique, Avril 2023)Document9 pagesCovid, Vaccins Et Science Aux Origines D'une Défiance, Par Ariane Denoyel (Le Monde Diplomatique, Avril 2023)rebuberPas encore d'évaluation
- Effets Indesirables Lies Aux Vaccins Autorises Contre La Covid 19Document3 pagesEffets Indesirables Lies Aux Vaccins Autorises Contre La Covid 19Journal L'Indépendant100% (1)
- Pharmacovigilance: DR A.Bousbia SalahDocument4 pagesPharmacovigilance: DR A.Bousbia SalahSabrina KoufiPas encore d'évaluation
- Carnet de Vaccination ElectroniqueDocument9 pagesCarnet de Vaccination ElectroniqueValentin BerchPas encore d'évaluation
- 2 - AFAR - Antibiotherapie Probabiliste Des Etats Septiques GravesDocument7 pages2 - AFAR - Antibiotherapie Probabiliste Des Etats Septiques GravesRamanantoaninaPas encore d'évaluation
- IAS: Infections Associées Aux SoinsDocument3 pagesIAS: Infections Associées Aux SoinsElsa BorvalPas encore d'évaluation
- Ad 1062225Document4 pagesAd 1062225emmanuelPas encore d'évaluation
- 2-Surveillance Epidemiologique PharmacieDocument31 pages2-Surveillance Epidemiologique PharmacieharounxgamerPas encore d'évaluation
- Surveillance Épidémiologique: Méthodes de Surveillance: Déclarations Obligatoires (DO)Document3 pagesSurveillance Épidémiologique: Méthodes de Surveillance: Déclarations Obligatoires (DO)Kawtar KaoutarPas encore d'évaluation
- Vaccin Covid19Document16 pagesVaccin Covid19Bendris OsmanPas encore d'évaluation
- 4 Rapport Grossesse Vaccins Covid Final VfaDocument29 pages4 Rapport Grossesse Vaccins Covid Final VfaSapPas encore d'évaluation
- 10 1177@0885066619828290Document5 pages10 1177@0885066619828290Asma Bahri0% (1)
- L'avenir de La Surveillance Du Contrôle Des Infections ?Document6 pagesL'avenir de La Surveillance Du Contrôle Des Infections ?nouhaPas encore d'évaluation
- Ad 070205Document4 pagesAd 070205Ny Fahendrena IhanyPas encore d'évaluation
- 2020 Article 4791Document8 pages2020 Article 4791Grâce KabengelePas encore d'évaluation
- Bacillus Calmette-Guerin Infection Following Intravesical InstillationDocument6 pagesBacillus Calmette-Guerin Infection Following Intravesical InstillationAdina PetrescuPas encore d'évaluation
- Mission Inspection Contrôle Audit ARS BFC - 2019 - 0Document40 pagesMission Inspection Contrôle Audit ARS BFC - 2019 - 0BENATMANE OTHMANEPas encore d'évaluation
- Soins Infirmiers Et Gestion Des RisquesDocument9 pagesSoins Infirmiers Et Gestion Des RisquesBenchadad OppoPas encore d'évaluation
- OFSP Recommandations VaxDocument7 pagesOFSP Recommandations VaxmikelsonPas encore d'évaluation
- La Surveillance Epidemiologique Cle4e19c4Document5 pagesLa Surveillance Epidemiologique Cle4e19c4Anwar SalamaPas encore d'évaluation
- Infections NosocomialesDocument19 pagesInfections NosocomialesHehe JianPas encore d'évaluation
- Accident D'exposition Au Sang Ou Aux Liquides BiologiquesDocument9 pagesAccident D'exposition Au Sang Ou Aux Liquides Biologiqueslucie tatyPas encore d'évaluation
- InfoSante Procedure Pour MCIDocument2 pagesInfoSante Procedure Pour MCIIsmaelKolbePas encore d'évaluation
- VaccinationDocument6 pagesVaccinationhind el hamriPas encore d'évaluation
- 7 Module 7 MPVIDocument11 pages7 Module 7 MPVIسيف الاسلام عبد الرحمانPas encore d'évaluation
- 2024 Article 1367Document11 pages2024 Article 1367Grâce KabengelePas encore d'évaluation
- Pharmacovigilance 36Document12 pagesPharmacovigilance 36SHANACOYPas encore d'évaluation
- Séquence 5 Veille SanitaireDocument23 pagesSéquence 5 Veille SanitaireMareva NyanitPas encore d'évaluation
- Synthese MG Vascularites Necrosantes Systemiques Periarterite Noueuse Et Vascularites Associees Aux AncaDocument6 pagesSynthese MG Vascularites Necrosantes Systemiques Periarterite Noueuse Et Vascularites Associees Aux AncaAhmed Filali AdibPas encore d'évaluation
- 142 Surveillance Des Maladies Infectieuses Transmissibles - 0Document2 pages142 Surveillance Des Maladies Infectieuses Transmissibles - 0Amine KssiliPas encore d'évaluation
- Bip No4 - 2021 CompressedDocument27 pagesBip No4 - 2021 CompressedEliott ThiryPas encore d'évaluation
- Surveillance Épidémiologique Diagnostic Sanitaire Collectif, Approche Par ProgrammeDocument6 pagesSurveillance Épidémiologique Diagnostic Sanitaire Collectif, Approche Par ProgrammeprypadwryPas encore d'évaluation
- PRETEST Covid Vaccination Course FRDocument2 pagesPRETEST Covid Vaccination Course FRCrios MPas encore d'évaluation
- Journal Américain de Contrôle Des InfectionsDocument4 pagesJournal Américain de Contrôle Des InfectionsGrâce KabengelePas encore d'évaluation
- Pe Ira Na 20240124Document6 pagesPe Ira Na 20240124azegtPas encore d'évaluation
- WHO FAQ AstraZeneca 26 March 2021 FINAL FRDocument3 pagesWHO FAQ AstraZeneca 26 March 2021 FINAL FRjhohanna talaPas encore d'évaluation
- Manuel de Surveillance de La Couverture Vaccinale Contre Le Papillomavirus Humain (PVH)Document48 pagesManuel de Surveillance de La Couverture Vaccinale Contre Le Papillomavirus Humain (PVH)83iryatPas encore d'évaluation
- Item 177 - Securite Sanitaire-Veille SanitaireDocument2 pagesItem 177 - Securite Sanitaire-Veille Sanitairemohammed blilPas encore d'évaluation
- Tous Les Vaccines Covid Peuvent Officiellement Porter PlainteDocument25 pagesTous Les Vaccines Covid Peuvent Officiellement Porter Plaintemoyonnathalie33Pas encore d'évaluation
- Fiche Vaccin HPV RisquesDocument1 pageFiche Vaccin HPV RisquesFREDERICK HENOPas encore d'évaluation
- 07 2023 Fiche Repere Tuberculose Respiratoire CPIAS ARADocument5 pages07 2023 Fiche Repere Tuberculose Respiratoire CPIAS ARAxavier.paulmierPas encore d'évaluation
- Synthese Technopolitique Crise SanitaireDocument4 pagesSynthese Technopolitique Crise SanitairemronaiPas encore d'évaluation
- S0bac21 Tle Spe St2s Stss Sujet 3 1328841Document8 pagesS0bac21 Tle Spe St2s Stss Sujet 3 1328841Floriane TecherPas encore d'évaluation
- 1 s2.0 S0399077X05000673 MainDocument5 pages1 s2.0 S0399077X05000673 MainGrâce KabengelePas encore d'évaluation
- Item 181Document13 pagesItem 181goku ssjPas encore d'évaluation
- VIDAL - Urétrite Masculine - Prise en ChargeDocument1 pageVIDAL - Urétrite Masculine - Prise en Chargeabdoul aziz dialloPas encore d'évaluation
- 6-Elaboration Cartographie Risques Soins PerfusionDocument36 pages6-Elaboration Cartographie Risques Soins Perfusionhajri khouloudPas encore d'évaluation
- Identification and Assessment of Weak Toxicovigilance Signals - 10.1684@ers.2013.0635Document8 pagesIdentification and Assessment of Weak Toxicovigilance Signals - 10.1684@ers.2013.0635Edwin Juan Mercado LenguaPas encore d'évaluation
- 1 2 s2 Cours N 2Document5 pages1 2 s2 Cours N 2mohamed nedjadiPas encore d'évaluation
- Livret de Presentation Sur Le Suivi de Lepidemie de Covid-19Document7 pagesLivret de Presentation Sur Le Suivi de Lepidemie de Covid-19Adagra Angodji jules martialPas encore d'évaluation
- 2022-07-21 Argumentaire Scientifique Reintegration Soignants (versionJJ SLS) Sans Signature-1Document21 pages2022-07-21 Argumentaire Scientifique Reintegration Soignants (versionJJ SLS) Sans Signature-1mercierprap2sPas encore d'évaluation
- Epidémiologie/ Prévention Des Infections NosocomialesDocument19 pagesEpidémiologie/ Prévention Des Infections NosocomialesRachida FAOUZIPas encore d'évaluation
- Confraternel 2Document11 pagesConfraternel 2GeraldPas encore d'évaluation
- Hygiene Hospitaliere: DR T. ChalloufDocument42 pagesHygiene Hospitaliere: DR T. ChalloufYassine MokaddemPas encore d'évaluation
- Le Secret Du BonheurDocument76 pagesLe Secret Du BonheurRabo Magagi Aboubacar100% (1)
- MCEDocument23 pagesMCEIssamPas encore d'évaluation
- Histoire de L'ecritureDocument4 pagesHistoire de L'ecrituremiloud rouabhiPas encore d'évaluation
- Lettre Moti CapésDocument1 pageLettre Moti CapésIbrahim MOHAMED-IBRAHIMPas encore d'évaluation
- Les PoumonsDocument64 pagesLes PoumonsMB SKOFIELDPas encore d'évaluation
- Bonjour NoelDocument2 pagesBonjour NoelCristina DurauPas encore d'évaluation
- GSM 1Document45 pagesGSM 1Taki EddinePas encore d'évaluation
- APPRENDRE LANGLAIS en PARLANT + LIVRE AUDIO Cours Danglais Pour Débutant - Intermédiaire. Apprendre Et Pratiquer Langlais,... (Natural Learning (Learning, Natural) )Document44 pagesAPPRENDRE LANGLAIS en PARLANT + LIVRE AUDIO Cours Danglais Pour Débutant - Intermédiaire. Apprendre Et Pratiquer Langlais,... (Natural Learning (Learning, Natural) )Grace BakoulouPas encore d'évaluation
- PDJ-074 Planos Hidraulicos JMC-1071 - 121059Document10 pagesPDJ-074 Planos Hidraulicos JMC-1071 - 121059daniel zevallosPas encore d'évaluation
- Maurice Herbette - Une Ambassade Persane Sous Louis XIV (1907)Document417 pagesMaurice Herbette - Une Ambassade Persane Sous Louis XIV (1907)Elvin MemmedliPas encore d'évaluation
- Mini Mémoire 2024Document45 pagesMini Mémoire 2024halimabn19Pas encore d'évaluation
- Séquence: Les Cercles Et Les Disques: Petite Section - Période 4Document2 pagesSéquence: Les Cercles Et Les Disques: Petite Section - Période 4api-396470330100% (1)
- CHAPITRE VI Comment Se Forme Et S'exprime L'opinion Publique (Version Élève)Document24 pagesCHAPITRE VI Comment Se Forme Et S'exprime L'opinion Publique (Version Élève)Joël Nké MbargaPas encore d'évaluation
- COURS Histoire Médiévale 20-21Document18 pagesCOURS Histoire Médiévale 20-21mouhamedcamara629Pas encore d'évaluation
- 08 Topologie PlancheDocument3 pages08 Topologie PlancheEmmanuel KaboréPas encore d'évaluation
- Matrice BourdieuDocument2 pagesMatrice BourdieuwayPas encore d'évaluation
- X - FRENCH - QP - Mock ExaminationDocument5 pagesX - FRENCH - QP - Mock ExaminationKrishna AggarwalPas encore d'évaluation
- Automatique Niveau1Document77 pagesAutomatique Niveau1ssssPas encore d'évaluation
- Fascicule ASL 2013-2014Document174 pagesFascicule ASL 2013-2014Arnaud RichardPas encore d'évaluation
- Starbucks Berthierville - Recherche GoogleDocument1 pageStarbucks Berthierville - Recherche GooglebiankaPas encore d'évaluation
- Datasecurity and Auditing ExerciceDocument6 pagesDatasecurity and Auditing ExerciceOumaima ZiatPas encore d'évaluation
- Participative BankingDocument6 pagesParticipative Bankingkarim meddebPas encore d'évaluation
- Éléments (Euclide) - WikipédiaDocument6 pagesÉléments (Euclide) - WikipédiaYves StutzPas encore d'évaluation
- GRHP001Document1 pageGRHP001sidouPas encore d'évaluation
- Progression 6eDocument2 pagesProgression 6eLauraChanteloup100% (1)
- ANZIEU Moi PeauDocument337 pagesANZIEU Moi Peauisabelle93100Pas encore d'évaluation
- Correction TD3Document30 pagesCorrection TD3selsabilhaddab2004Pas encore d'évaluation