Académique Documents
Professionnel Documents
Culture Documents
Thermo Indus Hirn Resurchauffe
Transféré par
tiessesh.koulessiCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
Thermo Indus Hirn Resurchauffe
Transféré par
tiessesh.koulessiDroits d'auteur :
Formats disponibles
Un exercice de physique appliquée aux enjeux climatiques et énergétiques
Thermodynamique industrielle
Cycle de Hirn d’une centrale thermique
chaudière 1 alternateur
surchauffeur
2 3
6
5 4
pompe condenseur
Figure 1 – Turbine à vapeur étagée.
On s’intéresse à l’installation représentée figure 1, qui modélise une centrale thermique à flamme (gaz ou charbon).
Le fluide thermodynamique est de l’eau, qui suit un cycle de Hirn avec resurchauffe.
L’eau liquide est chauffée par une chaudière thermique, qui débite de la vapeur d’eau à 550 °C et 100 bar (état
1). Cette vapeur subit une détente adiabatique réversible dans une première turbine dite haute pression, d’où elle
sort à la pression de 10 bar (état 2). Un surchauffeur isobare, lui aussi relié à la chaudière, ramène la vapeur à la
température initiale (état 3). La vapeur passe ensuite dans la seconde turbine, dite basse pression, d’où sort de l’eau
à la température de 40 °C (état 4). Cette eau est envoyée dans un condenseur d’où elle sort à l’état de liquide juste
saturant (état 5), puis elle est pompée de manière adiabatique réversible (état 6) et renvoyée en entrée du générateur
de vapeur où elle subit un échauffement isobare. Les arbres des deux turbines sont liés entre eux.
1 - Tracer le cycle parcouru par l’eau dans le diagramme entropique de la figure 2. Pourquoi le point 6 est-il confondu
avec le point 5 ? Commenter son sens de parcours.
2 - En déduire la température de l’eau dans l’état 2 et l’état de l’eau dans l’état 4.
3 - Déterminer les enthalpies massiques de l’eau aux six points du cycle. Comment interpréter physiquement l’éga-
lité h5 = h6 ?
4 - Déterminer le travail massique disponible sur l’arbre des turbines.
5 - Si on considère que l’alternateur a un rendement électromécanique de 90 %, déterminer le débit d’eau à imposer
pour obtenir une puissance électrique de 400 MW.
6 - Quelle est la quantité de chaleur massique dépensée au surchauffeur ?
7 - Calculer le rendement thermodynamique de l’installation.
1/4 Étienne Thibierge, 15 novembre 2022, www.etienne-thibierge.fr
Un exercice de physique appliquée aux enjeux climatiques et énergétiques Thermodynamique industrielle
Figure 2 – Diagramme entropique de l’eau.
Éléments de correction
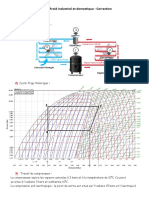
1 Le diagramme entropique est représenté figure 3.
▷ La transformation 1 → 2 est une adiabatique réversible, donc isentropique, donc une verticale dans le diagramme
entropique ;
▷ La transformation 2 → 3 suit l’isobare P = 10 bar ;
▷ L’énoncé ne précise rien sur l’étape 3 → 4, mais on peut considérer que la seconde turbine vérifie les mêmes
hypothèses que la première : il s’agit donc d’une détente adiabatique réversible ;
▷ La transformation 4 → 5 est par hypothèse isobare, donc isotherme car elle concerne un fluide diphasé ;
▷ La compression 5 → 6 est une adiabatique réversible jusqu’à atteindre 100 bar, mais dans le diagramme entropique
les isobares du domaine liquide sont toutes regroupées sur la courbe d’ébullition, si bien que le passage par la
pompe n’est pas visible sur le diagramme ;
▷ La transformation 6 → 1 suit l’isobare P = 100 bar en subissant successivement un échauffement de l’eau liquide
le long de la courbe d’ébullition (en diagramme entropique, toutes les isobares du liquide pur collent à la courbe
de saturation), puis un changement d’état, et enfin un échauffement de la vapeur sèche.
Le cycle est parcouru en sens horaire, ce qui est normal car on étudie une installation motrice.
2 On lit graphiquement T2 = 210 °C. Dans l’état 4 l’eau est diphasée, et le titre en vapeur vaut x4 = 0,93.
3 Le diagramme manque d’isenthalpes pour permettre une lecture précise ... On peut approximativement considérer
h1 = 3500 kJ · kg−1 h2 = 2850 kJ · kg−1 h3 = 3580 kJ · kg−1
h4 = 2400 kJ · kg−1 h5 = h6 = 100 kJ · kg−1 .
D’après le premier principe, avoir h5 = h6 signifie que le travail fourni par la pompe au liquide est négligeable devant
les autres échanges énergétiques, ce qui s’interprète par le fait que comprimer un liquide incompressible est une
opération relativement facile et donc peu coûteuse en énergie.
2/4 Étienne Thibierge, 15 novembre 2022, www.etienne-thibierge.fr
Un exercice de physique appliquée aux enjeux climatiques et énergétiques Thermodynamique industrielle
1 3
• •
•
2
4
5, 6 • •
Figure 3 – Diagramme entropique complété.
4 Le travail total disponible sur les turbines est l’opposé du travail indiqué reçu par le fluide. D’après le premier
principe, appliqué à la turbine haute pression,
∆h + ∆ec + ∆epp = w12 + q12
| {z } |{z}
≪∆h =0 adiab
soit
w12 = h2 − h1 .
De même pour la turbine basse pression,
w34 = h4 − h3
et finalement
wtot = −w12 − w34 donc wtot = (h1 − h2 ) + (h3 − h4 ) = 1830 kJ · kg−1 .
5 La puissance mécanique disponible sur la turbine s’écrit Pméca = Dm wtot , et comme Pélec = 0,9 Pméca on en
déduit
Pélec
Dm = = 240 kg · s−1 .
0,9 w
6 Par application du premier principe au surchauffeur, qui ne contient aucune pièce mobile (c’est un échangeur),
∆h = w23 +q23 d’où q23 = h3 − h2 = 730 kJ · kg−1 .
|{z}
=0
7 D’après le premier principe appliqué au générateur de vapeur, qui ne contient aucune pièce mobile (c’est également
un échangeur),
∆h = w61 +q61 d’où q61 = h1 − h6 = 3400 kJ · kg−1 .
|{z}
=0
3/4 Étienne Thibierge, 15 novembre 2022, www.etienne-thibierge.fr
Un exercice de physique appliquée aux enjeux climatiques et énergétiques Thermodynamique industrielle
En supposant que le transfert thermique dans le condenseur se fait avec le milieu extérieur et est donc gratuit, on en
déduit le rendement de l’installation sous la forme
wtot
η= = 0,44 .
q23 + q61
Attention à ne pas oublier dans le rendement le transfert thermique fourni par le surchauffeur ! En
pratique, ou bien le fluide repasse dans les fumées d’échappement de la chaudière, ou bien de la vapeur
est déviée avant ou pendant son passage dans la turbine haute pression (on parle de soutirage de
vapeur) et elle joue le rôle de fluide chaud dans le surchauffeur, le fluide froid étant la vapeur détendue
dans la turbine. On parle alors de soutirage.
4/4 Étienne Thibierge, 15 novembre 2022, www.etienne-thibierge.fr
Vous aimerez peut-être aussi
- Exercice Corrigé Cycle Frigorifique R134aDocument9 pagesExercice Corrigé Cycle Frigorifique R134aboussaid nejla83% (12)
- Cours - Turbine À Vapeur-TDocument12 pagesCours - Turbine À Vapeur-TSoumya Bouzidi67% (3)
- Cycle CombinéDocument45 pagesCycle CombinéOmar Erraji100% (1)
- TD 5 - CorrectionDocument5 pagesTD 5 - Correctioni s100% (5)
- Cours CO2Document22 pagesCours CO2Ezzedine AyariPas encore d'évaluation
- TD 4 Machines Thermiques PDFDocument5 pagesTD 4 Machines Thermiques PDFYudhfdjPas encore d'évaluation
- Machines Thermiques Exercices CorrigesDocument19 pagesMachines Thermiques Exercices CorrigesMouna Bz100% (1)
- Corrigé Série TD°2Document4 pagesCorrigé Série TD°2Ami NePas encore d'évaluation
- CH1 TavDocument91 pagesCH1 TavSaley Nouroudine100% (1)
- Turbines À GazDocument42 pagesTurbines À Gazismail ghourabiPas encore d'évaluation
- Exercice Pompe À ChaleurDocument6 pagesExercice Pompe À ChaleurĶhadija KhadijaPas encore d'évaluation
- TPE Thermo IndusDocument23 pagesTPE Thermo IndusYessine BouhamedPas encore d'évaluation
- Chapitre3cycle de RankineDocument19 pagesChapitre3cycle de RankineLuka ModrićPas encore d'évaluation
- Cours 1Document15 pagesCours 1Imen AkroutiPas encore d'évaluation
- SérieN4 20-21Document2 pagesSérieN4 20-21MounirPas encore d'évaluation
- Travaux Pratiques: Les Machines ThermiquesDocument26 pagesTravaux Pratiques: Les Machines ThermiquesThe MaverickPas encore d'évaluation
- Série N3Document5 pagesSérie N3Aisaoua BuobouPas encore d'évaluation
- Machines Thermiques MMTH 2021Document11 pagesMachines Thermiques MMTH 2021Islam Banchour 3Pas encore d'évaluation
- Machines Thermiques (Ex)Document29 pagesMachines Thermiques (Ex)Salim AttariPas encore d'évaluation
- Ch3 Turbine À GazDocument10 pagesCh3 Turbine À GazYahiyaoui SofyanePas encore d'évaluation
- 3ICMAnnaba ZemmouriDocument10 pages3ICMAnnaba Zemmourimustapha dmlPas encore d'évaluation
- Cours - 9 Cycles de Puissance À VapeurDocument20 pagesCours - 9 Cycles de Puissance À Vapeurrazak tiaPas encore d'évaluation
- Correction TD Thermodynamique Des SystemesDocument5 pagesCorrection TD Thermodynamique Des SystemesZ.I.D ZAKARIYAPas encore d'évaluation
- Exercice 1 Turbine Single Flash 2020Document4 pagesExercice 1 Turbine Single Flash 2020Hamza Zaouak100% (1)
- DS2 2009Document3 pagesDS2 2009ridhajamelPas encore d'évaluation
- Thermo ProjetDocument19 pagesThermo ProjetmarwaPas encore d'évaluation
- Exercices de TDDocument4 pagesExercices de TDWeld Saf100% (1)
- Série TD 1Document1 pageSérie TD 1Syphax HDPas encore d'évaluation
- Chapitre 3-Cycle de Puissance À GazDocument11 pagesChapitre 3-Cycle de Puissance À GazRaghib MohamedPas encore d'évaluation
- Thermo5 PDFDocument4 pagesThermo5 PDFBrahimloPas encore d'évaluation
- Cours Frigo Partie IIDocument13 pagesCours Frigo Partie IIayadiPas encore d'évaluation
- Pompe A ChaleurDocument4 pagesPompe A ChaleurMokrane SfaksiPas encore d'évaluation
- 03-Cycle de Carnot-A22Document16 pages03-Cycle de Carnot-A22Edwin RodriguezPas encore d'évaluation
- TP Pompe À ChaleurDocument9 pagesTP Pompe À ChaleurMaram FradiPas encore d'évaluation
- Fonctionnement D Un Congelateur EnonceDocument5 pagesFonctionnement D Un Congelateur EnonceAbdePas encore d'évaluation
- V TAG Diaporama2Document82 pagesV TAG Diaporama2brhomPas encore d'évaluation
- Cycle de RankineDocument8 pagesCycle de RankineLuka ModrićPas encore d'évaluation
- Exercice Docx1Document4 pagesExercice Docx1mbou chancellePas encore d'évaluation
- Polycopie MOOC CTC2 S3Document32 pagesPolycopie MOOC CTC2 S3Dalila AmmarPas encore d'évaluation
- Machines Thermiques - CMDocument8 pagesMachines Thermiques - CMabdo tm100% (1)
- EEM PBL2 - Moteur DieselDocument9 pagesEEM PBL2 - Moteur DieselMagis MakengoPas encore d'évaluation
- TP1 - PAC - Thermodynamique II - PR LamraniDocument10 pagesTP1 - PAC - Thermodynamique II - PR LamraniHafid El fdilPas encore d'évaluation
- L2P Thermo TD8Document2 pagesL2P Thermo TD8bbbbb100% (1)
- Rapport-Climat YassineDocument12 pagesRapport-Climat YassineMuhcinePas encore d'évaluation
- Cours de Thermo Appliqu+®eDocument38 pagesCours de Thermo Appliqu+®eAmadou CISSEPas encore d'évaluation
- Physique 2003Document6 pagesPhysique 2003Guylaine Bethy MOTOKA ESSIMENGANEPas encore d'évaluation
- TP 2 Pompe À Chaleur 2Document9 pagesTP 2 Pompe À Chaleur 2ayoubPas encore d'évaluation
- Chap I Machines Et Systèmes EnergétiquesDocument11 pagesChap I Machines Et Systèmes EnergétiquesAsma MensiPas encore d'évaluation
- TD M35 Machines Thermiques EnonceDocument8 pagesTD M35 Machines Thermiques EnonceImade DaoudiPas encore d'évaluation
- Examen 3lic EM 1415Document6 pagesExamen 3lic EM 1415Abd El Basset BeNmansour50% (2)
- Absorption CorrectionDocument5 pagesAbsorption CorrectionKãrîm KåhlìPas encore d'évaluation
- TD Centrale Thermique PDFDocument6 pagesTD Centrale Thermique PDFMOUSSA OUSMANE MAHAMAN SANIPas encore d'évaluation
- Stirling Motor PDFDocument15 pagesStirling Motor PDFomar el ghamri100% (1)
- TP Clim FDocument9 pagesTP Clim Ffarroukh med waelPas encore d'évaluation
- Serie N1 1Document4 pagesSerie N1 1ayoub darariPas encore d'évaluation
- Chapitre 5. Machines À Cycles RécepteursDocument7 pagesChapitre 5. Machines À Cycles RécepteursSofiane MehadjiPas encore d'évaluation
- Chap2f2020 PDFDocument61 pagesChap2f2020 PDFChaimaa BasasPas encore d'évaluation
- Mach ThermiquesDocument25 pagesMach ThermiqueswalidPas encore d'évaluation
- Sujet Bac TSE Chimie 2023Document3 pagesSujet Bac TSE Chimie 2023Toumany FofanaPas encore d'évaluation
- TD1 Diagrammes Déquilibres Des Alliagess-1Document4 pagesTD1 Diagrammes Déquilibres Des Alliagess-1jihed korbiPas encore d'évaluation
- 3D3 JNM2003Document5 pages3D3 JNM2003NigerPas encore d'évaluation
- Classification Périodique PDFDocument2 pagesClassification Périodique PDFRaja BenabPas encore d'évaluation
- Dossier Energies RenouvelablesDocument5 pagesDossier Energies RenouvelablesskitocPas encore d'évaluation
- 3.1-Série de TD BDocument2 pages3.1-Série de TD Byugensh2Pas encore d'évaluation
- Corrigé 06Document2 pagesCorrigé 06lmd200975% (4)
- TransiDocument5 pagesTransinouredine akliPas encore d'évaluation
- Resume de Cours Piles Chimique 4 Math+4sc +4 Tec (Enregistré Automatiquement)Document3 pagesResume de Cours Piles Chimique 4 Math+4sc +4 Tec (Enregistré Automatiquement)suiton fz100% (3)
- Ex RCDocument4 pagesEx RCPc KawtarPas encore d'évaluation
- PrincipéchangeurDocument5 pagesPrincipéchangeurAyoub Magroud100% (1)
- Cours Cycles Biogéochimique M2 BiodiversitéDocument10 pagesCours Cycles Biogéochimique M2 BiodiversitéFATIMA-ZAHRA JAPas encore d'évaluation
- TD Transformateurs Électriques LVDocument5 pagesTD Transformateurs Électriques LVIhssane IdrissiPas encore d'évaluation
- 16 Les AC MarquésDocument70 pages16 Les AC MarquésDr BENOUADFELPas encore d'évaluation
- TD Transferts de Chaleur Et de Matière FPN Master Chimie Des Matériaux S2 PDFDocument35 pagesTD Transferts de Chaleur Et de Matière FPN Master Chimie Des Matériaux S2 PDFAbir AbkariPas encore d'évaluation
- PFE Les SulfatesDocument14 pagesPFE Les SulfatesisabelpenamantePas encore d'évaluation
- Fiche05 Finition ZINTEKDocument1 pageFiche05 Finition ZINTEKValtessPas encore d'évaluation
- HH MergedDocument12 pagesHH Mergedbenaoua nourPas encore d'évaluation
- Bougies de Prechauffage: NGK France MFBP0905Document71 pagesBougies de Prechauffage: NGK France MFBP0905OS DiagnosticAutoPas encore d'évaluation
- 01 Controle #3 Semestre 2Document6 pages01 Controle #3 Semestre 2JOKER YTPas encore d'évaluation
- Cours de Geologie Petroliere OriDocument13 pagesCours de Geologie Petroliere OriSamba Koukouare ProsperPas encore d'évaluation
- Pharmacologie EndodontiqueDocument8 pagesPharmacologie EndodontiqueKamalo TrissePas encore d'évaluation
- TC - Examen - Emd 2 6728Document13 pagesTC - Examen - Emd 2 6728Ha NahPas encore d'évaluation
- Interrogation 01 Avec Corrigé - Physique 02 - 2020-2021Document5 pagesInterrogation 01 Avec Corrigé - Physique 02 - 2020-2021Ayoub FekharPas encore d'évaluation
- CO1 2S2 2023 Iakafrine - WahabdiopDocument2 pagesCO1 2S2 2023 Iakafrine - WahabdiopmohamedPas encore d'évaluation
- Sommaire: Le Soudage Au Gaz (Au Chalumeau)Document27 pagesSommaire: Le Soudage Au Gaz (Au Chalumeau)Menad Salah100% (1)
- Activité 2 Maille de Chlorure de Sodium CorrigéDocument3 pagesActivité 2 Maille de Chlorure de Sodium Corrigéschepes0% (1)
- Rapport Geotechnique CompletDocument65 pagesRapport Geotechnique CompletGORGUI SOWPas encore d'évaluation
- Chap1 VetdDocument3 pagesChap1 VetdDialloPas encore d'évaluation
- Fiche Technique de Sécurité 93/112/CEE M 220: 883816.0, 883816.00010, 9.3027.0 Oel - D.DotDocument6 pagesFiche Technique de Sécurité 93/112/CEE M 220: 883816.0, 883816.00010, 9.3027.0 Oel - D.DotSMM ENTREPRISEPas encore d'évaluation