Académique Documents
Professionnel Documents
Culture Documents
Cours 2 - Suivi Temporel
Transféré par
Hamza Berahma0 évaluation0% ont trouvé ce document utile (0 vote)
30 vues9 pagesTitre original
Cours 2 _ Suivi Temporel
Copyright
© © All Rights Reserved
Formats disponibles
PPTX, PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
0 évaluation0% ont trouvé ce document utile (0 vote)
30 vues9 pagesCours 2 - Suivi Temporel
Transféré par
Hamza BerahmaDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PPTX, PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 9
Cours 2 : Suivi temporel d’une réaction chimique – vitesse de la réaction
Introduction :
La surveillance en continu des
réactions chimiques est
indispensable pour assurer la
sécurité de l’installation et la
qualité des produits obtenus.
• Comment assurer le
contrôle d’une réaction
chimique ?
• Comment définir la vitesse
d’une réaction chimique ?
I. Suivi de l'évolution temporelle d'une transformation chimique :
Pour suivre temporellement l'évolution d'une transformation
chimique on doit connaître sa composition à chaque instant. Il
existe plusieurs méthodes qui permettent de suivre l'évolution
d'une transformation parmi lesquelles il y'a :
Les méthodes physiques : la conductimétrie – la pH-métrie –
la mesure de la pression – la mesure du volume ……
Les méthodes chimiques : sont basées sur le dosage.
1. Suivi de l'évolution temporelle d'une transformation
chimique par le dosage :
Activité 1 :
2. Suivi de l'évolution temporelle d'une transformation
chimique par la mesure de pression d’un gaz :
Activité 2 :
3. Suivi de l'évolution temporelle d'une transformation
chimique par la conductimétrie:
Activité 3 :
II-Vitesse de réaction et le temps de demi-réaction.
1-Vitesse volumique de réaction :
a-Définition :
La vitesse volumique v(t) d’une réaction se déroulant dans un
volume constant V est la valeur de la dérivée temporelle de
l’avancement x de la réaction , divisée par le volume V :
dx : l’accroissement de l’avancement x en mol
dt : l’accroissement du temps t (en s , en min ou en h) .
V : le volume réactionnel (en litre ou m3) .
L’unité de la vitesse volumique dans le SI est : mol.m -3.s-1
ou mol.L-1.s-1
b- Détermination graphique de la vitesse de réaction ti:
• on trace la tangente de la courbe x = f(t) au point d’abscisse
ti .
• en calculant le coefficient directeur a=dx/dt à l’instant ti de
la tangente à la courbe et en le divisant par le volume V.
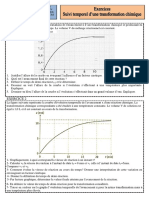
Remarque:
On observe (graphique ci-
contre) que le coefficient
directeur a diminue au cours du
temps, donc la vitesse
volumique de réaction
diminue au cours du temps.
2-Le temps de demi-réaction t1/2 :
a-Définition :
Le temps de demi-réaction t1/2 d’un système chimique est la
durée nécessaire pour que l’avancement parvienne à la moitié
de sa valeur finale . xf
x(t )=
1/2 2
x max
Si la transformation est totale on aura : x(t1/2 ) =
2
b. Utilisation de t1/2
+ Le temps de demi-réaction permet d’évaluer la durée
nécessaire à l’achèvement de la transformation chimique
étudiée .
+ La connaissance du temps de demi-réaction permet ainsi de
choisir une méthode de suivi adaptée au système étudié :
Une réaction lente :méthode de titrage .
Une réaction rapide : appareils de mesure programmer
( pH mètre , conductimétrie , pressiomètrie ,etc .. )
IV. Interprétation microscopique :
1. Agitation thermique
On considère deux entités A2 et B2 , les multiples chocs entre
ces entités sont à l’origine de leur transformation en
molécules AB
Pour qu’un choc soit efficace , c’est à dire pour qu’il y a
apparition de molécules A-B , il faut casser la liaison A-A et
la liaison B-B pour former deux liaisons A-B . la cassure des
liaisons nécessite un apport d’énergie .
2. Influence des facteurs cinétiques:
a-Influence de la concentration initiale :
Plus le nombre d’entités réactives est grand , plus la
fréquence des chocs efficaces est grande et plus la
transformation est rapide. Le nombre d’entités relatives est
proportionnel à la concentration des ces entités
b-Influence de la température :
Plus la température est élevée (augmentation de l’agitation
thermique) , plus la fréquence des chocs est grande et plus la
transformation est rapide (vitesse de réaction augmente).
Vous aimerez peut-être aussi
- Cours Suivi TemporelDocument3 pagesCours Suivi Temporelathn.maryamPas encore d'évaluation
- Chapitre-2 - Suivi Temporel D'une Transformation Chimique - Vitesse de RéactionDocument5 pagesChapitre-2 - Suivi Temporel D'une Transformation Chimique - Vitesse de Réactiona houssPas encore d'évaluation
- Cinétique Chimique PDFDocument6 pagesCinétique Chimique PDFAzizElheniPas encore d'évaluation
- Chapitre - CH2 - Vitesse de ReactionDocument5 pagesChapitre - CH2 - Vitesse de Reactionmohamed laghribPas encore d'évaluation
- Lecon 2 Chimie Vitesse D Une Reaction ChimiqueDocument1 pageLecon 2 Chimie Vitesse D Une Reaction ChimiqueKais GuesmiPas encore d'évaluation
- Cours Vitesse de ReactionDocument3 pagesCours Vitesse de ReactioncristyenPas encore d'évaluation
- Suivi Temporel D - Une TransformationDocument6 pagesSuivi Temporel D - Une TransformationerrairachidPas encore d'évaluation
- Resumé Suivi Temporel D'une Transformation ChimiqueDocument1 pageResumé Suivi Temporel D'une Transformation ChimiqueZakaria BelaaroussiPas encore d'évaluation
- Suivi Temporel D'une Transformation Chimique - Vitesse de RéactionDocument7 pagesSuivi Temporel D'une Transformation Chimique - Vitesse de RéactionKamal BdPas encore d'évaluation
- Cinétique S5 2016Document122 pagesCinétique S5 2016Mohamed EL FAGHLOUMIPas encore d'évaluation
- Cours - Suivi TemporelDocument7 pagesCours - Suivi TemporelRedouane Reda100% (2)
- Cinétique Chimique TleDocument2 pagesCinétique Chimique TleSafa CHAGRENPas encore d'évaluation
- Chapitre 2, Suivi Temporel D'une Transformation Chimique, Cours, Activités, Exercices D'application, 2BAC BIOF PR JENKAL RACHIDDocument11 pagesChapitre 2, Suivi Temporel D'une Transformation Chimique, Cours, Activités, Exercices D'application, 2BAC BIOF PR JENKAL RACHIDKarim EL HAJJIPas encore d'évaluation
- Modelisation Des Transformations Chimiques Bilan de La Matiere Resume de Cours 2Document2 pagesModelisation Des Transformations Chimiques Bilan de La Matiere Resume de Cours 2Lazreg ImedPas encore d'évaluation
- c9 TC Inter Prof Sbiro (WWW - Pc1.ma)Document2 pagesc9 TC Inter Prof Sbiro (WWW - Pc1.ma)cpm fessaisPas encore d'évaluation
- Cours 2 Chimie-eleve-TRAFI 2BACDocument9 pagesCours 2 Chimie-eleve-TRAFI 2BACEnidroun OutPas encore d'évaluation
- Cinetique Chimique Fiche CoursDocument2 pagesCinetique Chimique Fiche CoursmariePas encore d'évaluation
- Cours 1 - Suivi Temporel D'une Transformation (WWW - AdrarPhysic.Fr) - 7Document1 pageCours 1 - Suivi Temporel D'une Transformation (WWW - AdrarPhysic.Fr) - 7salhiPas encore d'évaluation
- Cinétique ChimiqueDocument30 pagesCinétique ChimiqueYounes MotraniPas encore d'évaluation
- Temps Et Evolution Chimique PDFDocument31 pagesTemps Et Evolution Chimique PDFludovicPas encore d'évaluation
- 2.déterminer La Vitesse de Réaction Et Le Temps de Demi-Réaction PDFDocument3 pages2.déterminer La Vitesse de Réaction Et Le Temps de Demi-Réaction PDFkimmikPas encore d'évaluation
- Cours Avancement D'une Reaction 2015Document2 pagesCours Avancement D'une Reaction 2015Daghsni SaidPas encore d'évaluation
- Chapitre 1 Cours Cinétique - 2021Document40 pagesChapitre 1 Cours Cinétique - 2021Li NaPas encore d'évaluation
- Cours - Chimie - RESUME CINETIQUE CHIMIQUE - Bac Sciences Exp (2015-2016) MR Daghsni SahbiDocument3 pagesCours - Chimie - RESUME CINETIQUE CHIMIQUE - Bac Sciences Exp (2015-2016) MR Daghsni SahbiKais Ben Aicha100% (2)
- Partie1 CorriDocument31 pagesPartie1 CorriMeryam MessaoudiPas encore d'évaluation
- Resume PC Biof Partie ChimieDocument8 pagesResume PC Biof Partie Chimielabiadsihame1Pas encore d'évaluation
- 2 Suivi Temporel D Une TransformationDocument5 pages2 Suivi Temporel D Une Transformationfoud18Pas encore d'évaluation
- 1 Cinétique ChimiqueDocument12 pages1 Cinétique ChimiqueYoucef KrPas encore d'évaluation
- Cours de La CinétiqueDocument12 pagesCours de La Cinétiqueazerty027391Pas encore d'évaluation
- Chapitre I Rappels Partie IDocument8 pagesChapitre I Rappels Partie IJojo BoubPas encore d'évaluation
- Cours DR BENAMIRA MESSAOUD Cinétique Chimique Master 2 Chimie Des MatériauxDocument66 pagesCours DR BENAMIRA MESSAOUD Cinétique Chimique Master 2 Chimie Des MatériauxaminePas encore d'évaluation
- Cinétique ChimiqueDocument15 pagesCinétique ChimiqueYounes JaaidaniPas encore d'évaluation
- Chapitre 1 Cinetique TFDocument4 pagesChapitre 1 Cinetique TFkathyPas encore d'évaluation
- Cinetique IDocument2 pagesCinetique INajimou Alade TidjaniPas encore d'évaluation
- II 04 CinetiqueDocument3 pagesII 04 CinetiqueMohamed ElouakilPas encore d'évaluation
- Serie 2 Suivi Temporelle D Une Transformation ChimiqueDocument7 pagesSerie 2 Suivi Temporelle D Une Transformation Chimiquee.maskarPas encore d'évaluation
- Cours de Cinétique L2Document49 pagesCours de Cinétique L2AndyTeck Pro (Android)0% (1)
- Cours de Cinétique ChimiqueDocument6 pagesCours de Cinétique Chimiqueilyes fellagPas encore d'évaluation
- 3.cinétique Chimique (DR - Chaal)Document9 pages3.cinétique Chimique (DR - Chaal)Neou Phors SoporsPas encore d'évaluation
- Cinetique ChimiqueDocument8 pagesCinetique ChimiqueFranck MomoPas encore d'évaluation
- CP I Chapitre I. Vitesse Et Lois de Vitesse 1 1Document17 pagesCP I Chapitre I. Vitesse Et Lois de Vitesse 1 1Section E GPPas encore d'évaluation
- Chapitre 1 Cinetique1Document6 pagesChapitre 1 Cinetique1stevPas encore d'évaluation
- Cours Machines ThermiquesDocument8 pagesCours Machines ThermiquesMedPas encore d'évaluation
- Cinetique Chimique (PR Belaribi)Document17 pagesCinetique Chimique (PR Belaribi)Zidani LinaPas encore d'évaluation
- Chapitre 1Document5 pagesChapitre 1Manel AbrichePas encore d'évaluation
- tp1 CRDocument15 pagestp1 CRhacenePas encore d'évaluation
- Cinétique Chimique MPSI Et MPDocument23 pagesCinétique Chimique MPSI Et MPmomoadamso07Pas encore d'évaluation
- CinetiqueDocument50 pagesCinetiquesidi mohamed el amine nekkalPas encore d'évaluation
- Série N°9-9Document3 pagesSérie N°9-9Jihad ELPas encore d'évaluation
- TS C 02 CinetiqueDocument4 pagesTS C 02 CinetiqueArtista NaniPas encore d'évaluation
- Cinétique ChimiqueDocument7 pagesCinétique ChimiquehajPas encore d'évaluation
- Chapitre 9: Temps Et Évolution Chimique: 1) RappelsDocument11 pagesChapitre 9: Temps Et Évolution Chimique: 1) Rappelspapa samba sarrPas encore d'évaluation
- Cours 1ere SVV Chimi2-ConvertiDocument20 pagesCours 1ere SVV Chimi2-ConvertiChahd Ikhlas RstPas encore d'évaluation
- Exercices 2 Suivi TemporelDocument1 pageExercices 2 Suivi TemporelayoubbouuderqaPas encore d'évaluation
- Exercices 2 Suivi TemporelDocument1 pageExercices 2 Suivi Temporelكورة لايفPas encore d'évaluation
- Station Physico ChimieDocument26 pagesStation Physico ChimieAghai MohamedPas encore d'évaluation
- TP N° 1 Synthèse Dun SavonDocument4 pagesTP N° 1 Synthèse Dun SavonAmina BadaouiPas encore d'évaluation
- Les Calculatrices Sont AutoriséesDocument5 pagesLes Calculatrices Sont AutoriséesIk RamPas encore d'évaluation
- Dosage D Un Anti Mousse 1Document2 pagesDosage D Un Anti Mousse 1غرباءPas encore d'évaluation
- Devoir de Synthese N°2: Epreuve: Sciences PhysiquesDocument5 pagesDevoir de Synthese N°2: Epreuve: Sciences PhysiquesNour NessahPas encore d'évaluation
- Absorption Dun Gaz Par Un SolvantDocument32 pagesAbsorption Dun Gaz Par Un SolvantAmina BelkacemiPas encore d'évaluation
- Cours Onde Mecanique ProgressiveDocument4 pagesCours Onde Mecanique Progressiveياسين أوطالب100% (1)
- Chapitre 7Document18 pagesChapitre 7nassima chenikhaPas encore d'évaluation
- Ephedra PDFDocument3 pagesEphedra PDFnehemie nwayPas encore d'évaluation
- TD - N°2-Thermo - 2 - CorréctionDocument10 pagesTD - N°2-Thermo - 2 - CorréctionSamahi Fatima Zahra100% (1)
- TD Section F 2021 2022Document2 pagesTD Section F 2021 2022Walid SlimaniPas encore d'évaluation
- Chapitre 3Document21 pagesChapitre 3Hadjer ZitounePas encore d'évaluation
- JUIN 2022: Saga Web Pour: Client: 99590300 Le: 16/10/2022 À 15:55Document55 pagesJUIN 2022: Saga Web Pour: Client: 99590300 Le: 16/10/2022 À 15:55Mohammed BoucherbaPas encore d'évaluation
- Ds3 CorrigeDocument16 pagesDs3 CorrigeKaren MTKPas encore d'évaluation
- Exercice 1: À Pression Constante, en Considérant Que, Dans Chaque Domaine de Température Étudié, LaDocument2 pagesExercice 1: À Pression Constante, en Considérant Que, Dans Chaque Domaine de Température Étudié, LaAabed omair100% (1)
- Pages Extraites de 1BAC CC2 CONTROLS 1bacDocument5 pagesPages Extraites de 1BAC CC2 CONTROLS 1bacTarik OuabrkPas encore d'évaluation
- Master abvtHistaminSO2Document46 pagesMaster abvtHistaminSO2Fatima IrjdalnPas encore d'évaluation
- Corrigier TD DescriptiveDocument32 pagesCorrigier TD DescriptiveMohamed mePas encore d'évaluation
- BAOUIA KaisDocument6 pagesBAOUIA KaischoaybPas encore d'évaluation
- TP TCMDocument19 pagesTP TCMMateus SenaPas encore d'évaluation
- TPN°2 Résumé PDFDocument4 pagesTPN°2 Résumé PDFNada DjenanePas encore d'évaluation
- Electron Affinity of Elements & Various MoleculesDocument8 pagesElectron Affinity of Elements & Various MoleculesYourMotherPas encore d'évaluation
- Cours Isoméries Et stéréoisoméries-ENSB-Dr S.BOUSSAHADocument57 pagesCours Isoméries Et stéréoisoméries-ENSB-Dr S.BOUSSAHALoukmen BiadPas encore d'évaluation
- 40-105 Mécanismes RéactionnelsDocument8 pages40-105 Mécanismes RéactionnelsSouheila TouatiPas encore d'évaluation
- 5 AlcoolDocument2 pages5 AlcoolRahouba Ben Dhieb100% (1)
- TD1 OuerglaDocument8 pagesTD1 OuerglaMahfoud OmarPas encore d'évaluation
- Chimie Organique: Exercices Et MéthodesDocument28 pagesChimie Organique: Exercices Et MéthodesLouisette MinatomboPas encore d'évaluation
- Evolution D'Un Systeme Chimique Ferme Mettant en Oeuvre Une Reaction A Stociometrie UniqueDocument10 pagesEvolution D'Un Systeme Chimique Ferme Mettant en Oeuvre Une Reaction A Stociometrie UniqueSarah sarahPas encore d'évaluation
- Etude Et Optimisation de La Solidification D'aciers Faiblement Alliés Lors Du Process de Fonderie Par InoculationDocument127 pagesEtude Et Optimisation de La Solidification D'aciers Faiblement Alliés Lors Du Process de Fonderie Par Inoculationbeey2001Pas encore d'évaluation
- L1S1 Cours 1a Molecules SimplesDocument21 pagesL1S1 Cours 1a Molecules SimplesAbii-RPas encore d'évaluation