Académique Documents
Professionnel Documents
Culture Documents
TD D'ingénierie Des Polymères
Transféré par
ASMAE BOULAALAM100%(2)100% ont trouvé ce document utile (2 votes)
214 vues2 pagesTitre original
TD d'ingénierie des polymères
Copyright
© © All Rights Reserved
Formats disponibles
PDF, TXT ou lisez en ligne sur Scribd
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
100%(2)100% ont trouvé ce document utile (2 votes)
214 vues2 pagesTD D'ingénierie Des Polymères
Transféré par
ASMAE BOULAALAMDroits d'auteur :
© All Rights Reserved
Formats disponibles
Téléchargez comme PDF, TXT ou lisez en ligne sur Scribd
Vous êtes sur la page 1sur 2
UNIVERSITE IBN TOFAIL Année universitaire : 2021-2022
Ecole Nationale Supérieure de Chimie
-KENITRA-
Série N° 1 Chimie des polymères
I/ 1) La polymérisation du propylène peut se faire de manière radicalaire. Écrire le
mécanisme réactionnel.
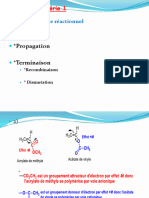
2) Pourquoi l’acétate de vinyle contrairement à l’acrylate de méthyle ne se prête pas à une
polymérisation anionique ?
3) On s’intéresse à la polymérisation de l’acrylonitrile par HCl ou par NaNH2. Écrire dans
chaque cas l’amorçage. Quelle est la voie préférable ?
II/ On considère la réaction de polymérisation cationique de l’isobutène et anionique de
l’acrylonitrile,
1) Donner les premières étapes d’amorçages de la polymérisation de l’isobutène par
les amorceurs (BF3 + H2O) et de l’acrylonitrile par NaNH2.
2) a- Donner le mécanisme de la polymérisation en chaîne de l’isobutène (2-
méthylprop-1-ène) en présence de peroxyde de benzoyle (Ph-C(O)-O-O-C(O)-Ph).
b- Ecrire les réactions de terminaison, correspondant à la dismutation et à la
duplication, de la polymérisation.
III/ a) Ecrire les étapes d’amorçage et de propagation lors de la polymérisation du styrène
amorcée par l’AIBN. Préciser la position du radical en fin de chaîne.
b) L’analyse élémentaire d’un échantillon de polystyrène indique une teneur en azote
égale à 0.075%. La masse molaire moyenne en nombre du polymère est égale à 37800g/mol.
Déterminer le mode de terminaison de la polymérisation.
IV/ La polymérisation du méthacrylate de méthyle en solution est amorcée par l’AIBN à
60°C. Les concentrations initiales sont MMA =2mol/l ; AIBN=0.02mol/l.
On suppose que l’efficacité est de 50%. Calculer :
1- La vitesse initiale de polymérisation,
2- Le temps nécessaire pour avoir 10% de conversion,
3- La conversion atteinte après 10h de réaction en considérant la concentration en
AIBN constante.
AIBN : Kd = 0.85 10-5 s-1
MMA: d= 0,94 ; M = 100g/mol ; kp = 705L.mol-1s-1 ; Kt =3.6 107L.mol-1.s-1.
V/ On effectue la polymérisation de l’acrylate de méthyle en masse à 60°C avec L’ABIN en
concentration 10 -3 mol/l. La terminaison se fait par dismutation. En supposant que la
concentration en AIBN reste constante pendant toute la durée de la réaction.
1) Donner le mécanisme de la polymérisation.
2) Calculer la masse molaire moyenne en nombre initiale.
3) Montrer que la longueur cinétique instantanée est proportionnelle à la concentration en
monomère.
4) Calculer le temps nécessaire pour avoir 95% de conversion.
AIBN : Kd = 0.85 10-5 s-1 , f = 0.6
Acrylate de méthyle : 11,046mol/l, d =0.95, Kp = 2090 l. mol-1s-1, Kt = 0.94 107l.mol-1.s-1.
Vous aimerez peut-être aussi
- Applications de la spectrophotomérie en phytochimie: sciencesD'EverandApplications de la spectrophotomérie en phytochimie: sciencesPas encore d'évaluation
- TD Nâ° 2 GMP 2020-2021Document7 pagesTD Nâ° 2 GMP 2020-2021Kamal Tourout33% (3)
- TD Polymères 3: Exercice 1Document2 pagesTD Polymères 3: Exercice 1Sou Lef JellaliPas encore d'évaluation
- CORRIGE SERIE 2-ConvertiDocument5 pagesCORRIGE SERIE 2-Convertiwail abdelli100% (5)
- TP Nylon 2018 CorrectionDocument8 pagesTP Nylon 2018 CorrectionHassanPas encore d'évaluation
- Série 01Document2 pagesSérie 01ibend376Pas encore d'évaluation
- TD N 1 17-18Document3 pagesTD N 1 17-18Mohamed KamalPas encore d'évaluation
- Correction TD 2Document4 pagesCorrection TD 2mahmoud bensassiPas encore d'évaluation
- Iutmosel Polymeres 2012 CHDocument2 pagesIutmosel Polymeres 2012 CHAbdallah AmmarPas encore d'évaluation
- Chimie Des Polymère - Exercices de RévisionDocument5 pagesChimie Des Polymère - Exercices de RévisionPeter Taha100% (4)
- LPro Polym PDFDocument23 pagesLPro Polym PDFRafik Dra100% (1)
- TD Polymère 1Document1 pageTD Polymère 1mostafa bounabPas encore d'évaluation
- LPro Polym PDFDocument29 pagesLPro Polym PDFzina allaouaPas encore d'évaluation
- Corrections Travaux Dirigés 2 2019-2020 PDFDocument2 pagesCorrections Travaux Dirigés 2 2019-2020 PDFLALEPas encore d'évaluation
- Chapitre 1 de Synthèse (PolycondensationDocument10 pagesChapitre 1 de Synthèse (PolycondensationHana Salah AiechPas encore d'évaluation
- Poly CondensationDocument63 pagesPoly Condensationismail mbarkiPas encore d'évaluation
- Ero Ds c03Document2 pagesEro Ds c03Nina HanPas encore d'évaluation
- Ero Ex c02Document3 pagesEro Ex c02maino100% (1)
- TD Polymères 1 Masses Moléculaires Moyennes, Indice de PolydispersitéDocument2 pagesTD Polymères 1 Masses Moléculaires Moyennes, Indice de PolydispersitéHana Salah AiechPas encore d'évaluation
- TD 2010 PlastiquesDocument2 pagesTD 2010 PlastiquesmortadaPas encore d'évaluation
- Master-G Nie-2Document42 pagesMaster-G Nie-2ayoub dahman100% (1)
- TD Polymère 3Document4 pagesTD Polymère 3mostafa bounabPas encore d'évaluation
- Cours 1 Polymères (Polymérisation Radicalaire) 2022Document12 pagesCours 1 Polymères (Polymérisation Radicalaire) 2022omatrPas encore d'évaluation
- Polymére ResuméDocument54 pagesPolymére ResuméAbdelillah feghoul100% (1)
- Réactions de PolymérisationDocument5 pagesRéactions de PolymérisationVincent Imad100% (1)
- Decouverte Polymeres PDFDocument48 pagesDecouverte Polymeres PDFOussama El Bouadi0% (1)
- Polymeres Corriges D ExercicesDocument3 pagesPolymeres Corriges D ExercicesMEed E-tanPas encore d'évaluation
- Orbitales Moléculaires Frontières en Chimie OrganiqueDocument33 pagesOrbitales Moléculaires Frontières en Chimie OrganiqueMathieu Péborde80% (5)
- Fonctions Thermodynamiques Des Solutions - Suite 4Document30 pagesFonctions Thermodynamiques Des Solutions - Suite 4Ryad Khelouf100% (1)
- Rapport Du PolymèreDocument8 pagesRapport Du PolymèreHamza Azzaari100% (1)
- Chimie Des Polymères - Chapitre1 - 3LRPDocument16 pagesChimie Des Polymères - Chapitre1 - 3LRPTahar Yahiaoui100% (2)
- 02 CORRECTION Exo Polymere PDFDocument2 pages02 CORRECTION Exo Polymere PDFzina allaoua100% (3)
- Expose PolymèreDocument9 pagesExpose PolymèreisaacPas encore d'évaluation
- Wa0006Document5 pagesWa0006Taouil MohamedPas encore d'évaluation
- Exercices PolymeresDocument1 pageExercices PolymeresHamza Dicko100% (1)
- Cours Poly. 2023 Etudiant (E) SDocument57 pagesCours Poly. 2023 Etudiant (E) SZakaria AlouanePas encore d'évaluation
- Exercices. Materiaux Polymeres OrganiquesDocument8 pagesExercices. Materiaux Polymeres OrganiquesYetd ToudiPas encore d'évaluation
- Cours de Chimie Des Polymères Master PDFDocument70 pagesCours de Chimie Des Polymères Master PDFManal ElaameryPas encore d'évaluation
- Série TD 2-1 4850Document2 pagesSérie TD 2-1 4850Assia ChadliPas encore d'évaluation
- Atg TD Melange G K CCDocument9 pagesAtg TD Melange G K CCEn Savoir Plus100% (1)
- C01 (Exos) Polymeres PlastiquesDocument2 pagesC01 (Exos) Polymeres PlastiquesAchwak Belfadel100% (1)
- Exercices Polymeres PDFDocument2 pagesExercices Polymeres PDFRobin33% (3)
- 5 2 PolymèresDocument38 pages5 2 PolymèresJoshua JordanPas encore d'évaluation
- TD NDocument3 pagesTD Nmodou BADIANEPas encore d'évaluation
- El Jouhari Exercices Smc5-M17-E3Document7 pagesEl Jouhari Exercices Smc5-M17-E3maino63% (8)
- Polymeres PDFDocument8 pagesPolymeres PDFKorichiKarimPas encore d'évaluation
- Cours PolymèresDocument17 pagesCours PolymèresJhee raaPas encore d'évaluation
- Catalyse HeterogeneDocument52 pagesCatalyse Heterogeneahmed100% (1)
- Cours Degradation Polymere N°3Document22 pagesCours Degradation Polymere N°3Ouahes HoudaifaPas encore d'évaluation
- TD04 Binaires PDFDocument4 pagesTD04 Binaires PDFAabed omairPas encore d'évaluation
- Cinetique Electroch PDFDocument7 pagesCinetique Electroch PDFJérôme KyabuPas encore d'évaluation
- Série 3 Loi de Faraday Et Indice de TransfertDocument2 pagesSérie 3 Loi de Faraday Et Indice de TransfertSection E GP50% (2)
- Des Applications Sur Les PolymèresDocument2 pagesDes Applications Sur Les PolymèresmortadaPas encore d'évaluation
- Polymerisation RadicalaireDocument36 pagesPolymerisation RadicalaireVincent ImadPas encore d'évaluation
- ChemDocument5 pagesChemAnonymous svBEhGhEIPas encore d'évaluation
- Binaire PiDocument9 pagesBinaire PiBasmã Alileche100% (1)
- TD #2 GMP 23-24Document7 pagesTD #2 GMP 23-24mennanesalaheddinePas encore d'évaluation
- Série N 3Document1 pageSérie N 3Zoheir TarekPas encore d'évaluation
- Corrigé de La Série 1 2024Document13 pagesCorrigé de La Série 1 2024aya.cherguiaPas encore d'évaluation
- Guide Et ProcédureDocument2 pagesGuide Et ProcédureASMAE BOULAALAMPas encore d'évaluation
- Lettre Dappuit Des StagesDocument1 pageLettre Dappuit Des StagesASMAE BOULAALAMPas encore d'évaluation
- Lettre Motivation Stage IngenieurDocument1 pageLettre Motivation Stage IngenieurASMAE BOULAALAMPas encore d'évaluation
- FlowsheetingDocument40 pagesFlowsheetingASMAE BOULAALAMPas encore d'évaluation
- Devoir de Synthèse N°1 - Physique - Bac Tech (2009-2010) MR Beni HassenDocument4 pagesDevoir de Synthèse N°1 - Physique - Bac Tech (2009-2010) MR Beni HassenAicha TennichPas encore d'évaluation
- Restaurer La Dent DépulpéeDocument138 pagesRestaurer La Dent DépulpéebenzimraPas encore d'évaluation
- Corrige CAPA Sept2014Document11 pagesCorrige CAPA Sept2014paulardPas encore d'évaluation
- Book TBP FRDocument6 pagesBook TBP FRDepanama FranckyPas encore d'évaluation
- Regime GlutenDocument15 pagesRegime Glutenhonore belloti100% (1)
- Modélisation Et Simulation D'un Moteur Asynchrone: 2 Année Master S3 (ELM)Document7 pagesModélisation Et Simulation D'un Moteur Asynchrone: 2 Année Master S3 (ELM)Khodja AymenPas encore d'évaluation
- Lloyd Tunisien Efd311215Document41 pagesLloyd Tunisien Efd311215manelweslati4Pas encore d'évaluation
- D31 - Bachelor GEST - Janvier 2019 - CorrigéDocument11 pagesD31 - Bachelor GEST - Janvier 2019 - CorrigéMicro ImmfPas encore d'évaluation
- Bonzon P-J Delph Le Marin 1955Document217 pagesBonzon P-J Delph Le Marin 1955Sorin YannickPas encore d'évaluation
- Stèle DDocument7 pagesStèle DAngelika ErhardtPas encore d'évaluation
- COURS Assainissement Chap 2 2011Document22 pagesCOURS Assainissement Chap 2 2011sabbanrachid100% (4)
- CURRICULUM VITAE - BOUTIRA BouchraDocument3 pagesCURRICULUM VITAE - BOUTIRA BouchrabouchghabtraPas encore d'évaluation
- BTS SIO Caledonie Nov 2020 DVDocument3 pagesBTS SIO Caledonie Nov 2020 DVcedric doussetPas encore d'évaluation
- L'etude de La Qualite D'energie A L'aide D'une Carte ArduinoDocument46 pagesL'etude de La Qualite D'energie A L'aide D'une Carte Arduinoجمال طيبيPas encore d'évaluation
- OdinismeDocument2 pagesOdinismeLonie WissangPas encore d'évaluation
- Centre de CisaillementDocument12 pagesCentre de CisaillementMohammed Mammar Kouadri100% (1)
- Guide Normes Etudes Reconnaissance Caracterisation SolsDocument22 pagesGuide Normes Etudes Reconnaissance Caracterisation SolsAndré Germain MbogbaPas encore d'évaluation
- Calcul Du Volume Du RéservoirDocument11 pagesCalcul Du Volume Du RéservoirAmel Hyd50% (2)
- Feuille D'exercices N 4Document3 pagesFeuille D'exercices N 4Mohamed Ben SalahPas encore d'évaluation
- Élaboration Du Projet de La Stratégie Nationale de LDocument5 pagesÉlaboration Du Projet de La Stratégie Nationale de LSara BouchikhiPas encore d'évaluation
- MSFRA130078Document81 pagesMSFRA130078Ines HMPas encore d'évaluation
- La Planète Des SingesDocument21 pagesLa Planète Des SingeslisaPas encore d'évaluation
- Technique Analyse UnivarieeDocument26 pagesTechnique Analyse Univarieekago1Pas encore d'évaluation
- Sermons de BossuetDocument807 pagesSermons de BossuetCapitalemoPas encore d'évaluation
- 111mémoire - Universite CasablancaDocument65 pages111mémoire - Universite CasablancaWalid ArhnouchPas encore d'évaluation
- TCS - Unité 1 - Cahier D'élève - ElalamiDocument70 pagesTCS - Unité 1 - Cahier D'élève - ElalamiMAKTABAT NOURPas encore d'évaluation
- SVT Spécialité S IndeDocument6 pagesSVT Spécialité S IndeLetudiant.frPas encore d'évaluation
- CYC5600ADocument3 pagesCYC5600AChafik AlbadraouiPas encore d'évaluation
- (WEB) Activité - ARPP Influenceurs Virtuels P1Document1 page(WEB) Activité - ARPP Influenceurs Virtuels P1le mrPas encore d'évaluation
- Travaux Dirigés Régulation Ind. 21Document54 pagesTravaux Dirigés Régulation Ind. 21Amina LazregPas encore d'évaluation