Académique Documents
Professionnel Documents
Culture Documents
TD N°9 RMGX Corrigé 2021
Transféré par
RobertoTitre original
Copyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
TD N°9 RMGX Corrigé 2021
Transféré par
RobertoDroits d'auteur :
Formats disponibles
Les organomagnésiens mixtes Corrigé de la feuille d’exercices n°9
Exercice 1 :
Les composés A à P sont les suivants :
(R) CH3CH2MgBr + I2 CH3CH2I + ½ MgBr2 + ½ MgI2
t=0 n0 n1 - - -
tf - n 1 - n0 n0 ½ n0
½ n0
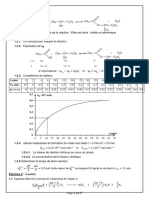
Le diiode restant est ensuite dosé par le thiosulfate S 2O32-, selon une récation
d’oxydoréduction : (D) I2 + 2 S2O32- 2 I- + S4O62-.
L'équivalence est repérée par la disparition de la couleur brune du diiode en
solution.
c) A l'équivalence de (D) : n1 - n0 = ½ c Ve, donc : n1 - n0 = 1,52.10-3 mol
Or : n1 = 20.10-3 x 40 / 252 = 3,17.10-3 mol donc n0 = 1,65 10-3 mol
Donc : CEtMgBr = 1,65.10 /10 = 1,65 mol.L = CEtMgBr
-3 -3 -1
Donc : r = 82,5%
Exercice 2 :
________________________________________________________
1.) Mg + CH3CH2Br CH3CH2MgBr
t=0 0,625 0,50 - Exercice 3 :
tf (si totale) 0,125 - 0,50 1. Le butan-2-ol est un alcool secondaire : il est obtenu par addition nucléophile
d’un organomagnésien sur un aldéhyde :
-
On a en effet : (nEtBr)0 = d.eau.VEtBr/MEtBr : 1,46*1*37,3/109 = 0,50 mol - O
+ 1) Et 2O OH
+ +
MgBr H 2) H + / H 2O
L'éther anhydre est un solvant de choix pour cette réaction (il est anhydre,
aprotique, base de Lewis ; cf. cours). Il reflue, même sans chauffage, car la ou -
O OH
réaction est exothermique. - +
CH3-MgBr +
+ 1) Et2O
H 2) H + / H 2O
2a) La solution de diiode doit être anhydre car l'eau détruit le magnésien (cf.
cours), ce qui fausserait le dosage !
2. L’alcool benzylique est un alcool primaire : il est obtenu par addition
nucléophile d’un organomagnésien sur le méthanal :
b) La 1 réaction qui se produit s'apparente à une substitution nucléophile (SN)
ère
-
(I2 est apolaire mais est polarisable ; le centre électrophile se forme à l'approche - + O
+ 1) Et 2O
de l'organomagnésien). Ph-MgBr + Ph-CH 2-OH
H H 2) H+ / H 2O
3. L’alcool est tertiaire, il est donc obtenu par addition nucléophile d’un
organomagnésien sur une cétone :
PCSI Page 1 sur 4
Les organomagnésiens mixtes Corrigé de la feuille d’exercices n°9
- O
-
b)
+ 1) Et 2O
CH3-MgBr + +
OH
2) H + / H 2O
ou -
O
4. CH
L’hexan-3-ol
- +
-MgBr +
est
+ un 1)alcool
Et 2O secondaire : il est obtenu par addition nucléophile
OH
d’un 3organomagnésien
Cl sur
2) H +un
/ H 2aldéhyde
O :
c)
4.
a)
________________________________________________________
Exercice 4 :
1. b)
2. a)
Mg , Et2O
2.b) + HBr
b) Br MgBr
Majoritaire (règle de Markovnikov)
OH
O 1) Et2O
+
2) H+ / H2O
MgBr ________________________________________________________
3. a) Exercice 5 :
1.
La réaction A B ne conduit pas à un milieu optiquement actif car on obtient un
mélange racémique (l’attaque de l’organomagnésien s’effectue de façon
équiprobable de part et d’autre du plan de la double liaison).
PCSI Page 2 sur 4
Les organomagnésiens mixtes Corrigé de la feuille d’exercices n°9
Nomenclature
éthanol 2-chloroéthanol 2,2-dichloroéthanol
2.
3-éthylhexan-2-ol 2,3,3-triméthylheptane 2-méthylhex-2-ène
3.
L’atome diode est plus volumineux que l’atome de chlore, la liaison C-I est plus
polarisable que la liaison C-Cl, ce qui explique que l’ion iodure est un meilleur 5-méthyl-4-propylhex-4-èn-3-one (E)-4-éthyl-5,7-diméthyloct-2-ène
nucléofuge que l’ion chlorure.
4.
3-tertiobutylpentane but-2-ènoate de 2-méthylbutyle 2-propylhex-1-ène
1-chloro-2-méthylcyclohexane 2-méthyl-3,4-dipropylnon-2-ène (4R)-4-méthylhexan-3-one
PCSI Page 3 sur 4
Les organomagnésiens mixtes Corrigé de la feuille d’exercices n°9
2-méthylhexane 5-éthyl-2,4-diméthyloctane
4-méthyloctane 4-isopropyl-5-propyldécane
Résolution de problème
Solubilité : l'acide maléique (acide Z-butènedioïque) est polaire alors que
l'acide fumarique (acide E-butènedioïque) est apolaire. On peut les distinguer
grâce à leur solubilité dans l’eau. Le composé polaire sera plus soluble dans
l’eau que le composé apolaire.
Point fusion : l'acide maléique (acide Z-butènedioïque) peut former des
liaisons H intramoléculaires et intermoléculaires alors que l'acide fumarique
(acide E-butènedioïque) ne peut former que des liaisons H intermoléculaires.
L'acide fumarique aura donc une température de fusion plus élevée.
RMN : les constantes de couplages des hydrogènes de la double liaison sont
différentes si la double liaison est Z ou E.
PCSI Page 4 sur 4
Vous aimerez peut-être aussi
- Les Principaux Défauts de SoudureDocument7 pagesLes Principaux Défauts de SoudureAli Clubist100% (3)
- TD 4 Avec Corrigé de Chimie Des SolutionsDocument7 pagesTD 4 Avec Corrigé de Chimie Des SolutionsETUSUP100% (2)
- Assemblages Boulonnés PDFDocument15 pagesAssemblages Boulonnés PDFyoussef essasnoui100% (3)
- Winkler DiagrammeDocument3 pagesWinkler Diagrammedemoiselle motivationPas encore d'évaluation
- TD3 Chimie Generale +CORRIGE 2016-2017Document6 pagesTD3 Chimie Generale +CORRIGE 2016-2017Awatif BePas encore d'évaluation
- Methode MagnetiqueDocument15 pagesMethode MagnetiqueHalim SarriPas encore d'évaluation
- Series 3eme Physique PDFDocument79 pagesSeries 3eme Physique PDFAmel Rhahlia75% (4)
- RapportDocument25 pagesRapportAlae IbenelrhaziPas encore d'évaluation
- Theorie Du Cycle FrigorifiqueDocument87 pagesTheorie Du Cycle Frigorifiquezizo46100% (3)
- Cours Chimie Organique SMC S3 2020 2021Document98 pagesCours Chimie Organique SMC S3 2020 2021MOHAMED MAZOUARIPas encore d'évaluation
- Chimie Des Polymère - Exercices de RévisionDocument5 pagesChimie Des Polymère - Exercices de RévisionPeter Taha100% (4)
- TP N° 5 - Oxydo-Réduction - PDFDocument7 pagesTP N° 5 - Oxydo-Réduction - PDFleilalargate_37809290% (1)
- TD 3 Avec Corrigé de Chimie en SolutionDocument7 pagesTD 3 Avec Corrigé de Chimie en SolutionETUSUPPas encore d'évaluation
- AlcynesDocument11 pagesAlcynesAssan Sanogo100% (1)
- TP00 H2O2corr PDFDocument2 pagesTP00 H2O2corr PDFEl Ouahabi SoufyanePas encore d'évaluation
- Serie Tableau AvancementDocument5 pagesSerie Tableau AvancementkkkkPas encore d'évaluation
- Corrigé Épreuve 2 Compo 1sem TS2 IEASNDocument5 pagesCorrigé Épreuve 2 Compo 1sem TS2 IEASNt87d4jyrqkPas encore d'évaluation
- Chimie RésuméDocument5 pagesChimie RésuméCloé LogeanPas encore d'évaluation
- 2016 AmSud Exo2 Correction Benzaldehyde 9ptsDocument5 pages2016 AmSud Exo2 Correction Benzaldehyde 9ptsShanthini JekumarPas encore d'évaluation
- Serie 1 Electrochimie Avec CorrectionDocument14 pagesSerie 1 Electrochimie Avec Correctionimad sahliPas encore d'évaluation
- Reactivité Chimique - Correction de TD3Document6 pagesReactivité Chimique - Correction de TD3abraham LincolnPas encore d'évaluation
- TD5 Transformation Chimique-CorrDocument3 pagesTD5 Transformation Chimique-CorrOut Of (Order)Pas encore d'évaluation
- Composition 2 Semestre de Sciences Physiques (3 Heures) : Exercice 1: (4 Points)Document4 pagesComposition 2 Semestre de Sciences Physiques (3 Heures) : Exercice 1: (4 Points)Ibzo ProPas encore d'évaluation
- SMC3 Session Rattrapage 20-21-CorrigéDocument4 pagesSMC3 Session Rattrapage 20-21-CorrigéTalel pdfPas encore d'évaluation
- CNC 2000 Chimie MP CorrectionDocument4 pagesCNC 2000 Chimie MP CorrectionNouhaila AfakirePas encore d'évaluation
- Chimie A Chap1 Correction ExosDocument3 pagesChimie A Chap1 Correction ExosAllaya AmeniiPas encore d'évaluation
- Sem 2 BghyuDocument3 pagesSem 2 BghyuAnonymous FikOnlapPas encore d'évaluation
- Epreuve Du 1: Corrige de L'Epreuve de Sciences PhysiquesDocument8 pagesEpreuve Du 1: Corrige de L'Epreuve de Sciences PhysiqueslionelPas encore d'évaluation
- Série 2 PH (1) - 2021-07-20T143107.674Document30 pagesSérie 2 PH (1) - 2021-07-20T143107.674Abdel OihabPas encore d'évaluation
- Introduction A La Science PolitiqueDocument8 pagesIntroduction A La Science PolitiqueAs NordinePas encore d'évaluation
- Exercices de Révision C132Document18 pagesExercices de Révision C132abraham LincolnPas encore d'évaluation
- Fich PC SP 3mDocument2 pagesFich PC SP 3mNemir MimirPas encore d'évaluation
- 2c Exos Tableau AvancementDocument5 pages2c Exos Tableau AvancementMahboub SabirPas encore d'évaluation
- Physique CDocument4 pagesPhysique CBachire MbenguePas encore d'évaluation
- Cu Ag MG Cu Ag MG POCDocument3 pagesCu Ag MG Cu Ag MG POCorsiny clinton TCHAPTCHETPas encore d'évaluation
- TD Sur Les Piles ÉlectrochimiquesDocument5 pagesTD Sur Les Piles ÉlectrochimiquesLina alikh100% (1)
- Corrigé Session Normale Descriptive & Diagramme de Phases 2022-2023Document4 pagesCorrigé Session Normale Descriptive & Diagramme de Phases 2022-2023Ali AtbirPas encore d'évaluation
- Exercices C9: Les Complexes: + 4 NH ZN (NH)Document4 pagesExercices C9: Les Complexes: + 4 NH ZN (NH)Silento SwordPas encore d'évaluation
- Chimie - IUT - Seance2 PDFDocument7 pagesChimie - IUT - Seance2 PDFaaraychePas encore d'évaluation
- (C2) TDDocument4 pages(C2) TDMenePas encore d'évaluation
- Cinetique Tpn°1 2020 GP 2eme Annee LicenceDocument4 pagesCinetique Tpn°1 2020 GP 2eme Annee LicenceChouYa OsPas encore d'évaluation
- Corrigé TD2 CSDocument5 pagesCorrigé TD2 CSSimo MaroPas encore d'évaluation
- Correction TD Série 4-20-21Document13 pagesCorrection TD Série 4-20-21ZouikrPas encore d'évaluation
- TD 4 SPRM Partie 2 Thermodynamique électrochimique GC GPI 2021 Aide Résolution PDFDocument9 pagesTD 4 SPRM Partie 2 Thermodynamique électrochimique GC GPI 2021 Aide Résolution PDFYang WuPas encore d'évaluation
- Chimie Corrigé1Document11 pagesChimie Corrigé1Raphaël AubertPas encore d'évaluation
- Corrigé Session Normale Descriptive & Diagramme de Phases 2022-2023Document5 pagesCorrigé Session Normale Descriptive & Diagramme de Phases 2022-2023Ali AtbirPas encore d'évaluation
- Ly 10Document3 pagesLy 10baatout oumaymaPas encore d'évaluation
- TD1 Chimie en Solution 2021Document3 pagesTD1 Chimie en Solution 2021Albert Sama100% (1)
- NH Ag Ag NH K: Correction Exercices de Revision: Les Reactions de ComplexationDocument3 pagesNH Ag Ag NH K: Correction Exercices de Revision: Les Reactions de ComplexationRitaj-Rayane Karim100% (1)
- Equilibre ChimiqueDocument5 pagesEquilibre ChimiqueJabri ImenePas encore d'évaluation
- Résolutions Des TDDocument41 pagesRésolutions Des TDghislain AlowakinnouPas encore d'évaluation
- Poly TD Dynamique 2018-19Document13 pagesPoly TD Dynamique 2018-19kasoolPas encore d'évaluation
- Chap IV Ox - RedDocument43 pagesChap IV Ox - RedyoussefPas encore d'évaluation
- Chap IV Ox - RedDocument43 pagesChap IV Ox - RedyoussefPas encore d'évaluation
- Chimie Bac - Transformations Chimiques - SpectrophotométrieDocument1 pageChimie Bac - Transformations Chimiques - SpectrophotométrieMohammed NiaguiPas encore d'évaluation
- Corrige TD1Document7 pagesCorrige TD1Mariam Ben AbdelouahabPas encore d'évaluation
- Série D'exercices N°1 - Sciences Physiques Avancement D'une Réaction Chimiquue - Bac Mathématiques (2012-2013) MR BARHOUMI EzedineDocument4 pagesSérie D'exercices N°1 - Sciences Physiques Avancement D'une Réaction Chimiquue - Bac Mathématiques (2012-2013) MR BARHOUMI Ezedinejuini rawiaPas encore d'évaluation
- 5 TD React Oxydoreduction SolutionDocument3 pages5 TD React Oxydoreduction SolutionJosé Ernest RamarosandratanaPas encore d'évaluation
- Corrigé Serie D 2021Document7 pagesCorrigé Serie D 2021ChristellePas encore d'évaluation
- CHAP 9 Réaction Rédox-DosageDocument3 pagesCHAP 9 Réaction Rédox-Dosagetoto TOTOROTOPas encore d'évaluation
- Physique CDocument3 pagesPhysique CRochdi BouzaienPas encore d'évaluation
- Correction Exercices de Revision: Les Reactions de PrecipitationDocument5 pagesCorrection Exercices de Revision: Les Reactions de PrecipitationRitaj-Rayane KarimPas encore d'évaluation
- TD2 Correction PDFDocument8 pagesTD2 Correction PDFKhadija LakhdiriPas encore d'évaluation
- OxydoreductionDocument1 pageOxydoreductionYa Cin Khaldi100% (2)
- AvancementDocument2 pagesAvancementYoussef Ben AmarPas encore d'évaluation
- Poster Sari-Ali 22-06-21Document1 pagePoster Sari-Ali 22-06-21Aurora ChanePas encore d'évaluation
- CHAP 9 Réaction Rédox-DosageDocument3 pagesCHAP 9 Réaction Rédox-Dosagetoto TOTOROTOPas encore d'évaluation
- Leçon4 Réactions de Quelques Matières Organiques Avec L'air Prof - Elmasaoudy (WWW - Pc1.ma)Document2 pagesLeçon4 Réactions de Quelques Matières Organiques Avec L'air Prof - Elmasaoudy (WWW - Pc1.ma)Agnaou MohamedPas encore d'évaluation
- 25/10/2008 Devoir Surveille 2 1 S: N H H HDocument1 page25/10/2008 Devoir Surveille 2 1 S: N H H HYannick DevosPas encore d'évaluation
- Thèse PDFDocument147 pagesThèse PDFfaouzi sellaliPas encore d'évaluation
- Irrifrance Presentation Pivot Jan 2023Document24 pagesIrrifrance Presentation Pivot Jan 2023Ghorbel Mohamed AliPas encore d'évaluation
- Binaires 2Document8 pagesBinaires 2محمد الفاتح100% (1)
- Paramètres de TextureDocument3 pagesParamètres de TextureDi SecrètePas encore d'évaluation
- Guide Entretien Et Réglages Des Portes D'entréeDocument15 pagesGuide Entretien Et Réglages Des Portes D'entréeAmirouche BenlakehalPas encore d'évaluation
- Guide D'utilisation Des Normes EN Pour La Conformité Des AccessoiresDocument75 pagesGuide D'utilisation Des Normes EN Pour La Conformité Des AccessoiresRami KsidaPas encore d'évaluation
- 2020 C CorrigeDocument15 pages2020 C CorrigeThomas JanèsPas encore d'évaluation
- Traitement Des Effluents Gazeux Issus de L'incinération: 1. DéfinitionDocument6 pagesTraitement Des Effluents Gazeux Issus de L'incinération: 1. DéfinitionChaimae BadourPas encore d'évaluation
- Cours RDM-1Document60 pagesCours RDM-1mohamed bananePas encore d'évaluation
- Catalogue Sem SoudageDocument20 pagesCatalogue Sem SoudagechelarucosminPas encore d'évaluation
- Filiere Granulats Pneus Usages 201506 Rapport Final PDFDocument200 pagesFiliere Granulats Pneus Usages 201506 Rapport Final PDFmatrixleblancPas encore d'évaluation
- 2007 ActualitChimique 308-309 79-93Document16 pages2007 ActualitChimique 308-309 79-93Mehdi BnsPas encore d'évaluation
- Bordereau Des Prix Unitaires Pour Avenue Ngoma REFDocument153 pagesBordereau Des Prix Unitaires Pour Avenue Ngoma REFDaniel K KalomboPas encore d'évaluation
- CALENDRIERDocument4 pagesCALENDRIERbabaurhumPas encore d'évaluation
- Cours Metamorphisme 2020Document94 pagesCours Metamorphisme 2020TCHONAYE MOLI DJIBRINE100% (1)
- 2de-T2-C1 - COURS Dynamique Des PaysagesDocument4 pages2de-T2-C1 - COURS Dynamique Des PaysagesnramdialePas encore d'évaluation
- Devis Bogoss ComplexeDocument5 pagesDevis Bogoss ComplexeMoundai RakseuhbePas encore d'évaluation
- F4972 Fbe042Document4 pagesF4972 Fbe042DENOUPas encore d'évaluation
- 2013 S 7 CorrigeeDocument28 pages2013 S 7 CorrigeeAly N'sibiPas encore d'évaluation