Académique Documents
Professionnel Documents
Culture Documents
1es Chap 1 Cours Poly Complete
Transféré par
David LandelleCopyright
Formats disponibles
Partager ce document
Partager ou intégrer le document
Avez-vous trouvé ce document utile ?
Ce contenu est-il inapproprié ?
Signaler ce documentDroits d'auteur :
Formats disponibles
1es Chap 1 Cours Poly Complete
Transféré par
David LandelleDroits d'auteur :
Formats disponibles
Première
Thème : Une longue histoire de la matière
Enseignement Scientifique
Chapitre 1 : Les éléments chimiques
I L’abondance des éléments chimiques
1) Rappel de Seconde : notion d’élément et d’isotope
• Un atome est constitué d’un noyau autour duquel gravitent un certain nombre d’électrons.
Le noyau est constitué de particules élémentaires appelées nucléons
(du latin nucleus : noyau).
Il en existe deux types : les protons et les neutrons.
𝐀
• Le noyau de l’atome est représenté symboliquement par la notation :
X est le symbole chimique de l’atome. 𝐙 𝐗
A est le nombre de masse. Il représente le nombre de nucléons (protons + neutrons).
Z est le numéro atomique. Il représente le nombre de protons.
Le nombre de neutrons N d’un atome est donné par la relation : N = A – Z
Exemple : noyau de l’atome d’uranium : 23592U :
Il comporte 92 protons et 235 nucléons, soient 235 – 92 = 143 neutrons (A – Z neutrons).
Exercices : 107
1) Donner la composition (nombre de neutrons et de protons) du noyau de l’atome d’argent. 47𝐀𝐠
L’atome d’argent contient : 47 protons et 107 – 47 = 60 neutrons. argent
107,9
2) Donner la composition du noyau de l’atome de plomb de notation symbolique 208
82𝑃𝑏.
L’atome de plomb contient : 82 protons et 208 – 82 = 126 neutrons.
• Deux isotopes ont le même nombre de protons, ils ont donc le même numéro atomique Z.
• Deux isotopes ont en revanche un nombre de neutrons différent. Le nombre de nucléons A
(neutrons + protons) est donc différent.
La plupart des atomes ont plusieurs isotopes naturels : certains sont stables,
d’autres sont instables donc radioactifs. Chaque isotope est présent dans des
proportions connues, dépendant de l’atome considéré.
On les représente par le même symbole. Pour les nommer, on donne le nom de
l’élément suivi du nombre de masse A (qui est différent pour chaque isotope).
Exemple : Il existe trois isotopes naturels du carbone : les atomes de carbone 12, de carbone 13 et de carbone 14.
Ces trois atomes ont tous 6 protons (Z = 6), mais un nombre de neutrons, donc de nucléons, différent.
carbone 12 carbone 13 carbone 14
symbole : 126C symbole : 136C symbole : 146C
Un élément chimique est caractérisé par son numéro atomique Z. Il est constitué de l’ensemble des entités
chimiques ayant le même nombre de protons.
Exemple : Le numéro atomique Z = 1 représente l’hydrogène, quel que soit le nombre de neutrons.
1 2 3
1H , 1H (appelé deutérium), 1H (appelé tritium) sont des entités appartenant à l’élément hydrogène.
1ère Ens. Scientifique Chapitre 1 : Les éléments chimiques 1/6
2) La répartition des éléments chimiques
Document : Abondance relative des éléments
Le tableau ci-dessous fait apparaître l’abondance relative* des principaux éléments chimiques (en % d’atomes)
dans certains « objets » de notre environnement :
Élément chimique Univers Terre Corps humain Végétaux
H (Hydrogène) 90 0,10 61 47,9
He (Hélium) 9
O (Oxygène) 0,10 49 24,1 21,9
C (Carbone) 0,06 0,02 12,6 27,9
N (Azote) 0,01 1,4 1,1
Mg (Magnésium) 0,005 16 0,008 0,13
Si (Silicium) 0,005 14
Fe (Fer) 0,004 14
Aluminium (Aℓ) 0,00022 1,6
* L’abondance relative d’un élément chimique est la mesure de sa proportion par rapport aux autres éléments dans
un environnement donné.
Les éléments chimiques ne sont pas répartis de manière homogène dans l’Univers.
• Dans l’Univers, les deux éléments les plus abondants sont l’hydrogène et
l’hélium (H et He).
• Sur Terre, les éléments les plus abondants sont l’oxygène, le magnésium, le fer
et le silicium (O Mg Fe Si).
• Dans la biosphère (ensemble des organismes vivants), on retrouve les mêmes
éléments chimiques, mais dans des proportions différentes, avec quatre
éléments majeurs : le carbone, l’hydrogène, l’oxygène et l’azote (C H O N).
II L’origine des éléments chimiques
1) Rappel de Seconde : les transformations nucléaires
Lors d’une transformation nucléaire, un ou plusieurs noyaux réactifs, instables, se transforment en de nouveaux
noyaux. Contrairement aux réactions chimiques, les éléments chimiques ne sont pas conservés : des éléments
disparaissent et de nouveaux éléments apparaissent.
Une transformation nucléaire est modélisée par une équation dans laquelle apparaissent les symboles des
noyaux des réactifs et des produits.
210
Exemple : Transformation du polonium en plomb : 84Po → 206
82Pb +
4
2He
On constate que : 210 = 206 + 4 et 84 = 82 + 2
L’équation d’une réaction nucléaire s’écrit :
𝐀𝟏 𝐀𝟐 𝐀𝟑 𝐀𝟒
𝐙𝟏 𝐗 𝟏 + 𝐙𝟐 𝐗 𝟐 → 𝐙𝟑 𝐗 𝟑 + 𝐙𝟒 𝐗 𝟒
Lors d’une transformation nucléaire, il y a :
• conservation du nombre de nucléons (nombre A) : A1 + A2 = A3 + A4
• conservation de la charge électrique (nombre Z) : Z1 + Z2 = Z3 + Z4
1ère Ens. Scientifique Chapitre 1 : Les éléments chimiques 2/6
Certains réactifs ou produits peuvent être des particules libres qui se trouvent en dehors d’un atome.
On pourra rencontrer : neutron : 10n proton : 11p électron : −10e positon : +10e
Leur symbole n’est pas à apprendre !
15 1 12 4
Exemple : Fission de l’azote bombardé par un proton : 7N + 1p → 6C + 2He
15 + 1 = 12 + 4
15 1 12 4
7N + 1p → 6C + 2He On a bien conservation des nombres A et Z.
7 + 1 = 6 + 2
Exercices : Compléter les pointillés dans les réactions nucléaires ci-dessous :
4 56
a) 166
76Os → 𝟏𝟔𝟐
74W + 𝟐He c) 𝟐𝟓 Mn → 56
26Fe + 𝟎
−1e
b) 𝟐𝟏𝟎
85At → 210
84Po + 0
𝟏e d) 235 1
92U + 0n → 𝟏𝟑𝟗
53I + 94
𝟑𝟗Y + 3 10n
2) Les différentes nucléosynthèses
Prise de notes à partir de la vidéo :
Le Big Bang et la nucléosynthèse primordiale
Durant les premières minutes après le Big Bang, les
particules élémentaires s’agglomèrent de manière stable et
forment les premiers noyaux d’atomes légers : l’hydrogène,
l’hélium et le lithium. C’est la nucléosynthèse primordiale.
La nucléosynthèse stellaire
La fusion nucléaire est une transformation nucléaire au cours de laquelle deux
noyaux légers s’assemblent pour former un noyau plus lourd (de nombre de masse A
plus grand), et éventuellement une particule libre.
1ère Ens. Scientifique Chapitre 1 : Les éléments chimiques 3/6
Exemple : Deux isotopes de l’hydrogène, le deutérium et le tritium, peuvent fusionner pour donner un noyau
d’hélium 4 ainsi qu’un neutron selon l’équation :
2
1H + 31H → 42He + 10n
Naturellement, les deux noyaux positifs, donc de même signe, se
repoussent. Une telle réaction ne peut donc intervenir qu’aux
températures très élevées présentes au cœur des étoiles.
Au cœur des étoiles, les noyaux légers sont écrasés les uns contre les autres et finissent par fusionner pour
former de nouveaux noyaux plus lourds. C’est la nucléosynthèse stellaire.
La plupart des étoiles peu massives, comme le Soleil, sont constituées essentiellement d’hydrogène et d’hélium.
Leurs noyaux d’hydrogène fusionnent pour produire de l’hélium.
Lorsque l’étoile a épuisé tout son hydrogène, elle évolue en géante rouge : son cœur est riche en noyaux d’hélium,
qui fusionnent en donnant des noyaux plus lourds de carbone et d’oxygène.
Si l’étoile est suffisamment massive (masse supérieure à 8 fois celle du Soleil), elle
pourra produire des noyaux encore plus lourds, comme des noyaux de fer.
En fin de vie, ces étoiles massives implosent, puis explosent. Cette explosion
appelée supernova créé des noyaux encore plus lourds comme le platine et l’or
et les diffuse dans l’espace autour de l’étoile. On parle de nucléosynthèse
explosive. Ces éléments dispersés participent à la formation des planètes.
Il existe aussi des réactions de fission nucléaire, lors desquelles un noyau atomique lourd est « cassé » en plusieurs
noyaux plus légers, avec souvent émission de particules libres. C’est ce qui se produit dans une centrale
nucléaire.
Exemple : Dans un réacteur nucléaire, la fission d’un noyau d'uranium 235 sous
l’impact d’un neutron donne lieu à la formation d’un noyau de Baryum 141, d’un
noyau de Krypton 92 et libère plusieurs neutrons 10n.
235 141 92
92U + 10n → 56Ba + 36Kr + 3 10n
Exercice :
Parmi les réactions proposées ci-dessous, préciser si ce sont des réactions de fusion ou de fission nucléaire.
Fusion ou Fusion ou
fission ? Equation de la réaction Equation de la réaction
fission ?
2 3 4 1
Fission 235
92U + 10n → 140
54Xe + 94
38Sr + 2 10n Fusion 1H + 2He → 2He + 1p
48 52 239 135 102
Fusion 24Cr + 42He → 26Fe Fission 94Pu + 10n → 52Te + 42Mo + 3 10n
III Les noyaux radioactifs
1) Noyaux atomiques et radioactivité
La radioactivité est découverte en 1896 par Henri Becquerel. Deux ans plus tard, Pierre et Marie Curie
découvrent deux éléments radioactifs : le polonium et le radium.
La plupart des éléments chimiques ont des noyaux stables, c’est-à-dire qu’ils restent identiques à eux-mêmes au
cours du temps. Certains noyaux sont instables, car ils possèdent trop de protons, de neutrons ou trop des deux.
Ils sont dits « radioactifs » et se désintègrent spontanément.
1ère Ens. Scientifique Chapitre 1 : Les éléments chimiques 4/6
Un noyau radioactif est un noyau instable qui se transforme en un autre noyau, au cours d’une
transformation naturelle appelée désintégration.
La désintégration est un phénomène spontané, inéluctable et aléatoire (au hasard) : il est impossible de
prévoir quand se désintégrera un noyau radioactif. Or, du fait de la désintégration régulière des noyaux,
la quantité d’éléments radioactifs présents dans un échantillon diminue avec le temps.
Chaque élément radioactif est caractérisé par sa demi-vie notée t1/2.
La demi-vie d’un élément t1/2 est la durée nécessaire pour que la moitié des
noyaux initialement présents se soit désintégrée. Il en reste donc encore la
moitié. (à savoir par cœur !! Très souvent demandé en évaluation)
À chaque fois que l’on compte le temps t = t1/2, le nombre de noyaux radioactifs
est divisé par deux. La demi-vie est très variable selon les éléments : de quelques
millisecondes à des milliards d’années.
Prenons un échantillon de 64 atomes d’iode 131 (demi-vie : t1/2 = 8 j) :
Au bout de Au bout de Au bout de Au bout de Au bout de Au bout de
Temps t=0
8j 2×8j 3×8j 4×8j 5×8j n×8j
Nombre
𝟔𝟒 𝟔𝟒 𝟔𝟒 𝟔𝟒 𝟔𝟒 𝟔𝟒
d’atomes 64 32 = 16 = 8 = 4 = 2 =
𝟐 𝟐𝟐 𝟐𝟑 𝟐𝟒 𝟐𝟓 𝟐𝒏
restant
𝟏𝟎𝟎 %
% restant 100 % 50 % 25 % 12,5 % 6,25 % 3,125 % 𝟐𝒏
Nombre
d’atomes
60
40
20
0 t1/2 2 t1/2 3 t1/2 4 t1/2 5 t1/2 t (jours)
La courbe représentant le nombre de noyaux radioactifs restant en fonction du temps est appelée courbe
de décroissance radioactive.
On constate que le nombre d’atomes restant ne suit pas une droite
en fonction du temps. Ce n’est pas parce que la moitié des atomes
radioactifs ont disparu au bout d’une demi-vie qu’ils auront tous
disparu au bout de deux demi-vies !
Si on note N0 le nombre initial de noyaux radioactifs d’un
𝑵𝟎
échantillon. Après n demi-vies, l’échantillon contient
𝟐𝒏
noyaux radioactifs.
1ère Ens. Scientifique Chapitre 1 : Les éléments chimiques 5/6
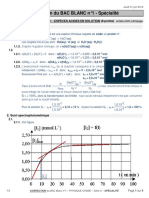
Point méthode : déterminer une demi-vie à l’aide d’une courbe de décroissance
Voici la courbe de décroissance radioactive du Césium 137. Au départ, il y a 1000 milliards de noyaux.
Par définition, après une demi-vie, il reste la moitié, donc 500 milliards de noyaux. Il faut donc trouver en abscisse
le temps correspondant à ce nombre de noyaux. Il peut être demander de laisser les traits de construction !
t1/2
On lit graphiquement que la demi-vie du Césium 137 est t1/2 = 30 ans (ne pas oublier l’unité).
2) Application : datation au carbone 14
La radioactivité est exploitée dans de nombreux domaines : dans les centrales nucléaires, en médecine, en
imagerie médicale et en archéologie avec la datation des objets anciens grâce au « carbone 14 ».
Le carbone 12 ( 126C, 6 protons et 6 neutrons) et le carbone 14 ( 146C, 6 protons et 8 neutrons) sont deux isotopes du
carbone. Le carbone 12 n’est pas radioactif, alors que le carbone 14 l’est.
Le carbone 14 se forme dans la haute atmosphère de la Terre, sa quantité est très faible et constante : il existe un
seul atome de carbone 14 pour 1 000 milliards de carbone 12 !
Comme tout isotope du carbone, le carbone 14 se combine avec l’oxygène de notre atmosphère pour former du
dioxyde de carbone (CO2). Ce dioxyde de carbone est assimilé par les végétaux grâce à la photosynthèse, puis
par l’ensemble des êtres vivants par l’alimentation.
Quand les organismes meurent, ils n’assimilent
plus le dioxyde de carbone. Le carbone 14 n’est
plus renouvelé. La quantité de carbone 14 présente
dans les organismes diminue alors au cours du
temps, tandis que celle de carbone 12 reste stable.
Le carbone 14 se désintègre en azote 14 en suivant
la courbe de décroissance radioactive, avec une
demi-vie de 5 730 ans.
Equation de la désintégration du carbone 14 :
14 14 0
6C → 7N + −1e
Il suffit donc de doser la quantité de carbone 14 restant dans un organisme pour estimer le temps écoulé depuis
sa mort. On peut ainsi remonter jusqu’à 50 000 ans, soit environ 8 demi-vies. Au-delà, la technique n’est pas
assez précise car la quantité de carbone 14 devient trop petite pour être mesurée.
La datation par le carbone 14 permet d’estimer l’âge de vestiges archéologiques de quelques centaines
d’années à 50 000 ans environ. Son principe est d’utiliser les propriétés de décroissance radioactive du
carbone 14, isotope du carbone présent dans toute matière organique.
1ère Ens. Scientifique Chapitre 1 : Les éléments chimiques 6/6
Vous aimerez peut-être aussi
- Introduction à la physique de la matièreD'EverandIntroduction à la physique de la matièreÉvaluation : 3 sur 5 étoiles3/5 (1)
- Physique QuantiqueDocument47 pagesPhysique QuantiquePatrick DedieuPas encore d'évaluation
- Introduction à la physique nucléaire et des particulesD'EverandIntroduction à la physique nucléaire et des particulesPas encore d'évaluation
- Chimie Des SolutionsDocument17 pagesChimie Des SolutionsamaghchichePas encore d'évaluation
- Fiche Revision 3eme DNB Physique - Chimie PDFDocument21 pagesFiche Revision 3eme DNB Physique - Chimie PDFBrunet67% (3)
- Décroissance RadioactiveDocument6 pagesDécroissance RadioactiveJosé Ahanda NguiniPas encore d'évaluation
- ElectrochimieDocument92 pagesElectrochimieThelegenge Isborn100% (3)
- Annales Sciences Physiques Tle CeDocument78 pagesAnnales Sciences Physiques Tle CePetit Frère À Jésus100% (4)
- Bombe HDocument5 pagesBombe HPhobos Elfa100% (1)
- Chapitre 2 L'énergie Solaire PDFDocument43 pagesChapitre 2 L'énergie Solaire PDFmboumbouePas encore d'évaluation
- Jancovici Mines ParisTech Cours 6 PDFDocument123 pagesJancovici Mines ParisTech Cours 6 PDFprénom nomPas encore d'évaluation
- Sa1 (1) 2021Document8 pagesSa1 (1) 2021Clement HergéPas encore d'évaluation
- 1 Stucture de La Matiere - Séance 1Document18 pages1 Stucture de La Matiere - Séance 1نور السلسبيلPas encore d'évaluation
- Chimie 9éme-1Document29 pagesChimie 9éme-1Hama Coulibaly86% (7)
- Chimie Minérale 2Document27 pagesChimie Minérale 2amineahlam311Pas encore d'évaluation
- Reactions Nucleaires Spontanees - ValidéDocument6 pagesReactions Nucleaires Spontanees - ValidéJean Aristide SoulamaPas encore d'évaluation
- Fiche de Revision DNB PDFDocument19 pagesFiche de Revision DNB PDFMohamed MeatiPas encore d'évaluation
- Chap 5 Cours Transformation Nucléaire ComplétéDocument6 pagesChap 5 Cours Transformation Nucléaire Complétéhugo.gloaguen44Pas encore d'évaluation
- Structure de Matière Partie 1Document16 pagesStructure de Matière Partie 1matseguetPas encore d'évaluation
- Chapitre 1 Oxydo-Reduction VersionDocument62 pagesChapitre 1 Oxydo-Reduction VersionMiss KPas encore d'évaluation
- C3Réactions nucléairesFT17Document15 pagesC3Réactions nucléairesFT17EthanPas encore d'évaluation
- Chapitre 1 Ne Structure de L Atome PDFDocument16 pagesChapitre 1 Ne Structure de L Atome PDFMokhtarBensaidPas encore d'évaluation
- Structure Et Etats de La Matière 'Atomistique'': Module: BCG 24Document110 pagesStructure Et Etats de La Matière 'Atomistique'': Module: BCG 24Youssef AkrPas encore d'évaluation
- ChimieMinSyst IRDDocument36 pagesChimieMinSyst IRDKalosoiretrotchgmail.com KalosoPas encore d'évaluation
- Fichier Produit 1927Document69 pagesFichier Produit 1927FlorinaPas encore d'évaluation
- Fichier Produit 1267Document49 pagesFichier Produit 1267Ikram Shin HyePas encore d'évaluation
- Atomistique SMPC Chapitre I 2020-2021Document57 pagesAtomistique SMPC Chapitre I 2020-2021Nadia Ait AhmedPas encore d'évaluation
- Corrigé Super Nova Chimie 2ndeDocument46 pagesCorrigé Super Nova Chimie 2ndeakikouassi11Pas encore d'évaluation
- Chapitre VDocument14 pagesChapitre VHåmēd Bën MåkhtārįPas encore d'évaluation
- 2010 Pondichery Exo1 Correction Polonium 6ptsDocument2 pages2010 Pondichery Exo1 Correction Polonium 6ptsla physique selon le programme FrançaisPas encore d'évaluation
- Oxydoreduction Cours 01Document19 pagesOxydoreduction Cours 01Sa LimPas encore d'évaluation
- Chapitre 01 Les Bases de La Chimie - Merged+ +elumensDocument78 pagesChapitre 01 Les Bases de La Chimie - Merged+ +elumensBobPas encore d'évaluation
- Ph07 Noyau Masse Et EnergieDocument4 pagesPh07 Noyau Masse Et Energiemohamed laghribPas encore d'évaluation
- Atome PDocument2 pagesAtome PToons LandPas encore d'évaluation
- Integrale Chimie Sauf OrgaDocument91 pagesIntegrale Chimie Sauf Orgaotikiri2004Pas encore d'évaluation
- Chapitre 4, Modèle de L'atomeDocument8 pagesChapitre 4, Modèle de L'atomeAyoub AymoPas encore d'évaluation
- TleD PHY L18 Réactions Nucléires SpontanéesDocument11 pagesTleD PHY L18 Réactions Nucléires SpontanéesYssah SerifouPas encore d'évaluation
- 3e - Leçon N°1 (Les Éléments Chimiques Dans L'univers) ClassRoomDocument6 pages3e - Leçon N°1 (Les Éléments Chimiques Dans L'univers) ClassRoomCrazyCookiePas encore d'évaluation
- Exercices Corriges Equilibrer Des Reactions Nucleaires Reaction de Fusion Dans Le SoleilDocument3 pagesExercices Corriges Equilibrer Des Reactions Nucleaires Reaction de Fusion Dans Le Soleilroudy100% (1)
- Brevet Partie A Chapitre 7 BlogDocument7 pagesBrevet Partie A Chapitre 7 BlogpetitmathisPas encore d'évaluation
- Atomistique 1Document17 pagesAtomistique 1mouadsmahi1Pas encore d'évaluation
- Travail A Faire - RadioactiviteDocument4 pagesTravail A Faire - Radioactiviteadjidavibruno7Pas encore d'évaluation
- 1 - Chap1 Liaison Chimique 2021Document34 pages1 - Chap1 Liaison Chimique 2021Belkcem OmaimaPas encore d'évaluation
- CHM101 - Chapitre 1Document7 pagesCHM101 - Chapitre 1abdoul djalil soumanaPas encore d'évaluation
- ATOMISTIQUEDocument20 pagesATOMISTIQUEmatseguetPas encore d'évaluation
- TD Radioactivite Et Reaction Nucleaire CCRDocument5 pagesTD Radioactivite Et Reaction Nucleaire CCROumar TraorePas encore d'évaluation
- L'électrochimieDocument46 pagesL'électrochimieSeçil ÖzdemirPas encore d'évaluation
- Cours Radioactivite 2009-2010 PDFDocument22 pagesCours Radioactivite 2009-2010 PDFSafa chagrenPas encore d'évaluation
- 4-Bases de La Liaison chimique-MD-SA-VB-1Document39 pages4-Bases de La Liaison chimique-MD-SA-VB-1Koùukoù AbbàssiiPas encore d'évaluation
- Chimie 1ère AnnéeDocument38 pagesChimie 1ère Annéeblack4wakandaPas encore d'évaluation
- 0809CCC13Document2 pages0809CCC13Rahim RashidyPas encore d'évaluation
- Entraînements 2022Document2 pagesEntraînements 2022Jojo JojoPas encore d'évaluation
- COURS Equilibre OxredDocument19 pagesCOURS Equilibre Oxredsembei1Pas encore d'évaluation
- ATOMISTIQUEDocument7 pagesATOMISTIQUEImmeed DaahmaniiPas encore d'évaluation
- TD Radioactivite Et Reaction Nucleaire CCRDocument5 pagesTD Radioactivite Et Reaction Nucleaire CCROumar TraorePas encore d'évaluation
- Oxydo ReductionsDocument35 pagesOxydo ReductionsDvni TvyPas encore d'évaluation
- Ch.3-Theorie Notebook - STE-2020 - ProfDocument21 pagesCh.3-Theorie Notebook - STE-2020 - ProfgabrielaPas encore d'évaluation
- Chapitre 1 Oxydoreduction (Nouveau) - ConvertiDocument17 pagesChapitre 1 Oxydoreduction (Nouveau) - ConvertiMiss KPas encore d'évaluation
- Cours AtomistiqueDocument75 pagesCours AtomistiqueZi NebPas encore d'évaluation
- Aurore-Chimie 2nde SDocument25 pagesAurore-Chimie 2nde SghislainhinkponPas encore d'évaluation
- Cap1 8Document140 pagesCap1 8Liviu Adrian PopescuPas encore d'évaluation
- Chap 1 Structure de L'atomeDocument19 pagesChap 1 Structure de L'atomeHaroun MohammedPas encore d'évaluation
- Cours 1 - Rayonnements Radioactivite Parties 1-2-3Document90 pagesCours 1 - Rayonnements Radioactivite Parties 1-2-312052000Pas encore d'évaluation
- TD#1-Entités Chimiques - 2020-2021 - CorrDocument7 pagesTD#1-Entités Chimiques - 2020-2021 - Corrrayan.delalayPas encore d'évaluation
- Devoir de Contrôle N°1 - Physique - 2ème TI (2008-2009) MR Hamza Hamrouni PDFDocument2 pagesDevoir de Contrôle N°1 - Physique - 2ème TI (2008-2009) MR Hamza Hamrouni PDFAYOUB BEN HASSINEPas encore d'évaluation
- Travaux Dirigés PH244 Année Academique 202-2023Document15 pagesTravaux Dirigés PH244 Année Academique 202-2023Ghislain Desire EtapePas encore d'évaluation
- (UEScF) 5. Radioactivité Naturelle Et ArtificielleDocument3 pages(UEScF) 5. Radioactivité Naturelle Et ArtificielleMounir LachhabPas encore d'évaluation
- Chapitre 4 Couleurs Et ImagesDocument8 pagesChapitre 4 Couleurs Et ImagesLqkchanPas encore d'évaluation
- Decroissance RadioactiveDocument4 pagesDecroissance RadioactiveYmelk RuthPas encore d'évaluation
- Sujet Physique FMSP 2006Document5 pagesSujet Physique FMSP 2006Karen DominiquePas encore d'évaluation
- Radio Activ It ÉDocument30 pagesRadio Activ It ÉlucasPas encore d'évaluation
- AtomistiqueDocument37 pagesAtomistiquebechir sidialyPas encore d'évaluation
- 2004 Maroc Sujet DatationDocument2 pages2004 Maroc Sujet Datationanon_441994392Pas encore d'évaluation
- Devoir de Synthèse N°3 2012 2013 (Nabil)Document6 pagesDevoir de Synthèse N°3 2012 2013 (Nabil)Ayoub Ben MlahPas encore d'évaluation
- Etude Et Exploitation D'un Mini Spectromètre Germanium PortableDocument69 pagesEtude Et Exploitation D'un Mini Spectromètre Germanium PortableKOULAPas encore d'évaluation
- CHM101 - Chapitre 1Document7 pagesCHM101 - Chapitre 1abdoul djalil soumanaPas encore d'évaluation
- Les Constituants de L'atome: Le NoyauDocument1 pageLes Constituants de L'atome: Le NoyauNawres MsakniPas encore d'évaluation
- Collection Demistified: Cours de Physique Pour Les Classes de Terminales ScientifiquesDocument61 pagesCollection Demistified: Cours de Physique Pour Les Classes de Terminales ScientifiquesEssohanam AwatePas encore d'évaluation
- Ec Chim4231-Chimie Structurale - Td2-2: Université de Yaoundé I-Ecole Normale Supérieure-Département de ChimieDocument2 pagesEc Chim4231-Chimie Structurale - Td2-2: Université de Yaoundé I-Ecole Normale Supérieure-Département de ChimieKeuamene Djogue MarozzottiPas encore d'évaluation
- Support de Cours PH244 Radioactivité 2021 2022Document16 pagesSupport de Cours PH244 Radioactivité 2021 2022Ghislain Desire EtapePas encore d'évaluation
- Eloc Base - La MatiereDocument10 pagesEloc Base - La MatiereLionel GilotPas encore d'évaluation
- Seriie #10 Noyau Atomique Et Reaction NucleaireDocument3 pagesSeriie #10 Noyau Atomique Et Reaction NucleaireMahmoud Essahbi Sahbi DaghsniPas encore d'évaluation
- Cours RadiometrieDocument61 pagesCours RadiometrieSaider SaidPas encore d'évaluation
- Série Corrigée Avec Correction - Chimie SERIE ATOME Et Élément Chimique - 2ème Sciences Exp (2012-2013) MR SASSI LASSAAD PDFDocument2 pagesSérie Corrigée Avec Correction - Chimie SERIE ATOME Et Élément Chimique - 2ème Sciences Exp (2012-2013) MR SASSI LASSAAD PDFPANDA MUSICPas encore d'évaluation
- EXERCICE (Datation Au Carbone C14)Document7 pagesEXERCICE (Datation Au Carbone C14)Imed Benrhouma100% (2)
- ILEPHYSIQUE Physique 2 Atomes Ions CoursDocument2 pagesILEPHYSIQUE Physique 2 Atomes Ions CoursMoussa BanaPas encore d'évaluation
- TS - BAC Blanc N°1 Corrigé - Spécialité PDFDocument4 pagesTS - BAC Blanc N°1 Corrigé - Spécialité PDFphytanjaPas encore d'évaluation
- PhysiqueDéfinitions MR Haidara-1Document8 pagesPhysiqueDéfinitions MR Haidara-1Amadou TraoréPas encore d'évaluation
- Corrections CAPES PCDocument195 pagesCorrections CAPES PCAugustin WiniguePas encore d'évaluation
- Af3530 Interaction Particules MatiereDocument13 pagesAf3530 Interaction Particules Matierezineb mhPas encore d'évaluation